UPLC-MS/MS测定阿莫西林脉冲片在犬体内的药动学和生物等效性
2016-11-22秦璐皮佳鑫祁东利张谦黄瑞韩润萍刘志东
秦璐,皮佳鑫,祁东利,张谦,黄瑞,韩润萍,刘志东
(天津市现代中药重点试验室制剂室-省部共建国家重点试验室培育基地,天津现代中药发现与制剂技术教育部工程研究中心,天津中医药大学,天津300193)
论著
UPLC-MS/MS测定阿莫西林脉冲片在犬体内的药动学和生物等效性
秦璐,皮佳鑫,祁东利,张谦,黄瑞,韩润萍,刘志东
(天津市现代中药重点试验室制剂室-省部共建国家重点试验室培育基地,天津现代中药发现与制剂技术教育部工程研究中心,天津中医药大学,天津300193)
目的:建立UPLC-MS/MS测定犬血浆中阿莫西林的方法并测定阿莫西林脉冲片的生物等效性。方法:以卡马西平为内标,血浆样品用高氯酸沉淀,并用UPLC-MS/MS测定血浆中阿莫西林含量。动物实验采用随机双交叉自身对照实验法,6只比格犬口服单剂量阿莫西林脉冲片参比制剂、受试制剂后测定其血药浓度,计算药动学参数,评价两制剂的等效性。结果:自制阿莫西林脉冲片单剂量给药其Ke为(0.50±0.16)h-1,t1/2为(1.53±0.57)h,AUC0-12h为(113.21±30.63)μg/(mL·h),Cmax为(31.53±7.37)μg/mL,Tmax为(1.83±0.41)h;市售阿莫西林脉冲片单剂量给药其Ke为(0.44±0.16)h-1,t1/2为(1.78±0.76)h,AUC0-12h为(122.11±28.65)μg/(mL·h),Cmax为(31.01±7.63)μg/mL,Tmax为(2.08±0.58)h,相对生物利用度为(92.09±9.95)%。结论:以AUC0-12h,Cmax和Tmax为评价指标,自制的阿莫西林脉冲释放片与市售的参比制剂在比格犬体内生物等效。
阿莫西林;脉冲片;生物等效;比格犬
阿莫西林属于青霉素类抗生素,抗菌谱广,杀菌力强,作用迅速,广泛用于尿道、呼吸道及皮肤的敏感菌感染[1-3]。因为羟基和氨基的引入,阿莫西林具有很好的耐酸性,比一般青霉素更适合口服且抗菌谱更广[4-5]。阿莫西林长效多脉冲片剂由美国MiddleBrook公司开发,于2008年1月获FDA批准上市,商品名为MOXATAG,尚未在国内上市。该片剂主要用于治疗成人及12岁以上儿童化脓链球菌引起的咽炎和(或)扁桃体炎,其剂量为775 mg/片,每日1片,减少了服药次数,增加了患者的顺应性[6-8]。有试验证明[9]在对链球菌咽炎的治疗中,阿莫西林混悬剂750 mg每日1次,疗程10 d的方案与青霉素V混悬剂250 mg每日3次,疗程10 d的方案同样有效。笔者自制了阿莫西林脉冲片,采用液质联用(UPLC-MS/MS)法作为检测方法[10-11],对阿莫西林脉冲片在犬体内的药动学特征及与市售的MOXATAG脉冲片的生物等效性进行了研究,为其临床研究提供参考。
1 材料与方法
1.1仪器与材料
1.1.1仪器UPLC/MS/MS(Agilent 1690型);质谱仪:Agilent Technologies 6460 Triple Quad LC/MS型三重四极杆串联质谱仪;XP205电子天平(瑞士METTLER TOLEDO公司);离心机(ThermoFisher Sorvall ST 16R);电子天平(德国ACCULAB公司ALC-110.4)等。
1.1.2药品和试剂自制阿莫西林脉冲片,北京汇诚瑞祥医药技术有限公司提供,每片含阿莫西林775 mg,批号为20141230。阳性药物为市售阿莫西林脉冲片,由Victory Pharma公司生产,每片含阿莫西林775 mg,批号为11019-6486。阿莫西林对照品:中国药品生物制品鉴定所,含量为85.8%,批号为130409-201011。卡马西平对照品:中国食品药品检定研究院,含量为99.7%,批号为100142-201004。甲酸:东京化成工业株式会社,含量>98.0%,批号为071206。甲醇:Fisher Scientific,色谱纯,批号为145629。乙腈:Fisher Scientific,色谱纯,批号为150788。
1.1.3实验动物6条健康Beagle犬,雄性,体质量11~13 kg,北京沙河通利实验动物养殖场提供,动物合格证:SCXK(京)2013-0007。
1.2方法
1.2.1给药与采血实验前,将6只Beagle犬随机分成两组,然后将自制阿莫西林脉冲片和市售阿莫西林脉冲片(775 mg)以完整片剂分别塞入Beagle犬的口腔会厌部,使Beagle犬自动吞咽并注入20 mL清水送下,给药后0、0.5、1、1.5、2、2.5、3、4、5、6、8、10、12 h共13个时间点,使用涂有肝素的真空采血针取前肢静脉血2 mL,5 000 r/min离心10 min,分离血浆,然后置-80℃冰箱保存待用。间隔1周后交叉服药,同样程序喂药,采血。
1.2.2色谱与质谱条件色谱柱为Agilent EclipsePlusC1(82.1 mm×50 mm,1.8μm),柱温为30℃,进样量5μL,采用内标法定量。流动相条件见表1。
质谱条件:电喷雾离子源(ESI),正离子模式,多级反应监测(MRM),雾化气流速13.0 L/min,雾化气温度350℃,其中阿莫西林和卡马西平碎裂电压分别为82 V和140 V,碰撞能分别为4 eV和14 eV,阿莫西林检测离子对为m/z 366.11→348.7,卡马西平检测离子对为m/z 237.1→193.8。
1.2.3对照品溶液配制阿莫西林储备液:精密称定阿莫西林对照品29.17 mg,置于25 mL量瓶中,用水溶解并定容,浓度为1.00 mg/mL。卡马西平工作对照液:精密称定卡马西平对照品2.90 mg,置于25 mL量瓶中,用乙腈溶解并定容,得到浓度为115.65 μg/mL的对照溶液,再精密吸取上述卡马西平对照溶液2 mL放入100 mL量瓶中用乙腈定容,得浓度为2.31 μg/mL的内标工作液。
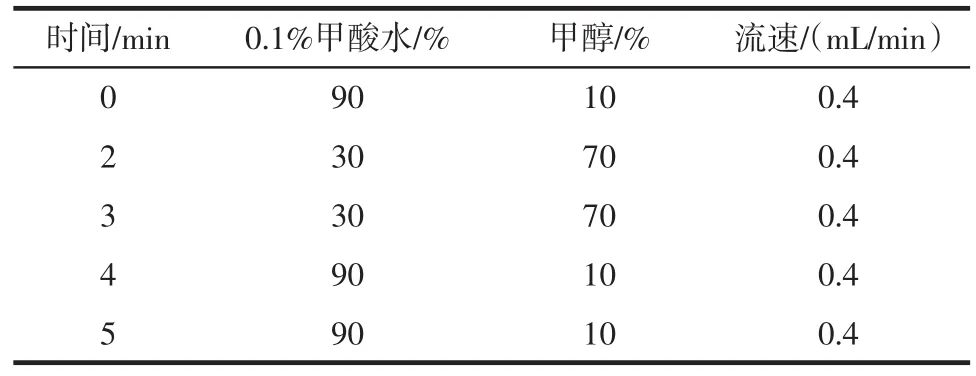
表1 流动相梯度Tab 1 M obile phase gradient
1.2.4血浆处理方法取200μL待测血浆置1.5 mL离心管中,加入500 μL高氯酸溶液(0.5 mol/L)和10 μL内标卡马西平对照溶液,涡旋1 min,12 000 r/min离心5 min,取上清液500 μL加入碳酸钾溶液(1 mol/L)100 μL,涡旋30 s,12 000 r/min离心5 min,取上清液进样,进样体积5 μL。
1.2.5方法学考察[12]
1.2.5.1特异性:分别用空白血浆经生物样品预处理后进样;阿莫西林和卡马西平的对照溶液加入空白血浆中,经生物样品预处理后进样,确定两者本色谱条件下的保留时间。
1.2.5.2线性:取空白血浆180 μL 8份,分别加入阿莫西林对照溶液20 μL,使其终浓度分别为0.10、0.25、0.50、2.50、5.00、25.03、50.05、100.11 μg/mL,再加入500 μL高氯酸溶液(0.5 mol/L)和10 μL卡马西平内标工作液。按生物样品预处理方法处理,取5 μL进样,作液质分析。以药物和内标的色谱峰面积比AVL/IS对血浆中药物浓度C作标准曲线。
1.2.5.3灵敏度:阿莫西林的工作液稀释成不同浓度,加入空白血浆中,按照生物样品预处理方法处理后,进样作质谱分析,找出最低检测限。
1.2.5.4精密度:制备低、中、高3种浓度的含药血浆,使其阿莫西林血浆浓度分别为0.25、25.03、80.09 μg/mL(n=5),加入内标工作液10 μL,按生物样品预处理方法处理,进样5 μL,作液质分析以测定该分析方法的日内精密度。使用同一方法分3 d测定3批样品,计算该分析方法的日间精密度。
1.2.5.5提取回收率:制备低、中、高3种浓度的含药血浆,使其阿莫西林血浆浓度分别为0.25、25.03、80.09 μg/mL(n=6),按上述方法作生物样品处理,进样5 μL,用液质测定阿莫西林的峰面积;将相同浓度的阿莫西林对照溶液直接进样,测定其峰面积。以两者的峰面积比计算回收率。
1.2.5.6基质效应:取200 μL空白血浆于1.5 mL离心管中,按上述方法作生物样品处理。分别用处理后的上清液和水稀释阿莫西林对照溶液,使两者终浓度分别为0.25、25.03、80.09 μg/mL,进样5 μL,用液质测定阿莫西林的峰面积。以上清液稀释的阿莫西林的峰面积比上直接进样等量阿莫西林对照品的峰面积作为基质效应。
1.2.5.7稳定性:直接将阿莫西林的对照储备液进行质谱分析,测定其峰面积。之后放于冰箱中4℃冷藏24 h,取出进行质谱分析,测定其峰面积。考察阿莫西林储备液在储存过程中的稳定性。制备3批低、中、高3种浓度的含药血浆,使其阿莫西林血浆浓度分别为0.25、25.03、80.09 μg/mL。将第一批直接按上述方法作生物样品处理,进行液质分析,另一批重复冻融3次,处理后,进行液质分析;第三批置于-80℃冰箱中冷冻7 d,再进行样品处理和液质分析,考察血浆中阿莫西林在冻存过程中的稳定性。另制备两批低、中、高3种浓度的含药血浆,使其阿莫西林血浆浓度分别为0.25、25.03、80.09 μg/mL。第一批在处理后0 h和24 h进行样品分析,另一批在室温放置6 h后进行样品处理和液质分析,考察样品在处理和进样过程中的稳定性。
1.3数据处理采用Phoenix WinNonLin 6.4软件对测定结果进行数据分析,求得药动学参数并对相关的药动参数进行统计分析。
2 结果
2.1特异性该方法血浆内源物质无干扰,阿莫西林和卡马西平的保留时间为1.2 min和2.8 min,结果见图1。
2.2线性与灵敏度标准曲线为AVL/IS=0.513 993× C+0.532 129,相关系数r=0.999 7,表明血药浓度在0.10~100.11 μg/mL范围内线性良好。最低检测限(信噪比为3时)血药浓度约为0.63 ng/mL。
2.3精密度低、中、高浓度的日内RSD分别为2.50%、4.46%和2.77%,日间RSD分别为5.14%、4.03%和4.63%。结果表明日内日间精密度均符合要求。
2.4提取回收率与基质效应低、中、高3种浓度的回收率分别为(69.18±2.86)%、(73.08±6.01)%、(69.84±6.26)%,基质效应分别为(64.87±0.80)%、(78.13±1.32)%、(68.58±2.68)%,结果表明回收率稳定,且无明显的离子抑制。
2.5稳定性储备液冷藏24 h前后峰面积比为101.10%;低、中、高3种浓度进样室放置24 h前后浓度比为(102.76±3.54)%、(99.41±3.81)%和(99.33±2.07)%;血浆室温放置6 h后峰面积比(91.62±2.34)%、(89.10±1.03)%和(96.75±2.70)%;冻融3次峰面积比(89.88±8.77)%、(93.56±4.34)%和(97.62±3.94)%;长期冻存7 d峰面积比(103.56± 6.47)%、(98.01±2.55)%和(97.87±3.46)%,结果表明在储存及处理测定过程中样品稳定。
2.6药动学参数使用UPLC-MS/MS测定血药浓度,并使用Phoenix WinNonLin 6.4软件对测定结果进行数据分析,求得生物学参数。血药浓度-时间曲线详见图2,生物学参数见表2。
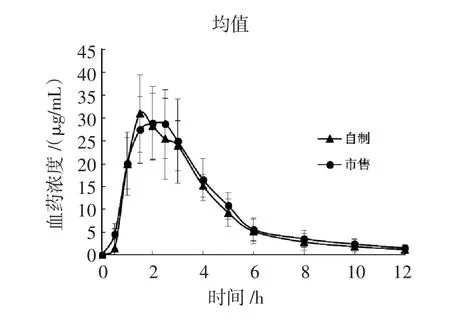
图2 交叉给自制和市售阿莫西林脉冲片后比格犬血浆中阿莫西林的浓度随时间的变化曲线图(n=6)Fig 2 The concentration-time curves of amoxicillin in beagle dog plasm a after taking developed and comm ercial amoxicillin pulsatile-release tablets(n=6)
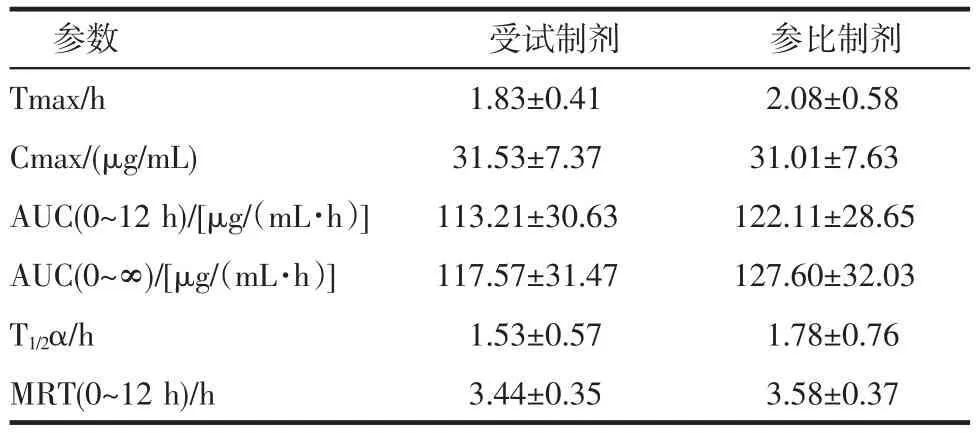
表2 比格犬交叉给药后药动学参数(n=6)Tab 2 The pharm acokinetic parameters
2.7生物等效分析单剂量给药后自制和市售的阿莫西林脉冲片的LnAUC制剂间、周期间没有差异,LnAUC的90%置信区间在82.53%~101.72%的范围内,落在80%~125%的范围内,表明自制和市售的阿莫西林脉冲片的AUC生物等效。两者LnCmax的90%置信区间在89.08%~116.23%的范围内,落在75%~133%的范围内,制剂间、周期间没有差异,表明自制和市售的阿莫西林脉冲片的Cmax生物等效。对两者的Tmax进行秩和检验,结果P>0.05,无统计意义,表明自制和市售的阿莫西林脉冲片的Tmax生物等效。另外由单剂量试验计算受试制剂的相对生物利用度为:F相对=[(AUC受试)/(AUC参比)]×100%=92.09±9.95%。两者在比格犬体内生物等效。
3讨论
本试验采用一步沉淀法处理血浆样品,样品预处理时间短[13],先使用高氯酸进行血浆蛋白沉淀,之后用碳酸钾中和酸性并沉淀高氯酸根,起到了保护色谱柱和提高回收率的作用[14-16]。除使用高氯酸沉淀外本次试验还尝试使用了甲醇、乙腈和甲醇乙腈等比例混合液作为沉淀剂[10],虽然也可使血浆中的蛋白沉淀,但处理后的样品进样后均会峰形异常甚至出现裂峰,猜测可能是因为阿莫西林极性较大,使用有机溶剂沉淀后上清液直接进样可能会出现溶剂效应。
脉冲释药系统具有提高疗效、降低毒副作用和昼夜节律性的特点[17-19]。本品采用的脉冲释药技术可在短时间内多次脉冲释药,快速杀伤细菌,减少细菌芽孢形成,增强了抗生素的抗菌效力,实验证明该方法杀菌效果优于传统治疗方案[9,20],为其他抗生素的脉冲给药提供了参考。
本次通过对受试制剂(自制)和参比制剂(市售)生物学参数的比较可知两者在比格犬体内生物学等效,为进一步的临床试验提供了参考。
[1]刘小平,苏登科,王双云.西药阿莫西林在临床上的应用研究[J].齐齐哈尔医学院学报,2013,34(3):385
[2]王艳秋.西药阿莫西林的临床应用探究[J].中国卫生产业,2012, 9(16):67
[3]高贵平.浅析西药阿莫西林在临床上的应用[J].中国实用医药,2010,5(24):150
[4]杨淑玲.阿莫西林的化学性质以及在临床中的应用[J].中国伤残医学,2013,21(9):90
[5]王虹.阿莫西林的理化特性及临床应用[J].中国民族民间医药,2012,21(14):60
[6]黄胜炎.最近上市的口服择时控释制剂[J].上海医药,2009,30(7):331
[7]王芳,郑琴,伍振峰,等.应答式释药系统构建方法的研究进展[J].中国中药杂志,2013,38(22):17
[8]孟建强,任麒,刘丽媛.时辰药理学与多次脉冲给药的应用[J].中国新药与临床杂志,2010,29(8):576
[9]Feder H M,Gerber M A,Randolph M F,et al.Once-daily therapy for streptococcal pharyngitis with amoxicillin[J].Pediatrics,1999,103(1):47
[10]林楠.LC/MS/MS法测定血浆中氨溴索、克仑特罗和阿莫西林[D].沈阳药科大学:2007
[11]陈苏宁,文爱东,丁莉坤,等.LC-MS/MS同时测定人血浆中阿莫西林-氨溴索浓度及其药动学研究[J].中国药学杂志,2009,44(14):1092
[12]国家药典委员会.中华人民共和国药典:2010年版二部[S].北京:中国医药科技出版社,附录XIX B:2010:195-199
[13]袁文博,丁永娟,徐静静.直接蛋白沉淀-超高效液相色谱法测定氟尿嘧啶血药浓度[J].中国药科大学学报,2015,46(1):81
[14]贾萌萌,李杰,丁何晓梦,等.液相-质谱联用法同时测定人血浆中阿莫西林及克拉维酸钾的浓度[J].中国医院药学杂志,2014,34(9):715
[15]Matsui Y J,Nakamura S,Kondou N,et al.Liquid chromatographyelectrospray ionization-tandem mass spectrometry for simultaneous analysis of chlorogenic acids and their metabolites in human plasma[J]. Chromatography B,2007,858(1/2):96
[16]孙丽荣,严华成,曹雄,等.不同血浆样品制备方法对芍药苷血液药物浓度测定的影响[J].中国药物与临床,2008,8(11):846
[17]冯航,李迎,梅兴国.脉冲释药微丸的研究进展[J].国际药学研究杂志.2015,42(4):483
[18]Kumar S,Siddiqua A,Thanusha G,et al.Comprehensive review on pulsatile drug delivery system[J].JDDT,2013,1(4):15
[19]Patil N D,Bari M M,Barhate S D.A review on novel approach pulsatile drug delivery system[J].IJPSRR,2013,21(1):209
[20]Saigal N,Baboota S,Ahuja A,et al.Multiple-pulse drug delivery systems:setting a new paradigm for infectious disease therapy[J]. Expert Opin Drug Deliv,2009,6(4):441
(2016-01-07收稿)
Study on pharmacokinetics and bioequivalence of amoxicillin pulsatile-release tablets by UPLC-MS/MS in beagle dogs
QIN Lu,PI Jia-xin,QI Dong-li,ZHANG Qian,HUANG Rui,HAN Run-ping,LIU Zhi-dong
(Tianjin Modern Chinese Medicine Key Laboratory-Province and Ministry Co-established State Key Laboratory Cultivation Base,Engineering Research Center of Modern Chinese Medicine Discovery and Preparation Technique,Ministry of Education,Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China)
Objective:To establish a UPLC-MS/MS method for determination of amoxicillin pulsatile-release tablets in dog plasma,and evaluate the pharmacokinetics and bioequivalence of amoxicillin pulsatile-release tablets after single oral dose administration.Methods:Carbamazepine was used as an internal standard,and the protein of plasma samples were precipitated by perchloric acid.According to randomized two-period self crossover study,six dogs were given single oral doses of the test preparation and reference preparation,then the concentration of amoxicillin in plasma were determined,and the pharmacokinetic parameters were calculated and the bioequivalence of the two preparations were evaluated.Results:The pharmacokinetics of developed amoxicillin pulsatile-release tablets were as follows:Ke(0.50±0.16)h-1,t1/2(1.53±0.57)h,AUC0-12h(113.21±30.63)μg/(mL·h),Cmax(31.53±7.37)μg/mL,Tmax(1.83±0.41)h;the pharmacokinetics of commercial amoxicillin pulsatile-release tablets were as follows:Ke(0.44±0.16)h-1,t1/2(1.78±0.76)h,AUC0-12h(122.11±28.65)μg/(mL·h),Cmax(31.01±7.63)μg/mL,Tmax(2.08±0.58)h.The relative bioavailability of the test tablet was(92.09±9.95)%.Conclusion:The developed amoxicillin pulsatile-release tablets may be bioequivalent to the commercial amoxicillin pulsatile-release tablets.
amoxicillin;pulsatile-release tablets;bioequivalent;beagle dogs
R9
A
1006-8147(2016)05-0448-04
秦璐(1990-),男,硕士在读, 研究方向:药物制剂;通信作者:刘志东,E- mail: lonerliuzd@163.com。
