应用紫外分光光度法测定人血白蛋白中氨浓度
2016-06-21张磊,粟珊,张茂
张 磊,粟 珊,张 茂
(四川省宜宾市第一人民医院,四川 宜宾 644000)
应用紫外分光光度法测定人血白蛋白中氨浓度
张 磊,粟 珊,张 茂
(四川省宜宾市第一人民医院,四川 宜宾 644000)
目的 探讨紫外分光光度法测定人血白蛋白中氨浓度的价值,加强药剂科对人血白蛋白的管理。方法 将同一生产批号的人血白蛋白中加入过量定量的钨酸钠溶液、硫酸溶液,使蛋白沉淀的同时,氨与硫酸形成硫酸铵留在滤液中,再加入酚显色剂、碱性次氯酸钠溶液显色后于波长630 nm处测定吸光度。结果 人血白蛋白内的氨在10~300 μmol/L范围内的浓度与吸光度呈良好的线性关系,本方法具有较好的精密度、稳定性及回收率。结论 紫外分光光度法测定人血白蛋白中氨浓度方法简单、准确,易于操作,适合基层医院监测人血白蛋白内的氨浓度。
人血白蛋白;氨;紫外分光光度法
人血白蛋白系由乙肝疫苗免疫健康人的血浆或血清中分离提取制成的外源性白蛋白制剂,对增加循环血容量和维持血浆胶体渗透压有很好的作用。然而输注人血白蛋白也可引起一些不良反应,甚至诱发肝性脑病,其原因与人血白蛋白内可能含有一定浓度的氨有关。以往有报道[1]发现国产血制品存放时间越久,其中含有的氨浓度越高。而鉴于存在一定的技术难度及条件限制,人血白蛋白内氨浓度的测定在基层医院中很少开展。本研究结合现有实验条件,探讨检测人血白蛋白内氨浓度的简单易行方法,为患者提供安全保障,为药剂科对人血白蛋白的管理提供理论依据。
1 材料与方法
1.1 仪器与试剂 电子天平BN-V9型(昆山巨天仪器设备有限公司);紫外可见分光光度仪 Lambda 25型(美国Perkin-Elmer公司);离心沉淀器80-2型(江苏金南仪器制造有限公司);液体快速混匀器SK-1型(江苏金坛市天竟实验仪器厂);电热恒温水箱HH-W420型(江苏金坛市国旺实验仪器厂);人血白蛋白注射液(同路生物制药有限公司,25 ml:5 g,生产批号:20141023);钨酸钠;硫酸铵;亚硝基铁氰化钠;苯酚;氢氧化钠;次氯酸钠;硫酸,所用试剂均为分析纯,水为新制无氯蒸馏水。
1.2 方法 将同一生产批号的新鲜人血白蛋白注射液(距离生产日期30天内)采用紫外分光光度法检测其内部的氨浓度。同时,对于该方法下的精密度、稳定性、回收率进行评定。①无氨水的制备:参考文献[2]取重蒸水1000 ml,加入稀硫酸1 ml与高锰酸钾溶液1 ml,蒸馏即得备用。②酚显色剂:取亚硝基铁氰化钠25.0 mg,与适量苯酚混合后加无氨水至100 ml,过滤即得。③碱性次氯酸钠溶液:取次氯酸钠250 mg,氢氧化钠2500 mg,溶于100 ml无氨水中即得。同时配制0.5 mmol/L硫酸溶液、5 mmol/L硫酸铵溶液。④分别取③中配制的5 mmol/L硫酸铵溶液100、200、500、1000、1500、2000、3000 μl置于50 ml容量瓶内,加无氨水定容至刻度,即得10、20、50、100、150、200、300 μmol/L的硫酸铵标准溶液。⑤标准曲线的制备[1]:将④中的标准溶液1 ml分别加入10%钨酸钠溶液、0.5 mol/L硫酸溶液各0.5 ml,震荡离心,取上清液1 ml,再加入酚显色剂、碱性次氯酸钠溶液各1 ml,水浴后以空白管校正后在630 nm处测定吸光度,将所得的吸光度(见表1)对浓度进行线性回归处理。⑥回收率试验:按照④中的方法配制三个浓度(100、50、10 μmol/L)的硫酸铵标准溶液适量,各取1 ml分别精密加入10%钨酸钠溶液、0.5 mol/L硫酸溶液各0.5 ml,再通过与酚显色剂、碱性次氯酸钠溶液反应显色后,测定OD值,代入标准曲线计算测得量与回收率。⑦精密度实验:配制低、中、高(25、50、75 μmol/L)3个浓度的硫酸铵溶液各3份,日内4 ℃冷藏保存,每间隔1 h测定OD值1次,连续测定5次。另取相同样本4 ℃冷藏保存,每日测定1次,连续测定5日。所得到的OD值代入标准曲线换算成氨浓度,评估精密度。⑧白蛋白样本的测定及稳定性试验:1 ml新鲜的人血白蛋白注射液中加入过量定量的10%钨酸钠溶液、0.5 mol/L硫酸溶液,使其蛋白质完全沉淀,其中的氨与硫酸生成硫酸铵,再以酚显色剂、碱性次氯酸钠溶液显色后于波长630 nm处测定OD值,共测定8次。取硫酸铵溶液适量配制成75 μmol/L硫酸铵溶液,加入等量的新鲜人血白蛋白注射液。经上述方法处理后,分别取1 ml置于30 ℃及4 ℃下保存。30 ℃下保存的样本在1 d内每间隔2 h测定1次,每次测定5份,共测定8次;4 ℃下保存的样本每天定时测量1次,每次平行测定5份,连续测定7 d,共测定8次;将所得到的OD值代入标准曲线换算成游离氨浓度,评估稳定性。
1.3 统计学方法 应用SPSS 19.0软件进行统计学处理。计量资料的表示采用均数±标准差,组间比较采用t检验。P< 0.05为差异有统计学意义。
2 结果
2.1 标准曲线与线性关系 标准曲线见图1。计算回归方程OD=0.002C+0.266(r=0.999,P< 0.01)。
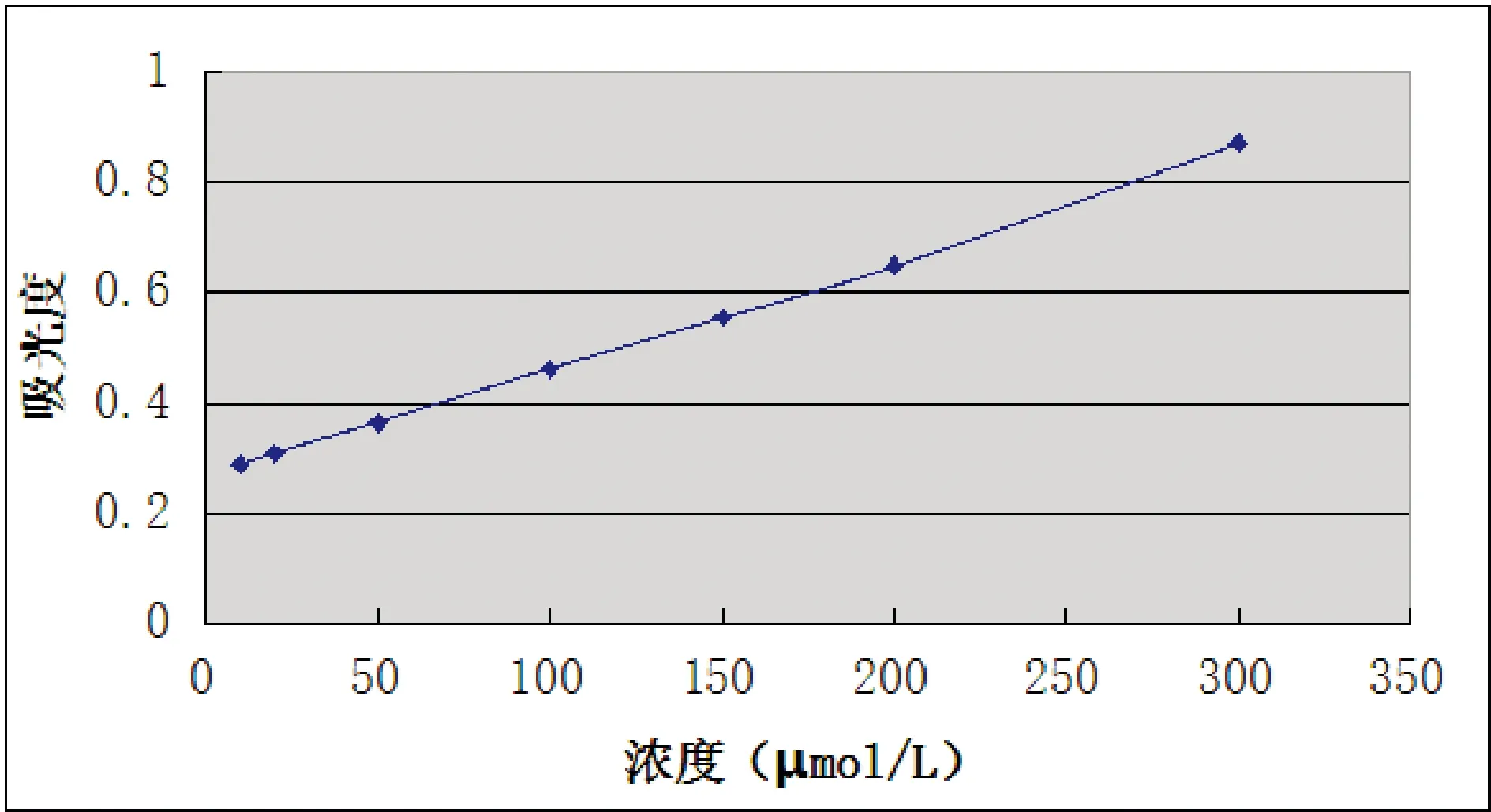
图1 氨的标准曲线
2.2 稳定性 根据回归方程计算得出新鲜的人血白蛋白注射液中氨浓度为(25.98±2.32) μmol/L,见表1。
2.3 回收率 见表2。
2.4 精密度 见表3。
3 讨论
白蛋白是人体细胞外液中含量最多的蛋白质,由585个氨基酸组成,分子量约66.2 kD。其中白蛋白40%分布于血液,60%分布于细胞外液中,循环半衰期约16~18 h[3]。肝硬化患者由于肝功能受损,引起白蛋白合成减少,易引起低白蛋白血症。输注人血白蛋白是纠正低白蛋白血症的常用方法。人血白蛋白中白蛋白含量在96%以上[4]。上世纪80年代时有报道[1]提出:一些国产人血白蛋白注射液的氨浓度为97~199 μmol/L,而正常人血氨浓度为20~60 μmol/L。这些血制品中的氨浓度超过了正常人血氨上限,一旦肝衰竭患者输注此类药物则可能诱发昏迷。然而,该报道中没有提到对人血白蛋白中氨的具体检测方法,且之后未再见到类似的报道。时隔近30年,人血白蛋白的生产工艺较前有了一定进步,是否其中还含有一定浓度的氨尚不清楚。大多数医院的检验科由于技术设备受限,没有开展对人血白蛋白内氨浓度的检测。本研究结合现有实验条件,建立了一套对人血白蛋白内的氨浓度检测的简易方法,易于操作,且具有较好的精密度、稳定性及回收率。
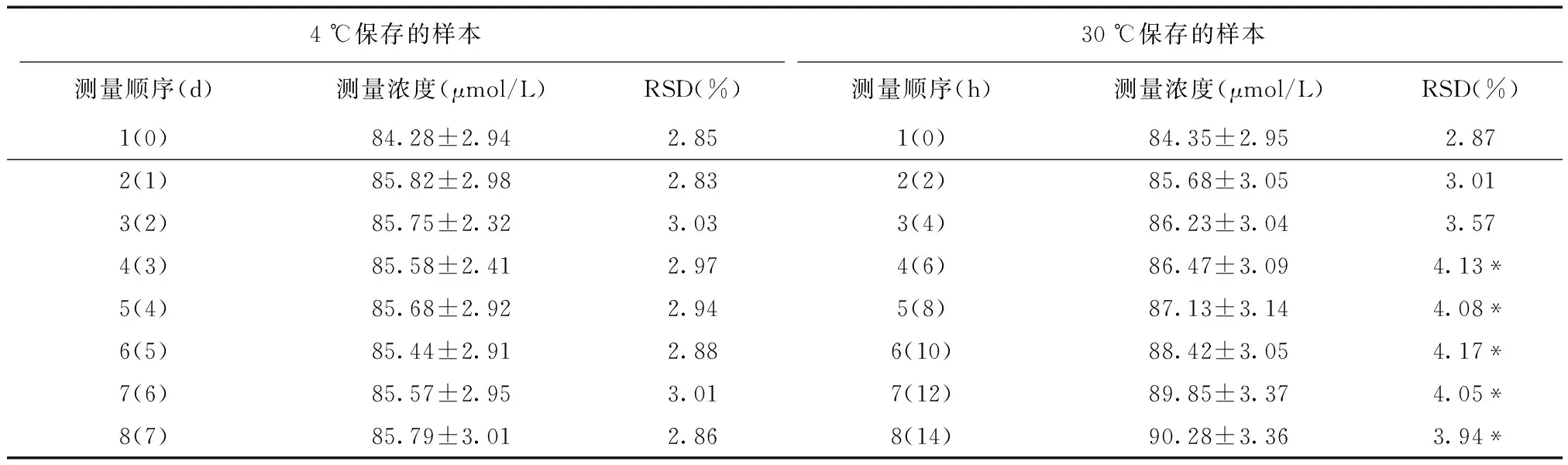
表1 氨浓度稳定性试验
*与第1次(0)比较,P< 0.05

表2 氨回收率试验
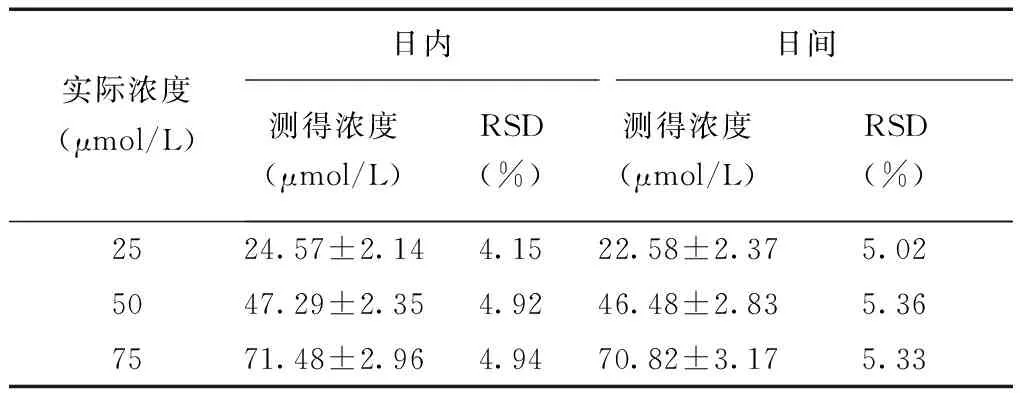
表3 氨浓度精密度试验
本实验结果发现,新鲜的人血白蛋白内含有微量的氨,氨的浓度在4 ℃条件下不会随着保存时间的延长而显著增多,而在30 ℃保存条件下,24 h内人血白蛋白中的氨浓度则会显著升高,而人体正常的血氨浓度为20~60 μmol/L[5]。因此,人血白蛋白在4 ℃保存条件下具有较好的安全性:不会产生高浓度的氨,不会引起人体血氨浓度的增高、诱发肝性脑病。人血白蛋白内含有微量的氨,可能与其制备原料-血浆中含有一定浓度的代谢性氨有关。
通过检测人血白蛋白内的氨浓度,能够为患者提供安全保障,也为药剂科对人血白蛋白的管理提供了依据。
[1] 张木森.肝硬化病例静脉输入血制品引起肝昏迷5例报告[J].空军总医院学报,1987,3(2):159-160.
[2] 中华人民共和国药典委员会.中华人民共和国药典(二部)[S].2005年版.2005,附录:134.
[3] 安友仲.合理应用人血白蛋白-正确认识生理物质在病理过程中的作用[J].中国临床营养杂志,2008,16(1):1-4.
[4] 陈新谦,金有豫.新编药物学[M].第14版.北京:人民卫生出版社,1998:633.
[5] 李影林.临床医学检验手册[M].吉林:吉林科学技术出版社,1990:503.
R917
A
1672-6170(2016)01-0078-04
宜宾市重点科技计划项目(编号:2014SF011);宜宾市卫生局医学科研项目
2015-06-04;
2015-09-13)
