布洛芬-伪麻黄碱衍生物的合成
2016-03-27易八贤
孙 丹,吕 敏,吕 振,李 泉,易八贤
(1.黑龙江中医药大学,黑龙江 哈尔滨 150040; 2.哈尔滨三联药业股份有限公司,黑龙江 哈尔滨 150025;3.中国医药工业研究总院,上海 201403)
布洛芬-伪麻黄碱衍生物的合成
孙 丹1,吕 敏2,吕 振2,李 泉2,易八贤3
(1.黑龙江中医药大学,黑龙江 哈尔滨 150040; 2.哈尔滨三联药业股份有限公司,黑龙江 哈尔滨 150025;3.中国医药工业研究总院,上海 201403)
目的 合成、制备高纯度布洛芬-伪麻黄碱衍生物,探讨其理化性质及波谱特征。方法 以布洛芬和伪麻黄碱为起始原料,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)为缩合剂,经柱层析及重结晶纯化,制备布洛芬-伪麻黄碱的酯化和酰胺衍生物,并对其结构进行检测。结果 所得化合物纯度均大于99.5%,其波谱特征与目标化合物相符。结论 该合成方法简单易行,产物纯度高,可作为杂质对照品,用于布洛芬-伪麻黄碱复方制剂的质量控制。
布洛芬;伪麻黄碱;酯化;酰胺化;杂质对照品
布洛芬(α-甲基-4-(2-甲基丙基)苯乙酸,ibuprofen)和盐酸伪麻黄碱([S-(R*,R*)]-α-1-[1-(甲氨基)乙基]-苯甲醇盐酸盐,pseudoephedrine hydrochloride)的复方制剂广泛用于治疗感冒[1-2],常见的有布洛伪麻片和布洛伪麻胶囊等[3]。布洛芬化学结构中有羧基,盐酸伪麻黄碱结构中有羟基和胺基,在复方制剂中,两者充分接触,经长期放置,可发生酰胺化或酯化反应,生成微量的布洛芬-伪麻黄碱酰胺或布洛芬-伪麻黄碱酯[4-6]。1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC)是活性较高的碳二亚胺类脱水剂,是一种实用、高效的酰胺键、酯键形成试剂,且所需反应条件温和,反应收率高,选择性好,污染少[7-9]。本研究中选择酰胺化反应和酯化反应的缩合剂。伪麻黄碱结构中的氨基活性强,酯化反应时需进行保护,选择有机合成广泛应用的叔丁氧羰基(BOC)[10-11]进行氨基保护,采用盐酸脱保护的方法[12],同时使布洛芬 -伪麻黄碱酯成盐酸盐。
1 仪器与试药
1.1 仪器
JJ-I型电动搅拌器(江苏器械厂);DLSB-5/20型低温冷却液循环泵(郑州长城科工贸有限公司);SHB-Ⅲ型循环水式真空泵(郑州长城科工贸有限公司);RE-52AA型旋转蒸发器(上海亚荣生化仪器厂);全自动 YRT-3型熔点仪(上海精密科学仪器有限公司);LC-2010AHT型高效液相色谱仪(日本岛津公司);Inova-600型核磁共振仪(美国Varian公司);6520四极杆 -飞行时间串联质谱仪(美国 Agilent公司);FTIR-650型傅立叶红外光谱仪(天津港东科技发展股份有限公司)。
1.2 试药
布洛芬(批号为C100-1303199M,纯度为98.5%)和伪麻黄碱(批号为130423,纯度为98.0%),由哈尔滨三联药业股份有限公司研发中心提供;1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC,批号为E1216007,纯度为98.5%),购自上海晶纯试剂有限公司;其余试剂均为市售分析纯。
2 方法与结果
2.1 试验方法
2.1.1 合成路线
布洛芬与盐酸伪麻黄碱的分子结构见图1。合成反应路线见图2。
2.1.2 布洛芬-伪麻黄碱酰胺化衍生物的合成
将布洛芬13.56 g和EDC 24.97 g溶于300 mL二氯甲烷中,室温反应30min后加入伪麻黄碱固体11.28g,反应至薄层色谱(TLC)无原料斑点。有机相水洗至水相pH为7;无水硫酸钠干燥,滤除干燥剂,减压浓缩后,经硅胶柱层析(石油醚/乙酸乙酯)分离,可同时得到2种白色固体,为化合物Ⅰ和化合物Ⅱ,分别经二氯甲烷/石油醚重结晶得到高纯度化合物。

图1 布洛芬和盐酸伪麻黄碱分子结构

图2 合成反应路线图
2.1.3 布洛芬-伪麻黄碱酯化衍生物的合成
将伪麻黄碱固体18.06 g溶于350 mL二氯甲烷中,0℃下滴加(Boc)2O 28.76 g/二氯甲烷50 mL溶液,滴毕,室温反应至 TLC检测无原料斑点。有机相用1 mol/L柠檬酸、饱和食盐水和水依次洗至pH为6,无水硫酸镁干燥,减压浓缩至干,得淡黄色油状物,正己烷重结晶得白色固体,纯度为 99.6%,MS m/z:288.2 [M+Na]+,553.3[2M+Na]+。
将布洛芬14.20 g和EDC 26.44 g溶于300 mL的二氯甲烷中,室温反应30 min,加入上述固体15.50 g,反应至TLC检测体系无原料斑点。有机相水洗,无水硫酸钠干燥,浓缩得淡黄色油状物,硅胶柱层析(石油醚/乙酸乙酯),得无色油状物。
将上述油状物用二氯甲烷120 mL溶解,于-10℃滴加氯化氢乙醇溶液32 mL,保温反应至TLC无原料斑点,加水100 mL搅拌5 min,静置分层,水相二氯甲烷萃取,有机相水洗,干燥,减压浓缩得淡黄色油状物;正己烷重结晶得白色固体,即化合物Ⅲ。
2.1.4 酰胺化及酯化衍生物纯度检测
所得化合物纯度检测参考布洛伪麻那敏复方制剂含量检测方法[13-14],采用高效液相色谱(HPLC)法,色谱条件:色谱柱为WatersSymmetryShieldRP8柱(150mm× 4.6 mm,3.5 μm);流动相为 0.020 mol/L的 Na2HPO4(H3PO4调pH至3.5)-乙腈(50∶50);检测波长为220nm;柱温为25℃。
2.2 试验结果
合成制备了3个化合物,所得化合物纯度检测结果均大于99.5%,理化性质稳定,波谱特征与目标化合物相符。详见表1、表2和图3。
3 讨论
酯化和酰胺化衍生物结构中均包括布洛芬和伪麻黄碱2个基本构架,区别在于羧基结合位点,其理化性质及波谱特征会有所不同。化合物的1HNMR及H-H COSY数据存在明显区别,参考质谱、红外光谱数据分析可判断化合物结构。
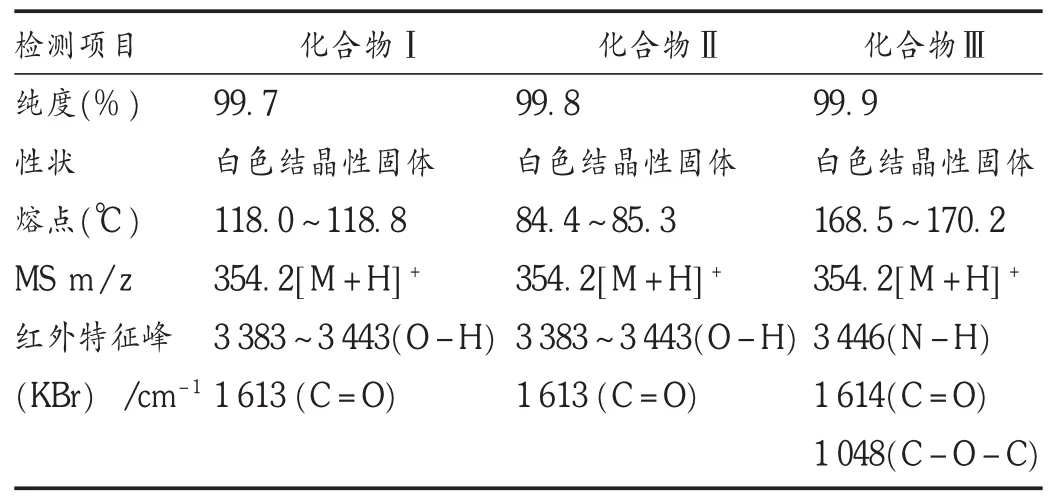
表1 化合物的理化性质、质谱及红外光谱数据

图3 布洛芬和伪麻黄碱结构氢编号

表2 化合物1HNMR的核磁共振氢谱数据
在化合物Ⅰ的1HNMR 中,δ0.839(6H,d,J=6.6Hz),0.869(3H,dd,J=3.0,6.6Hz),1.191(3H,d,J=7.2Hz),2.725(3H,s)处有 5个甲基氢信号;在δ2.388(2H,d,J=7.2Hz)处有 1个亚甲基氢信号;在δ1.791(1H,m),3.907(1H,q,J=6.6Hz),4.513(1H,dd,J=4.8,8.4Hz),4.705(1H,m)存在 4个次甲基信号;结合重水交换氢谱,在δ5.312(1H,d,J=4.2Hz)处为活泼氢信号;同时在方向区域存在9个芳香氢信号。在H-H COSY谱中可见δ5.312(1H,d,J=4.2 Hz)活泼氢信号与δ4.513(1H,dd,J=4.8,8.4 Hz)处的次甲基信号存在相关性。由此可推断化合物Ⅰ以酰胺键的方式连接,结合质谱信号给出的准分子离子信号,红外光谱中3 383~3 443 σ/cm-1的双峰,符合羟基形成氢键后的O-H伸缩振动特征,可确定化合物结构为布洛芬-伪麻黄碱酰胺。
在化合物Ⅱ的1HNMR中,通过分析化合物Ⅱ的1HNMR及H-H COSY谱,可发现其与化合物Ⅰ存在较大相似性,其δ5.512(1H,d,J=4.2 Hz)处活泼氢信号与δ4.456(1H,dd,J=4.2,8.4 Hz)处的次甲基信号存在相关性,其红外光谱数据与化合物Ⅰ一致。可推断其化合物结构与化合物Ⅰ一致,即布洛芬-伪麻黄碱酰胺,与化合物Ⅰ是非对映异构体。
化合物Ⅲ中,与酯羟基相连的亚甲基氢 δ5.711(1H,d,J=9.0 Hz)的只与相邻亚甲基氢有耦合而成双峰,活泼氢成盐后不再与碳上的氢有耦合,红外光谱中3 446 σ/cm-1的为尖单峰,符合仲胺的N-H伸缩振动特征,与化合物Ⅰ、化合物Ⅱ相比,1 048 σ/cm-1的较强吸收符合酯基C—O—C的伸缩振动特征,推断化合物Ⅲ是布洛芬-伪麻黄碱酯的盐酸盐。
本研究中通过化学合成得到高纯度产物,通过MS,IR,1HNMR,H-H COSY等确定其结构,可作为杂质对照品,用于布洛芬-伪麻黄碱的复方制剂的质量控制。
[1]张玉洁,罗永煌,戈振凯,等.布洛芬复方制剂的研究概况[J].中国卫生产业,2011,8(8):5-6.
[2]邱 枫,孙亚欣,肇丽梅,等.布洛伪麻泡腾颗粒剂与片剂在健康人体的生物等效性[J].中国新药与临床杂志,2015,34(1):58-63.
[3]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:119.
[4]陈诗语,杭 琪,敖桂珍,等.新型布洛芬衍生物的合成及其抗炎活性[J].合成化学,2014,22(6):781-784.
[5]陈 卓,冯锁民,杨建全,等.前药布洛芬扁桃酸酯的合成[J].应用化工,2013,42(10):1 806-1 807.
[6]宋 妮,李英霞,孙 雪,等.布洛芬糖衍生物的合成[J].药学学报,2004,39(2):105-109.
[7]喻 平,胡泉源,祁小云,等.EDC在有机合成中的应用研究进展[J].广州化工,2011,39(8):9-11.
[8]Christian AGN,Falgue V.Amide bond formation and peptide coupling[J].Cheminform,2005,61(46):10 827-10 852.
[9]王哲清.实用高效的酰胺键形成试剂[J].中国医药工业杂志,2006,37(12):855-858.
[10]高旭红,李炳奇.有机合成中的氨基保护及应用(综述)[J].石河子大学学报:自然科学版,1999,3(1):76-86.
[11]王 阁,曹小辉.Boc或Cbz保护的 L-脯氨醇衍生物的稳定性[J].有机化学,2011,31(6):908-911.
[12]赵 艳,姚金水,戴 罡,等.N-Boc保护基脱除的原理与方法简介[J].山东轻工业学院学报,2009,23(2):6-7.
[13]朱自红,曹玉梅.HLPC法测定布洛伪麻那敏片中马来酸氯苯那敏的含量[J].中国科技博览,2011(28):602.
[14]殷三福,邱宗荫.高效液相色谱同时测定布洛伪麻那敏片中布洛芬、盐酸伪麻黄碱和马来酸氯苯那敏的含量[J].南方医科大学学报,2010,30(7):1 704-1 709.
Synthesis of Ibuprofen-Pseudoephedrine Derivatives
Sun Dan1,Lyu Min2,Lyu Zhen2,Li Quan2,Yi Baxian3
(1.Heilongjiang University of Chinese Medicine,Harbin,Heilongjiang,China 150040; 2.Harbin Medisan Pharmaceutical Company,Harbin,Heilongjiang,China 150025; 3.China State Institute of Pharmaceutical Industry,Shanghai,China 201403)
Objective To synthesize and prepare the high-purity derivatives of ibuprofen-pseudoephedrine and demonstrate their structure depending on physicochemical properties and spectral characteristics.M ethods Ibuprofen and pseudoephedrine were used as the starting material,with EDC as condensing agent in esterification and amidation.The finished products were purified by silica gel column chromatography and recrystallization and the structure of the products was detected.Results The purity of each product was more than 99.5%,and their spectral characteristics were consistent with the target compound.Conclusion The synthetic method works easily and the finished products are highly pure.Products can be used as impurity reference for the quality control of compound preparation of ibuprofen-pseudoephedrine.
ibuprofen;pseudoephedrine;esterification;amidation;impurity reference
R914.5;TQ460.3
A
1006-4931(2016)08-0020-04
孙丹(1990-),女,黑龙江哈尔滨人,硕士研究生,研究方向为药物的质量,(电子信箱)sun1990dan@163.com;李泉(1968-),男,山东淄博人,硕士研究生导师,主要从事新药研究与开发工作,本文通讯作者,(电话)0451-57355586(电子信箱)hasanlianjinan@aliyun.com。
2015-10-14;
2016-01-15)
