2-甲基-9-芴酮的合成*
2016-01-17汪家宏龙中柱张程亮吕心渊王巧纯华东理工大学精细化工研究所结构可控先进功能材料及其制备教育部重点实验室上海0037江苏启东东岳药业有限公司江苏启东600
汪家宏,龙中柱,张程亮,吕心渊,王巧纯(.华东理工大学精细化工研究所结构可控先进功能材料及其制备教育部重点实验室,上海 0037; .江苏启东东岳药业有限公司,江苏启东 600)
2-甲基-9-芴酮的合成*
汪家宏1,龙中柱2,张程亮2,吕心渊1,王巧纯1
(1.华东理工大学精细化工研究所结构可控先进功能材料及其制备教育部重点实验室,上海200237; 2.江苏启东东岳药业有限公司,江苏启东226200)
摘要:对甲苯胺与苯甲酰氯经酰胺化反应制得N-对甲苯基苯甲酰胺(1); 1经傅克酰基化反应和脱酰胺保护制得2-氨基-5-甲基二苯甲酮(2); 2经Pschorr环合反应合成了2-甲基-9-芴酮,总收率64%,其结构经1H NMR 和HR-ESI-MS确证。
关键词:2-甲基-9-芴酮;傅克酰基化; Pschorr环合;合成
9-芴酮是重要的精细化学品原料,用于制备功能高分子、医药、农药、染料等。其代表性化合物2-甲基-9-芴酮(3)在有机功能材料[1-2]及医药[3-5]领域有着重要的应用前景。目前,3的合成方法主要有甲基芴的氧化法[6]、联苯羧酸及其衍生物的Friedel-Crafts环化[7]、钯或铜催化卤代二苯甲酮环合[8-9]及二苯甲酮钯催化脱氢[10-11]等。方法一原料不易得,而后三种方法均需贵金属催化,成本较高。
本文以对甲苯胺和苯甲酰氯为起始原料,在缚酸剂NEt3存在下经酰胺化反应制得N-对甲苯基苯甲酰胺(1); 1和苯甲酰氯在路易斯酸催化下经傅克酰基化反应,再在70%硫酸中脱酰胺保护制得2-氨基-5-甲基二苯甲酮(2); 2经Pschorr环合反应合成了3(Scheme 1),其结构经1H NMR 和HR-ESI-MS确证。
该合成方法具有原料易得、操作简单、成本低等优点,为其他芴酮及其衍生物的合成提供参考。
1 实验部分
1.1仪器与试剂
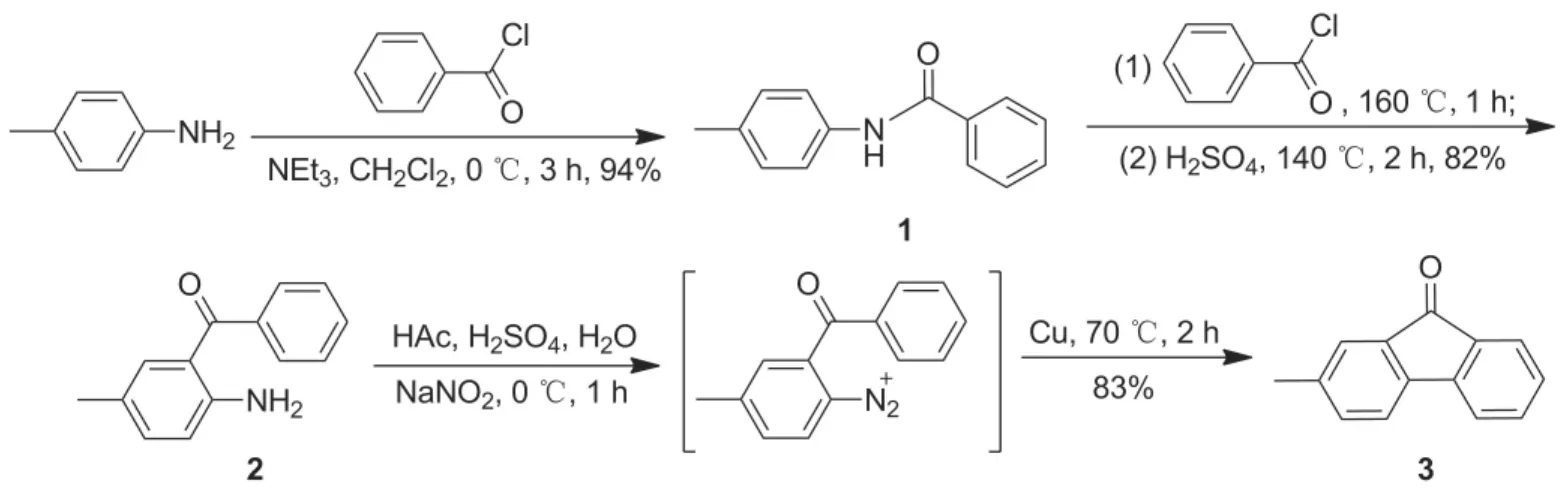
Scheme 1
海能MP100型全自动熔点仪(温度未校正); WFH-203B型三用紫外分析仪; Bruker-400MHz型核磁共振仪(CDCl3为溶剂,TMS为内标); Waters LCT Premier XE型质谱仪。
对甲苯胺,苯甲酰氯,亚硝酸钠和铜粉,分析纯,国药集团化学试剂有限公司;其余所用试剂均为分析纯。
1.2合成
(1)1的合成
在反应瓶中依次加入对甲苯胺53.58 g(500 mmol),三乙胺75.89 g(750 mmol)和二氯甲烷400 mL,搅拌使其溶解;冰浴冷却至0℃,缓慢滴加苯甲酰氯77.32 g(550 mmol),滴毕,于5℃反应3 h。旋蒸除去二氯甲烷,加入石油醚350 mL,过滤,滤饼分别用石油醚(2×50 mL)和乙酸乙酯(2×10 mL)洗涤,加水200 mL,搅拌0.5 h,过滤,滤饼干燥得白色粉末1 99.22 g,收率94%,m.p.154℃~156℃(154℃~157℃[12]);1H NMR δ:7.87(d,J=7.3 Hz,2H),7.76(s,1H),7.57~7.47(m,5H),7.18(d,J=8.1 Hz,2H),2.35(s,3H)。
(2)2的合成
数字化课程建设中要遵循学生受教育原则,在建设过程中要选用优质的教学知识载体,知识体系要从浅入深,知识内容要简单易懂,以此方便课程设计和制作。数字化课程建设需要完整的课程教学标准、教学资源,特别是一些能够促使学生学习课外知识的内容,这样才能够发挥数字化课程作用。在建设时要依据学生学习情况来建设知识体系,设置内容要符合学生认知心理与知识理解规律。
在反应瓶中加入1 84.44 g(400 mmol),无水氯化锌70.88 g(520 mmol)和苯甲酰氯84.01 g(600 mmol),搅拌下缓慢升温至160℃,反应1 h。冷却至100℃,用水(4×200 mL)洗涤,加入70%硫酸200 mL,搅拌于下140℃反应2 h。冷却至室温,倒入大量水中,用氨水调至pH 8~10,用乙酸乙酯(2×300 mL)萃取,合并萃取液,用无水硫酸钠干燥,旋蒸除溶,剩余物用95%乙醇重结晶得黄色固体2 69.41 g,收率82%,m.p.66℃~67℃(65℃~66℃[13]);1H NMR δ:7.64(d,J=6.8 Hz,2H),7.54(t,J=6.8 Hz,1H),7.47(t,J=6.8 Hz,2H),7.23(s,1H),7.13(d,J=8.0 Hz,1H),6.68(d,J=8.0 Hz,1H),5.91(s,2H),2.18(s,3H)。
(3)3的合成
在反应瓶中依次加入水120 mL,乙酸120 mL,硫酸37.80 g和2 40.00 g(190 mmol),搅拌使其溶解;冷却至0℃,缓慢滴加亚硝酸钠13.25 g(190 mmol)水(25 mL)溶液,滴毕;保温反应1 h。加入铜粉4.00 g,于70℃反应2 h(有气体放出)。冷却至室温,用二氯甲烷(2×200 mL)萃取,合并萃取液,用无水硫酸钠干燥,旋蒸除溶后用90%乙醇重结晶得黄色晶体3 30.04 g,收率83%,m.p.90℃~91℃(91℃~92℃[14]);1H NMR(DMSO-d6)δ:7.74(d,J=7.6 Hz,1H),7.68(d,J=7.7 Hz,1H),7.59(t,J=7.6 Hz,2H),7.42(d,J=7.4 Hz,2H),7.34(t,J=7.4 Hz,1H),2.35(s,3H); HR-ESI-MS m/z:Calcd for C14H10O{[M + H]+} 195.081 0,found 195.079 3。
2 结果与讨论
2.1合成
(1)1的合成
1的合成相对比较容易,反应完后直接除去溶解性较好的二氯甲烷,加入溶解性较差的石油醚,过滤后用石油醚和乙酸乙酯的混合溶剂洗去未反应完的苯甲酰氯,再用水洗去三乙胺盐酸盐,干燥即得1,收率较高。
(2)2的合成
(3)3的合成
2的环合过程实际上是分子内的Gomberg-Bachmann反应,即Pschorr反应,其机理是芳胺经重氮化后重氮盐分解为自由基,然后与芳环偶联环合,主要副产物是重氮盐转化为酚。为了提高3收率,本文对3的合成条件进行了优化。
增加溶剂中乙酸含量,直至用纯乙酸作溶剂,考察乙酸用量对3收率的影响,实验结果见表1。由表1可见,增加乙酸用量对3的收率提高不明显,较佳的乙酸用量为50%。
考察不同铜催化剂对3收率的影响,实验结果见表2。由表2可见,以氯化铜、氯化亚铜、硫酸铜和铜粉为催化剂,3收率基本不变。选择铜粉为催化剂较佳。
考察反应温度对3收率的影响,结果见表3。由表3可见,反应温度分别为70℃和80℃时,3收率较高(83%和80%),高于或低于该温度区间收率均明显下降。因此较佳的反应温度为70℃。

表1 乙酸用量对3收率的影响*Table 1 Effect of acetic acid amount on the yield of 3
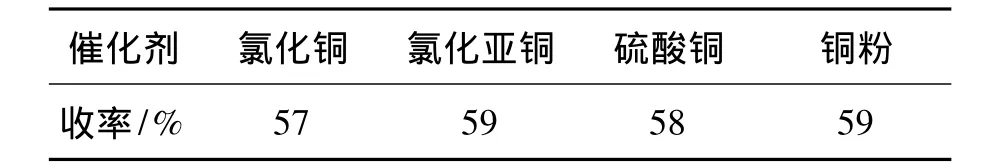
表2 催化剂对3收率的影响*Table 2 Effect of the catalyst on the yield of 3
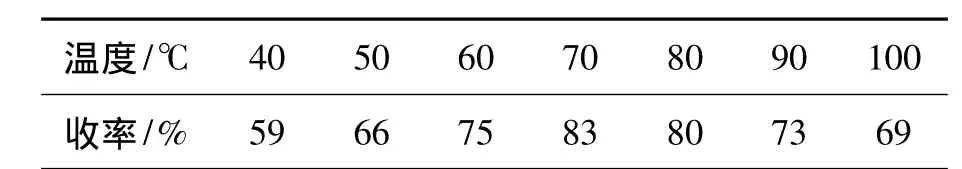
表3 反应温度对3收率的影响*Table 3 Effect of reaction temperature on the yield of 3
综上所述,合成3的最佳反应条件为:以50%乙酸水溶液为溶剂,铜粉为催化剂,反应温度为70℃。
参考文献
[1]Bergmann E D,Berthier G,Fischer E.Fulvenes and thermochromicethylenes.ⅩⅧ.Synthesis,ultraviolet spectra,and dipole moments of certain Δ9,9'-bifluorene[J].Bulletin de la SocieteChimique de France,1952,78-83.
[2]杨慧慧.有机小分子光电材料的合成及性能研究[D].苏州科技学院,2013.
[3]Stephen H,Sébastien G,Ludivine R.Targeting ACE and ECE with dual acting inhibitors[J].Bioorganic&Medicinal Chemistry Letters,2008,18:1058-1062.
[4]Yuri Y,Makiko S,Yurika M.Synthesis and structureactivity relationships of benzophenone-bearing diketopiperazine-type anti-microtubule agents[J].Bioorganic &Medicinal Chemistry,2012,20:4279-4289.
[5]Chih-Hung L,Vernon H.Trisubstituted-N-[(1S)-1,2,3,4-tetrahydro-1-naphthalenyl]benzamides which inhibit P2X3 and P2X2/3 containing receptors[P].US 20 020 173 665,2002.
[6]Qian W X,Jin E L,Bao W L.Clean and highly selective oxidation of alcohols in an ionic liquid by using an ion-supported hypervalent iodine(ⅲ)reagent[J].Angew Chem Int Ed,2005,44:952-955.
[7]Stefanie R,Matthias L,Peter L.Synthesis of fuorenones based on a‘[3 +3]cyclization/Suzuki cross -coupling/Friedel-Crafts acylation’strategy[J].Tetrahedron Lett,2006,47:6903-6905.
[8]Couture A,Dubiez R.Comparative study of the photoreactivity of tertiary aromatic enamides and thioenamides [J].Tetrahedron,1984,40(10):1835-1844.
[9]Haggam,Reda A.Cu(Ⅰ)-catalyzed intramolecularcyclizations of substituted 2-iodobenzophenones under thermal and microwave conditions[J].Tetrahedron,2013,69(31):6488-6494.
[10]Li H,Ru Y,Shi W J.Synthesis of fluorenone derivatives through Pd-catalyzed dehydrogenative cyclization [J].Organic Letters,2012,14(18):4850-4853.
[11]Gandeepan P,Hung C H,Cheng C H.Pd-catalyzed double C-H bond activation of diaryl ketones for the synthesis of fluorenones[J].Chemical Communications,2012,48(75):9379-9381.
[12]Heine H W,Zibuck R.Mechanisms for the reactions of nitrones with aroyl chlorides[J].J Am Chem Soc,1982,104(13):3691-3694.
[13]Davies R E,Openshaw H T,Spring F S.Derivatives of arsacridine.Ⅱ[J].Journal of the Chemical Society,1948,295-299.
[14]Dickinson J D,Eaborn C.Preparation of some substituted 9-carboxy-,9-hydroxy-,and 9-halofluorenes[J].Journal of the Chemical Society,1959,2337-2340.
·研究简报·
Synthesis of 2-Methyl-9H-fluoren-9-one
WANG Jia-hong1,LONG Zhong-zhu2,
ZHANG Cheng-liang2,LÜXin-yuan1,WANG Qiao-chun1
(1.Laboratory for Advanced Materials and Institute of Fine Chemicals,East China University of Science and Technology,Shanghai 200237,China; 2.Qidongdongyue Pharm.Co.,Ltd.,Qidong 226200,China)
Abstract:N-(p-tolyl)benzamide(1)was obtained by acylation of p-toluidine with benzoyl chloride.(2-Amino-5-methylphenyl)(phenyl)methanone(2)was synthesized by Friedel-Crafts acylation and amide deprotection from 1.2-Methyl-9H-fluoren-9-one with the total yield of 64% was synthesized by Pschorr cyclization of 2.The structure was confirmed by1H NMR and HR-ESI-MS.
Keywords:2-methyl-9H-fluoren-9-one; Friedel-Crafts acylation; Pschorr cyclization; synthesis
作者简介:汪家宏(1990-),男,汉族,安徽六安人,硕士研究生,主要从事药物中间体的研究。E-mail:jiahong22@126.com
基金项目:江苏省企业院士工作站(BM2013038)
收稿日期:2014-06-09;
修订日期:2015-01-15
DOI:10.15952/j.cnki.cjsc.1005-1511.2015.05.0428 *
文献标识码:A
中图分类号:O625.15
通信联系人:王巧纯,博士,教授,博士生导师,Tel.021-64252758,E-mail:qcwang@ ecust.edu.cn
