一种1,8-萘酰亚胺类铁离子荧光探针的合成和性能研究
2015-12-16姜思泉周子彦
姜思泉,周子彦
(山东理工大学 化学工程学院, 山东 淄博 255049)
一种1,8-萘酰亚胺类铁离子荧光探针的合成和性能研究
姜思泉,周子彦
(山东理工大学 化学工程学院, 山东 淄博 255049)
摘要:设计并合成了以1,8-萘酰亚胺为发光基团,以希夫碱结构为识别基团的铁离子荧光探针,使用核磁共振氢谱对其结构进行了表征.研究了其发光性能,并对其作为荧光探针检测Fe3+进行了研究. 研究发现在四氢呋喃THF/H2O (95/5, v/v)体系中其对Fe3+具有很高的选择性,加入Fe3+会导致体系的荧光淬灭.该探针对Fe3+的检出限可达到8.12×10-7mol/L,是一种很有前景的含水介质Fe3+荧光探针.
关键词:1,8-萘酰亚胺;希夫碱;荧光探针;Fe3+
金属离子与环境科学、生命科学、医学等多个领域的关系都是十分密切的,其识别、检测在分析化学中也占据着重要的地位,尤其是生命科学中离子分析方向,更是人们所瞩目的前沿课题[1]. 铁作为地壳中含量第三的元素,其在含水介质中的定向检测和测量更是受到了极大的关注[2]. 铁离子在许多细胞水平上的生理代谢中起到了关键作用[3]. 当机体内铁离子浓度超出或低于细胞所需的浓度范围时就会扰乱生命系统的正常活动而使细胞中毒, 从而引起严重的铁代谢障碍疾病,比如阿耳茨海默氏老年痴呆病[4],帕金森氏综合症[5]和其他神经退化性疾病[6]. 因此,对铁离子荧光传感器的研究对于环境及生命科学都具有重大的意义[7]. 与其他过渡金属如铜离子、汞离子相比,关于铁离子的荧光传感器的报道相对较少.Gao等人报道了以香豆素衍生物作为铁离子荧光探针,但无水的检测体系限制了其应用[8]. 铁离子由于顺磁特性,所报道的铁离子传感器绝大多都是荧光淬灭型的. 本文以1,8-萘酰亚胺为荧光基团,以希夫碱结构为识别基团,合成了一种新的荧光物质,并对其在含水介质中检测铁离子的能力进行了研究.
1 实验部分
1.1试剂和仪器
核磁共振波谱仪(AV-400 瑞士布鲁克)紫外-可见分光光度计(UV-3600 日本岛津)荧光分光光度计(F-380 中国港东) 数字熔点仪(WRS-1B上海物光)数显智能控温磁力搅拌器(SZCL-A郑州长城)真空干燥箱(DZF-6021 上海一恒).
4-溴-1,8-萘酐;80%水合肼;正辛胺;β-萘酚;六次甲基四胺;无水乙醇;乙二醇丁醚;冰乙酸;浓硫酸;所用试剂和溶剂为国内市售分析纯. 各种不同金属离子溶液的配制为:Ag+,Pb2+由其硝酸盐配制,其他金属离子由其氯化物配制.
1.2探针化合物的合成(图1)

图1 探针化合物的合成路线
1.2.1N-氨基-4-溴-1,8-萘酰亚胺(Inter-M1)的合成
在装有搅拌磁子,恒压漏斗和回流冷凝管的100mL三口烧瓶中加入4-溴-1,8-萘酐 (0.75g,2.7mmol),50mL无水乙醇,搅拌加热回流条件下缓慢加入80%水合肼(0.17g, 2.7mmol),加毕,回流反应过夜.TLC跟踪反应完全,趁热抽滤,用热无水乙醇洗涤滤饼(50mL×3). 真空干燥,得淡绿色固体0.75g,产率95%.1HNMR(氘代DMSO,TMS)δ:8.66~8.49 (m, 2H), 8.40~ 8.29 (m, 1H), 8.28~8.16 (m, 1H), 8.08~7.94 (m, 1H), 5.81 (s, 2H).
1.2.2N-氨基-4-((N-正辛基)-氨基)-1,8-萘酰亚胺(Inter-M2)的合成
在装有搅拌磁子和回流冷凝管的50mL三口烧瓶中加入Inter-M1 (0.29g, 1.0mmol),正辛胺(0.26g, 2.0mmol),20mL乙二醇丁醚,搅拌加热至回流反应3h. 反应结束后,冷却至室温,将反应液倾入到200mL蒸馏水中析出大量固体,剧烈搅拌1h后静置过夜,抽滤,得深黄色固体,滤饼用蒸馏水洗涤,真空干燥得产物0.28g,产率86%.1HNMR(氘代DMSO,TMS)δ: 8.73 (d,J= 8.0Hz, 1H), 8.45 (d,J= 7.0Hz, 1H), 8.27 (d,J= 8.3Hz, 1H), 7.84 (s, 1H), 7.69 (t,J= 7.1Hz, 1H), 6.77 (d,J= 8.1Hz, 1H), 5.73 (s, 2H), 3.43 ~3.33 (m, 2H), 1.79~ 1.61 (m, 2H), 1.51~1.16 (m, 10H), 0.85 (s, 3H).
1.2.32-羟基-1-萘甲醛(Inter-M3)的合成
参考文献[9]的方案,在装有搅拌器、滴液漏斗和回流冷凝管的三口瓶中加入15mL乙酸,加热搅拌下依次加入β-萘酚(10.5g, 0.073mol)和六次甲基四胺(12g, 0.086mol). 在90℃滴加浓硫酸(9mL, 0.166mol). 滴毕,于97℃搅拌反应2.5 h后倾入100mL蒸馏水中,抽滤,滤饼水洗至中性,干燥,无水乙醇重结晶得浅黄色针状晶体8.68g,产率69%. 熔点:81.0~81.7℃(文献值80 ~ 81℃).1H NMR (CDCl3, TMS) δ:13.12 (s, 1H), 10.83 (s, 1H), 8.36 (d, J = 8.3 Hz, 1H), 7.99 (d, J = 7.1 Hz, 1H), 7.83 (d, J = 8.1 Hz, 1H), 7.63~ 7.43 (m, 1H), 7.45~7.32 (m, 1H), 7.15 (d, J = 8.0 Hz, 1H).
1.2.4探针化合物1的合成
在装有搅拌磁子和回流冷凝管的100mL三口烧瓶中加入Inter-M2 (0.28g, 0.8mmol),Inter-M3 (0.18mg,1.0mmol),催化剂量的冰乙酸和40mL无水乙醇.搅拌加热至回流反应2h,反应结束后,冷却至室温,析出黄色沉淀. 抽滤, 滤饼用无水乙醇重结晶,得淡黄色絮状固体0.38g,产率90.0%.1HNMR(氘代DMSO, 400MHz,TMS)δ(ppm) 12.72 (s, 1H), 9.79 (s, 1H), 8.80 (d,J= 8.4Hz,1H),8.54(d,J=7.2Hz,1H),8.47(d,J=8.8Hz,1H),8.36(d,J=8.8Hz,1H),8.11(t,J=9.2Hz,1H),7.96~7.94(m,2H),7.77(dd,J1=8.0Hz,J2=7.6Hz,1H),7.63(dd,J1=7.6Hz,J2=7.6Hz,1H),7.47(dd,J1=7.6Hz,J2=7.2Hz,1H),7.32(d,J=8.8Hz,1H),6.86(d,J=8.4Hz,1H),1.75~1.71(m,2H),1.43~1.27(m,12H),0.86~0.84(m,3H).
2 结果与分析
2.1化合物1发光性能的研究
1,8-萘酰亚胺类化合物在可见光下可以发出强烈的黄绿色荧光且具有较高的荧光量子产率,因此是最早被广泛研究的荧光类发光物质,并且已经广泛的应用于纺织、油墨、印染、涂料、染料等行业. 本方案设计合成的探针化合物1不仅具有1,8-萘酰亚胺骨架,并且含有C=N双键使其共轭链得到增强,因此也应该具有良好的发光性能.
为了探究化合物1的发光性能,对化合物1在THF溶液中的发光光谱进行了测试,结果如图2所示,化合物1的最大激发波长λex为467nm,最大发射波长λem为512nm,这属于典型的萘酰亚胺衍生物的发射光谱. 为了研究化合物1的发光能力,使用相对值法对化合物1的荧光量子产率(φf)进行了测量,公式(1)如下:

(1)
其中φfstand=0.55,nx和nstand分别为样品溶液和标准物溶液的折射率,Fx和Fstand分别为样品和标准物的荧光发射强度.

图2 探针化合物1在四氢呋喃溶液中的发光光谱(激发,发射狭缝均为2.5nm)
标准物的成分是硫酸奎宁浓度为1.0×10-5mol·L-1的稀硫酸溶液,样品溶液是化合物1浓度为1.0×10-5mol·L-1的THF溶液. 测量方法是分别测定两种溶液的紫外-可见吸收光谱,选取化合物1吸收曲线与硫酸奎宁标准曲线交点处的波长作为激发波长,测试化合物1的荧光发射光谱,得到其荧光发射光谱的强度,然后利用式(1)计算得到化合物1的荧光量子产率[10]. 化合物1的荧光量子效率的相关测试结果列于表1中.
表1化合物1荧光量子产率的测定结果

化合物1硫酸奎宁折射率相交处波长/nmλex/λemFxFstandϕfx1.407353467/51258.57532.51.337353384/452109.695
表1中φfx为样品的荧光量子产率.
2.2化合物1荧光探针性能的研究
2.2.1化合物1的选择性研究
通过研究发现,化合物1在不同溶剂中发射光谱和吸收光谱的研究,我们决定使用THF/H2O(95/5,v/v)系对化合物1的识别能力进行检测. 当1浓度为在25μmol/L时,在溶液中加入过量的常见金属离子(包括Fe3+,Ag+,Ca2+,Cd2+,Fe2+,Ba2+,K+,Mg2+,Mn2+,Na+,Pb2+,Zn2+,Co2+)实验结果如图3所示,当加入过量的上述金属离子后,其他金属离子并没有对1的荧光发射产生明显影响,只有Fe3+对1的荧光发射产生了显著的影响. 当Fe3+加入到1的溶液中后,荧光强度剧烈下降,同时溶液颜色也由黄绿色变成深褐色,并且这个颜色变化可以用肉眼所观察到. 因此,化合物1表现出了对Fe3+特有的选择性,并且整个传感过程肉眼可见,因此1在比色传感Fe3+方面有潜在的应用空间.

图3 化合物1 (25 μmol/L, THF/H2O =95/5, v/v)中加入不同金属离子(100 μmol/L)荧光强度的变化
2.2.2不同浓度的Fe3+对化合物1荧光光谱的影响
为了进一步研究化合物1对Fe3+的传感性能,一系列的荧光滴定实验用以探究不同浓度的Fe3+对1荧光光谱的影响. 将不同浓度的Fe3+加入到化合物1浓度为25μmol/L的THF/H2O(95/5,v/v)溶液中,分别测定不同Fe3+浓度下体系的发射光谱,结果如图4所示,在Fe3+浓度在0~25μmol/L范围内,体系的荧光强度逐渐下降,当加入Fe3+浓度也为25μmol/L时,体系荧光几乎完全淬灭,继续增加体系中Fe3+含量对体系的发光影响基本不大,这说明化合物1与Fe3+是化合物1是1:1络合的. 同时,在Fe3+浓度为0~25μmol/L范围内,体系荧光强度与Fe3+和1的浓度比存在相对良好的线性关系,如图4插图所示,在[Fe3+]/[1]在0~1之间时,体系荧光强度呈线性下降,当[Fe3+]/[1]大于1时,体系荧光强度基本不发生变化. 这同样说明化合物1与Fe3+是1:1络合的.
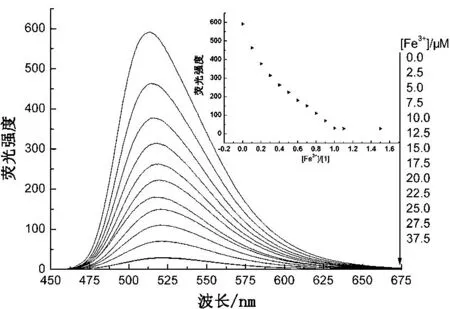
图4 化合物1中逐渐加入Fe3+的荧光发射光谱的变化图(25μmol/L, 298 K, THF/H2O =95/5, v/v)
2.2.3化合物1对Fe3+检出限的研究
通过荧光滴定实验可以发现Fe3+可以导致探针化合物1发射光谱的线性淬灭,为了进一步研究1对Fe3+的传感性能,使用统计计量学的方法对Fe3+的检出限进行了研究.在化合物1浓度为10μmol/L的THF/H2O(95/5,v/v)中分别加入不同浓度的Fe3+(0.25,0.5,0.75,1.0,1.25,1.5,1.75,2.0,2.25,2.5μmol/L),并分别测定其荧光光谱,结果如图5所示.

图5 化合物1(10μmol/L)在THF/H2O=95/5, v/v溶液中512nm处的发射强度与Fe3+浓度(0~2.5μmol/L)的工作曲线
在化合物1浓度为10μmol/L,Fe3+浓度为0~2.5μmol/L范围内,溶液体系的荧光强度随着Fe3+的线性增加而线性降低,其变化关系为F=239.72-24.21C(R=0.99674,N=11),结果分析如下:
线性方程组:Y=-24.21×X+239.72,R= 0.99674,S= 2.421×107,K=3.3
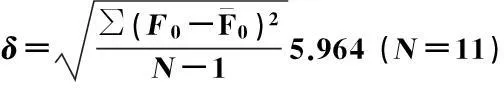
化合物1在THF/H2O(95/5,v/v)溶液中对Fe3+的检出下限为8.12×10-7mol/L.
3 结论
本文设计合成了一种以1,8-萘酰亚胺为发光基团,以C=N结构作为识别基团的一种希夫碱类化合物1,并通过核磁共振氢谱对其结构进行了表征. 研究了化合物1的发光性能,发现其在四氢呋喃溶液中的最大激发和发射波长分别为467nm和512nm,荧光量子效率为0.36. 研究了化合物1在THF/H2O(95/5,v/v)溶液中对常见的金属离子的识别能力,研究发现,体系中引入Fe3+能使化合物1的荧光完全淬灭,其他离子对1的发射强度影响不大,同时,随着Fe3+的加入量逐渐增大,1的荧光强度呈现线性下降. 通过统计计量学的方法对1检出Fe3+的下限进行了研究,发现1对Fe3+的检出下限达到了8.12×10-7mol/L,远远低于国家规定的Fe3+检测标准. 我们合成的探针是一种比色比率荧光探针,并且可以在含水介质中工作,其对Fe3+的选择性和高灵敏性使得其值得广泛推广.
[1]张平, 周程琳, 秦大斌. 同时探测Fe3+和Cu2+的荧光化学传感器的合成及性质研究[J]. 西华师范大学学报, 2012, 33(2): 189-191.
[2]YangL,YangW,XuD, et al.AhighlyselectiveandsensitiveFe3+fluorescentsensorbyassemblingthree1,8-naphthalimidefluorophoreswithatris(aminoethylamine)ligand[J].DyesPigments, 2013, 97: 168-174.
[3]D′AutreauxB,TuckerNP,DixonR, et al.Anon-haemironcentreinthetranscriptionfactorNorRsensesnitricoxide[J].Nature, 2005, 437(7059): 769-772.
[4]ConnorJR,MenziesSL,StMartinSM, et al.Ahistochemicalstudyofiron,transferrin,andferritininAlzheimer’sdiseasedbrains[J].JNeurosciRes, 1992, 31(1): 75-83.
[5]HirschEC,FaucheuxBA.IronmetabolismandParkinson′sdisease[J].MovDisord, 1998, 13(1): 39-45.
[6]ZhangP,LandW,LeeS, et al.Electrontomographyofdegeneratingneuronsinmicewithabnormalregulationofironmetabolism[J].JStructBiol, 2005, 150(2): 144-53.
[7]庄进. 用于铜、锌或铁离子检测的新型荧光探针分子合成及性能研究[D]. 南京: 南京师范大学, 2011.
[8]GaoGY,QuWJ,ShiBB, et al.Ahighlyselectivefluorescentchemosensorforironionbasedon1H-imidazo[4,5-b]phenazinederivative[J].SpectrochimicaActaPartA, 2014, 121: 514-519.
[9]邓继勇, 衷涌, 宋欣荣, 等.N-甲基-3,3-二甲基叫噪琳螺蔡并毗喃的合成[J]. 精细石油化工, 2007, 24(2): 46-49.
[10]高选民. 双官能团有机小分子电致发光材料的合成及性能研究[D].延吉:延边大学, 2009.
(编辑:姚佳良)
Synthesisandcharacterizationofafluorescentprobe
forironionbasedon1,8-naphthalimide
JIANGSi-quan,ZHOUZi-yan
(SchoolofChemicalEngineering,ShandongUniversityofTechnology,Zibo255049,China)
Abstract:A novel fluorescent probe for the recognition of iron ionsthat utilizes naphthalimide as a luminescent group and schiff base as a recognizing group was designed and synthesized. The compound was characterized by1H NMR and the luminescence behavior was investigated. A series of Host-Guest recognition experiments revealed that the new fluorescent probe exhibited excellent selectivity for iron ions among several common metal ions in THF/H2O (95/5, v/v) solution, Fe3+could cause THF-water (95/5, v/v) solution of probe fluorescence quenching and the detection limit of Fe3+was 8.12×10-7mol/L.
Key words:1,8-naphthalimide; schiff base; fluorescent probe; Fe3+
中图分类号:O625.63
文献标志码:A
文章编号:1672-6197(2015)04-0056-04
通信作者:
作者简介:姜思泉,男,274715036@qq.com; 周子彦,男,zyzhou@sdut.edu.cn
基金项目:山东省自然科学基金资助项目(ZR2009BL024)
收稿日期:2014-10-24
