HPLC法测定炙甘草中主要化学成分含量的研究
2015-12-13刘亚萍曹雨诞
刘亚萍,曹雨诞
(1.南京中医药大学附属医院,江苏 南京 210029;2.南京中医药大学,江苏 南京 210046)
甘草为豆科植物(Leguminosae)甘草(Glycyrrhiza uralensis Fisch.)的干燥根和根茎,味甘、偏凉,具有泻火解毒、化痰止咳的功效。甘草蜜制后可以益气补中[1],主要用于心气不足而导致的脉结代、心动悸等症状[2]。炙甘草含有甘草中的主要成分,其中的主要化学成分有黄酮类、三萜类、香豆素类和多糖类等成分[3]。甘草经蜜制后,所含化学成分的含量与甘草相比有所变化,如甘草苷和甘草酸含量下降[4],同时产生糠醛衍生物等化学成分[5]。与甘草相比,炙甘草的补益作用更强[6]。近年来对炙甘草的含量测定有一些报道,指纹图谱研究也有一定进展[6-7],为进一步研究炙甘草的化学成分,为炙甘草药效研究提供依据,本实验对炙甘草中的4种主要成分甘草苷、甘草素、甘草酸和甘草次酸进行了含量测定。
1 仪器与试药
1.1 仪器 HPLC分析采用Waters2695高效液相色谱仪,Waters2489 UV检测器,Empower色谱工作站;Shimadzu AY220电子分析天平。
1.2 试剂 甲醇为色谱纯(批号:20140126),购自江苏汉邦科技有限公司,水为自制重蒸水,其余试剂为分析纯。
1.3 材料 炙甘草饮片样品1(批号20121126),购自安徽丰源铜陵中药饮品有限公司;样品2(批号20130608),购自江苏省中医药;样品 3(批号20130711),购自南京同仁堂汉中路药店,所购饮片经南京中医药大学鉴定教研室吴德康教授鉴定为豆科甘草属植物乌拉尔甘草(Glycyrrhiza uralensis Fisch.)的蜜制炮制品。
甘草苷(批号111610-201106)和甘草酸(批号101050-201101)对照品购自中国食品药品检定研究院,甘草素购自成都曼思特生物科技有限公司(批号MUST-13012506),甘草次酸购自江苏省药品鉴定所(批号20130312)。
2 方法与结果
2.1 色谱条件 色谱柱为Kromasil-C18色谱柱(250 mm ×4.6 mm,5 μm);进样量:10 μL;流速:1.0 mL·min-1;其它色谱条件设定为柱温:30℃;检测波长:230 nm。流动相为磷酸—乙腈系统,其中A为0.1%磷酸水溶液,B为乙腈,洗脱梯度洗脱设定为0~8 min,19% ~19%B;8 ~35 min,19% ~50%B;35 ~50 min,50% ~85%B;50 ~55 min,85% ~100%B;55~57 min,100% ~19%B,色谱图见图1。
2.2 对照品溶液的制备 各对照品经五氧化二磷减压干燥24 h,精密称取甘草苷2.90 mg、甘草素2.30 mg、甘草酸 2.50 mg,甘草次酸 2.04 mg,分别置于5 mL容量瓶中。样品以甲醇溶解并稀释至刻度,制备成4种对照品贮备溶液。精密吸取上述对照品贮备液各2.5 mL于10 mL容量瓶中,以甲醇定容,摇匀后即得炙甘草中4种混合对照品溶液。
2.3 供试品溶液制备 炙甘草饮片粉碎,过四号筛,称取约0.5 g,精密称定。粉末置于三角锥形瓶中,以70%乙醇50 mL超声提取30 min,趁热抽滤后减压回收溶剂。残渣以甲醇溶解,置于25 mL量瓶中,以甲醇稀释至刻度,摇匀。精密量取1 mL至5 mL容量瓶中,以甲醇稀释至刻度,摇匀,即得。
2.4 线性关系与线性范围 分别吸取上述混合对照品溶液 2.5、5.0、7.5、10.0、12.5、15.0、17.5 μL,在上述“2.1”项下色谱条件下进样并测定。4种对照品以进样量为横坐标,峰面积为纵坐标,进行回归计算。所得回归方程为甘草苷:Y=60 634X-19 319,r=0.999 2,在 0.73 ~5.08 μg呈良好的线性关系;甘草素:Y=34 464X-9 969,r=0.999 3,在0.58~4.53μg呈良好的线性关系;甘草酸:Y=33 602X-5 669,r=0.998 4,在 0.61 ~4.29 μg 呈良好的线性关系;甘草次酸:Y=27 696X-4 739,r=0.998 1,在0.51 ~3.57 μg呈良好的线性关系。
2.5 系统适用性试验 分别吸取对照品溶液和供试品溶液各10μL,按“2.1”项下色谱条件测定,结果显示:在此条件下供试品溶液色谱中甘草苷、甘草素、甘草酸和甘草次酸的保留时间分别为11.337、22.960、31.744、51.179 min,与其他的成分有较好的分离效果,理论塔板数均在6 000以上,结果见图1。
2.6 精密度试验 吸取混合对照品溶液10μL,连续进样6次进行测定并分别计算4个成分的峰面积,结果混合对照品中甘草苷、甘草素、甘草酸和甘草次酸的 RSD 分别为 1.75%、2.18%,1.60%和 1.60%。
2.7 重复性试验 取同一样品(炙甘草饮片样品1)溶液6份,按照“2.3”项下的方法操作,结果甘草苷的平均含量为1.32%,RSD为2.52%;甘草素的平均含量为0.27%,RSD为2.60%;甘草酸的平均含量为4.87%,RSD为2.77%;甘草次酸的平均含量为0.16%,RSD为2.14%。
2.8 稳定性试验 取同一样品(炙甘草饮片样品1),照“2.3”项下的方法操作。室温条件下,分别在0、2、4、8、12 h 进样 10 μL,结果炙甘草中甘草苷、甘草素、甘草酸和甘草次酸在12 h内稳定,RSD分别为 2.15%、2.60%、2.77%和 2.14%。
2.9 加样回收率试验 分别精密量取上述6份已知含量(炙甘草饮片样品1,其中甘草苷含量为1.32%,甘草素含量为 0.27%,甘草酸含量为4.87%,甘草次酸含量为0.16%)的供试品溶液2.5 mL至5 mL容量瓶中,精密加入甘草苷、甘草素、甘草酸和甘草次酸 3.57、1.92、14.09、0.84 mg,加甲醇定容至刻度,按上述色谱条件分别进样并计算,结果甘草苷、甘草素、甘草酸和甘草次酸的平均回收率分别为 99.0%、96.6%、103.0% 和 104.9%,RSD 分别为 0.6%、0.4%、0.3%和 1.4%。
2.10 样品含量测定 取各炙甘草样品,分别按照“2.3”项下所述方法制备成供试品溶液。各样品分别进样10μL,进行测定并以外标法计算各成分含量,结果见表1。
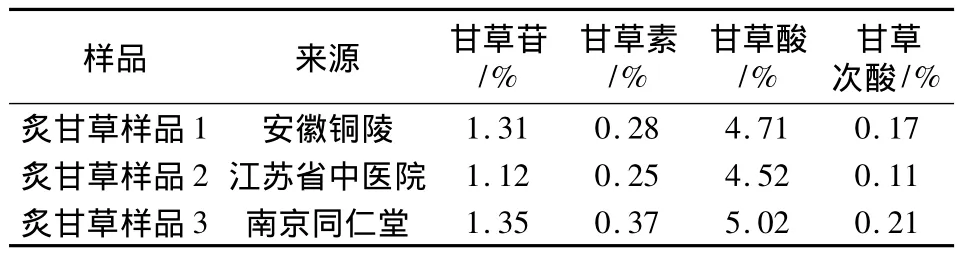
表1 不同炙甘草饮片的含量测定(n=3)
3 讨论
炙甘草中主要化合物有甘草酸、甘草次酸等三萜类、甘草苷、甘草素等二氢黄酮类以及异甘草素等查尔酮类成分。研究表明甘草素为甘草中的主要活性成分之一,具有抗癌[8]、预防糖尿病的应激反应[9]等活性,甘草素的提取分离及分析方法也日益受到关注[10]。炙甘草同时测定以上4种成分的文献较少,所以我们选择甘草素作为炙甘草的测定成分。炙甘草样品提取经70%甲醇、70%乙醇及甲醇3种溶剂的考察,确定其提取工艺为70%乙醇提取30 min。由于甘草酸和甘草次酸结构中都有羧基,所以在流动相中加入0.1%的磷酸,使得各组分均达到基线分离,获得较好的分离效果。综合考虑各组分的紫外最大吸收且经过紫外扫描确定测定波长为230 nm。本实验在同一色谱条件下同时测定了炙甘草中4种主要成分,所测样品中甘草酸和甘草苷都符合《中国药典》的规定,不同样品中含量的差异可能与产地和加工方法有关。本实验所用测定方法快捷准确,可为炙甘草质量控制及为今后炙甘草饮片的炮制和药效学研究提供依据。
[1]齐方洲,朱慧芳,徐辽寅,等.炙甘草汤新论[J].吉林中医药,2009,29(9):811-812.
[2]王 龙,王化良.炙甘草抗心律失常临床应用研究[J].吉林中医药,2012,32(10):1074-1075.
[3]孙良明,杨永安.胀果甘草化学成分的分离与鉴定[J].安徽医药,2013,17(7):1121-1123.
[4]耿家玲,康绍建,柴文英.甘草、炙甘草饮片中甘草苷和甘草酸含量考察[J].中国药师,2011,14(12):1751-1753.
[5]周 倩,孙立立.蜜炙对甘草化学成分影响研究[J].中国药学杂志,2013,48(10):768-772.
[6]孙付军,周 倩,王春芳,等.甘草炮制前后药效学比较[J].中国实验方剂学杂志,2010,16(14):115-118.
[7]伏秦超,王 钢,赵 乐.HPLC检测蜜炙甘草中主要成分含量的研究[J].长春中医药大学学报,2010,26(4):587-589
[8]Wang D,Wong HK,Feng YB ,et al.Liquiritigenin exhibits antitumour action in pituitary adenoma cells via Ras/ERKs and ROS.dependent mitochondrial signalling pathways[J].J Pharm Pharmacol,2014,66(3):408- 417.
[9]Suh KS,Rhee SY,Kim YS,et al.Protective effect of liquiritigenin against methylglyoxal cytotoxicity in osteoblastic MC3T3.E1 cells[J].Food Funct,2014,5(7):1432-1440.
[10]Chen M,Liu L,Chen X.Preparative isolation and analysis of alcohol dehydrogenase inhibitors from Glycyrrhiza uralensis root using ultrafiltration combined with high.performance liquid chromatography and high.speed countercurrent chromatography [J].J Sep Sci,2014,37(13):1546-1551.
