5种输液调配的生脉注射液成品输液稳定性考察
2015-12-13杜红芳耿魁魁何梦璇
杜红芳,刘 圣,耿魁魁,何梦璇
(1.安徽中医药大学,安徽合肥 230038;2.安徽医科大学附属省立医院,安徽 合肥 230001)
生脉注射液由红参、麦冬和北五味子组成,具有益气养阴,复脉固脱之功效,临床上用于气阴两亏,脉虚欲脱的心悸、气短、四肢厥冷、汗出、脉欲绝及心肌梗死、心源性休克、感染性休克等具有上述证候者。随着生脉注射液在临床上应用越来越广泛,不良反应报道也越来越多[1]。主要不良反应有皮疹、恶心、呕吐、腹泻、心悸、口干、头晕、头痛、颜面潮红等。其不良反应的发生常与适应证、浓度、溶媒、滴速等密切相关,其中与溶媒相关的不良反应达到22%[2-3],故临床医师在临床用药时,应严格按照说明书使用,保证合理用药,以减少不良反应的发生。生脉注射液说明书用法用量规定,一次20~60 mL,用5%葡萄糖注射液(5%GS)250~500 mL稀释,但患者伴有糖尿病或需补充电解质时,临床经常将其与0.9%氯化钠注射液(0.9%NS)和葡萄糖氯化钠注射液(GNS)配伍使用,且静脉用药集中调配后不能及时用于患者,室温下常需存放约4 h。为了保证临床用药安全,提高成品输液质量,本文分别用5%GS、10%葡萄糖注射液(10%GS)、0.9%NS、GNS和乳酸钠林格注射液(SLR)调配生脉注射液为成品输液,室温(25℃)下8 h内观察5种成品输液的性状、pH、不溶性微粒数及五味子醇甲的含量变化,为生脉注射液调配后的成品输液质量控制提供参考。
1 仪器与试药
1.1 仪器 LC-2010A HT岛津高效液相色谱仪(紫外检测器,四元低压泵,自动进样器,LabSolutions Version 5.51色谱工作站);FA2004B电子天平(上海精科天美科学仪器有限公司);PHS-3C型电子pH计(上海雷磁仪器厂);GWF-5JS微粒分析仪(天河医疗仪器有限公司)。
1.2 试药 生脉注射液(雅安三九药业有限公司,规格:50 mL,批号:131008050);五味子醇甲对照品(上海源叶生物科技有限公司,规格:20 mg,批号:20130905);5%GS(批号:14010892)、10%GS(批号:13091698)、0.9%NS(批号:14023092)、GNS(批号:14011695),均由安徽丰原药业股份有限公司提供;SLR(中国大冢制药有限公司,批号:4D88G4);甲醇为色谱纯;水为纯化水。
2 方法及结果
2.1 溶液的制备
2.1.1 对照品溶液制备 精密称取五味子醇甲对照品1.0 mg于10 mL容量瓶中,用甲醇定容至刻度,制备成 100 mg·L-1的储备液。
2.1.2 供试品溶液的制备 取5瓶生脉注射液(规格:50 mL),分别用100 mL 5%GS、10%GS、0.9%NS、GNS和SLR调配为成品输液(成品1~5)。
2.2 色谱条件及系统适用性试验[3-5]色谱柱:Inertsil ODS-SP(4.6 mm ×150 mm,5 μm);流动相:甲醇—水(57∶43);流速:1 mL·min-1;检测波长:250 nm;柱温:35℃;进样量:20μL。按上述色谱条件,分别注入五味子醇甲对照品溶液(4 mg·L-1),成品输液及空白输液,五味子醇甲对照品出峰时间为9.250 min,理论塔板数按五味子醇甲计不低于3 000,阴性对照处未见干扰,色谱图见图1。
2.3 方法学考察
2.3.1 标准曲线制备 用移液枪精密移取贮备液100、200、400、600、800、1 000 μL 分别置于10 mL 容量瓶中,依次用甲醇定容至刻度,得 1、2、4、6、8、10 mg·L-1的对照品溶液。按“2.2”项下色谱条件进样,测定峰面积,以峰面积(Y)为纵坐标,质量浓度(X)为横坐标,绘制标准曲线,得回归方程Y=49 031X-648.52,r=0.999 8。结果表明,五味子醇甲质量浓度在1~10 mg·L-1范围内与峰面积有良好的线性关系。
2.3.2 精密度试验 取“2.3.1”项下 2、4、6 mg·L-1的对照品溶液,按“2.2”项下色谱条件进样,同一浓度连续进样3次,RSD分别为0.47%,0.35%,0.21%。
2.3.3 回收率试验 取已知浓度的生脉注射液4 mL置于10 mL的容量瓶中,精密加入100 mg·L-1的对照品溶液 380μL,分别用 5%GS、10%GS、0.9%NS、GNS和 SLR 定容至刻度,按“2.2”项下色谱条件进样。每种输液平行操作6次,计算平均回收率,结果见表1。

表1 加样回收率实验结果
2.4 稳定性考察
2.4.1 外观及pH检测 在室温条件下,分别于0、2、4、6、8 h测定5种成品输液的 pH,并观察其外观变化情况,结果表明,在8 h内外观均呈淡黄色,pH均在6~7之间,且符合2010版《中国药典》输液标准(pH4~9)的规定,即生脉注射液用5种溶媒调配后的成品输液在8 h内外观及pH均无明显变化,表明外观及pH稳定性良好,结果见表2。
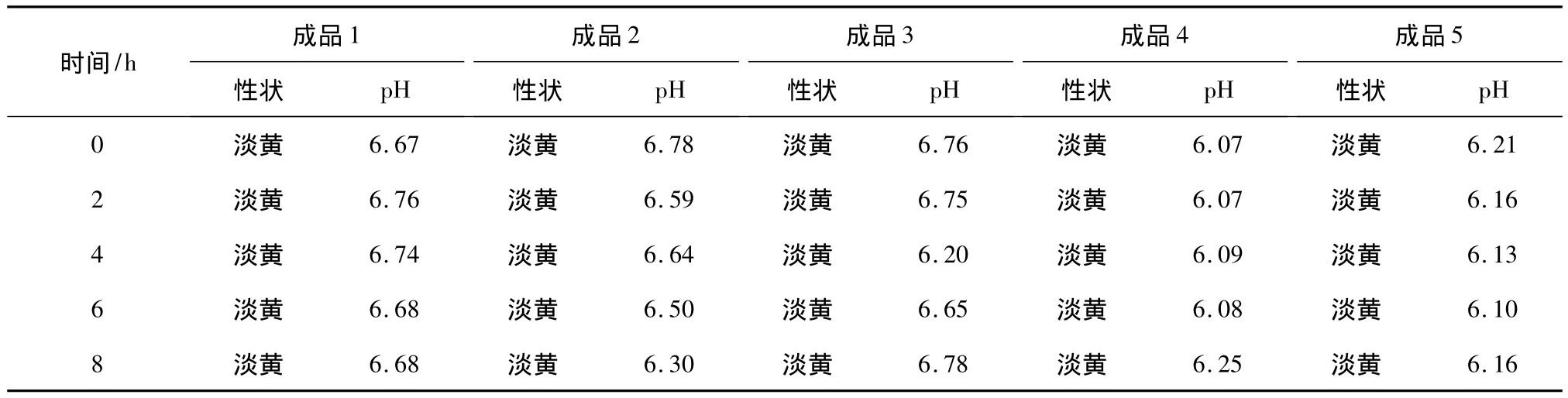
表2 成品输液外观及pH检测结果
2.4.2 不溶性微粒检测 在室温条件下,分别于0、2、4、6、8 h 测定 5 种成品输液的不溶性微粒数,不溶性微粒检测方法同《中国药典》2010年版一部附录IX R不溶性微粒检查法(光阻法)。标示装量为25 mL或25 mL以上的静脉用注射液,除另有规定外,取成品输液,用水将输液袋外壁洗净,小心翻转20次,使溶液混合均匀,先倒出部分输液冲洗开启口及取样杯,再将输液倒入取样杯中,静置2 min或适当时间脱气,置于取样器上。开启搅拌,使溶液混匀(避免气泡产生),依法测定4次,每次取样不少于5 mL,第1次数据不计,取后续3次测定结果的平均值计算。结果表明,生脉注射液与5%GS、10%GS、0.9%NS、GNS 调配的成品输液,4 h 内不溶性微粒均符合《中国药典》2010年版一部标准,但与SLR调配的成品输液中≥10μm不溶性微粒数超出该标准,结果见表3。
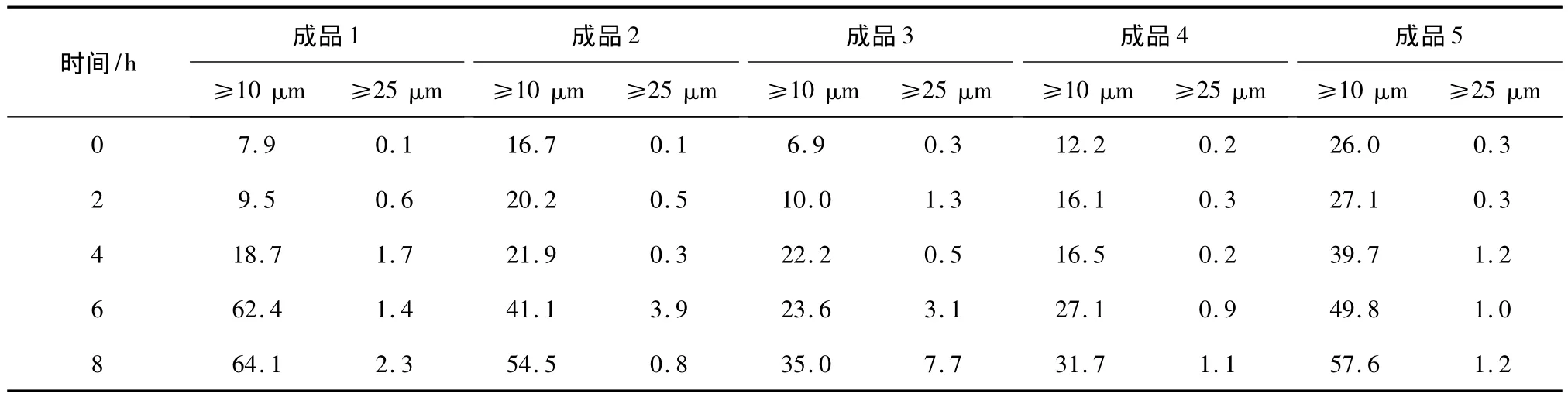
表3 成品输液不溶性微粒检测结果/粒·mL-1
2.4.3 含量测定 取5种成品输液,按“2.2”项下色谱条件于0、2、4、6、8 h 分别进样,测定峰面积,代入线性回归方程计算五味子醇甲的含量,同时以0 h的含量为100%分别计算5种成品输液在2、4、6、8 h的相对含量,结果表明,5种成品输液在8 h内含量无明显变化,结果见表4。
表4 各成品输液中五味子醇甲的相对含量变化(±s)
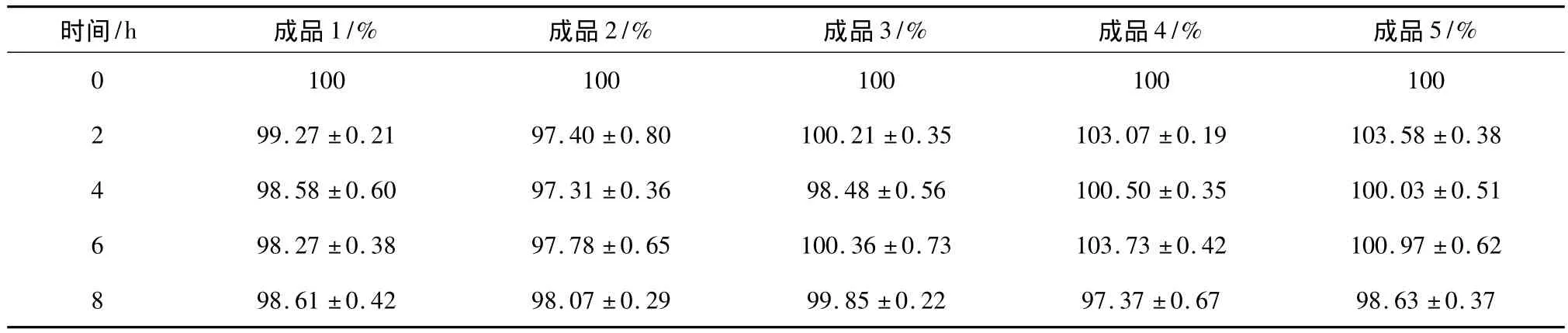
表4 各成品输液中五味子醇甲的相对含量变化(±s)
注:成品1~5分别为5%GS、10%GS、0.9%NS、GNS和SLR与生脉注射液调配的成品输液。
时间/h 成品1/% 成品2/% 成品3/% 成品4/% 成品5/%0 100 100 100 100 100 2 99.27 ±0.21 97.40 ±0.80 100.21 ±0.35 103.07 ±0.19 103.58 ±0.38 4 98.58 ±0.60 97.31 ±0.36 98.48 ±0.56 100.50 ±0.35 100.03 ±0.51 6 98.27 ±0.38 97.78 ±0.65 100.36 ±0.73 103.73 ±0.42 100.97 ±0.62 8 98.61 ±0.42 98.07 ±0.29 99.85 ±0.22 97.37 ±0.67 98.63 ±0.37
3 讨论
生脉注射液的性状为淡黄色澄明液体,用5种输液调配后的成品输液,在进行外观及pH检测时,无明显的变化。
静脉输液中微粒过多会造成局部血管堵塞,供血不足,产生静脉炎和水肿、肉牙肿、过敏反应、热源样反应等[6-7]。《中国药典》2010年版一部规定标示装量为100 mL或100 mL以上的静脉用注射液,除另有规定外,每1 mL中含10μm及10μm以上的微粒不得过25粒,含25μm及25μm以上的微粒不得过3粒[8]。本实验结果表明,用5%GS、10%GS、0.9%NS及GNS调配的成品输液在4 h内不溶性微粒数符合该标准。但与SLR调配的成品输液≥10μm不溶性微粒数超出该标准。各成品输液随着保存时间的延长,其不溶性微粒数增加,8 h后均超过《中国药典》2010年版一部之规定。导致不溶性微粒不合格的原因有很多,一方面可能是由于中成药成分复杂,一些成分如色素、鞣质、淀粉、蛋白质等以胶态形式存在于药液中,另一方面可能是因为药物与输液调配后发生氧化、聚合等反应[9],其次一些生物碱、皂苷在调配后由于pH值改变而析出,这些因素都可能导致不溶性微粒大大增加[10]。
由于HPLC具有高效、高灵敏度、速度快等优点,故本实验采用HPLC法测定生脉注射液中五味子醇甲的含量。本实验通过多次实验摸索流动相系统及比例,最终确定流动相为甲醇∶水(57∶43),此时的分离效果较好,出峰时间及峰面积值均较为理想。根据《药品注射剂使用指南》2005年版有关规定,在静脉注射液中大于10% 的有效成分被分解,则认为该药品与输液不宜配伍。五味子醇甲在5%GS、10%GS、0.9%NS、GNS 及 SLR 配伍液中 8 h含量下降均未超出10%。说明五味子醇甲在该五种输液中稳定。
此次实验数据说明,生脉注射液采用5%GS、10%GS、0.9%NS和GNS调配后成品输液的稳定性均较好,但建议临床调配后4 h内使用。
中药注射液是中药剂型现代化的产物,是我国中医药文化的组成部分,是现代中医药创新的成果,已经成为临床疾病治疗的独特手段,正在发挥着不可替代的作用。
中药注射剂在活血化淤、改善微循环方面起到了西药不可替代的作用,但是由于中药注射剂成分比较复杂,多为复方制剂,稳定性差[11],而有关应用基础研究薄弱,临床使用常出现不良反应[12]。且中药注射剂的成品输液缺乏统一的质量控制标准,对成品输液的性状、pH值、不溶微粒数、药品含量等没有规范要求,导致直接给患者使用的成品输液质量无法控制,给患者用药带来严重安全风险。我国应尽快制订更加严格的静脉用药成品输液的质量标准,临床上中药注射液调配后的成品输液,只有在通过标准后,方可用于患者[13]。
[1]池善留.144例新的药品不良反应报告分析[J].中国医院用药评价与分析,2014,14(11):1029-1032.
[2]郭锦辉,高卫芳,贾素洁.生脉注射液不良反应的Meta分析[J].中药药理与临床,2013,29(6):168-171.
[3]龙海燕,李文莉.HPLC法测定复方益肝灵胶囊中五味子醇甲含量[J].药物分析杂志,2010,30(2):282-284.
[4]黄文倩,李 丽,肖永庆,等.HPLC同时测定五味子中6种木脂素类成分[J].中国实验方剂学杂志,2011,17(10):63-66.
[5]范文成,常美玲,张国良,等.不同产地野生五味子的含量研究[J].中国药房,2011,22(3):248-250.
[6]吴秀荣,林焕泽,李 桃,等.5种中药注射液与输液配伍前后不溶性微粒变化[J].中国药业,2012,21(7):6-7.
[7]孙冲环,杨文清,陈玲玲.静脉注射液中药物配伍后不溶性微粒的考察[J].中国药业,2011,20(5):41-42.
[8]国家药典委员会.中国药典(二部)[S].北京:中国医药科技出版社,2010:附录71-73.
[9]沈文炯,侯建华.静脉输液中不溶性微粒的来源及预防对策[J].中国医药指南,2010,8(8):153-154.
[10]唐素芳.静脉注射剂中不溶性微粒的来源、危害及预防措施[J].天津药学,2008,20(5):65-68.
[11]徐 帆,梁晓方,苏 琍,等.注射剂配伍稳定性研究方法学分析与评价[J].中国医院药学杂志,2009,29(10):840-842.
[12]丁长玲,宿振国,张玉杰,等.316份中药注射剂不良反应报告分析[J].中国药房,2013,24(39):3718-3721.
[13]郭 青,吴晓燕,史清水,等.中药注射剂质量评价的有关研究思路、方法和建议[J].药物评价研究,2010,33(5):351-360.
