硫酸头孢喹肟乳房(干乳期)注入剂在奶牛乳汁中的残留消除研究
2015-04-27魏占勇刘欣魏丽娟耿智霞张樱宋婷婷贾兴连丽娟夏曦
魏占勇,刘欣,魏丽娟,耿智霞∗,张樱,宋婷婷,贾兴,连丽娟,夏曦
(1.河北远征药业有限公司,石家庄050041;2.中国农业大学,北京100083)
硫酸头孢喹肟乳房(干乳期)注入剂在奶牛乳汁中的残留消除研究
魏占勇1,刘欣1,魏丽娟1,耿智霞1∗,张樱1,宋婷婷1,贾兴1,连丽娟1,夏曦2
(1.河北远征药业有限公司,石家庄050041;2.中国农业大学,北京100083)
建立了牛奶中硫酸头孢喹肟残留超高效液相色谱-串联质谱检测方法(UPLC-MS/MS)。选取18头刚进入干乳期的健康奶牛,随机分为6个组,分别于预产期前的42、35、28、21、14和7 d进行乳房注入硫酸头孢喹肟乳房注入剂(3 g∶150 mg/支),只用药一次,产犊后采集奶样。结果表明:预产期前7 d给药,奶牛产犊72 h后采集的奶样中头孢喹肟残留量降至MRL(20 μg/kg)附近;预产期前14 d和21 d给药,奶牛产犊12 h后采集的奶样中头孢喹肟残留量降至MRL以下,均低于检测限;预产期前28、35和42 d给药,所有采集奶样的头孢喹肟残留量均低于检测限。建议在预产期前7、14和21 d给药硫酸头孢喹肟乳房注入剂的弃奶期分别为产犊后5、1和0 d。
头孢喹肟;牛奶;残留;超高效液相色谱-串联质谱法
头孢喹肟(Cefquinome)是目前第四代头孢菌素中唯一的动物专用药,具有抗菌谱广、抗菌活性强、动力学特点优良的特点,对革兰氏阳性菌和革兰氏阴性菌均显示良好的抗菌活性[1-3]。目前国内关于头孢喹肟乳房注入剂的研究越来越多[4-6],因此加强头孢喹肟在奶牛乳汁中的残留消除研究显得尤为重要。本试验在建立的奶牛乳汁中头孢喹肟的超高效液相色谱-串联质谱检测方法(UPLCMS/MS)的基础上,进行了奶牛给药硫酸头孢喹肟乳房(干乳期)注入剂后在乳汁中的残留消除研究,旨在为制定硫酸头孢喹肟乳房(干乳期)注入剂的休药期和临床合理使用提供理论依据。
1 材料与方法
1.1 材料
1.1.1 药品与试剂 头孢喹肟对照品:含量≥80.1%,批号K0320906,购自中国兽医药品监察所;硫酸头孢喹肟乳房(干乳期)注入剂(3 g∶150 mg/支),批号:111021,由河北远征药业有限公司提供;乙腈、甲醇、正己烷与甲酸均为色谱纯;氯化钠为分析纯。
1.1.2 仪器与设备 液相色谱-串联质谱仪(Micromass Quattro LC,配电喷雾离子源);分析天平(Sartorius CPA225D,赛多利斯科学仪器(北京)有限公司);天平(JJ500,常熟市双杰测试仪器厂);组织匀浆机(AM-2,日本Nissei公司);高速冷冻离心机(5804R,德国Eppendorf公司);涡旋混合器(HQ-60-II,北方同正生物技术发展有限公司);超声清洗仪(KQ2200型,昆山市超声仪器有限公司);固相萃取装置(美国Waters公司);氮吹仪(N-Evap 112,美国Organomation Associates公司);Oasis HLB固相萃取柱(美国Waters公司)。
1.1.3 主要溶液配制 精密称取头孢喹肟对照品约12.48 mg,于10 mL容量瓶中,用乙腈溶解并定容,配制成浓度为1 mg/mL的头孢喹肟标准贮备液。准确量取1 mg/mL头孢喹肟标准贮备液1 mL和0.1 mL,于10 mL容量瓶中,用乙腈稀释并定容,配制成浓度为100 μg/mL和10 μg/mL的标准工作液。
1.1.4 实验动物 18头刚进入干乳期的健康奶牛,由四川凉山州科华奶牛繁育有限公司奶牛场提供。给予正常饲料,自由饮水,饲料和饮水中不含头孢类等抗菌药物。
1.2 方法
1.2.1 给药及采样 将试验奶牛随机分为6个组(I、II、III、IV、V、VI组,每组3头),根据每头奶牛的配种记录计算预产期。I、II、III、IV、V、VI组每头奶牛的4个乳区分别在预产期前42、35、28、21、14、7 d进行给药,灌注硫酸头孢喹肟乳房(干乳期)注入剂,给药剂量为1支/乳区,仅给药一次。各试验奶牛在产犊后第0、12、24、36、48、60、72 h采集奶样,-20℃低温保存,备用。
1.2.2 样品前处理
1.2.2.1 提取 取解冻的空白或供试牛奶试料(5.00±0.02)g,于50 mL离心管中,加水8 mL、NaCl 3 g,涡动2 min,超声20 min,10000 r/min 0℃离心10 min。上清液转移至另一50 mL离心管中,加正己烷10 mL,涡动30 s,10000 r/min 0℃离心10 min。弃上层正己烷,下层水相备用。
1.2.2.2 净化 依次用甲醇2 mL和水2 mL活化Oasis HLB固相萃取柱,取备用液过柱,再用水2 mL淋洗,用甲醇-水溶液(60∶40,V/V)2 mL洗脱。洗脱液30℃水浴氮气吹至小于500 μL,加入含0.1%甲酸的水溶液定容至1 mL,涡动1 min复溶,14000 r/min离心10 min,过滤膜后供UPLC-MS/MS测定。
1.2.3 色谱条件
1.2.3.1 液相色谱条件 色谱柱:BEH C18(1.7 μm,50 mm×2.1 mm);流动相:A相为0.1%甲酸水溶液;B相为0.1%甲酸乙腈溶液;梯度洗脱:0、0.5、1.5、2.0、2.1、3.5 min时,B相分别为10%、10%、90%、90%、10%、10%;流速:0.3 mL/min;柱温:30℃;进样量:10 μL。
1.2.3.2 质谱条件 离子源:电喷雾离子源;扫描方式:正离子扫描;检测方式:多反应监测;电离电压:3.0 kV;源温:100℃;雾化温度:350℃;锥孔气流速:30 L/h;雾化气流速:600 L/h;测试药物定性、定量离子对及对应的锥孔电压、碰撞能量见表1。

表1 头孢喹肟的定性、定量离子及锥孔电压、碰撞能量
2 试验结果
2.1 方法学验证
2.1.1 线性范围 制备基质匹配标准曲线,浓度分别为0、50、250、500、2500、5000、10000、15000 μg/L,以测得特征离子峰面积为纵坐标,对应的标准溶液浓度为横坐标,绘制标准曲线,得回归方程为:y=25.027x+78.4327,相关系数r为0.9998,表明药物在50~15000 μg/L的浓度范围内,峰面积与浓度线性关系良好。
2.1.2 特异性 处理不同来源空白样品,目标化合物的保留时间附近没有杂质干扰,空白样品、空白牛奶添加样品、基质标准溶液的特征离子质量色谱图见图1-图3。

图1 空白牛奶样品特征离子质量色谱图
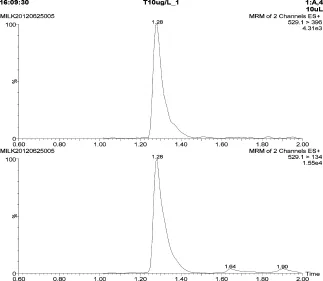
图2 空白牛奶添加样品特征离子质量色谱图(10 μg/kg)

图3 基质标准溶液特征离子质量色谱图(50 μg/L)
2.1.3 准确度和精密度 进行添加回收试验,选择1/2MRL(10 μg/kg)、MRL(20 μg/kg)、2MRL(40 μg/kg)三个浓度,各浓度制备6个平行样品,重复3批次。表2结果表明,药物在10、20、40 μg/kg添加浓度水平上的回收率为80%~110%之间,批内变异系数≤7.4%,批间变异系数≤6.3%。
2.1.4 灵敏度 添加适量标准工作液于5 g空白样品,经提取净化后测定。以3倍信噪比为方法的检测限,测得牛奶中头孢喹肟的检测限为2 μg/kg,以10倍信噪比为方法的定量限,测得牛奶中头孢喹肟的定量限为10 μg/kg。
2.2 试验牛产犊后乳汁中头孢喹肟的残留消除情况 由表3数据可看出,预产期前7 d给药(VI组),奶牛产犊后0 h采集奶样的头孢喹肟残留量最高,约为3000 μg/kg,产犊后12 h采集奶样的头孢喹肟残留量迅速降为257.6~627.8 μg/kg,之后消除趋于缓慢,产犊后72 h采集奶样的头孢喹肟残留量降至MRL(20 μg/kg)附近,浓度为17.1~31.3 μg/kg。预产期前14 d给药(V组),奶牛产犊后0 h采集奶样的头孢喹肟残留量为243.2~809.7 μg/kg,产犊后12 h采集奶样的头孢喹肟残留量迅速降至MRL以下,均低于检测限。预产期前21 d给药(IV组),奶牛产犊后0 h采集奶样的头孢喹肟残留量为37.3~83.1 μg/kg,产犊后12 h采集奶样的头孢喹肟残留量均低于检测限。预产期前28 d给药(III组),奶牛产犊后所有采集奶样的头孢喹肟残留量均低于检测限。

表2 牛奶中头孢喹肟添加回收试验结果

表3 单次使用(150 mg/乳区)硫酸头孢喹肟乳房(干乳期)注入剂奶牛产犊后各时间点采集奶样的头孢喹肟残留量检测结果
2.3 休药期计算 根据上述试验所得的残留消除数据,根据我国牛奶中头孢喹肟MRL(20 μg/kg)规定和欧盟关于休药期计算的要求,以双单侧95%置信区间计算,按推荐用法和用量[干乳期乳房内注入,1支(150 mg)/乳区,只用药一次]给奶牛使用硫酸头孢喹肟乳房(干乳期)注入剂,在预产期7 d前给药,建议弃奶期为产犊后5 d;在奶牛预产期14 d前给药,建议弃奶期为产犊后1 d;在奶牛预产期21 d前给药,建议弃奶期为产犊后1 d;在奶牛预产期28 d前给药,产犊后分泌乳汁已检测不到头孢喹肟残留,建议弃奶期为产犊后0 d。
3 讨论
目前,检测头孢喹肟在可食性组织和牛奶中的残留方法主要有微生物法[7]、酶联免疫法[8]、HPLC法[9-11]以及HPLC-MS/MS[12-13],其中以HPLC法和HPLC-MS/MS应用最多。本试验采用HPLCMS/MS方法检测牛奶乳汁中头孢喹肟残留,专属性好,峰形良好,灵敏度高,测定牛奶中头孢喹肟的检测限为2 μg/kg,定量限为10 μg/kg,欧盟制定头孢喹肟在牛奶中的最大残留量(MRLs)为20 μg/kg,因此能够满足头孢喹肟在乳中残留检测的要求。
国内外关于头孢喹肟的残留研究结果均表明按合理的给药方案,经过休药期后,各种组织器官的残留量均低于规定的限度[14]。头孢喹肟在动物可食性组织和乳中残留消除速度较快[14]。乳房灌注头孢喹肟后在泌乳牛中的残留消除研究结果显示[9],仅能在治疗后24 h的肾脏检出头孢喹肟,且含量低于200 μg/kg,而在用药后第一次的挤奶中残留最高,在第10次泌乳期后,所有批次的牛奶样品的残留浓度均低于20 μg/kg。Ehinger等[4]研究了奶牛干乳期应用头孢喹肟后在可食性组织和乳汁中残留,药物未进入体循环,产后乳汁和所有可食性组织中头孢喹肟的残留浓度均低于最大残留限量。从本实验的结果来看,在干乳期给药硫酸头孢喹肟乳房注入剂后,药物在奶牛乳汁中代谢较快,硫酸头孢喹肟残留量可很快降至MRL(20 μg/kg)以下。
[1] CVMP(Committee for Veterinary Medicial Products).Cefquinome Summary Report[R].London:European Agency for the Evaluation of Medicinal Products,1995.
[2] CVMP(Committee for Veterinary Medical Products).Cefquinome Summary Report-1[R].London:European Agency for the Evaluation of Medicinal Products,1999.
[3] CVMP(Committee for Veterinary Medical Products).Cefquinome Summary Report-2[R].London:European Agency for the Evaluation of Medicinal Products,2003.
[4] Ehinger A M,Allan M J,Hartmann M,et al.Deletion of residues in edible tissues and milk following treatment with a new cefquinome dry cow formulation[R].Quebec:Intervet Innovation GmbH,2004.
[5] 魏占勇,刘欣,魏丽娟,等.硫酸头孢喹肟乳房注入剂在牛奶中的药代动力学研究[J].中国兽药杂志,2014,48(12):22-26.
[6] 闫星,刘义明,路永强,等.硫酸头孢喹肟乳房注入剂对泌乳期奶牛的安全性研究[J].中国畜牧兽医,2014,41(11):278-282.
[7] Errecalde C A,Clin MV E C,Prieto G F,et al.Cefquinome pharmacokinetics in calves by intramuscular administration[J].Rev Col Pec Vol,2002,15(3):281-285.
[8] Zhang X1,Li J,Jiang H,et al.Residue depletion of cefquinome in swine tissues after intramuscular administration[J].J Agric Food Chem,2007,55(25):10493-10498.
[9] 高金兴.头孢喹肟在牛奶中残留的HPLC检测及消除规律研究[D].扬州:扬州大学,2009.
[10]徐向明,杨海峰,金礼琴,等.头孢喹肟注射液在猪组织中的残留消除研究[J].江苏农业科学,2008,(6):193-195.
[11]刘利锋,覃少华,赵杰,等.猪组织中硫酸头孢喹肟含量测定和肌注给药残留研究[J].甘肃农业大学学报,2008,43(2):1-7.
[12]王林,束建花,赵宁,等.牛奶和牛血浆中头孢喹肟HPLCMS/MS检测方法的建立[J].畜牧与兽医,2012,44(11):55-59.
[13]严凤,李丹妮,顾欣,等.超高效液相色谱-串联质谱检测动物源性食品中头孢喹肟残留[J].中国兽药杂志,2012,46(7):23-25.
[14]王付民,陈杖榴.头孢喹肟的研究进展[J].动物医学进展,2004,25(4):50-53.
(编辑:李文平)
Residual Study of Cefquinome Sulfate Intramammary Infusion(Dry Period)in Milk
WEI Zhan-yong1,LIU Xin1,WEI Li-juan1,GENG Zhi-xia1∗,ZHANG Ying1,SONG Ting-ting1,JIA Xing1,LIAN Li-juan1,XIA Xi2
((1.HeBei Yuanzheng Pharmaceutical Co.,Ltd.Shijiazhuang 050041,China;2.China Agriculturial University,Beijing 100083,China)
The high performance liquid chromatography and tandem mass spectrometry method(UPLC-MS/MS)was established for the residual study of cefquinome sulfate in milk.18 healthy cows that just entering the dry period were selected and were randomly divided into 6 groups.The 6 groups of cow were respectably administrated cefquinome sulfate intramammary infusion(dry period)once in mammary region at the dose of 3 g for each region and their milk were collected after calving.The results demonstrated that:administrated 7 days before preterm birth,concentration of cefquinome in milk collected 72h after calving decreased to about MRL;administrated 14 and 21 days before preterm birth,concentration of cefquinome in milk collected 12h after calving dropped below MRL,all below the detection limit;administrated 28、35 and 42 days before preterm birth,concentration of cefquinome in all the milk were below the detection limit.It is suggested that the milk withholding period were respectably 5,1 and 0 days that administrated cefquinome sulfate intramammary infusion7,14 and 21 days before preterm birth.
cefquinome;milk;residue;UPLC-MS/MS
2015-02-05
A
1002-1280(2015)05-0049-05
S859.84
魏占勇,高级工程师,从事药物制剂研究方面的研究。
耿智霞。E-mail:gengzhixia2011@aliyun.com
