正十二醇与β-环糊精包合物的制备研究
2014-10-15薛小连刘金龙马瑞燕刘红霞聂艳丽
薛小连,刘金龙,马瑞燕,刘红霞,聂艳丽
(1.山西农业大学文理学院 化学生态研究所,山西 太谷030801;2.山西农业大学农学院,山西 太谷030801)
正十二醇是一种重要化工原料,用于制备高效洗涤剂、表面活性剂、乳化剂、杀菌剂、植物生长调节剂以及其它一些特种化学品[1-4],也是梨小食心虫性信息素的组分之一。梨小食心虫(Grapholita molesta)是一种世界性主要蛀果害虫[5-7]。随着绿色农业的普遍实施及害虫可持续控制策略的推广,利用昆虫性信息素对有害昆虫进行管理,是保护环境、有效控制害虫的可行途径之一,逐渐成为害虫种群动态监测和防治的主要手段[8]。但是,昆虫性信息素在田间应用过程中存在溶解性差、易挥发等问题亟待解决。由于正十二醇是性信息素的成分之一,具有不溶于水的特性,限制了性信息素的使用。因此,将正十二醇与β-环糊精(β-CD)制成包合物,以改变正十二醇的性质,增大其在水溶液中的溶解度、减缓释放速度,进而提高正十二醇在梨小食心虫性信息素中的利用率,促进缓释型性诱剂的研制,推动昆虫性信息素的田间应用。作者在此采用饱和溶液电动搅拌法和超声法制备正十二醇与β-CD的包合物,对两种方法进行比较,并初步探讨了包合物的形成机理。
1 实验
1.1 试剂与仪器
β-CD,天津光复精细化工研究所;正十二醇,上海恒彬生物科技有限公司;95%乙醇;无水乙醇(分析纯);KBr,天津光复科技发展有限公司;二次重蒸水。
IR200型傅立叶变换红外光谱仪,美国赛默飞;电子天平,北京赛多利斯仪器有限公司;循环水式多用真空泵,北京神泰伟业仪器公司;SK5200H型超声波清洗器(53kHz),上海科导超声仪器有限公司;磁力加热搅拌器,常州国华电器有限公司;鼓风干燥箱,山东龙口先科仪器公司。
1.2 包合方法
据文献报道[9-11],客体分子与β-CD的包合比例在1∶(6~9)(mL∶g)之间时,包合物得率较高。原料不同时适宜的比例也有差异。通过预实验筛选,本实验采用正十二醇乙醇溶液(浓度0.1g·mL-1)与β-CD以1.5∶8(mL∶g)的比例进行包合。
1.2.1 饱和溶液电动搅拌法
1.2.1.1 溶液的配制
β-CD饱和溶液的配制:准确称取8gβ-CD,加入100mL二次重蒸水,在65℃下配制成β-CD饱和溶液。
正十二醇乙醇溶液的配制:准确称取1g固体正十二醇,溶解于10mL 95%乙醇中,配制成浓度为0.1 g·mL-1的正十二醇乙醇溶液。
1.2.1.2 步骤
在250mL烧瓶中加入β-CD饱和溶液,逐渐升温,缓慢加入1.5mL浓度为0.1g·mL-1的正十二醇乙醇溶液,电动搅拌至均匀。当温度上升到40℃时,保持此温度,搅拌反应2h,得到正十二醇与β-CD的混合液。将混合液在4℃冰箱中放置24h,观察发现形成黏稠物后迅速用真空泵抽滤,并用无水乙醇反复洗涤3次,得到正十二醇与β-CD包合物的白色晶体。40℃充分干燥后得到粉末状的包合物,置于干燥器中备用。依下式计算包合物得率:

1.2.2 超声法
准确称取8gβ-CD溶于100mL沸水中,将溶液转移到250mL的烧瓶中,缓慢加入1.5mL浓度为0.1g·mL-1的正十二醇乙醇溶液,控制温度为40℃,在超声波清洗器中超声反应2h,得到正十二醇与β-CD的混合液。后续处理同1.2.1.2,计算包合物得率。
2 结果与讨论
2.1 包合条件的选择
(1)文献报道[11-12],β-CD 在水中的溶解度随温度的升高而增大,常温下,其在水中的溶解度较小。因此,包合温度不宜过高或过低,温度过高,包合物可能分解;温度过低,包合不完全。40℃时,β-CD在水中的溶解度比室温大,且与正十二醇的接触面较大,故选择包合温度为40℃。
(2)包合时间太短,包合不充分;时间太长,影响实验进程。实验选择包合时间为1.5h左右。
(3)包合物的干燥温度也不宜过高。因为温度越高,包合物的稳定性越低。实验选择包合物的干燥温度为40℃且包合物需要贮存于干燥的环境中,不宜接触高温。
2.2 红外光谱鉴定
分别取一定量的β-CD、正十二醇、正十二醇与β-CD的包合物、正十二醇与β-CD的物理混合物制成KBr压片,进行红外光谱检测,结果见图1。
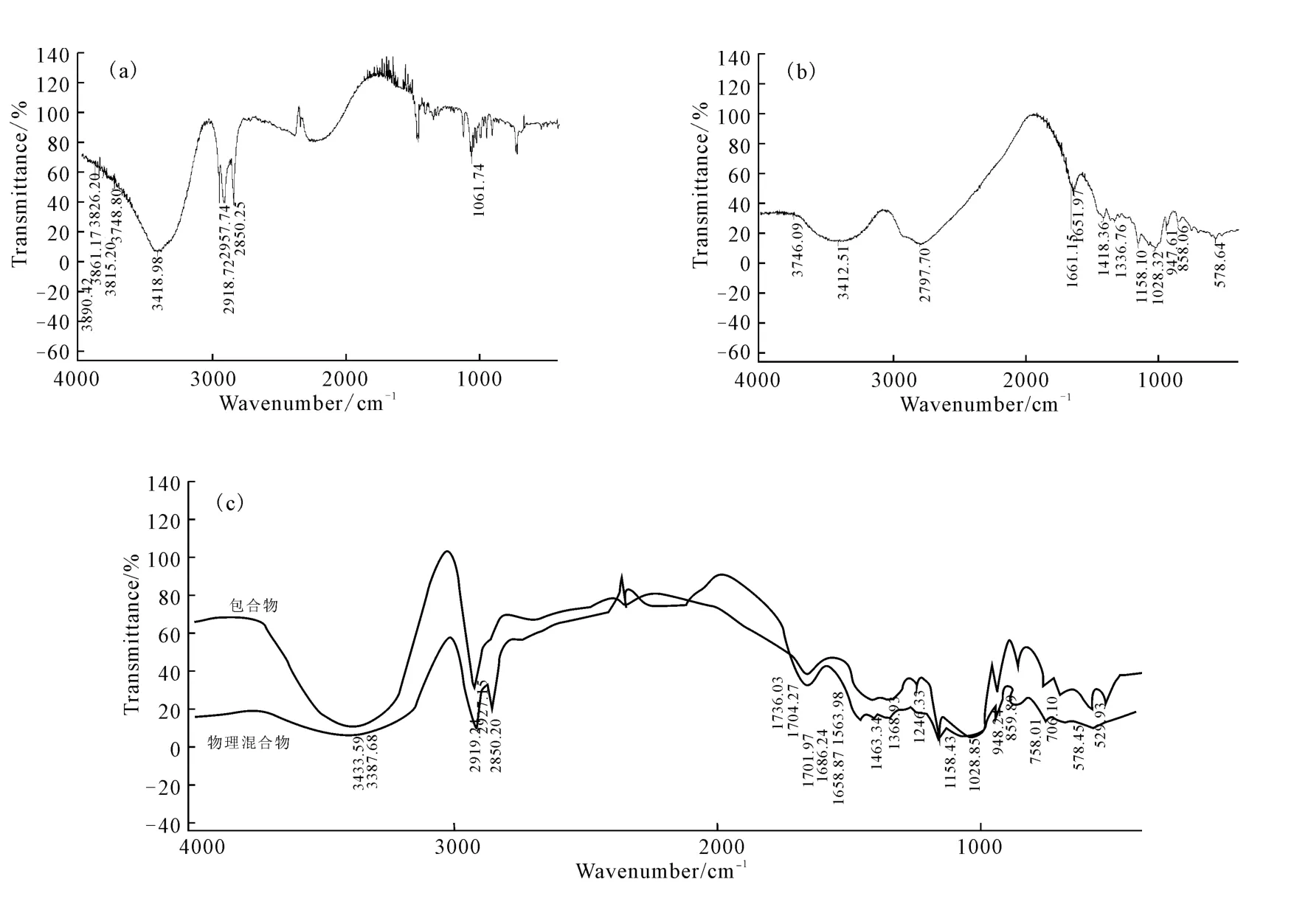
图1 正十二醇(a)、β-CD(b)、正十二醇与β-CD的包合物及物理混合物(c)的红外光谱Fig.1 The IR spectra of dodecanol(a),β-cyclodextrin(b),inclusion compound and physical mixture ofβ-cyclodextrin with dodecanol(c)
由图1可知:正十二醇与β-CD的物理混合物和包合物相比,正十二醇的特征峰(羟基官能团)发生了改变,物理混合物的正十二醇伸缩振动吸收峰位于3 433.59cm-1处,而包合物的相应峰向低波数方向移动到了3 387.68cm-1处;包合物中,羟基吸收峰的峰形比物理混合物的窄;物理混合物的长碳链中C—H伸缩振动吸收峰位于2 919.24cm-1和2 850.20cm-1处,而包合物的相应峰移到了2 927.15cm-1处,且2 850.20cm-1处的吸收峰明显变弱,说明正十二醇受到了β-CD的影响。综上,推断正十二醇与β-CD形成了包合物。
2.3 两种包合方法的比较(表1 )

表1 两种制备正十二醇与β-CD包合物方法的比较Tab.1 The comparison of two preparation methods of inclusion compound ofβ-cyclodextrin with dodecanol
从表1 可以看出,超声法包合物得率较高。原因可能是:超声振荡时,功率非常大,液体内部会因剧烈振动产生小空洞,这些小空洞迅速胀大和闭合,促使液体微粒之间发生猛烈的撞击作用,液体温度骤然升高,从而使正十二醇与β-CD(两种不相溶的液体)更有效地发生相互作用,加速化学反应,有利于包合物的形成。
2.3 包合物包合机理的初步探讨
β-CD是由6、7、8个β-D-吡喃葡萄糖单元以β-1,4糖苷键首尾相连而成的环状化合物,成锥形圆筒状,其中伯羟基和仲羟基分别位于环糊精的较小和较大的开口端,致使其外侧为亲水性,内侧为C-3、C-5氢原子和糖苷氧原子组成的空腔,因此其内侧具有疏水性[13-15]。β-CD特有的外亲水、内疏水的性质,使其可与许多有机分子、无机离子、药物及生物小分子等客体结合形成包合物[16-20]。
依据正十二醇和β-CD的结构、体积匹配、亲水性原则等,推测二者可以形成包合物,这由红外光谱分析得到了证实。红外光谱中,正十二醇与β-CD形成包合物之后,与正十二醇和β-CD的物理混合物相比较,包合物的羟基特征峰的峰形变窄、羟基特性明显增强。推测其原因,包合前多个游离的正十二醇分子的长碳链相互交错,分子间缔合作用较弱,故物理混合物的羟基特性较弱、特征峰峰形较宽。但在搅拌、超声振荡以及温度等条件的影响下,正十二醇在包入β-CD的空腔中时重新进行了排列,从而使多个正十二醇的羟基有序裸露在β-CD的空腔外侧,这样有利于正十二醇与β-CD的羟基进行分子间缔合,形成以氢键相连的多聚体,使包合物的羟基吸收峰向低波数(3 387.68 cm-1)方向移动,峰形变窄。
结合红外光谱和实验结果推测正十二醇和β-CD包合物的形成机理如图2所示。
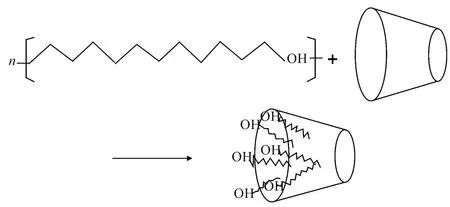
图2 正十二醇和β-CD包合物的形成机理Fig.2 The formation mechanism of inclusion compound ofβ-cyclodextrin with dodecanol
3 结论
采用饱和溶液电动搅拌法和超声法制备了正十二醇与β-环糊精的包合物。傅立叶红外光谱分析表明β-环糊精可与正十二醇形成包合物;比较发现,超声法包合物得率较高,可达86.22%。该实验结果可为多碳伯醇[21]、昆虫性信息素的包合提供参考。
[1]崔益顺,赵勇.十二醇改性沉淀白炭黑工艺研究[J].四川理工学院学报(自然科学版),2011,24(2):228-230.
[2]田勇,胡永玲,穆传义,等.十二醇取代制正十二碳硫醇[J].化学工程师,2010,(4):62-64.
[3]吕波,王亚明,贾庆明,等.正十二醇表面改性沉淀二氧化硅[J].无机盐工业,2011,43(7):32-35.
[4]余飞,陈中华,曾幸荣,等.正十二醇相变储热微胶囊的制备与表征[J].高分子材料科学与工程,2009,25(6):135-138.
[5]陈梅香,骆有庆,赵春江,等.梨小食心虫研究进展[J].北方园艺,2009,(8):144-147.
[6]冯明祥,姜瑞德,王佩圣,等.桃园梨小食心虫发生规律研究[J].中国果树,2002,(4):30-31.
[7]文丽华,刘海青.梨小食心虫测报及防治研究[J].天津农林科技,2001,(5):1-3.
[8]翟小伟,刘万学,张桂芬,等.苹果蠹蛾性信息素的研究和应用进展[J].昆虫学报,2009,52(8):907-916.
[9]毛春芹,谢辉,狄留庆.片姜黄挥发油β-环糊精包合物的制备研究[J].中成药,2002,24(8):581-583.
[10]周长新,邹建凯,赵昱.β-环糊精包合技术在当归精油新剂型研究中的应用[J].中国中药杂志,2002,27(11):832-834.
[11]刘书堂,郑国和,闫亚强.β-环糊精挥发油粉末化技术在中药制剂中的研究与应用[J].中草药,1997,28(12):749-751.
[12]姜佳峰,刘宗成,郝广启.β-环糊精包结当归饮片中挥发油的实验研究[J].山东医药工业,2002,21(3):6-7.
[13]宋乐新,孟庆金,游效曾.环糊精和环糊精包合物[J].无机化学学报,1997,13(4):368-374.
[14]江云宝,黄贤智,陈国珍.荧光光谱法测定环糊精包络物的形成常数[J].化学通报,1990,(9):46-49,60.
[15]张力田.环状糊精(续)[J].淀粉与淀粉糖,1990,(4):1-9.
[16]屠一锋.3,3′,5,5′-四甲基联苯胺-β-环糊精包合物的紫外可见光谱和电化学研究[J].光谱学与光谱分析,2000,20(5):736-738.
[17]王中慧,潘景浩.用电化学分析法研究碱性染料与β-环糊精的包结作用[J].分析化学,2004,32(7):889-892.
[18]KNAPP M,KOHLER G.Supra molecular inclusion complexes between a coumarin dye and beta-cyclodextrin,and attachment kinetics of thiolated beta-cyclodextrin to gold surface[J].Journal of Molecular Structure,2001,598(1):49-56.
[19]路平,刘彬,吴峰,等.β-环糊精与甲基橙包合物的形成及其光催化脱色[J].应用化学,2003,20(2):108-110.
[20]古俊,常雁,潘景浩.环糊精的实际应用进展[J].应用化学,1996,13(4):5-9.
[21]童林荟,王仁礼.环糊精与乙烯和三十烷醇包结物的研究[J].有机化学,1984,(1):29-32.
