猕猴桃根提取物体外抗氧化作用的研究
2012-12-02杨艳杰何弘水
杨艳杰,何弘水
(漯河医学高等专科学校,河南 漯河 462002)
氧在生物体内通过单电子还原产生化学性质活泼的物质称为活性氧,包括超氧阴离子自由基(·O2-)、过氧化氢(H2O2)、羟基自由基(·OH)等[1]。活性氧的半衰期很短,但它们可以与多元不饱和脂肪酸作用,造成脂质过氧化。脂质过氧化是造成生物体氧化损伤的主要原因。不饱和脂肪酸是生物膜的基本组成成分,极易被活性氧氧化损伤,造成生物膜结构和功能的破坏,从而诱发多种慢性疾病[2]。因此,消除自由基、抑制脂质过氧化已成为生命科学领域的一项重要课题。本实验从清除DPPH自由基、清除·O2-、清除H2O2,抑制·OH、还原力等方面比较猕猴桃根提取物的抗氧化效果,为猕猴桃根生物活性成分的综合开发利用提供科学依据。
1 材料
1.1 仪器
HP8453紫外可见分光光度计:美国惠普;pH25-S型酸度计:北京华瑞博远科技公司;800型离心沉淀器:河南斯泰仪器有限公司。
1.2 试剂
还原性辅酶Ⅰ(NADH),二甲基酚嗪硫酸盐(PMS),氮四唑蓝(NBT),二苯基苦基苯(DPPH),菲洛嗪,氯化亚铁,氯化铁,亚铁氰化钾(K4[Fe(CN)6]),邻菲咯啉,过氧化氢,三氯乙酸(CCl3COOH),钼酸铵[(NH4)2MoO4],硫代硫酸钠(NaS2O3),碘化钾,淀粉,VC,硫脲,乙酸乙酯,无水乙醇。试剂均为分析纯,实验用水为重蒸馏水(ddH2O)。
2 方法与结果
2.1 样品(猕猴桃根提取液)制备
猕猴桃根10 kg切碎,80℃以下烘干至水分小于10%,粉碎小于20目,用乙醇(65%)45℃以下回流提取3次,提取液于50℃减压浓缩,得约300 g深黄色流浸膏,然后取200 g膏状物,加入适量蒸馏水,搅成糊状混合液,依次用乙酸乙酯萃取3次(每次500 mL),合并提取液,减压回收溶剂得猕猴桃根提取固体,用65%乙醇精确配制成浓度分别为 5.0、10.0、20.0、40.0、60.0、80.0、100.0、200.0、400.0、600.0、800.0μg/mL 和 1.0、2.0、3.0、4.0、5.0 mg/mL 的样品(ERHM)溶液。
2.2 ERHM对DPPH自由基的消除作用
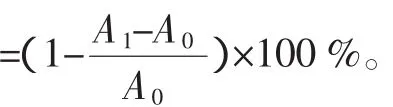
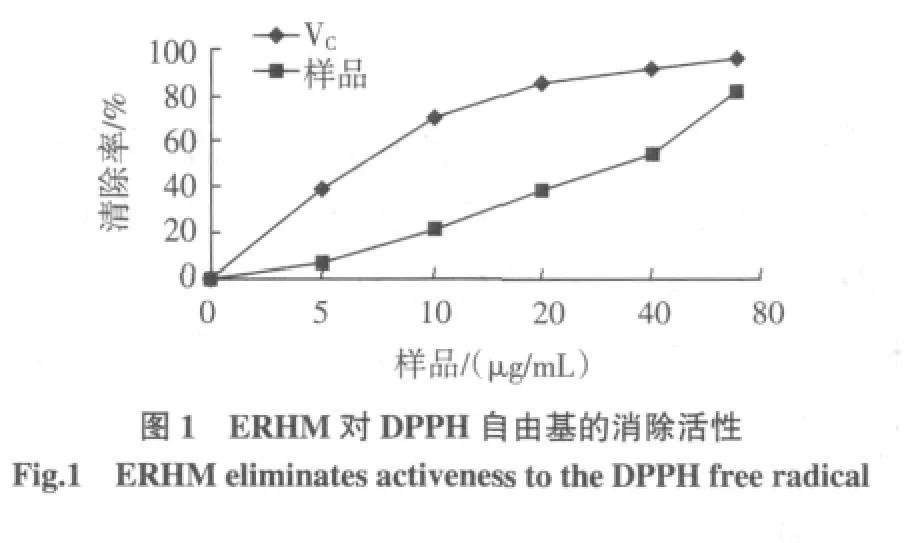
同时计算清除DPPH的半数有效浓度EC50。用VC作对照,进行平行实验。ERHM对DPPH有较强的清除作用,且呈现浓度依赖性。VC的EC50为7.2μg/mL,ERHM 的 EC50为 8.03μg/mL。
2.3 ERHM对超氧阴离子(·O2-)的清除作用
参考Liu等[4]的方法检测ERHM对超氧阴离子的清除能力。取不同浓度的ERHM溶液0.3mL分别加入由120μmol/L的PMS、936μmol/L的NADH、300μmol/L的NTB溶液(均用0.1 mol/L的pH=7.4的磷酸盐缓冲溶液配制)各0.75 mL所建立的反应体系中,混匀,室温静置反应10 min,于560 nm处测定吸光度值A0;以65%乙醇代替ERHM,560 nm处测定A0;以磷酸盐缓冲溶液代替PMS溶液,在560 nm处测定A2;65%乙醇调零。均平行测定3次。对超氧阴离子清除率和EC50的计算方法同前。ERHM对超氧阴离子具有较强的清除作用,在 1.0、2.0、3.0、4.0、5.0 mg/mL 时,清除率分别是 35.57%、48.65%、66.74%、72.11%、76.18%,EC50为1.28 mg/mL。
2.4 ERHM对羟基自由基(·OH)的抑制能力
参考Fenton反应体系[5]检测ERHM抑制羟基自由基(·OH)的能力。反应体系组成:60μL 1.0 mmol/L Fe2+溶液,90μL 1.0 mmol/L 邻菲咯啉溶液,150μL 0.12%H2O2溶液,2.4 mL pH=7.8的磷酸盐缓冲溶液,分别加入不同浓度的ERHM溶液300μL,混匀,室温反应20 min,510 nm处测定A1;65%乙醇代替抗氧化剂,测定A0;pH=7.8的磷酸盐缓冲溶液代替邻二氮菲,测定A2,65%乙醇调零。均平行测定3次。清除率及EC50计算方法同前。结果见图2。
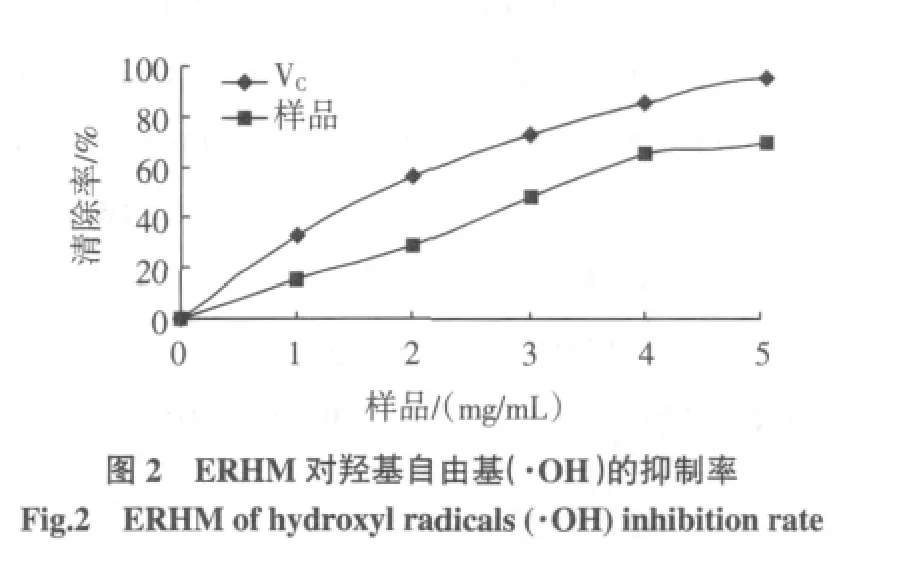
在0~4 mg/mL,ERHM抑制羟基自由基的能力呈现浓度依赖性。ERHM浓度达5.0 mg/mL时,抑制羟基自由基(·OH)能力可达69.4%,其EC50为1.57 mg/mL。
2.5 还原力比较
参考Oyaizu方法[6]依次加入0.75 mL磷酸盐缓冲溶液(pH=6.6)、0.75 mL 1%的 K4[Fe(CN)6]、0.75 mL 不同浓度的ERHM溶液,混匀,50℃水浴30 min,冰水浴冷却,加入0.75 mL 1%CCl3COOH,4℃下离心10 min(3000 r/min)。取上清液1.5 mL,加入 ddH2O 1.5 mL、1%FeCl30.75 mL,混匀,室温静置 10 min,700 nm 处测定A1;以ddH2O代替ERHM溶液,测定A0;ddH2O调零。均平行测定3次。以110 mg/mL VC在700 nm处的A为标准,按下式计算相对还原力:RP=×100%,结果见图3。
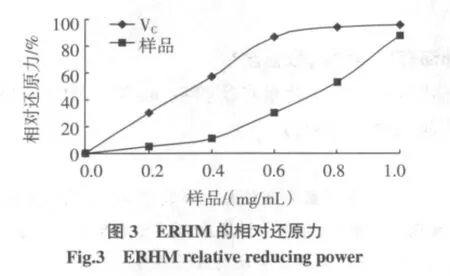
同时计算ERHM还原力的EC50。ERHM还原力较强,其EC50为0.28 mg/mL,约是VC(EC50为0.08 mg/mL)的3.5倍。
2.6 ERHM对H2O2的消除能力
H2O2是强氧化剂,且易透过细胞膜,并引起氧化损伤。本实验采用置换滴定法检测H2O2浓度。取不同浓度的ERHM溶液各1.0 mL分别与1.0 mL 0.1 mol/mL H2O2混合,加入 2 滴 3%的(NH4)2MoO4、2 mol/L H2SO410 mL、1.8 mol/L KI 7.0 mL,用 0.005 mol/L NaS2O3滴定,待体系变黄,加入1 mL淀粉溶液,继续滴定到无色即为终点。滴定样品试剂的体积为V1,滴定H2O2所用体积为V0。平行滴定3次。计算清除率100%。结果见图4。

结果显示样品ERHM对过氧化氢具有一定的消除作用,在浓度为100μg/mL时对过氧化氢的清除率为42%,比VC要小(同样条件下VC清除率为91%)。
3 讨论
本实验结果表明,ERHM具有较强的还原力,这与较强抑制羟基自由基的产生及消除过氧化氢有关,同时也具有消除DPPH和超氧阴离子等活性氧的能力。实验结果证明了ERHM的多方面抗氧化活性,且随其浓度增加而增大。所以,ERHM有效成分具有较为显著的抗氧化作用。
现代研究已经证实,在生命活动的氧化代谢过程中会不断产生各种自由基,其中超氧阴离子、过氧化氢、羟基自由基等引起的细胞损伤过程是微粒体脂质过氧化和多不饱和脂肪酸(PUFA)氧化变性的主要原因[2]。当PUFA遭受到氧化损伤时细胞即失去完整性,破坏了镶嵌于膜系统上的许多酶的空间构型,使得酶的空隙扩大、通透性增加,出现退行性变化,从而使内质网膜、线粒体膜、溶酶体膜等生物膜系统的镶嵌状态发生变化,导致广泛损伤和病变。自由基一般都不稳定,寿命很短,检测自由基的清除能力是评价抗氧化物质抗氧化活性的重要方法。还原力反映了一种物质作为电子供体的能力,药物还原力和捕获过氧化氢能力的大小在一定程度上反映了其预防性抗氧化功能的强弱。
[1]杨宏杰,陈咸川,郑敏,等.黄芪和丹参清除自由基能力的研究[J].复旦学报:自然科学版,2003(6):935-938
[2]崔剑,李兆陇,洪啸吟,等.自由基生物抗氧化与疾病[J].清华大学学报:自然科学版,2000(6):9-12
[3]Amarow icz R,N aczk M.Shahidi F1Antioxidant activity of various fractions of non-tanin pheno lics of cano lahulls[J].J A gric Food Chem,2000,48:2755-2759
[4]Liu F,OoiV E C,Chang S T.Free radicals scavenging activity of mush room polysaccharide extracts[J].Life Sci,1997,60:763-771
[5]Yu W L,Zhao Y P,Shu B.The radical scavenging activitiesof Radix Puerariae isoflavonoids:A chem ilum inescencestudy[J].Food Chem,2004,86:525-529
[6]Oyaizu M.Studies on products of browning reactions:antioxidant activities of products of browning reaction prepared fromglucose amine[J].J P J Nutr,1986,44:307-315
