卡培他滨治疗化疗失败的非小细胞肺癌对照研究
2012-05-30蔺强刘月娥王娜任小沧陈雪霁田艳生胡靖郭志军赵彦南
蔺强 刘月娥 王娜 任小沧 陈雪霁 田艳生 胡靖 郭志军 赵彦南
河北医科大学附属华北石油管理局总医院肿瘤科,河北 任丘 062552
2008年,肺癌的发病率和死亡率均居所有癌症的首位,当年新发病例160万,死亡140万[1]。非小细胞肺癌(non-small cell lung cancer,NSCLC)约占全部肺癌的80%,其中大部分患者在临床确诊时已是晚期无法手术根治切除[2]。对于晚期患者标准的一线化疗方案为含铂类的两药联合化疗,大部分患者在一线化疗后往往因出现复发或转移而需接受二线化疗。美国国家综合癌症网(the National Comprehensive Cancer Network,NCCN)指南推荐:NSCLC标准二线化疗方案包括单药多西他赛、单药培美曲赛[3],其中多西他赛是第一个被证实在二线治疗中优于最佳支持治疗的化疗药,因而应用也更加广泛和成熟。但是多西他赛对于NSCLC的二线治疗效果不能令人满意,总有效率(response rate,RR)为14%~25%,中位生存期(median survival time,MST)为6.1~9.5个月,1年总生存率仅为23%~44%[4]。因此探索两药联合化疗方案治疗NSCLC具有重要临床意义。卡培他滨是氟尿嘧啶类的前体药物,国外有基础和临床研究均证实对NSCLC有效[5-7],而国内有应用此方案二线化疗8例NSLCC的单组报道[8]。本研究旨在评价卡培他滨联合多西他赛的两药方案治疗化疗失败的NSCLC的初步疗效,并观察其不良反应。
1 资料和方法
1.1 病例选择
1.1.1 入组标准
病理学或细胞学证实为NSCLC的复治患者,至少接受过一个含铂类的双药化疗方案后进展,至少有一处可评价病灶,临床分期ⅢB~Ⅳ期、距离上次化疗21 d以上,年龄18~75岁,KPS评分≥60。WBC≥4.0×109/L,PLT≥100×109/L,HGB≥100 g/L,肝、肾功能正常,预计生存期≥3个月。无第二原发恶性肿瘤(皮肤和宫颈原位癌已治愈5年以上者除外)。无其他疾病需住院治疗者。签署知情同意书。排除妊娠或哺乳女性、临床有症状的中枢神经系统转移、曾经应用紫杉类化疗方案的患者。
1.1.2 病例资料
选择2009年7月—2011年6月化疗失败的NSCLC住院患者48例,应用随机数字表,分为卡培他滨加多西他赛组(联合组)和单药多西他赛组(单药组)。联合组23例:男性14例,女性9例,年龄48~73岁,中位年龄65岁,ⅢB期13例,Ⅳ期10例,腺癌15例,鳞癌8例;单药组25例:男性15例,女性10例,年龄50~71岁,中位年龄62岁,ⅢB期12例,Ⅳ期13例,腺癌20例,鳞癌5例。两组一般临床资料差异无统计学意义(P>0.05)。
1.2 治疗方法
1.21 方案选择
移植瘤的动物模型研究表明多西他赛能够提高胸苷磷酸化酶(thymidine phosphorylase,TP)活性,并且和卡培他滨有协同作用[5]。已有Ⅱ期研究证实了卡培他滨联合多西他赛的初步疗效和安全性[6-7]。本研究采用了韩国研究的推荐剂量[7]。临床前研究提示多西他赛提高TP活性的作用在用药后第6~10天最强,并得到临床证实,因此本研究调整了韩国方案中的给药时间,即卡培他滨自治疗开始第5天开始口服[5]。已证实每周多西他赛给药在获得相同疗效的同时能够明显降低粒细胞减少的风险[9],因此研究中多西他赛采用了来自台湾地区的每周给药方案,即第1、8天给药[10]。
1.2.2 化疗方案
联合组:卡培他滨625 mg/m2,每天2次,第5~18天;多西他赛30 mg/m2,第1、8天;预防性抗过敏治疗,地塞米松8 mg,每天2次,治疗开始前1天给药,治疗开始后第1、2天,连用3 d,每21 d重复,1~6个周期。单药组:多西他赛35 mg/m2,第1、8天;预防性抗过敏治疗,地塞米松8 mg,每天2次,治疗开始前1天给药,治疗开始后第1、2天,连用3 d,每21 d重复,1~6个周期。
1.2.3 支持治疗
为保证化疗的连续性,适当给予升白细胞、升血小板、纠正贫血、止吐、静脉补液等支持治疗。
1.3 评价标准
治疗前1周内完成病史、体检、KPS评分、血常规、肝功能、肾功能检查、胸部CT和腹部CT或腹部B超、心电图。
应用NCI/NIH不良事件评价标准CTC AE 3.0评价不良反应。化疗2个周期后应用RECIST1.1评价客观疗效。疗效分为:完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)和进展(progression disease,PD)[11]。有效率(response rate,RR)=CR+PR,疾病控制率(disease control rate,DCR)=CR+PR+SD。
1.4 研究终点
主要研究终点为至肿瘤进展时间(time to progression,TTP),次要研究终点为总生存期(overall survival,OS)、RR和DCR。
1.5 随访
全部病例采取门诊复查随访和电话随访,截止到2011年9月31日,无失访病例,两组随访率均为100%。
1.6 统计学处理
数据分析应用SPSS 13.0软件,构成比进行χ2检验或Fisher确切概率法,采用Kaplan-Meier法计算TTP、OS,差异检验应用Log-Rank法。P<0.05为差异有统计学意义。
2 结 果
2.1 治疗完成情况
48例患者均至少完成了1个周期化疗,联合组共完成78个周期化疗,平均3.39个周期,中位数为3(范围1~6),入组前应用过的化疗方案中位数为1(范围1~3),共应用的化疗周期中位数为3(范围1~7)。单药组共完成88个周期化疗,平均3.52个周期,中位数为3(范围1~6),入组前应用过的化疗方案中位数为1(范围1~3),化疗周期中位数为3 (范围1~6)。
2.2 生存分析
中位随访时间10个月(范围2~28个月),联合组和单药组的中位TTP分别为7个月和3个月,联合组显著高于单药组,差异有统计学意义(χ2=4.763,P=0.029,图1)。联合组和单药组的MST和1年OS分别为12个月、47.6%和12个月、39.6%,两组OS差异无统计学意义(χ2=0.446,P=0.504,图2)。
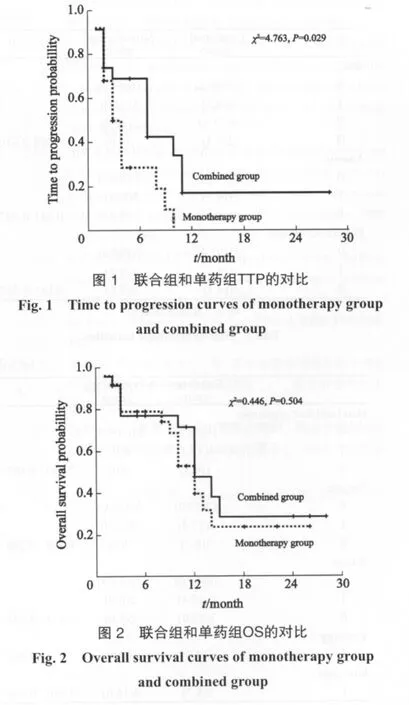
2.3 客观疗效
联合组:CR 0例,PR 3例,SD 15例,PD 5例,RR为13.0%(3/23),DCR为78.3%(18/23)。单药组:CR 0例,PR 3例,SD 16例,PD 6例,RR为12.0%(3/25),DCR为76.0%(19/25)。两组差异无统计学意义(P>0.05)。
2.4 不良反应
常见的不良反应是粒细胞减少、乏力和恶心,程度大部分均较轻,两组相比差异无统计学意义(P>0.05)。但手足综合征(hand feet syndrome,HFS)发生率联合组显著高于单药组,差异有统计学意义(χ2=7.993,P=0.005,表1、2)。
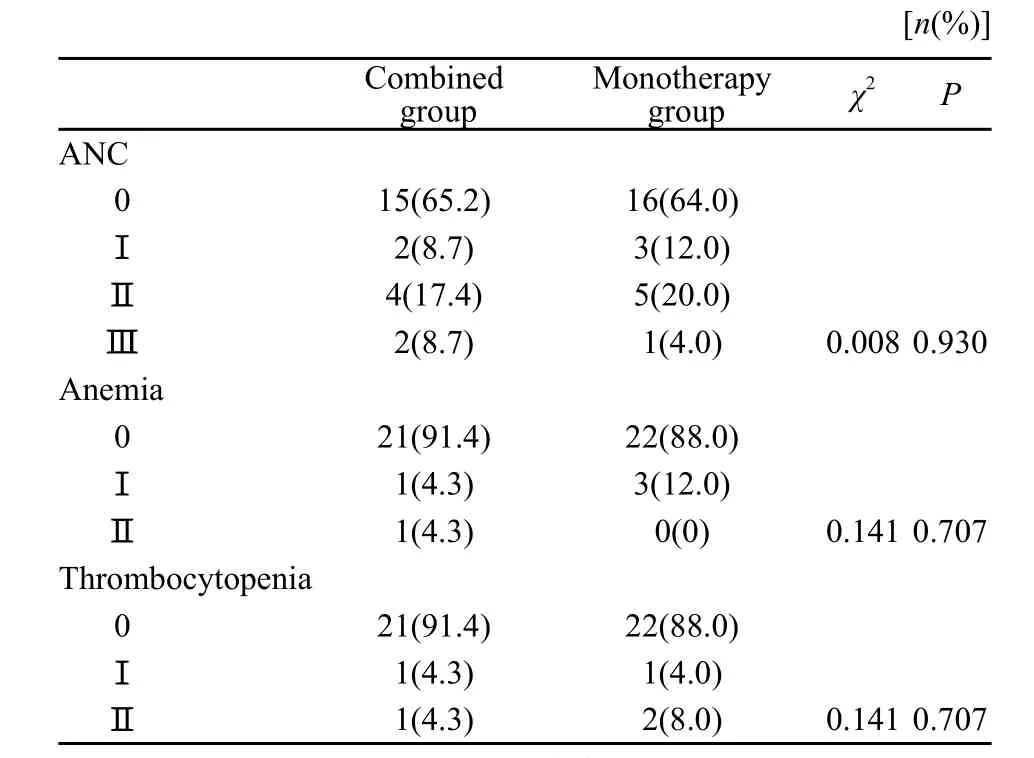
表 1 血液学毒性Tab.1 Hematologic toxicities
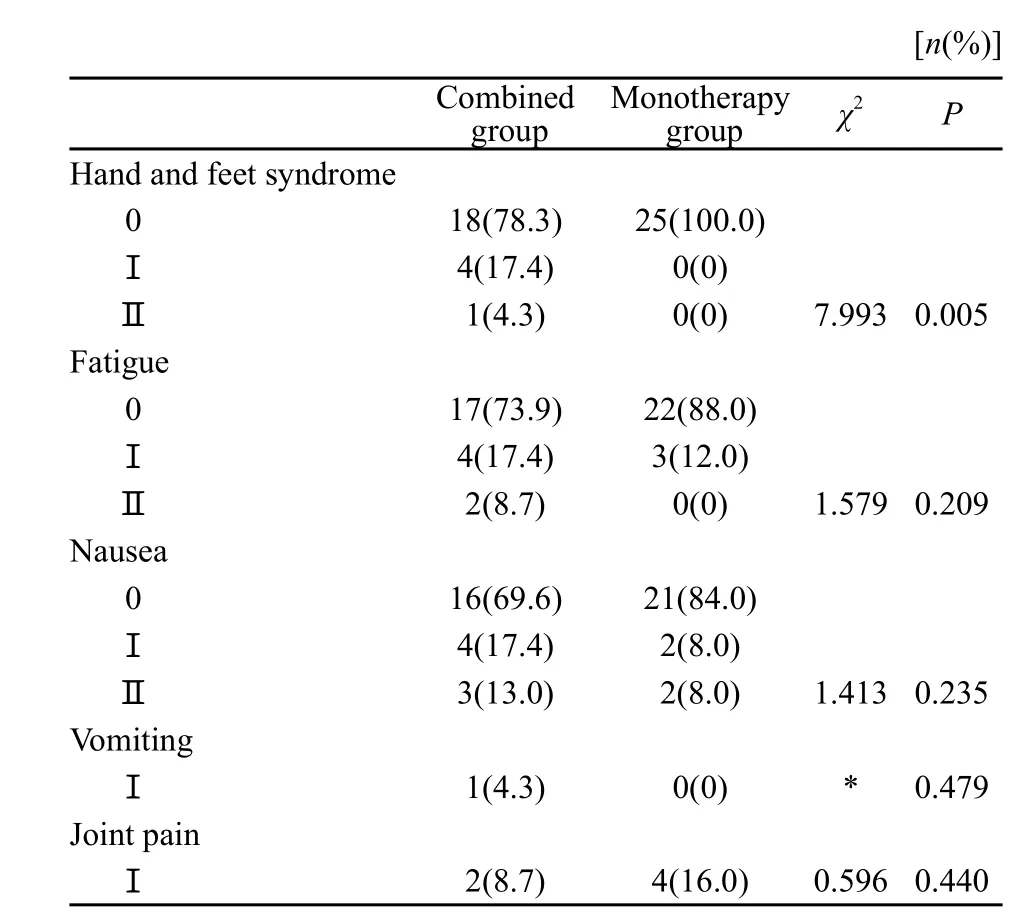
表 2 非血液学毒性Tab.2 Non-hematologic toxicities
3 讨 论
NSCLC一线化疗失败后治疗困难,疗效总体较差,尽管NCCN指南推荐的二线治疗均为单药,但由于单药的疗效有限,因此探索两药联合方案在治疗化疗失败的NSCLC患者中的作用具有重要临床意义。
多西他赛在NSCLC二线治疗中研究最广泛,被认为是标准治疗药物[4,12],因此大多数两药联合方案以多西他赛为基础,再加上一个铂类或其它化疗药物。尽管国内外已有较多的多西他赛两药的报道,但多为Ⅰ、Ⅱ期研究,并且结果并不一致。有研究显示,多西他赛两药联合方案优于单药方案,显著延长了TTP或无进展生存期[13-15]。而另有研究显示,单药多西他赛无论是RR、还是OS均能达到两药联合方案的效果[16]。因此多西他赛两药联合治疗化疗失败的NSCLC患者的疗效尚未形成共识。
卡培他滨是氟尿嘧啶前体药物,吸收后经过3步酶级联反应转化成氟尿嘧啶,从而发挥抗肿瘤作用。由于TP是限速酶,而肿瘤组织高表达TP,因此卡培他滨可以高浓集于肿瘤组织,起到一定靶向杀伤肿瘤的作用[17]。动物实验表明卡培他滨对于NSCLC有一定的抗肿瘤作用,并与TP活性相关[18]。多西他赛能够上调TP活性,并与卡培他滨有协同作用[5],理论上二者的联合应用能够取得比单药更好的疗效。
已有临床试验初步证实了卡培他滨联合多西他赛治疗化疗失败的NSCLC患者的疗效。Kindwall-Keller等[6]报道了卡培他滨联合多西他赛的Ⅱ期结果:RR为26%,MST为9.1个月,1年OS为37%,并且患者耐受性良好,因此作者推荐进行随机对照试验来评价这一两药方案。Lee等[7]报道Ⅱ期临床研究结果:RR为15.4%,MST为8.7个月,1年OS为34.4%。虽然卡培他滨联合多西他赛治疗化疗失败的NSCLC患者获得了一定的近期疗效,但是尚无随机对照研究报道其长期生存结果。
本研究达到了预期的主要研究终点,即卡培他滨联合多西他赛显著延长了患者的TTP,并且获得了较好的疗效:RR为13%,TTP为7个月,1年OS为47.6%,与国内外同类研究具有良好的可比性[13,16,19-20]。由于本研究的样本量较小、随访时间相对较短,长期的生存情况仍需要进一步观察。
[1]FERLAY J, SHIN H R, BRAY F, et al.Estimates of worldwide burden of cancer in 2008: GLOBOCAN 2008[J].Int J Cancer, 2010, 127(12):2893-2917.
[2]PARKIN D M, BRAY F, FERLAY J, et al.Global cancer statistics, 2002[J].CA Cancer J Clin, 2005, 55(2):74-108.
[3]NCCN.NCCN guidelines for treatment of non-small cell lung cancer [EB/OL].http://www.nccn.org/professionals/physician_gls/f_guidelines.asp.
[4]COMER A M, GOA K L.Docetaxel:a review of its use in nonsmall cell lung cancer[J].Drugs Aging, 2000, 17(1):53-80.
[5]SAWADA N, ISHIKAWA T, FUKASE Y, et al.Induction of thymidine phosphorylase activity and enhancement of capecitabine efficacy by taxol/taxotere in human cancer xenografts [J].Clin Cancer Res, 1998, 4(4):1013-1019.
[6]KINDWALL-KELLER T, OTTERSON G A, YOUNG D, et al.Phase Ⅱ evaluation of docetaxel-modulated capecitabine in previously treated patients with non-small cell lung cancer[J].Clin Cancer Res, 2005, 11(5):1870-1876.
[7]LEE J J, HAN J Y, LEE D H, et al.A phase Ⅱ trial of docetaxel plus capecitabine in patients with previously treated non-small cell lung cancer[J].Jpn J Clin Oncol, 2006,36(12):761-767.
[8]刘志辉, 廖小莉, 周文献, 等.多西他赛联合氟尿嘧啶类药物二线治疗晚期非小细胞肺癌的Ⅱ期临床研究[J].广西医科大学学报, 2008, 25(5):706-708.
[9]GERVAIS R, DUCOLONE A, BRETON J L, et al.Phase Ⅱrandomised trial comparing docetaxel given every 3 weeks with weekly schedule as second-line therapy in patients with advanced non-small cell lung cancer (NSCLC)[J].Ann Oncol, 2005, 16(1):90-96.
[10]LAI C L, TSAI C M, CHIU C H, et al.Phase Ⅱ randomized trial of tri-weekly versus days 1 and 8 weekly docetaxel as a second-line treatment of advanced non-small cell lung cancer[J].Jpn J Clin Oncol, 2005, 35(12):700-706.
[11]EISENHAUER E A, THERASSE P, BOGAERTS J, et al.New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J].Eur J Cancer, 2009, 45(2):228-247.
[12]DAVIES A M, LARA P N J R, MACK P C, et al.Docetaxel in non-small cell lung cancer: a review[J].Expert Opin Pharmacother, 2003, 4(4): 553-565.
[13]PECTASIDES D, PECTASIDES M, FARMAKIS D, et al.Comparison of docetaxel and docetaxel-irinotecan combination as second-line chemotherapy in advanced non-small cell lung cancer: a randomized phase Ⅱ trial[J].Ann Oncol, 2005,16(2):294-299.
[14]张怡飞, 虞永峰, 陆舜.多西他赛单药与多西他赛联合铂类方案二线治疗晚期非小细胞肺癌的比较[J].中华医学杂志, 2009, 89(22): 1544-1448.
[15]顾琳萍, 沈盛萍, 陈智伟.多西他赛单药与多西他赛联合奈达铂与多西他赛单药二线治疗晚期非小细胞肺癌的临床研究[J].中华肿瘤杂志, 2010, 32(12):939-942.
[16]TAKEDA K, NEGORO S, TAMURA T, et al.Phase Ⅲ trial of docetaxel plus gemcitabine versus docetaxel in second-line treatment for non-small-cell lung cancer: results of a Japan Clinical Oncology Group trial (JCOG0104) [J].Ann Oncol,2009, 20(5):835-841.
[17]MIWA M, URA M, NISHIDA M, et al.Design of a novel oral fluoropyrimidine carbamate, capecitabine, which generates 5-fluorouracil selectively in tumours by enzymes concentrated in human liver and cancer tissue [J].Eur J Cancer, 1998,34(8):1274-1281.
[18]MENDIOLA C, VAZ M A.Is capecitabine a new choice of treatment for lung adenocarcinoma? A case report involving partial response in second line of treatment and hypothesis of the biological basis[J].Clin Transl Oncol, 2009, 11(8):554-557.
[19]刘书林, 顾小侠, 沈水杰, 等.多西他赛每周给药联合奥沙利铂二线治疗晚期非小细胞肺癌[J].临床肿瘤学杂志,2010, 15(8):749-751.
[20]柳影, 程颖.周剂量多西他赛联合顺铂二线治疗晚期非小细胞肺癌临床观察[J].癌症进展杂志, 2008, 6(5):528-531.
