米格列醇片溶出度HPLC检测方法改进研究*
2011-06-21郝光启李进启孙彦余姜合田沈庆钦
郝光启,李进启,葛 梅,孙彦余,姜合田,李 伟,沈庆钦
(鲁南制药集团股份有限公司,临沂 276006)
米格列醇(C8H17NO5)为去氧野尻霉素衍生物,是一种新型口服α-葡萄糖苷酶抑制剂。其降糖作用的机制是通过在小肠内可逆性抑制α-葡萄糖苷酶,减少糖类分解为葡萄糖,并能延迟小肠中葡萄糖的吸收,从而降低饭后血糖升高的幅度[1]。但依据国家食品药品监督管理局标准(YBH00592010)检测时发现:米格列醇峰与其杂质峰分不开、重复性试验差(主峰响应值逐渐变小,连续进样分析时米格列醇峰面积的RSD大于20%。)且保留时间亦有变动,导致无法正常检测。实验通过改变流动相组成及pH值建立新方法,新方法专属性强、灵敏度高、准确度和重复性好、方法简便,可用于米格列醇片溶出度的定量测定。
1 仪器与试药
1.1仪器 Agilent 1100高效液相色谱系统:G1379A脱气机、G1311A四元泵、G1313A自动进样器、G1316A柱温箱、G1315B DAD检测器、A.10.01化学工作站(美国安捷伦公司),ZRS-8G智能溶出试验仪(天津海益达科技有限公司),YB系列真空恒温干燥箱(天津药典标准仪器厂),TTL-10B超纯水系统(北京同泰联科技发展有限公司),PHS-3C型精密pH计(上海精密科学仪器有限公司),XS204型电子天平(瑞士梅特勒-托利多公司)。
1.2试药 米格列醇对照品(本公司生产的原料药,经HPLC面积归一化法测定纯度为99.8%以上),米格列醇片(本公司生产,批号081201、081202、081203)。乙腈为色谱纯(山东禹王实业集团化工分公司),磷酸二氢铵、三乙胺均为分析纯,实验用水为超纯化水。
2 方法与结果
2.1色谱条件及系统适用性 色谱柱:Lichrospher氨丙基硅烷键合硅胶色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈-0.01 mol/L磷酸二氢铵溶液(三乙胺调pH至7.5)(65∶35);检测波长210 nm;流速1.0 ml/min;进样量20 μl;柱温25 ℃;检测器:二极管阵列检测器(DAD)。理论塔板数按米格列醇峰计算应不低于1000。
2.2溶液制备
2.2.1供试品溶液 取本品,照溶出度测定法(《中国药典》2010年版二部附录Ⅹ C第一法),以水500 ml为溶剂,转速为100 r/min,依法操作。经20 min时,取溶液适量,滤过(滤膜孔径不得大于0.45 μm),取续滤液作为供试品溶液。
2.2.2对照品溶液 取经60 ℃减压干燥至恒重的米格列醇对照品适量,精密称定102.7 mg,置50 ml量瓶中,加水溶解并稀释至刻度,摇匀,作为对照品储备溶液。精密量取溶液5 ml置于100 ml量瓶中,加水稀释至刻度,摇匀,滤过,作为对照品溶液。
2.2.3空白辅料溶液 依处方取不含米格列醇的空白辅料适量(约相当于50 mg的米格列醇处方量)置于500 ml溶出杯中,照“2.2.1”项下供试品溶液制备方法配制。
2.3专属性试验 分别依次取对照品溶液、供试品溶液和空白辅料溶液依上述色谱条件进样分析,色谱图见图1,可见空白辅料不会干扰米格列醇的测定。
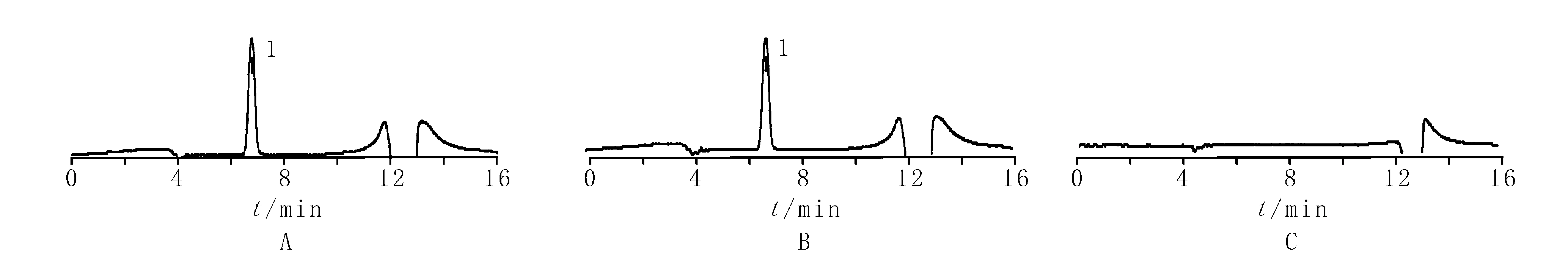
1. 米格列醇
2.4线性试验 取“2.2.2”项下对照品储备溶液,分别精密量取溶液1.0、3.0、5.0、7.0和9.0 ml,分置于100 ml量瓶中,加水稀释至刻度,摇匀,依法测定。以米格列醇峰面积对其浓度(μg/ml)进行线性回归,回归方程为:Y=7.23X+1.97(r=0.999 9)。结果表明:米格列醇在20.54~184.86 μg/ml浓度范围内线性关系良好。
2.5精密度试验 取“2.2.2”项下对照品溶液,依法连续进样6次,结果米格列醇峰面积的RSD为0.082%(n=6),说明进样精密度良好。
2.6稳定性试验 取“2.2.1”项下溶出度供试品溶液1份,依法分别于0、1、2、4、6和8 h后进样分析,结果米格列醇峰面积的RSD为0.13%(n=6),表明米格列醇溶液在8 h内稳定。
2.7回收率试验 称取经60 ℃减压干燥至恒重的米格列醇对照品约30、40和50 mg,各6份,均精密称定,分置于500 ml溶出杯中,并按处方比例分别加入辅料,分别依“2.2.1”和“2.2.2”项下方法制备回收率试验溶液和对照品溶液,依法测定,计算回收率,结果平均回收率为99.4%,RSD为0.76%,见表1。
2.8定量限和检测限试验 精密称取米格列醇对照品适量,用水溶解并稀释制成一系列不同浓度的溶液,依法测定。当信噪比S/N=10±1时,米格列醇浓度为0.21 μg/ml,米格列醇的定量限为4.20 ng;当信噪比S/N=3±1时,米格列醇浓度为0.066 μg/ml,米格列醇的检测限为1.32 ng。
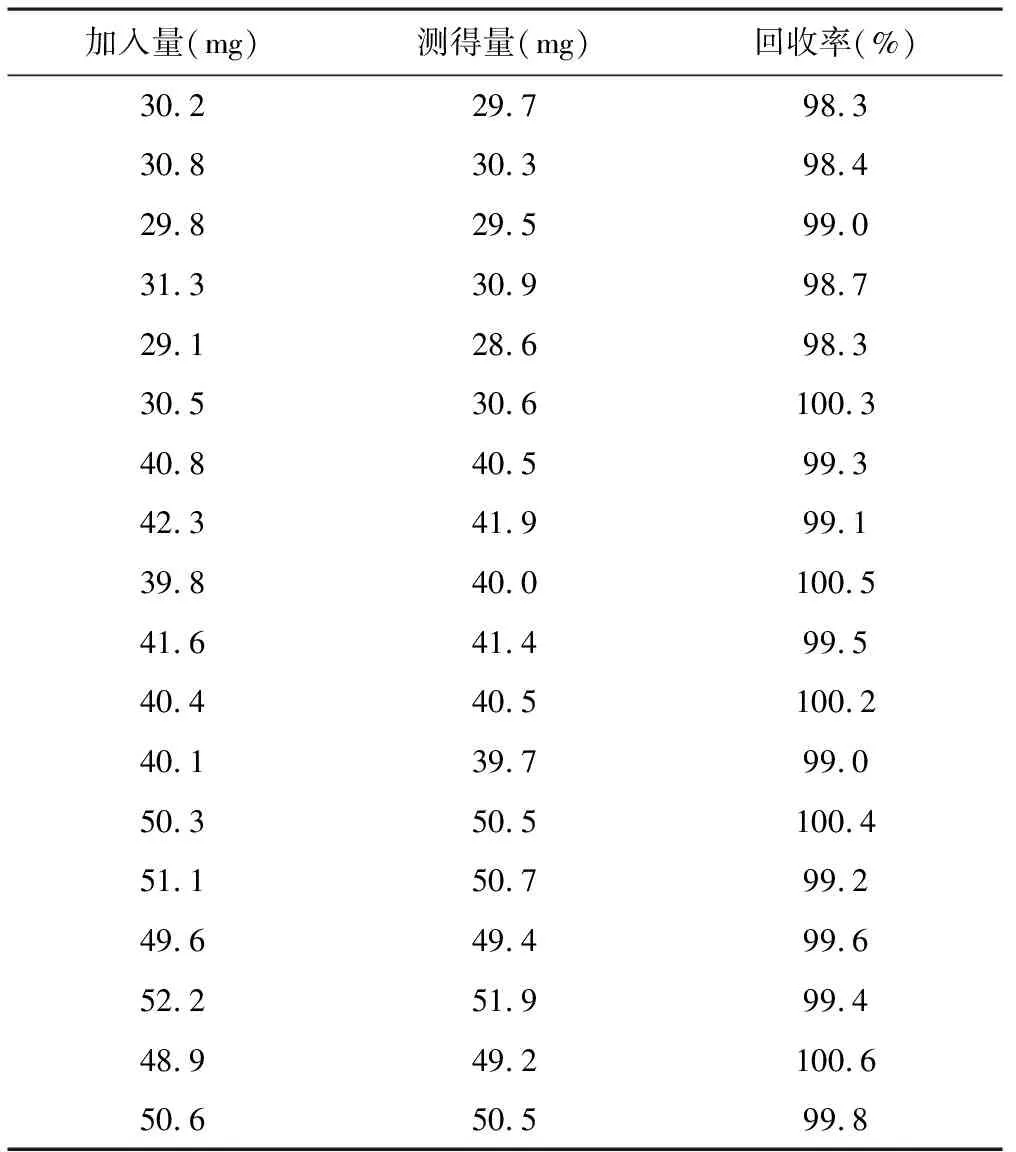
表1 溶出度回收率试验结果
2.9样品检查结果 取3批米格列醇片(批号081201、081202、081203)依法测定,结果3批样品溶出量(占标示量)平均值分别为96.8%、95.6%和97.0%,均大于溶出限度75%,符合规定。
3 讨论
经相关文献检索,目前世界主要药典如USP、EP、BP等均无米格列醇及其制剂的检测质量标准,而依国家药监局批准的质量标准如前言所述情况无法正常检测,原因可能是其流动相配制过程中用磷酸调pH值至4.0,导致在酸性环境中流动相中的酸与色谱柱固定相键合的氨丙基发生相互作用,使色谱柱柱效降低。同时,由于米格列醇结构式中N原子有孤对电子,易与酸性流动相中H+结合产生质子化,降低其色谱分配系数(K),从而缩短米格列醇在色谱柱固定相的保留行为,导致其较快流出(保留时间短)和分离情况较差。试验曾应用0.01%氨水溶液(含5%乙腈)对氨丙基色谱柱进行再生,效果理想。由此联想到在0.01 mol/L磷酸二氢铵溶液中滴加三乙胺调pH值至中性到弱碱性,试验曾考查在0.01 mol/L磷酸二氢铵溶液中用三乙胺调pH值至6.0、6.5、7.0、7.5等不同pH值时米格列醇重复性试验和分离度(R)情况,发现随着pH值的不断增加米格列醇重复性试验和分离度(R)越来越好。这主要是因为随着pH值的不断增加,溶液逐渐由酸性变为弱碱性,抑制了米格列醇质子化而增大其色谱分配系数(K),从而增加米格列醇在色谱柱固定相上的保留行为,提高了其色谱分离性能。同时,流动相的弱碱性亦阻止原标准流动相中的酸与色谱柱固定相键合的氨丙基发生相互作用,从而提高了氨丙基色谱柱的柱效,增加其色谱行为的稳定性。同时考虑到色谱柱pH的应用范围(pH 2~8),经反复试验、不断优化,最终确定本色谱条件。
新建立的本方法专属性强、准确度高、重复性好,可用于米格列醇片的溶出度检查方法。
1 黄雅琴,田成科.米格列醇片.中国新药杂志,2005,14(5): 638
