甲氨蝶呤联合环磷酰胺治疗类风湿关节炎的临床研究
2010-02-01陈宜恒
陈宜恒
(附属菏泽市立医院,山东 菏泽 274031)
类风湿关节炎(RA)是一种高度致残性自身免疫性疾病,其最佳治疗策略是早期诊断、早期给予抗风湿药(DMARDs)的治疗,以有效控制骨关节破坏,降低疾病活动度[1-3]。近年来,造血干细胞移植、抗CD20单克隆抗体治疗难治性RA,均是缘于血液病治疗的成功经验[4-5]。鉴于此,我们在临床实践中,依据肿瘤联合化疗的基本理论——细胞增殖动力学原理,联合细胞周期特异性药物甲氨蝶呤(MTX)与周期非特异性药物环磷酰胺(CTX)小剂量按细胞增殖周期间歇给药治疗RA。国内报道体外及动物实验均已证实两药联合后作用增强[6-9],不良反应无明显增加[7-9]。为了较客观地评估MTX联合CTX治疗RA的疗效和安全性,我们进行了较为系统的临床研究,取得了满意疗效,现将报道如下。
1 临床资料
1.1 一般资料 所选患者均来自我院风湿科门诊及住院患者,均符合美国风湿病学会(ACR)1987年RA分类标准。纳入标准:年龄18~65岁,男女不限,在入选前4周患者未服用除MTX以外的其他DMARDs药物,服用糖皮质激素(相关于泼尼松的剂量)必须稳定在10 mg/d或至少4周未服用,服用非甾体抗炎药(NSAIDs)的剂量至少已稳定4周或至少于已1周未服用;筛选时疾病处于活动期,即同时满足下面4条:1)随访当日晨僵持续时间60 min。2)≥3个关节肿胀。3)≥8个关节触痛。4)红细胞沉降率(ESR)≥28 mm/h或C反应蛋白(CRP)≥正常上限的1.5倍。排除标准:残疾、卧床、依赖轮椅等生活不能自理者;患有全身性炎症疾病者,如系统性红斑狼疮(SLE)等其他风湿性疾病;曾有或现患恶性肿瘤;有慢性感染病史、近2个月有严重感染的病史或近6个月内有过机会感染;当前患有活动性肝炎或有丙型肝炎病史者;人类免疫缺陷疾病及病毒感染者;有如淋巴瘤等淋巴增殖性疾病病史者;有多发性硬化或者其他中枢神经脱髓鞘疾病者;曾有或现患充血性心力衰竭者;有严重、进行性、未控制的肝、肾、血液、胃肠道、内分泌、心、肺、神经和脑等疾病;结核纯蛋白衍生物(PPD)皮试阳性或(和)胸部X线片显示肺部有感染的征象或与结核病患者有密切接触者;筛选前4周内使用过肌肉注射或静脉滴注皮质激素;近期应用过生物制剂者。所有患者均自愿参与试验并签署知情同意书。
1.2 试验方法 经筛选符合试验条件的受试者按照先后顺序随机进入单用甲氨蝶呤(MTX)组(7.5 mg/周,口服)、单用环磷酰胺(CTX)组(400 mg/2周,静脉滴注)以及MTX+CTX联合用药组(MTX7.5 mg周,口服;CTX 400 mg/2周,静脉滴注)。在治疗期间继续服用或加用剂量稳定NSAIDs或小剂量糖皮质激素(10 mg泼尼松或等效剂)。试验过程中禁止使用其他DMARDs细胞毒药物及肿瘤坏死因子(TNF)-α拮抗剂等生物制剂。
1.3 临床观察指标 治疗前及第6、12、24周对下列指标进行评估:疼痛目视模拟测试表(VAS)评分、医生对患者健康状况的总体评估、压痛关节数(TJC)、压痛关节指数(TJI)、肿胀关节数(SJC)、肿胀关节指数(SJI)。
1.4 实验室指标 包括血、尿常规、血生化、ESR、CRP,并按规定进行胸部X线片、心电图和B超检查。
1.5 疗效评估 采用ACR推荐的RA改善标准和欧洲抗风湿病联盟(EULAR)疗效标准来进行评价[9-12]。1)ACR 所制定的标准:ACR20、ACR50、ACR70。2)EULAR疗效标准:疾病活动指数(DAS)采用DAS28。3)主要疗效评价指标:治疗终点时达到ACR20改善的患者比例;次要疗效评价指标:治疗终点时达到 ACR50、ACR70改善的患者比例,达到EULAR有效和显效的患者比例以及各种具体临床观察指标的改善情况。
1.6 安全性评价 随时记录所有在试验期间发生的不良事件,并判断这些不良事件与试验药物的因果关系。根据不良事件的发生频率及类型,比较试验用药的安全性。对于任何在观察结束时仍异常的安全性实验室检查项目,进行跟踪随访,直到这些指标恢复或临床稳定。
1.7 统计学处理 采用SPSS 11.0统计软件进行分析。计量资料采用t检验,统计分析采用单因素方差分析,多重比较采用SNK-q检验,当方差不齐时采用Dunnett T3进行多重比较。计数资料的比较采用χ2检验。
2 结果
2.1 一般情况 180例RA患者进入观察研究,随机分为单用MTX、单用CTX、MTX+CTX联合治疗组。28例患者失访。共152例患者(MTX组56例,CTX组40例,MTX+CTX组56例)进行安全性评估及基线时的统计学分析。其中6例患者(MTX组2例,CTX组2例,MTX+CTX组2例)在第6周,2例患者(MTX+CTX)在第12周临床评估后因不良反应而停止治疗,4例患者(CTX组)在第12周评估后失访,在随后的观测点不再进行疗效分析。按方案规定完成试验的患者共140例(MTX组54例,CTX组34例,MTX+CTX组52例),3组患者治疗前一般情况及各项评价指标的差异无统计学意义。所有患者均口服剂量稳定的NSAID治疗。3组有不同比例的患者口服小剂量泼尼松(10 mg/d)治疗,但3组间口服泼尼松的患者比例差异无统计学意义。完成试验的140例患者中有12例患者(其中MTX组6例,MTX+CTX组6组例)在入选前曾服用MTX,均为小剂量口服(≤7.5 mg/周),入选前服用MTX时间为2~4周,均为在外院就诊给予MTX口服后2~4周内来我院就诊,符合入选及排除标准后入组观察。MTX组56例,男18例,女38例,平均41岁。平均使用糖皮质激素24个月,疼痛30例,占54%。VAS评分平均68分,PGA评分平均66分,医生总体评估平均62分。CTX组40例,男14例,女26例,平均48岁;平均使用糖皮质激素21个月,疼痛28例,占70%。VAS评分平均60分,PGA评分平均62分,医生总体评估59分。MTX+CTX组56例,男10例,女46例,平均48岁;平均使用激素34个月,疼痛20例,占43%。VAS评分平均59分,PGA评分平均62分,医生总体评估平均59分。

x±s)表1 各项评价指标的比较(
2.2 疗效分析
2.2.1 主要疗效指标ACR20结果 治疗6周后,各组改善达ACR20标准的患者比例为:MTX组25%(14/56),CTX 组10%(14/40),MTX+CTX 组32%(18/56),但差异无统计学意义;12周时改善达ACR20标准的比例为:MTX组44%(24/54),CTX组21%(8/38),MTX+CTX 组 59%(32/54),MTX+CTX组明显高于CTX组(P<0.01),但与MTX组比较差异无统计学意义;第24周时各组改善达ACR20标准的患者比例迅速升高,分别为:MTX组56%(30/54),CTX 组35%(12/54),MTX+CTX 组81%(42/52),MTX组、CTX组均低于 MTX+CTX组,差异均有统计学意义(分别为 P<0.05,P<0.01)。
2.2.2 次要疗效指标结果
2.2.2.1 ACR50、ACR70 的结果:第 6 周时,仅MTX+CTX组有2例患者改善达到ACR50标准,无患者改善达ACR70标准。治疗12周后,各组均有一定比例的患者改善达到ACR50标准,分别为MTX组15%(84/54),CTX组5%,MTX+CTX组26%(2/38)仅MTX+CTX组有2例患者改善达到ACR70标准。24周时,改善达ACR50标准的患者比例分别MTX组41%(22/54),CTX组12%(4/34),MTX+CTX 组 58%(30/52),MTX+CTX 组和MTX组之间差异无统计学意义。24周时,改善达ACR70标准的患者比例分别为MTX组11%(6/54),CTX 组 0,MTX+CTX 组 19%(10/52),但差异无统计学意义。
2.2.2.2 EULAR 疗效标准的结果:第6 周时,各组有效率分别为MTX组18%(10/56),CTX组5%(2/40),MTX+CTX组21%(12/56)。随治疗时间延长,各组达有效的患者比例均呈上升趋势,12周时分别为MTX组37%(20/54),CTX组16%(6/38),MTX+CTX组56%(30/54)。24周时分别为MTX组48%(26/54),CTX 组35%(12/34),MTX+CTX组77%(40/52)。在12和24周时MTX+CTX组和CTX组之间达到有效的患者比例差异均有统计学意义(P<0.01),24周时MTX+CTX组和MTX组之间差异有统计学意义(P<0.05)。25周时MTX+CTX组有16例,MTX组有10例患者达到显效和疾病低度活动,MTX+CTX组有6例,MTX组有4例患者达到疾病缓解,CTX组无患者达到显效、疾病低度活动或缓解。各组达显效、疾病低度活动或缓解的患者比例差异无统计学意义。
2.2.2.3 各项具体评价指标的结果:治疗12周后,MTX组和MTX+CTX组各项评价指标均显著低于基线水平(P <0.01 ~0.05,CTX 组除 TJC/TJI,SJC/SJI、HAQ外各项评价指标均低于基线水平(P<0.05)。24周时CTX组除TJC/TJI外各项指标均显著低于基线水平(P<0.05)。24周时比较不同治疗组间的改善程度,MTX+CTX组在疼痛 VAS评分 TJC/TJI、ESR的改善程度高于MTX组(P<0.05),MTX+CTX组各项指标的改善程度均高于CTX组(P<0.01),见表 2、3、4。
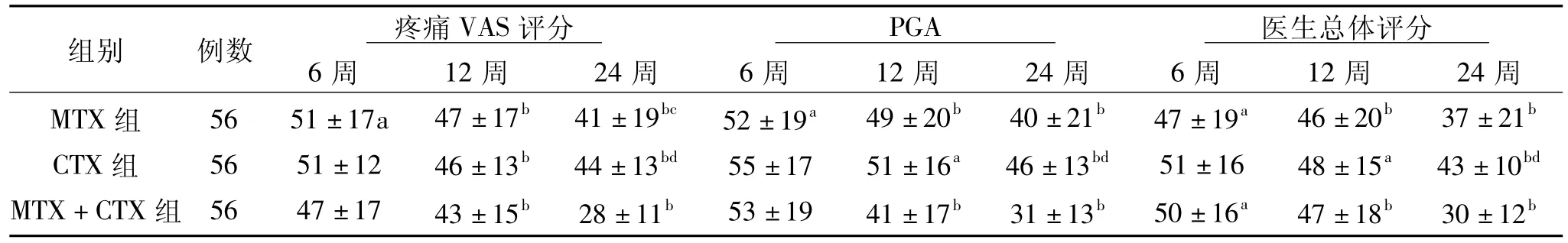
表2 3组各项具体评价指标的变化情况(x±s,分)

表3 3组不同周数关节压痛指数评分(x±s,分)

表4 3组不同因素关节肿胀指数与血沉评分(x±s,分)
2.3 药物安全性 在24周观察期间,无严重感染、骨髓抑制、出血性膀胱炎、肿瘤等严重不良事件发生,共有50例患者发生与药物直接相关的不良事件,分别为MTX组有18例患者、28例次、CTX组有12例患者20例次、MTX+CTX组有20例患者34例次。各组中不良事件发生率分别为MTX组32%、CTX组30%,MTX+CTX组36%,差异比较无统计学意义(P=0.912)。出现的不良反应主要包括胃肠道症状、肝酶异常、白细胞减低、呼吸道感染、脱发、月经紊乱、乏力等。其中导致停药的重要不良反应包括肝酶升高、白细胞减低,停药后全部恢复。各种不良事件的发生率差异无统计学意义。
MTX组有2例患者在用药6周后出现谷丙转氨酶(ALT)升高,超过正常值3倍以上,停止治疗后终止研究,给保肝治疗后肝功能恢复正常。其余8例患者ALT升高均在正常值的2倍以内,其中MTX组2例,治疗12周后出现;CTX组2例,治疗12周后出现;MTX+CTX组4例,分别在治疗6周、12周后出现。MTX+CTX组有2例患者不愿继续用药终止研究,其余患者均坚持治疗,并经保肝治疗后随访,肝功能恢复正常。MTX组、CTX组和MTX+CTX组各有2例患者出现外周血白细胞数减少,出现时间分别为治疗后12周、12周、6周。白细胞计数的范围为(3.1~3.9)×109/L、其中因CTX组的2例患者不愿继续用药而终止研究,其余患者在延长用药间隔后,白细胞总数均自行恢复正常,未给予特殊药物治疗。
3 讨论
本研究借鉴肿瘤联合化疗方案的细胞增殖动力学,其精髓是细胞周期特异性药物与细胞周期非特异性药物联合及按照细胞增殖周期间歇给药。基于细胞动力学原理,周期联合MTX和CTX治疗RA。周期联合的含义:首先是选用作用于不同细胞周期的药物联合,选用细胞周期特异性药物与周期非特异性药物联合,于不同环节阻断异常的免疫反应,旨在取得治疗的协同作用,以提高疗效;其次按照细胞增殖周期间歇给药,CTX遵循细胞周期小剂量间歇点式给药,给骨髓及其他正常组织细胞恢复时间,是降低不良反应的关键[3]。本研究结果显示:给予MTX治疗后,RA患者的症状、体征及实验室炎性指标均得到有显改善。
在该研究中,76例RA患者接受了CTX治疗,治疗时间为6~40个月,患者对CTX的反应率达到75%。既往文献报道CTX[12-15]均为口服治疗,剂量50 mg~150 mg/d。本研究中,CTX为400 mg/2周静脉滴注。结果表明可部分改善患者的症状体征及实验室炎性指标,与既往文献报道结果类似。
MTX属于细胞周期特异性药物,主要作用于细胞周期的S期,对G0/G1至S期起到转换延缓作用。有研究表明MTX能抵制G1/S期转换的正性调节蛋白cyclin E的过度表达,从而达到抑制细胞生长的作用[15]。CTX是双功能烷化剂,属细胞周期非特异性药物,对各期细胞均有杀伤作用。故理论上,每周给予小剂量MTX将多数细胞阻滞在G0/G1期。同时,每2周给予1次小剂量CTX,能更有效杀伤阻滞于G0/G1期的细胞,且CTX为小剂量按细胞周期间歇点式给药,给正常细胞恢复时间,从而减少骨髓及体内重要脏器组织的功能损伤。本研究的疗效数据表明:MTX联合CTX治疗可显著改善RA患者的症状,降低疾病活动度及炎性实验室指标,改善患者关节功能状态,提高生活质量,且疗效优于单用MTX及单用CTX。自治疗第6周起,MTX+CTX组达到 ACR20改善的患者比例高于MTX组和CTX组,并在整个观察期间维持这种趋势。治疗24周后,3组之间达ACR20改善的患者比例差异有统计学意义。各项次要疗效指标的改善情况与主要疗效指标的特点基本一致。24周时MTX+CTX组达EULAR有效的患者比例高于MTX组及CTX组,差异有统计学意义。对各项具体评价指标的改善情况分析显示:MTX+CTX组在TJC/TJI、疼痛VAS评分、ESR等的改善程度上优于MTX及CTX组,在SJC/SJI、PGA的改善程度上优于CTX组。本研究结果也表明:MTX联合CTX治疗RA具有较好的安全性和耐受性。与单用相比,治疗相关的不良事件发生率差异无统计学意义,无严重感染、骨髓抑制、出血性膀胱炎、肿瘤等疾患发生,多数不良事件为一过性表现。在本研究中,胃肠道症状是最常见的不良反应,主要表现为食欲下降、恶心、胃区不适等,均为轻中度,改变MTX服药时间(晚饭后服用)或静脉滴注CTX时给予舒可捷5 ml,3次/日,可减轻上述症状,1~2 d后上述症状均可消失。其它不良事件包括肝酶异常、一过性白细胞减低、上呼吸道感染等,经对症治疗后均得到改善。另外,有少数患者出现脱发、乏力,女性患者出现月经紊乱等,症状轻微,不需要特殊治疗。
MTX 是治疗 RA 的有效药物[12-14],CTX 对 RA患者也有一定的疗效[15],但既往文献报道CTX为每日给药(剂量50 mg~150 mg/d),没有给正常组织细胞恢复时间,导致其不良反应较大。
本研究中,CTX按照细胞增殖周期间歇给药,两者联合治疗RA在增强疗效的同时,也降低了不良反应。
总之,本研究结果表明MTX联合CTX疗效好,不良反应小,且该联合方案价格低廉,使用方便。本文对短期的疗效和安全性数据进行了总结,而长期疗效和安全性数据仍在进一步观察中。
[1] Verschueren P,Essens G,Westhovens R.Daily practice effectiveness of a step-down treatment in comparison with a tight step-up for early rheumatoid arthritis[J].Rheumatology(Oxford),2008,47:59-64.
[2] Boers M.COBRA combination therapy in daily practice- getting back to the future[J].R heumatology(Oxford),2008,47:1 -2.
[3] 李小峰.周期联合免疫抑制剂治疗类风湿关节炎的新思路[J].中华风湿病学杂志,2008,12:491 -492.
[4] Snowden JA,Kapoor S,Wilson AG.Stem cell transplantation in rheumatoid arthritis[J].Autoimmunity,2008,28:1.
[5] Nemec P.Rituximab(MabThera) - a new biological medicine in rheumatoid artritis therapy[J].Vnitr Lek,2007,53:1199 - 1210.
[6] 李小峰,王晓霞,王来远,等.联合甲氨蝶呤和环磷酰胺治疗类风湿关节炎114例分析[J].中华风湿病学杂志,2005,9(增刊):185-186.
[7] 王彩虹,李小峰,张奉春,等.周期联合甲氨蝶呤和环磷酰胺对大鼠胶原诱导性关节炎滑膜细胞周期蛋白D1表达的研究[J].中华风湿病学杂志,2008,12:812 -815.
[8] 曲世晶,李小峰,王彩虹,等.甲氨蝶呤联合环磷酰胺对胶原诱导性关节炎大鼠滑膜细胞P53表达的研究[J].中华风湿病学杂志,2009,13:42 -44.
[9] Fransen J,van Riel PL.The Disease Activity Score and the LAR response criteria[J].Clin Exp Rheumatol,2005,23(539);S93 - 99.
[10] Fransen J,Creemers MC van Riel PL.Remission in rheun-arthritis:agreement of the disease activity score(DAS28)the ARA preliminary remission crieria[J].Rheumatology(Oxfe)2004,43:1252-1255.
[11] 牛红青,李小峰,张莉芸,等.周期联合甲氨蝶呤环磷酰类风湿关节炎患者外周血淋巴细胞周期及凋亡的影响[J].医药杂志,2008,37:306 -308.
[12] Verstappen SM,Jacobs JW,van der Veen MJ,et al.Inten treatment with methotrexate in early rheumatoid arthritis:ain for remission.Computer Assisted Management in Early Rheuntoid Arthritis(CAMERA,an open - label strategy trial)[J].Rheum Dis,2007,66:1443-1449.
[13] Van Dongen h,van Aken J,Lard LR,et al.Efficacy methotrexate treatment in patients with probable rheumat arthritis:a doubleblind,randomized,placebo - controlled[J].Arthritis Rheum,2007,56:1424 -1432.
[14] Braun J,Kastner P,Flaxenberg P,et al.Comparison of the clical efficacy and safety of subcutaneous versus oral administrati of methotrexate in patients wifh active rheumatoid arthritis:msults of a sixmonth,multicenter,radomized double - blind,cotrolled,phase IV trial[J].Arthritis Rheum,2008,58:73 -81.
[15] Sgambato A,Camerini A,Pani G,et al,Increased expression oeyclin E in associated with an inereased resistance to doxorubicir in rat fibroblasts[J].Br J Cancer,2003,88:1956 - 1962.
