电针胃俞募配穴对胃扩张模型大鼠海马c-fos表达水平及神经细胞活动的影响
2021-10-21申国明蔡荣林王溪阳
崔 敏,申国明,蔡荣林,王 浩,王溪阳,黄 顺
(安徽中医药大学,安徽 合肥 230012)
俞募配穴是中医临床诊疗应用广泛的配穴方法。俞募相配,阴阳协调,相辅相成,对脏腑的阴阳平衡起调节作用,以期“阴平阳秘,精神乃治”,进而达到治疗病症的目的。实验研究发现,电针胃俞募穴可有效改善胃动力,促进胃功能恢复。但俞募配穴的作用机制尚不明确,其中针刺穴位与靶器官的关系已经成为众多学者研究的重点。
前期研究表明,俞募配穴针刺信号发挥对靶器官的调控作用是通过神经环路完成的。海马等参与调节胃运动相关的脑核团之间存在丰富的纤维联系。化学遗传学和膜片钳技术显示,电针足三里可通过激活海马谷氨酸能神经细胞参与对胃运动的调节。海马在边缘系统中占关键地位,参与调节胃肠运动。玻璃微电极技术发现,胃扩张刺激信号传入到海马,影响海马CA1区神经细胞的电活动。CA1区神经细胞可能在海马对胃扩张刺激的反应中起着整合作用,参与胃肠功能的调控。基于此,本研究借助免疫荧光和微电极阵列的方法分别测定大鼠海马c-fos表达水平和神经细胞放电频率,观察海马是否参与胃俞募配穴对胃扩张模型大鼠胃运动的调节。
1 材料
1.1 实验动物及分组 选用40只7周龄SPF级雄性SD大鼠,体质量250~300 g,购自郑州市惠济区华兴实验动物养殖场[生产许可证号:SCXK(豫)2019-0002]。置于(25±2)℃的室温中常规饲养,确保大鼠自由及充足的摄食和饮水。适应性饲养1周后,随机分为5组,每组8只,分别为模型组、中脘组、胃俞组、中脘+胃俞组、非经非穴组。实验过程中严格遵循《医学实验动物管理实施细则》,所有动物实验均按照科技部2006年颁布的《关于善待实验动物的指导性意见》的规定进行。
1.2 主要仪器与试剂 胃肠压力换能器(型号 YP200):北京新航兴业科贸有限公司;双导智能胃肠电图仪(型号 EGEG-2D):合肥奥源科技发展有限公司;生物信号采集系统(Power Lab 8/30):埃德仪器国际贸易有限公司;异氟烷(批号 20052802):深圳瑞沃德生命科技有限公司;包埋机(型号 JB-P5):武汉俊杰电子有限公司;c-fos一抗(货号 sc-166940):Santa Cruz;DAPI染液(批号 071618190213)、抗荧光淬灭封片剂(批号 111318190306):Beyotime。
2 方法
2.1 模型复制方法 参考宗勇等的模型复制方法。取乳胶条状气球和聚乙烯软管,制成原始容积为0.1 mL的胃内留置球囊。腹腔注射2%戊巴比妥钠(40 mg/kg)麻醉大鼠,将大鼠固定于鼠台。并将石蜡油涂在软管管壁上,然后将球囊紧贴大鼠口腔后壁插入胃内,在胃窦部(见图1)固定,从胃窦引出的聚乙烯软管与Power Lab 8/30生理信号采集系统相连,以记录到大鼠胃内压≥40 mmHg时为模型复制成功的标志。每天予以20 min胃扩张刺激,连续7 d。

图1 胃扩张模型球囊位置示意图
2.2 干预方法 模型复制7 d后开始干预,每次20 min,共7 d。模型组予以胃扩张刺激,电针组依据华兴邦《大鼠穴位图谱的研制》以及在实验期间观察到的大鼠体表的骨性标志,“中脘”穴定位于大鼠腹正中线脐上约20 mm,“胃俞”穴定位于第13胸椎下旁开约5 mm。非经非穴组对照刺激点则选取双胁下髂嵴上10 mm,后正中线旁开20 mm处。各电针组分别行毫针直刺相应穴位2~3 mm,在确保毫针与电针仪导线连接好的基础上,选择疏密波,电压9 V,频率20~100 Hz,电流2~3 mA。
2.3 胃内压记录 大鼠于实验前禁食不禁水12 h,实验时腹腔注射麻醉,束缚于鼠台,在聚乙烯软管管壁上涂上石蜡油,将气囊插入胃内,在胃窦部固定,从胃窦引出的聚乙烯软管与Power Lab 8/30生理信号采集系统连接,记录大鼠胃内压振幅变化情况,每次记录时间为60 min。
2.4 胃电图记录 将大鼠麻醉后并仰卧位固定于鼠板上,以大鼠肚脐与胸剑结合部连线的中点为胃窦体表投影处,胃窦体表投影处向左旁开1 cm稍上方为胃体体表投影区。分别将电极放置在胃窦、胃体体表投影区,其中参考电极、接地电极分别置于大鼠右上肢内侧、右下肢内侧踝部(图2)。打开仪器,开始采集体表胃电信号,记录时间为5 min。

图2 体表胃电实验电极接放位置示意图
2.5 免疫荧光法检测海马CA1区c-fos表达水平 将固定好后的脑组织常规脱水、包埋、制成5 μm石蜡切片、抗原修复。接着进行封闭、抗体孵育、DAPI染色等处理,将切片置于荧光显微镜下,于低倍镜下明确视野,高倍镜下采集图像。采用Image-Pro Plus 6.0图像处理与分析系统分析所选视野的c-fos阳性细胞,以高倍镜下海马同一区域c-fos阳性细胞数代表c-fos表达水平。
2.6 微电极阵列技术记录海马CA1区神经细胞放电 将大鼠麻醉后,先将其固定于脑立体定位仪上,调平之后在大鼠头部正中剪一平滑切口,暴露前囟(Bregma)点,墨水标记。依据《大鼠脑立体定位图谱》,精确定位于海马CA1(前囟后3.0~3.8 mm,中线旁开2.0~2.4 mm,颅骨平面以下2.0~3.0 mm)。在海马CA1区钻开颅骨窗,将8通道微电极阵列固定于脑立体定位仪上,用紫铜网覆盖以屏蔽干扰信号。电极匀速向下推进,速度1 μm/s,直至目标脑区。打开在体电生理信号记录系统,观察放电活动情况,待观察到稳定的神经电活动后,开始记录5 min。

3 结果
3.1 电针胃俞募配穴对胃扩张大鼠胃内压的影响 5组大鼠的胃收缩波形具有显著性差异,见图3。与模型组比较,中脘组、胃俞组、中脘+胃俞组大鼠胃内压显著升高(P
<0.
05),而非经非穴组大鼠胃内压无明显变化(P
>0.
05);中脘+胃俞组胃内压较中脘组、胃俞组显著升高(P
<0.
05)。见图4。
图3 5组大鼠的胃收缩波形
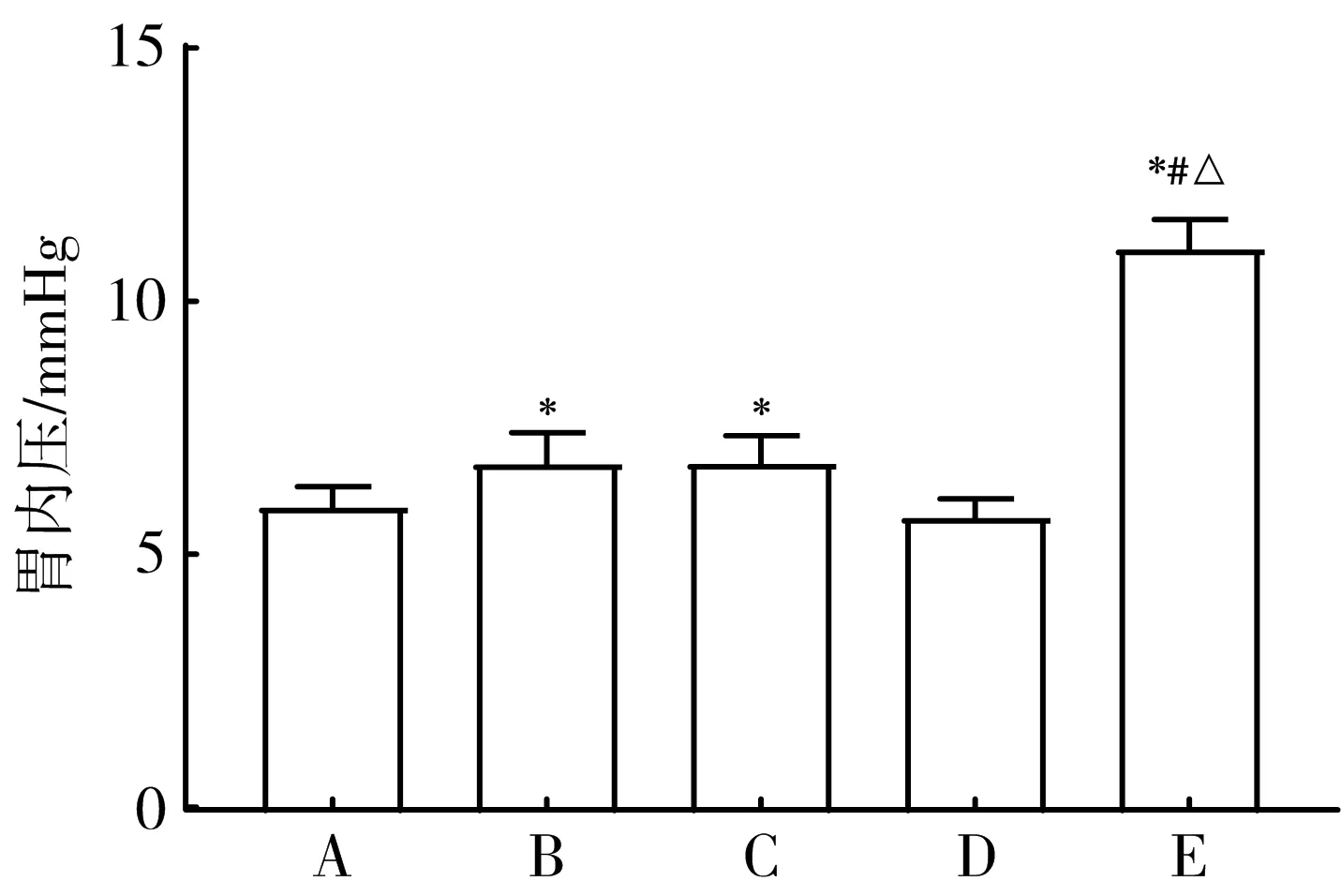
注:A.模型组;B.中脘组;C.胃俞组;D.非经非穴组;E.中脘+胃俞组;与模型组比较,*P<0.05;与中脘组比较,#P<0.05;与胃俞组比较,△P<0.05
3.2 电针胃俞募配穴对胃扩张大鼠胃电振幅的影响 5组大鼠胃电振幅有明显差异,见图5。与模型组比较,中脘组、胃俞组、中脘+胃俞组胃电幅值显著升高(P
<0.
05),非经非穴组胃电振幅无明显变化(P
>0.
05);中脘+胃俞组较中脘组、胃俞组胃电振幅显著升高。见图6。
图5 5组大鼠的体表胃电波形

注:A.模型组;B.中脘组;C.胃俞组;D.非经非穴组;E.中脘+胃俞组;与模型组比较,*P<0.05;与中脘组比较,#P<0.05;与胃俞组比较,△P<0.05
3.3 电针胃俞募配穴对胃扩张大鼠海马CA1区c-fos蛋白表达水平的影响 荧光显微镜下,可见c-fos呈阳性表达,细胞核呈绿色染色,见图7。与模型组比较,中脘组、胃俞组以及中脘+胃俞组大鼠海马CA1区c-fos蛋白表达水平显著增加(P
<0.
05),非经非穴组大鼠海马CA1区c-fos蛋白表达水平无明显变化(P
>0.
05);中脘+胃俞组c-fos蛋白表达水平显著高于中脘组和胃俞组(P
<0.
05)。见图8。
注:红色箭头示c-fos阳性表达
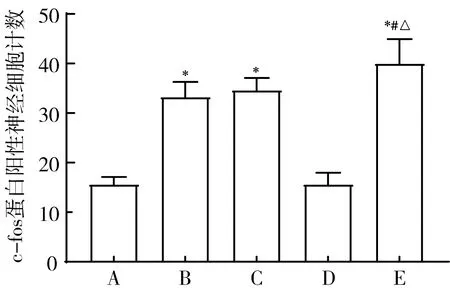
注:A.模型组;B.中脘组;C.胃俞组;D.非经非穴组;E.中脘+胃俞组;与模型组比较,*P<0.05;与中脘组比较,#P<0.05;与胃俞组比较,△P<0.05
3.4 电针胃俞募配穴对胃扩张大鼠海马CA1区神经细胞放电频率的影响 5组大鼠海马CA1区神经细胞60 s内放电的光栅图见图9。通过实时频谱分析发现,中脘+胃俞组局部场电位频谱能量较模型组显著增强,中脘组、胃俞组局部场电位频谱能量低于中脘+胃俞组,模型组和非经非穴组频谱能量变化无明显差异,见图10。与模型组比较,中脘组、胃俞组、中脘+胃俞组神经细胞放电频率显著增加(P
<0.
05),而非经非穴组神经细胞放电频率无明显变化(P
>0.05);与中脘组、胃俞组比较,中脘+胃俞组神经细胞放电频率增多(P
<0.
05)。见图11。
图9 5组大鼠海马CA1区神经细胞放电的光栅图
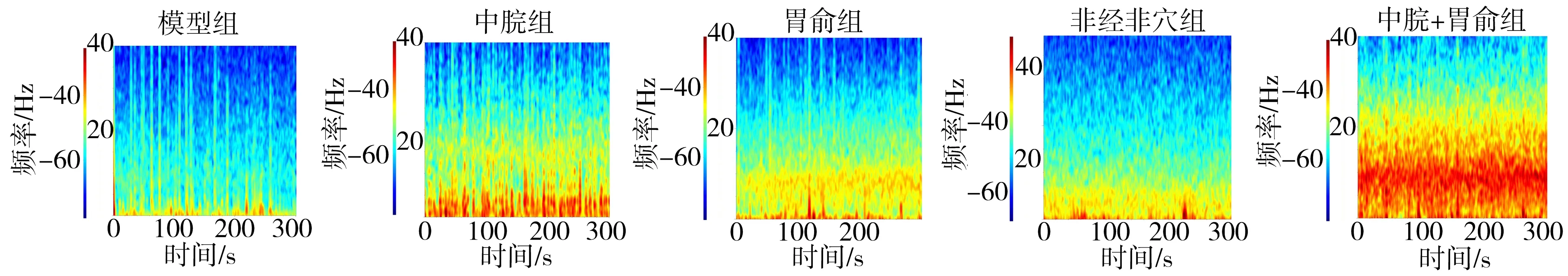
图10 5组大鼠海马CA1区神经细胞放电实时频谱图
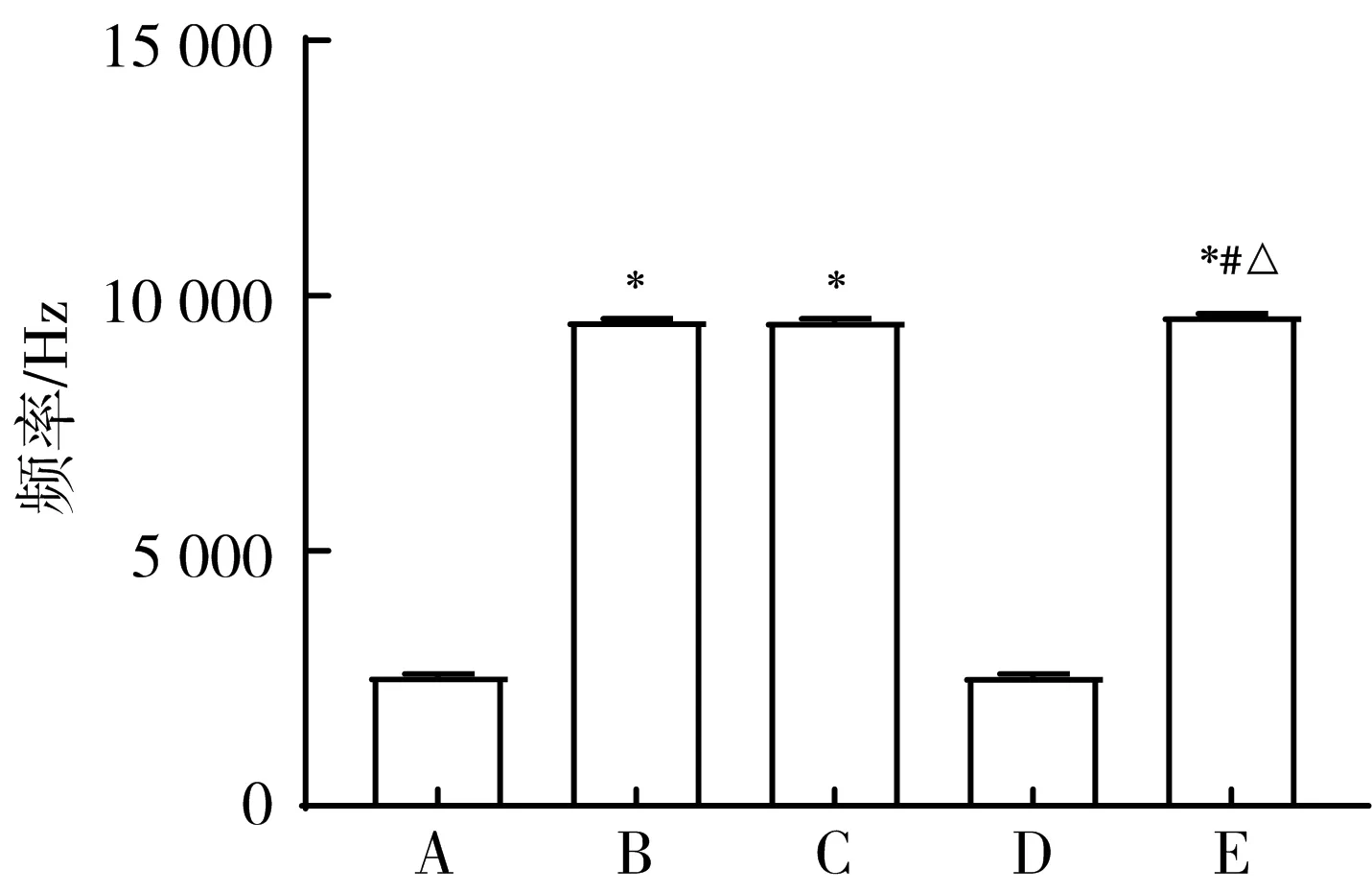
注:A.模型组;B.中脘组;C.胃俞组;D.非经非穴组;E.中脘+胃俞组;与模型组比较,*P<0.05;与中脘组比较,#P<0.05;与胃俞组比较,△P<0.05
4 讨论
胃扩张属于中医学“痞满”范畴,主要病因是由脾胃失调,正气受损。脾虚不升,胃弱不降,气机失和,致使胃脘胀满疼痛。主要表现为持续性胀痛,可有阵发性加重。针刺可改善胃扩张患者的胀痛等不适症状,且胃俞募穴相配使用效果优于单穴,俞募配穴法是始见于《黄帝内经》的一种取穴简便、配伍精炼的经典配穴方法,对临床疗效有显著影响。《难经·六十七难》:“五脏募皆在阴,而俞皆在阳者,何谓也?然阴病行阳,阳病行阴。故令募在阴,俞在阳。”俞募相配,脏病取腰背之背俞穴,腑病取胸腹之腹募穴,一阴一阳、前后相应,两穴相配有补虚化滞、理气健脾、强胃壮腑的功效。因此,当胃腑有病时,所属胃俞穴和中脘穴常配伍使用。研究发现,电针俞募配穴可以一定程度调节功能性消化不良大鼠胃排空率和胃泌素水平,改善胃运动。前期研究显示,电针胃俞募穴可调节正常大鼠、功能性消化不良模型大鼠的胃运动。本研究结果显示,电针胃俞募配穴可以加强胃扩张模型大鼠胃运动,并且俞募穴相配具有协同作用,与前期研究结果一致。
针灸治疗效果能够产生的关键原因之一就是腧穴配伍,腧穴配伍能够整合并部分增强单穴对胃肠激素的调节效应。边缘系统在腧穴配伍针刺调节胃运动中起着重要的作用,大脑-边缘系统是协调内脏-躯体行为的高级整合中枢,海马作为边缘系统的重要组成部分,能参与内脏活动,协调机体行为的变化,适应躯体活动和情绪反应。海马结构主要包括海马体、齿状回、下托,由CA1、CA2、CA3和CA4组成。信息进入海马时由齿状回流入CA3再经过CA1整合输出,边缘系统海马与下丘脑核团联系紧密,纤维投射复杂并广泛参与胃功能的调节,纤维自海马发出,经穹窿周区到达下丘脑,再经由中脑、脑桥、延髓和自主神经系统等逐级下传,参与调节胃运动。中医讲究辨证论治和整体观念,认为在机体中存在着脑与脏器的相互作用以及反馈调节机制。因此,脑功能与相关脏器功能间作用机制的研究将成为脑科学研究领域的热点,并兼具生物医学及临床实践意义。研究表明,海马CA1区神经细胞激活可对胃运动有调节作用。电生理实验发现,大鼠海马中有胃扩张敏感神经细胞,促进胃肠蠕动。c-fos蛋白参与多种神经细胞活动,c-fos的表达在脑内与海马、边缘系统等密切相关。基础状态下,c-fos蛋白在中枢神经系统的表达水平非常低甚至无表达,神经细胞受到外界刺激后会迅速表达c-fos,c-fos蛋白的表达通常被认为是神经细胞活动的重要标志。
胃运动实验结果提示,电针组和模型组振幅差异明显,胃俞募配穴的针刺信息参与了胃运动的调节;通过免疫荧光法在各组大鼠海马CA1区发现c-fos阳性表达,中脘和胃俞针刺信号聚集在海马CA1中。微阵列电极实验发现,电针能够刺激海马神经细胞产生电活动且放电明显。这说明胃扩张时海马区神经细胞放电频率下降,而电针逆转了此现象。实时频谱显示各组色彩的明暗和光谱的变化情况,清晰地展现出神经细胞放电活动在电针前后能量的高低变化。颜色越深说明局部场电位频谱能量越强,这与频率光栅图的变化趋于一致。海马CA1区神经细胞电活动参与了电针调节胃扩张模型大鼠胃运动的机制且具有随时间变化的特点。电针中脘穴和胃俞穴可以激活海马CA1区神经细胞,并且针刺信号可能在海马CA1区汇聚。胃扩张信号能够传入海马,电针俞募配穴的针刺信号也在海马CA1区汇聚,为海马参与胃功能调节提供直接依据。这表明胃扩张信号和针刺信号可在海马内发生作用,通过激活海马CA1区神经细胞活性参与调节胃运动。
综上所述,电针可以调节胃运动,且俞募配穴具有协同作用,海马CA1区可能是胃俞募配穴调节胃运动的具有代表性的中枢特异性靶点。因此,为深入研究针刺胃俞募配穴调节胃运动的中枢机制,下一步课题组拟聚焦海马CA1区orexin-A,海马是否通过orexin-A神经通路参与电针胃俞募穴对胃运动的调节作用,有待于进一步探讨。
