2型糖尿病合并腹型肥胖男性患者胰岛素抵抗与内脏脂肪面积相关性研究*
2020-06-11杨亚锋齐学林
杨亚锋,王 萍,王 利,齐学林
陕西省咸阳市中心医院(咸阳712000)
2017年全国进行横断面研究,随机抽样人数170287例进行2型糖尿病流行病学研究,新诊断糖尿病患病率6.9%,男性7.7%,女性6.1%。中国成人糖尿病患病率10.9%[1],男性和女性分别是11.7%、10.2%,并且40岁以下患病率高达5.9%,可是中国2型糖尿病发病年轻化。糖尿病在肥胖以及超重人群中的发病率分别为41%、24.3%[2]。由于人种的不同,体内脂肪积聚的部位不同,黄种人尤其是中国人更易在腹腔内积聚形成腹型肥胖,然而肥胖的程度却不及白种人。体重的增加,尤其腹围的增加均增加了胰岛素抵抗,其中内脏脂肪堆积引起面积的增加占主要原因。有研究显示,内脏脂肪增多患者血糖水平高于皮下脂肪增多患者,提示腹内脂肪对糖代谢的影响较皮下脂肪更为显著[3]。目前国内外研究或实验中常采用核磁共振或断层扫描(CT)测量内脏脂肪面积(Visceral fat area,VFA)。现代医学中常采用生物电阻抗精确测定内脏脂肪面积,我们采用与CT方法有较准确的相关性生物电阻抗法测量2型糖尿病合并腹型肥胖的男性患者内脏脂肪,探索内脏脂肪和胰岛素抵抗、血甘油三酯的关系,早期测量VFA,尽早评价其糖尿病等代谢指标,为糖尿病早期筛查及预防提供思路和方法,对胰岛素功能早期评价有一定指导意义,另外通过早期降低VFA减少胰岛素抵抗,也是一种促进胰岛素功能恢复的思路和有效方法。
对象和方法
1 研究对象 选择2型糖尿病合并腹型肥胖男性患者120例,静脉空腹血糖在3.9~6.1 mmol/L;血压在正常范围内。病例纳入标准:①年龄25~80岁;②依据2型糖尿病诊断标准(1999年)筛选均符合诊断的患者;③体重、身高均可测量或同意测量;④所入选的患者顺应性较好,配合度高,并签署告知书及知情同意书。病例排除标准:①空腹血糖较高,大于11.1 mmol/L;②存在糖尿病急性并发症或严重慢性并发症;③合并精神障碍者或沟通有障碍者、④合并妊娠者、装有心脏起搏器者、心脏功能及肝肾功能不全者;⑤ 1型糖尿病及成人晚发糖尿病等特殊类型糖尿病,并且除外合并高胰岛素血症患者。
2 研究方法 采用韩国进口人体成分分析仪(InbodyS10)测定所有入组患者VFA,根据不同的VFA分为三组:A组小于75 cm2,B组75~100 cm2,C组大于100 cm2。三组患者空腹血糖、血脂检查及血压比较均无统计学差异(均P>0.05),具有可比性。所有入组患者均禁饮食12 h,抽取静脉血送检检测糖化血红蛋白,采用美国贝克曼全自动生化分析仪(型号AU5800)对胰岛素抵抗指标β-抑制蛋白2运用比色法测定血清标本进行观察并进行统计分析比较。
3 观察指标 使用同仪器测量身高、体重,计算体质量指数(BMI)=体质量(kg)/身高(m)2。观察三组BMI、VFA、血压情况。静脉血观测糖化血红蛋白、血甘油三酯、β-抑制蛋白2。
4 统计学方法 选用SPSS23.0统计学软件分析,采用Pearson相关分析β-抑制蛋白2水平级代谢指标,采用多元线性回归分析β-抑制蛋白2相关影响因素。计量资料以均数±标准差表示,采用t检验;计数资料以率(%)表示,采用卡方检验。P<0.05表示差异具有统计学意义。
结 果
1 三组临床监测及生化指标比较 三组患者年龄、空腹血糖、血脂检查及血压、病程比较均无统计学差异(均P>0.05),具有可比性。见表1。
2 各组患者各实验室检测指标比较 三组糖化血红蛋白两两比较,无统计学差异(P>0.05);三组β-抑制蛋白2比较均有统计学差异(均P<0.05)。见表2。
3 β-抑制蛋白2相关影响因素的多元逐步回归分析 患者的VFA水平是血清β-抑制蛋白2水平的独立相关因素,甘油三酯水平不是血清β-抑制蛋白2水平的影响因素,见表3。
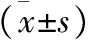
表1 入组患者一般资料及分组情况
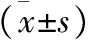
表2 三组人群生化指标及VFA比较
注:A组与C组比较,▲P<0.05;A组与B组比较,*P<0.05; C组与B组比较,△P<0.05;三组比较均有统计学差异。

表3 β-抑制蛋白2相关影响因素的多元逐步回归分析
讨 论
本研究中,对2型糖尿病合并腹型肥胖男性患者120例采用生物电阻抗方法测定VFA,根据不同的VFA分三组,A组小于75 cm2,B组75~100 cm2,C组大于100 cm2。三组β-抑制蛋白2比较均有统计学差异(均P<0.05),提示VFA越大,胰岛素敏感性越下降,胰岛素抵抗越强。β-抑制蛋白2相关影响因素的多元逐步回归分析显示,VFA水平是血清β-抑制蛋白2水平的独立相关因素,甘油三酯水平不是血清β-抑制蛋白2水平的影响因素。多项研究结果[4-5]也提示,内脏脂肪含量与 2 型糖尿病及胰岛素抵抗存在相关关系。Kang 等[6]通过生物电阻抗法对 24791 名志愿者进行 VFA 测量,结果显示男性 VFA 高于女性,VFA 与糖尿病、高血压病的发病率相关,并与 WHR、BMI、空腹血糖、TC、TG 及尿酸等代谢指标相关。肥胖与 IR 伴随发生,在糖尿病的独立危险因素中占据重要地位[7],两者互为因果,共同促进疾病发展。
2型糖尿病是一种由于胰岛细胞功能降低而导致的内分泌代谢疾病,以血糖的持续性升高为主要表现。而体内发病机制[8]主要有胰岛素抵抗及肥胖。近年来,国内外许多研究发现β-抑制蛋白2水平是胰岛素抵抗的危险因素[9]。内脏脂肪与β-抑制蛋白2有着负相关的关系。相关的动物学实验发现,缺乏β-抑制蛋白2基因的小鼠,能够加重其体内的胰岛素抵抗水平;为小鼠注射β-抑制蛋白2,则能够让小鼠的胰岛素敏感性得到恢复。当小鼠的体内缺少β-抑制蛋白2时,其体内的胰岛素无法使Akt和酪氨酸蛋白激酶(Src)与胰岛素受体结合,对胰岛素信号通路造成干扰,从而导致发生胰岛素抵抗[10]。β-抑制蛋白2与2型糖尿病和动脉粥样硬化等[11]多种疾病的发生和发展有着密切的关系。所以,评价胰岛素功能水平以及内脏脂肪对胰岛素抵抗的影响程度选用β-抑制蛋白2作为评价指标,得出的结论与相关研究结论一致。
人体脂肪分布因性别存在差异,男性体内脂肪占比约15%,一般认为,脂肪含量在男性超过25%,即为肥胖[12]。研究[13]表明,体重指数的快速增长与2型糖尿病的发生具有明显的相关性。研究[14]显示,尽管2型糖尿病各部分脂肪组织均存在胰岛素抵抗,但不同部位脂肪与胰岛素抵抗关系存在差异。腹型肥胖是糖尿病的危险因素,而内脏脂肪含量与糖代谢异常、胰岛素抵抗等密切相关。腹部皮下、腹腔内和腹膜后脂肪组织的脂肪分解代谢较其他部位的脂肪组织旺盛,这些部位的脂肪组织分解产生的游离脂肪酸较其他部位多,且此处的游离脂肪酸大多直接汇入门脉系统到达肝脏[15]。腹内脂肪组织释放过多游离脂肪酸从脂肪组织外溢,流向非脂肪细胞,如肝细胞、骨骼肌、胰岛细胞、心肌细胞、内皮细胞等,并在该处发生脂质的异位沉积,导致或加重这些细胞胰岛素抵抗,促进细胞凋亡,引发脂肪肝、糖尿病、内皮功能障碍和心血管疾病等[16]。游离脂肪酸会促进胰岛素分泌,降低胰岛β细胞的敏感性,长期会损害胰岛素分泌功能。长时间胰岛β细胞的损害将会加剧胰岛功能衰竭。刘峰等[17]的一项研究表明,BMI、腰臀比和糖尿病患病率有密切的关系,对糖尿病患病率有着密切的关系,对糖尿病发病有一定的预测功能。故在体重达到超重或肥胖、糖耐量异常以及空腹血糖调节受损的这一阶段,胰岛素抵抗、胰岛素敏感性降低已发生,早期控制体重及生活方式、药物等多因素干预,可以有效降低胰岛素抵抗,改善胰岛素功能,延缓糖尿病的发生发展,具有重要意义。对于体重正常但内脏脂肪增多的2型糖尿病也应该积极评估内脏脂肪,早评估、早预防、早干预,可以延缓或推迟不良事件的发生及发展。
目前,腹围是临床上常用衡量腹部脂肪的手段,但腹围较为笼统,不能区分内脏脂肪和皮下脂肪,不能准确反映内脏脂肪堆积的量。生物电阻抗测量法与目前的“金标准”[18]CT测量内脏脂肪面积VFA具有良好的相关性,并具有有操作简单、无创、无害等特点,而且测量结果准确、测量可重复性高。因此在临床工作中,因CT行腹部VFA测量时价格相对昂贵,不能常规监测VFA来预测胰岛素等代谢异常指标,可以用人体成分分析仪来筛选内脏脂肪肥胖的患者重点干预,早期预防。故在2型糖尿病合并腹型肥胖尤其是VFA超标的男性患者中,早期测量VFA,尽早评价其糖尿病等代谢疾病,对胰岛素敏感性以及胰岛素功能恢复有较好的指导意义,另外通过早期降低VFA减少胰岛素抵抗,也是一种思路和有效的方法。
