盐酸右美托咪定对颅内手术患者肾上腺素、去甲肾上腺素和S100β蛋白质浓度的影响
2015-12-18刘晓云,刘艳丽,刘晓等
盐酸右美托咪定对颅内手术患者肾上腺素、去甲肾上腺素和S100β蛋白质浓度的影响
刘晓云刘艳丽刘晓张岚张树立徐凯智
(华北理工大学附属唐山工人医院麻醉科河北唐山063000)
[摘要]①目的探讨盐酸右美托咪定对颅内肿瘤手术患者肾上腺素(E)、去甲肾上腺素(NE)和脑损伤标志物(S100β)蛋白浓度的影响。②方法随机选择颅内肿瘤手术患者30例。随机分为右美托咪定组(A组)和对照组(B组)两组,每组15例。A组在麻醉诱导前15min内静脉泵入右美托咪定1.0μg/kg,并以0.5μg/(kg·h)维持,B组患者泵入等体积的生理盐水。其他麻醉用药及剂量两组均相同。分别于全麻诱导前(T0)、手术开始(T1)、切开硬脑膜即刻(T2)、术毕(T3)、手术后1h(T4)5个时间点同步采集颈内静脉球部静脉血和桡动脉血进行血气分析,并检测静脉血E、NE、S100β蛋白的浓度。③结果B组患者E及NE在T1~T4浓度升高,与T0相比差异有统计学意义(P<0.05);A组的E及NE水平在T1~T4时间点低于B组,差异有统计学意义(P<0.05)。A组患者E及NE浓度在T2~T4时间点均低于T0,差异有统计学意义(P<0.05);两组患者的血浆S100β蛋白在T1~T4时间点均显著升高,与T0相比差异有统计学意义(P<0.05);A组患者S100β蛋白在T1~T4时间点低于B组,差异有统计学意义(P<0.05或P<0.01)。④结论右美托咪定通过降低颅内手术患者血浆E、NE和血浆S100β蛋白浓度,起到脑保护作用。
[关键词]颅内手术麻醉盐酸右美托咪定肾上腺素去甲肾上腺素S100β蛋白
[中图分类号]R 614
【作者简介】刘晓云(1989-),女,硕士研究生。研究方向:临床麻醉。
【通讯作者】徐凯智。
Effect of dexmedetomidine on epinephrine,norepinephrine and S100 protein in patients undergoing intracranial tumor surgeryLIUXiaoyun,LIUYanli,LIUXiao,etal(DepartmentofAnesthesiology,AffiliatedTangshanGongrenHospitalofNorthChinaUniversityofScienceandTechnology,Tangshan063000,China)
ABSTRACT[]ObjectiveTo study effect of dexmedetomidine on epinephrine and norepinephrine and damage markers(S100) protein in patients undergoing intracranial tumor surgery.Methods30 patients,undergoing intracranial tumor surgey were randomly divided into two groups:the dexmedetomidine group (group A)and the control group (group B),15 cases each group.Patients in group A,dexmedetomidine 1.0μg/kg were injected within 15 minutes before anesthesia induction,and continuous intravenous injection 0.5μg/kg·h,patients in group B was injected equal volume of physiological saline.Other narcotic drugs and dosage were consistent with the control group.Blood samples were obtained at before general anesthesia(T0),skin incision(T1),open dural immediately(T2),end of surgery(T3),1h after of the surgery(T4) synchronization acquisition of internal jugular vein ball and radial artery blood gas analysis respectively.Using ELISA method to detect venous blood E,NE,S100β protein.ResultsE and NE concentration in group B increased at T1~T4,compared with the T0,the difference was statistically significant(P<0.05);E and NE concentration at T1~T4 was lower than that of group C,there were significant difference between two group(P<0.05).E and NE concentration at T2~T4 are lower than T0 in group B.the difference was statistically significant(P<0.05);Compared with the Tm0,plasma S100 β protein at Tm1~T4 were significantly increased,the difference was statistically significant(P<0.05);S100β protein at T1~T4 in group A were significantly lower than that of group B,there were significant difference between two group(P<0.05 or P<0.01).ConclusionDexmedetomidine has a certain brain protection in the patients undergoing intracranial tumor surgey by reducing the serum E,NE and S100β protein.
[KEYWORDS]Intracranial operation.Anaesthesia.Dexmedetomidine.Epinephrine.Norepinephrine.S100β protein
脑组织高代谢、低储备的特点导致其在常温下对缺血缺氧的耐受能力低下。颅内肿瘤手术患者经常会因为肿瘤体积大而产生颅内压增高。脑细胞和组织的缺血缺氧、水肿和坏死等病理性改变,手术操作中电凝、电切、吸引等机械性刺激与体液失衡等医源性因素可以引起或加重脑缺血缺氧性损伤,甚至导致脑组织氧供需失衡及能量代谢障碍。因此,围术期脑保护及其防治措施一直以来是临床研究的热点和重点。本文探讨盐酸右美托咪定作为一种新型的高选择性α2肾上腺素能受体激动剂的脑保护作用。
1资料与方法
1.1一般资料本研究经我院伦理委员会审查和批准,并与患者签署知情同意书。选择行颅内肿瘤切除术患者30例,年龄28~65岁,体质量60~70kg。随机分为右美托咪定组(A组)和对照组(B组)。所有患者均为首次择期颅内脑膜瘤切除术,术前无明显颅内高压,无冠心病、糖尿病、肾脏疾病以及其他合并症。术中不应用吸入性麻醉药,剔除输血病例,术中不应用含糖的液体,以免对试验造成影响。
1.2麻醉方法麻醉前肌注阿托品0.5mg。局麻下行桡动脉穿刺置管和右颈内静脉穿刺并逆行置管至颈内静脉球部。两组患者均采用咪达唑仑-丙泊酚-苯磺酸阿曲库铵-芬太尼全麻诱导,全麻维持采用瑞芬太尼-丙泊酚-顺苯磺酸阿曲库铵静脉复合麻醉。A组在麻醉诱导前15min内缓慢静脉泵注右美托咪定1.0μg/kg,然后顺次缓慢静脉注射咪达唑仑(0.1~0.15)mg/kg,丙泊酚(1.5~2.0)mg/kg,芬太尼4μg/kg,阿曲库铵0.6mg/kg,吸氧去氮3min后气管插管,并采用丙泊酚-瑞芬太尼-顺阿曲库铵静脉复合液维持麻醉平稳,同时右美托咪定以0.5μg/(㎏·h)的速率维持;B组给予等容量的0.9%氯化钠溶液,其他用药均与A组相同。根据有创动脉压、心率、脑电双频谱指数(BIS)值和患者的反应等综合判断麻醉的深浅,通过增减麻醉药的用量维持麻醉平稳。
1.3监测指标常规监测ECG、心率(HR)、SPO2、平均动脉压(MAP)、BIS、IBP、体温、尿量、电解质和血气分析等。分别于全麻诱导前(T0)、手术开始(T1)、切开硬脑膜即刻(T2)、术毕(T3)、手术后1h(T4)5个时间点同步采集颈内静脉球部和桡动脉血进行血气分析并取血液标本5mL至真空试管,2000r/min,离心10min后,用移液器分别取0.4mL血浆加入1.2mL无水甲醇,混合均匀后12000r/min低温离心30min,用移液器取上清液体1mL,-80℃低温冰箱保存待测。颈内静脉球部静脉血E、NE和S100β蛋白浓度检测釆用ELISA法。

2结果
2.1两组患者一般情况比较两组患者的年龄、体质量、手术时间、麻醉时间、围术期麻醉药用量及其他用药和输液量均无明显差异(P>0.05),见表1。

表1 两组患者一般情况比较
2.2术中血压及心率的比较手术过程中两组患者MAP和HR均无明显差异(P>0.05),见表2。
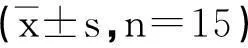
表2 两组患者不同时间点MAP和HR的比较
2.3两组患者血E、NE、S100β蛋白比较B组患者T1~T4时间点血E及NE水平均升高,与全麻诱导前基础值(T0)相比,差异有统计学意义(P<0.05),A组患者E及NE水平在T2~T4时间点也均低于T0,差异有统计学意义(P<0.05); A组血E及NE水平在T1~T4时间点较低于B组,差异有统计学意义(P<0.05)。两组患者的血浆S100β蛋白在T1~T4时间点均显著升高,与全麻诱导前基础值(T0)相比差异有统计学意义(P<0.05);A组患者S100β蛋白在T1~T4时间点均显著低于B组,差异有统计学意义(P<0.05或P<0.01),见表3。
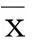
表3 两组患者不同时间点血浆E、NE和S100β蛋白质浓度比较( ±s)
注:与T0比较,aP<0.05,bP<0.01;与B组比较,cP<0.05
3讨论
神经外科手术中理想的脑保护药物不但应在一定程度上抑制脑细胞和组织的缺血缺氧、水肿和坏死等病理性改变,且要具备起效迅速、维持血流动力学及脑氧供需与能量代谢稳定、减少脑血容积(CBV)、降低颅内压、保持脑自身调节的功能。脑内的α2肾上腺素能受体主要集中在脑桥和延髓,参与交感神经信号从中枢向外周的传递。α2肾上腺素能受体激活是反射弧的必要成分,因此,α2肾上腺素能受体与周围及中枢自主神经的调节功能密切相关。动物实验表明,α2肾上腺素能受体缺陷可导致压力反射效率减低,即中枢α2肾上腺素能受体的激活具有加强压力反射活动的作用[1]。本研究表明,在麻醉期间应用右美托咪定后血浆E和NE浓度下降,说明右美托咪定通过抑制交感神经系统的活性使去甲肾上腺素能神经末梢儿茶酚胺类递质的释放减少,也可能直接作用于脑内的单胺能神经元胞体及树突上的α2肾上腺素能受体,减少儿茶酚胺类物质的释放,从而降低中枢及血浆中儿茶酚胺类物质的浓度,减轻神经元损伤,间接起到神经保护的作用。
右美托咪定可减少脑部血流量,同时降低大脑代谢率,并呈剂量依赖性地减少脑血流,降低大脑代谢率从而起到脑保护作用[2]。有学者在蛛网膜下腔出血兔的研究中发现,右美托咪定对海马神经元有保护作用[3],在沙土鼠短暂脑缺血试验中,其可防止局部缺血性神经损伤[4]。右美托咪定的神经保护作用机制各家言论不一,Huang等[5]的研究表明,右美托咪定能够促进星形胶质细胞对谷氨酸盐的代谢,减轻谷氨酸盐的神经毒性而起到脑保护作用。而Engelhard等[6]研究显示,脑缺血时周围循环中儿茶酚胺的浓度的增加受到右美托咪定的抑制,但是,神经保护作用和抑制颅内突触前去甲肾上腺素或谷氨酰胺释放并不相关。
S100β蛋白是一种小分子量酸性钙结合蛋白,高浓度存在于神经胶质细胞和中枢周围神经系统的Schwann细胞和Langerhans细胞以及垂体前叶细胞内,主要存在于中枢神经系统中,大多数由星形胶质细胞合成和分泌。瑞典学者Anderson等[7]的研究发现,即使影像学及人体检查未发现颅脑损伤的早期复合伤患者,其早期 S100β蛋白的浓度也升高,其浓度达2~10μg/L。由此可以认为,S100β蛋白可预示脑损伤的发生。Kapural等[8,9]则认为血清中检测到S100β蛋白也是血脑屏障受损的标志。本研究表明,右美托咪定组患者的S100β蛋白水平明显低于对照组,说明右美托咪定在一定程度上抑制了S100β蛋白的释放,可为多种脑缺血实验模型、高度可疑的神经损伤提供神经保护作用,减轻大脑手术中发生的低氧缺血性脑损伤,并且可以显著改善脑损伤后神经功能预后[10]。虽然其具体作用机制仍不清楚,但是本研究发现,给予右美托咪定,术中部分时间点血浆肾上腺素、去甲肾上腺素较对照组降低,这可能是由于儿茶酚胺通路发挥着重要作用,α2肾上腺素能受体可以调节中枢及外周的神经递质的释放,部分解释了其神经保护作用。
由脑缺血缺氧性损伤而导致的神经细胞的损伤并不是单一的病理生理过程,而是包含着许多复杂的生化级联反应。作为一种新型的麻醉辅助用药,右美托咪定的脑保护作用近年来越来越受到重视。右美托咪定的脑保护作用可能机制有:①抑制交感神经系统的活性使去甲肾上腺素能神经末梢儿茶酚胺类递质的释放减少,也可直接作用于脑内的单胺能神经元胞体及树突上的α2-AR,减少儿茶酚胺类物质的释放,从而降低中枢及血浆中儿茶酚胺类物质的浓度,减轻神经元损伤[11]; ②通过减少IL-1β、TNF-α的生成抑制炎性反应产生的,并呈现一定的剂量依赖性;③在脑缺血缺氧的情况下右美托咪定可以激活突触前膜Go蛋白耦联的α2-AR,直接抑制N型电压门控性钙离子通道的开放,使前膜内钙离子浓度降低;同时可激活Gi蛋白耦联的α2-AR,使外向型钾离子通道开放,突触前膜去极化,间接抑制钙离子内流;胞内钙离子浓度的下降阻止了谷氨酸的释放[12]; ④抑制了交感神经的活动,却相对地激活了胆碱能抗炎通路,从而发挥抗炎作用[13]; ⑤抑制手术中的应激反应,抑制交感-肾上腺素轴反应,降低血皮质醇浓度,使血皮质醇的浓度处于相对稳定的水平。
综上所述,右美托咪定作为一种围术期的镇静药和麻醉辅助用药,在维持麻醉中血流动力学平稳的同时,也达到了良好的脑保护效果。随着人们对右美托咪定在神经外科围术期脑保护作用机制的深入了解,相信其临床价值也会逐渐得到体现。
参考文献
[1]Niederhoffer N,Hein L,Starke K.Modulation of the baroreceptor reflex by alpha 2A-adrenoceptors:a study in alpha 2A knockout mice[J].Br J Pharmacol,2004,141(5):851-859
[2]Prielipp RC, Wall MH, Tobin JR, et al. Dexmedetomidine-induced sedation in volunteers decreases regional and global cerebral blood flow[J] Anesth Analg , 2002, 95(4):1052-1059
[3]Cosar M, Eser O, Fidan H, et al. The neuroprotective effect of dexmedetomidine in the hippocampus of rabbits after subarachmoid hemorrhage[J].Surg Neurol, 2009,71(1):54-59
[4]Kuhmonen J, Pokorny J, Miettinen R, et al .Neuroprotective effects of dexmedetomidine in the gerbil hippocampus after transient global ischemia[J].Anesthesiology,1997,87(2):371-377
[5]Huang R, Chen Y, Yu AC,et al. Dexmedetomidine-induced stimulation of glutamine oxidation in astrocytes: a possible mechanism for its neuroprotective activity[J].Cereb Blood Flow Metab,2000, 20(6):895-898
[6]Engelhard K, Werner C, Kaspar S, et al. Effect of the alpha2-agonist dexmedetomidine on cerebral neurotransmitter concentrations during cerebral ischemia in rats[J].Anesthesiology,2002, 96(2):450-457
[7]Anderson RE, Hansson LO, Nilsson O, et al. High serum S100β levels for trauma patients without head injuries[J].Neurosurgery,2001,48(6): 1255-1258
[8]Kapural M, Krizanac-Bengez LJ, Bamett G,et al. Serum S-100 beta as a possible marker of blood- brain barrierl dis-ruption[J].Brain Reserch,2002,940(1-2):102-104
[9]Ali MS, Harmer M,Vaughan R,et al. Serum SI00 protein as a marker of cerebral damage during cardiac surgery[J]. Br Anaesthsia,2000,85(2):287-298
[10]Ma D, Hossain M, Rajakumaraswamy N, et al. Dexmedetomidine produces its neuroprotective effect via the alpha2A-adrenoceptor subtype[J]. Eur J Pharmacol,2004,502:87-97
[11]Matsumoto M, Zornow MH, Rabin BC, et al. The alpha-2 adrenergic agonist, dexmedetomidine selectively attenuates ischemia-induced increases in striatal norepinephrine concentrations[J]. Brain Res, 1993,627(2):325-329
[12]Bickler PE, Hansen BM. Alpha-2 adrenergic agonists reduce glutamate release and glutamate receptor-mediated calcium changes in hippocampal slices during hypoxia[J]. Neuro- pharmacology, 1996,35(6);679-687
[13]Nance DM, Sanders VM. Autonomic innervation and regulation of the immune system (1987-2007)[J]. Brain Behav Immun, 2007, 21(6):736-745
(2015-04-28收稿)(岳静玲编辑)
