MMP2基因多态性与盐酸多奈哌齐治疗阿尔茨海默病的血药浓度和效果的关系
2024-04-08孙秀媛梁洪波
王 恒, 付 丹, 孙秀媛, 梁洪波
(徐州市东方人民医院1老年精神科, 2精神康复科, 江苏 徐州 221000)
盐酸多奈哌齐是乙酰胆碱酯酶抑制剂,在临床上用作轻中度阿尔茨海默病(Alzheimer′s disease,AD)的治疗[1]。在临床治疗过程中AD患者使用盐酸多奈哌齐的效果会产生较大差异,遗传因素是引起这种差异存在的重要原因[2]。盐酸多奈哌齐对 AD治疗疗效的评估主要采用简明精神状况(Mini-mental state examination,MMSE)量表,但这种效果评估检测只适用于患者开始盐酸多奈哌齐治疗3~4个月后,具有一定滞后性[3]。由于AD是一种神经退行性疾病,因此早期评估药物的治疗疗效对选择合适的治疗方案至关重要。基因单核苷酸多态性(Single nucleotide polymorphism,SNP)是人类可遗传变异中最常见的一种[4]。研究表明[5]CYP2D6、ABCA1基因SNPs与盐酸多奈哌齐治疗AD的疗效有关,但这些基因SNPs还不能完全解释盐酸多奈哌齐治疗AD效果的差异性。基质金属蛋白酶(Matrix metalloproteinase,MMP)引起的神经炎症与AD的发病和进展有关[6]。最近的研究表明[7],MMP2基因多态性与多种疾病的治疗治疗效果及不良反应有关。本研究探究MMP2基因单核苷酸多态性对AD患者盐酸多奈哌齐血药浓度和治疗效果的影响,现报道如下。
1 材料与方法
1.1 研究对象选择2020年1月-2023年1月徐州市东方人民医院老年精神科收治的97例AD患者为AD组,其中男性47例,女性50例,平均年龄(73.89±4.27)岁。纳入标准:(1)符合AD诊断标准的轻、中度患者[8];(2)年龄≥65周岁;(3)有稳定可靠的陪护人员,能够在研究过程内全程陪伴患者,并辅助研究者对患者进行认知障碍诊断。排除标准:(1)合并严重心脏血管疾病、肝、肾功能不全;(2)患有恶性肿瘤;(3)重度痴呆、伴意识障碍、患抑郁症或精神分裂症;(4)入组前半年内长期服用胆碱酯酶抑制剂、抗焦虑药、安眠药等其他影响认知功能的药物;(5)对盐酸多奈哌齐不耐受;(6)依从性差或中途退出研究者。选取同期在我院进行体检的100名健康老年人为健康对照组,其中男性50名,女性50名,平均年龄(73.02±4.61)岁。两组性别、年龄比较差异无统计学意义(P>0.05)。本研究通过徐州市东方人民医院医院伦理委员会批准,所有患者家属均签署知情同意书。
1.2 方法
1.2.1 治疗及疗效评估方法 AD组入院后口服盐酸多奈哌齐5 mg/d,连续30 d。所有依从性良好(定期服药且无相关药物不良事件)的患者将盐酸多奈哌齐剂量增加至10 mg/d,连续150 d。于治疗前及治疗6个月后,由同一位临床主治医师采用MMSE量表对患者的认知功能进行评估。若最后一次MMSE评分与第一次MMSE评分相比没有下降,即为应答者,否则为未应答者。
1.2.2 盐酸多奈哌齐血浆浓度的测定 在最后一次用药后24 h采集AD组的空腹静脉血,保存在-20℃条件下备用。采用高效液相色谱-串联质谱联用法测定患者的血浆盐酸多奈哌齐浓度,并记录。
1.2.3 MMP2基因分型检测 治疗前抽取AD组和健康对照组空腹静脉血2 mL置于EDTA抗凝管中,采用改良苯酚-氯仿方法从经EDTA处理的全血样本中提取AD患者和健康对照组的DNA。采用PCR和限制性片段长度多态性分析检测MMP2基因rs243865(C>T)、rs2285053(C>T)分型。引物序列如下:rs243865:上游引物:5′-ATTGGTGA-
GGCTTAGTTAATGATA-3′,下游引物:5′-AAG-
TTGTTCTCTATGTATTGTCATA-3′,扩增产物长度为102 bp;rs2285053:上游引物:5′-CTAGTGTACACCTATTCATG-3′,下游引物:5′-ACACTTCATTTGGATACCGC-3′,扩增产物长度为98 bp。PCR扩增采用三步法进行,反应条件为:95℃条件下预变性5 min;95℃条件下变性10 s,55℃条件下退火30 s,72℃条件下延伸45 s,共扩增35个循环。使用1.5%的琼脂糖凝胶电泳对PCR扩增产物的完整性进行检测。
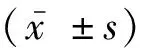
2 结果
2.1 AD组和健康对照组MMP2基因位点基因型分布的比较与健康对照组比较,AD组MMP2基因rs243865、rs2285053基因型分布差异均无统计学差异(P>0.05),rs243865位点遗传模型、rs2285053位点相加模型、隐性模型差异均无统计学意义(P>0.05),rs2285053位点显性模型差异有统计学意义(P<0.05),见表1。

表1 AD组和健康对照组MMP2基因位点基因型分布的比较
2.2 应答组和未应答组一般资料的比较与未应答组比较,应答组性别、年龄、病程、BMI和基线MMSE得分差异无统计学意义(P>0.05),见表2。
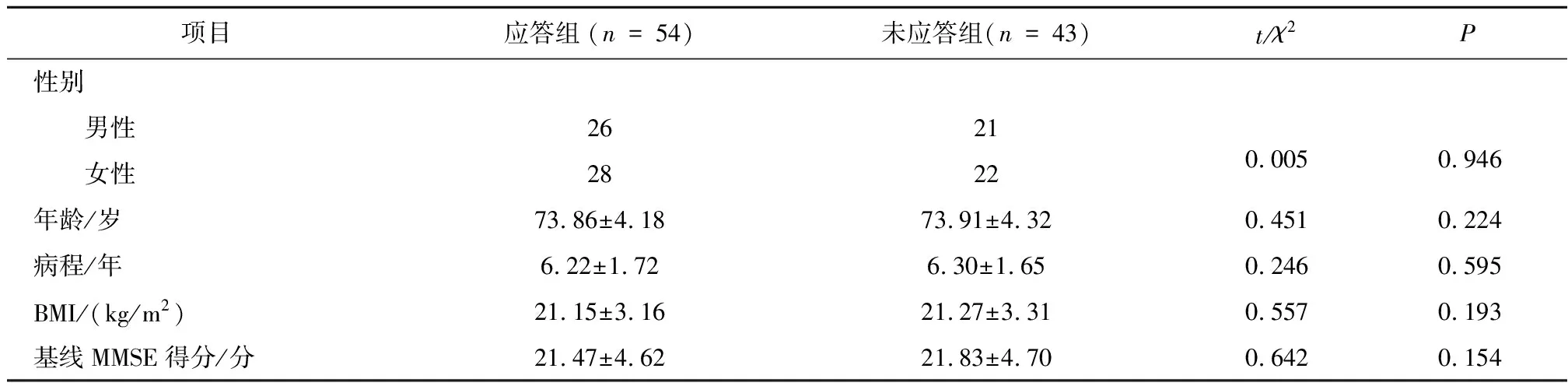
表2 应答组和未应答组一般资料的比较
2.3 应答组和未应答组MMP2基因位点多态性比较与未应答组比较,应答组MMP2基因rs243865基因型分布、遗传模型及隐性模型差异均无统计学意义(P>0.05),rs2285053位点相加模型、显性模型差异有统计学意义(P<0.05),见表3。
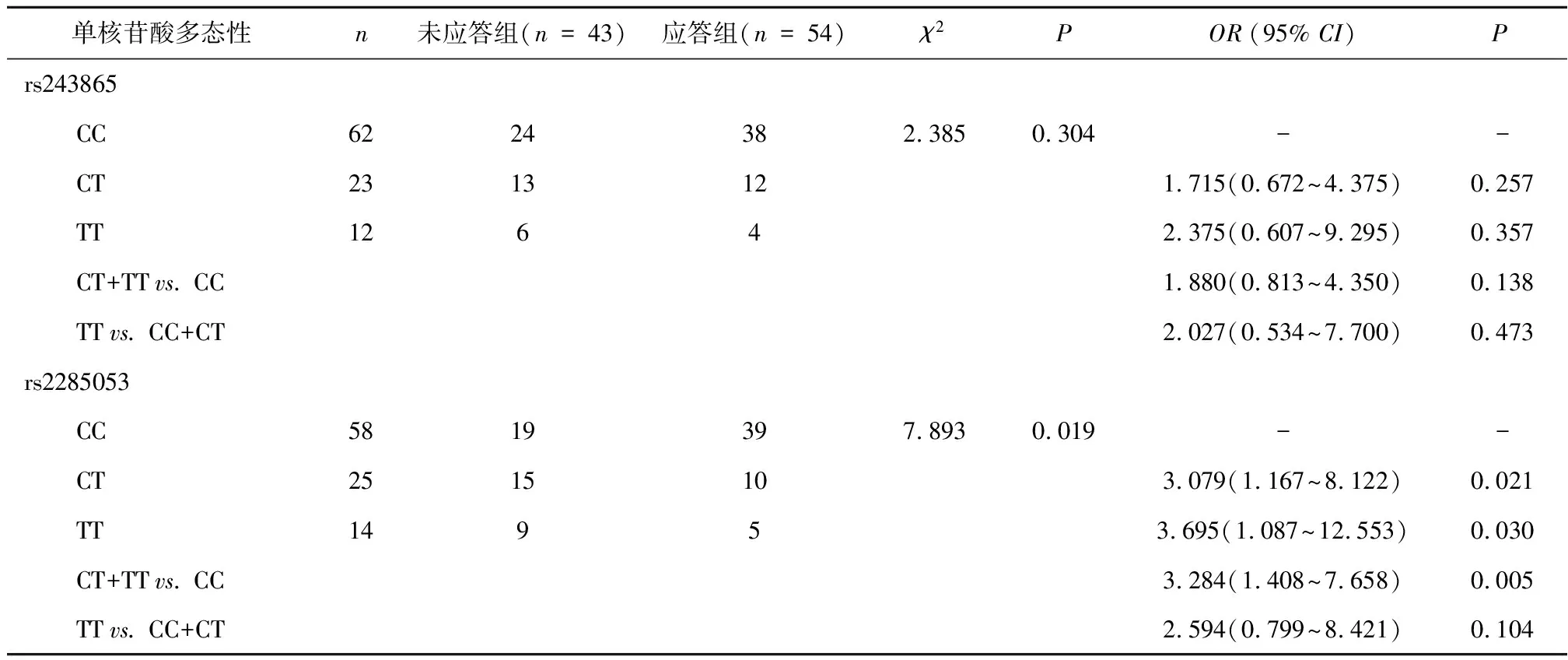
表3 不同治疗效果AD患者的MMP2基因位点多态性比较
2.4 AD患者MMP2基因位点多态性与盐酸多奈哌齐血药浓度的关系不同MMP2基因位点rs243865位点基因型AD患者的盐酸多奈哌齐血药浓度比较差异无统计学意义(P>0.05)。与rs2285053位点TT基因型AD患者比较,CC、CT基因型患者的盐酸多奈哌齐血药浓度增大,差异有统计学意义(P<0.05),见表4。
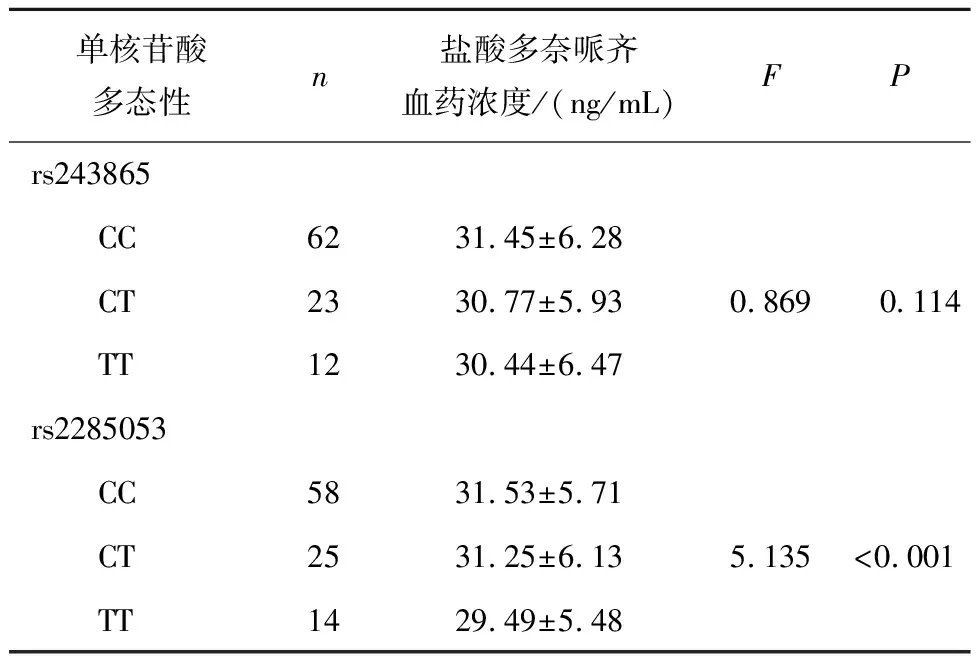
表4 AD患者MMP2基因位点多态性与盐酸多奈哌齐血药浓度的关系
2.5 应答组和未应答组盐酸多奈哌齐血药浓度的比较未应答组的盐酸多奈哌齐血药浓度为(30.82±6.02)ng/mL,应答组的盐酸多奈哌齐血药浓度为(31.44±5.82)ng/mL,差异无统计学意义(t=1.276,P=0.106)。
3 讨论
盐酸多奈哌齐对AD患者的治疗效果有差异,部分患者经盐酸多奈哌齐治疗后效果欠佳[8-9]。研究表明[10-12],遗传背景是造成这种差异出现的重要原因。本研究结果显示,AD组和健康对照组的MMP2基因rs2285053位点的显性模型比较差异有统计学意义,即携带T等位基因是AD发生风险增高的危险因素,使AD发生风险上升了1.914倍。Ocenasova等[13]研究显示,MMP2基因多态性与AD患者的发病年龄有关,发生MMP2基因变异的AD患者发病年龄显著提前。另一项研究[14]显示rs2285053位点T等位基因与HIV相关神经认知障碍的易感性存在显著关联。
本研究发现MMP2基因rs2285053多态性对盐酸多奈哌齐治疗AD的效果和血药浓度有影响。相较于携带野生型CC基因型的AD患者,携带T等位基因(CT或TT患者)的AD患者对盐酸多奈哌齐治疗后未应答的风险显著增高,且血药浓度显著降低。研究表明,MMP2基因变异与心脏瓣膜置换术后华法林治疗疗效有关[6],MMP2基因多态性与卵巢癌含铂化疗方案的治疗疗效及不良反应有关[7]。rs243865和rs2285053位点位于MMP2基因启动子区,其等位基因C与T的变异可对其与转录因子的结合产生干扰。与携带等位基因C的患者相比,携带T等位基因的AD患者因MMP2基因rs243865位点与转录因子结合受阻,启动子活性减低,从而使MMP2的转录活性降低,导致MMP2基因表达水平下降[15]。本研究分析MMP2基因rs2285053位点变异影响盐酸多奈哌齐治疗AD患者疗效和血药浓度的原因如下:(1)MMP2基因的rs2285053位点变异可导致酶活性的变化。MMP2是一种金属基质蛋白酶,在AD患者的脑组织中表达增加,该位点的变异通过影响MMP2的活性,从而影响AD患者大脑中淀粉样蛋白的清除和神经元的损伤。(2)MMP2基因的rs2285053位点变异对影响盐酸多奈哌齐的代谢造成影响。盐酸多奈哌齐是一种胆碱酯酶抑制剂,用于治疗AD。该药物在体内通过多种酶进行代谢,包括胆碱酯酶和肝药酶。MMP2基因的变异通过影响酶的活性,从而影响盐酸多奈哌齐的代谢和疗效。因此,对于携带MMP2基因rs2285053位点T等位基因的AD患者,应用盐酸多奈哌齐治疗的效果有限。
综上所述,MMP2基因rs2285053位点变异会影响盐酸多奈哌齐治疗AD的血药浓度和疗效,对于临床治疗用药的指导具有一定价值。
