多参数监护仪不良事件的影响因素分析
2024-01-17桑元顺杨昭霞邵琳雯胡晓梅
桑元顺,杨昭霞,杨 玲,邵琳雯,胡晓梅
(1.镇江市第四人民医院,镇江市妇幼保健院设备科,江苏 镇江 212001 ;2.镇江市第四人民医院,镇江市妇幼保健院神经外科,江苏 镇江 212001 ;3.镇江市食品药品监督检验中心,江苏 镇江 212001)
多参数监护仪是通过传感器采集人体生理信号,持续监测患者心电图(ECG)、心率(HR)、血氧饱和度(Sp02)及血压(BP)等重要参数的设备[1],是临床监测的重要设备之一。不安全医疗导致的不良事件已成为患者死亡和残疾的十大原因之一,其中发展中国家每年因不安全医疗造成260 万人死亡[2]。2021年,国家药品不良反应监测中心调查显示,医用诊察和监护器械类不良事件的报告数量排名第二,共63 385 份,占10.80%,导致严重伤害、死亡共36 773份,占5.66%[3]。由于医疗机构是使用医疗器械的主体,也是医疗器械不良事件上报的主体[3]。因此,监测医疗器械不良事件可加强器械管理,维护患者安全。目前有研究对多参数监护仪不良事件进行分析,总结出黑屏、无法测量血压、血氧探头故障等常见不良事件,但尚未采用统计学方法进一步分析,结果具有一定偏倚性。本研究旨在对我院中多参数监护仪不良事件发生情况及影响因素进行深入的研究,为保障患者用械安全提供理论与决策依据。
1 对象与方法
1.1 调查对象
采用整群抽样法调查2022 年1 月1 日—2023 年4 月11 日在我院使用多参数监护仪的医疗单元,包括新生儿科、急诊重症监护室等。纳入标准:(1)我院所有使用多参数监护仪的医疗单元;(2)医护人员知情同意参与本研究。排除标准:(1)电脑胎儿监护仪相关数据;(2)上报不规范;(3)错误的数据。根据样本量为协变量数10 ~15 倍计算[4],其中协变量(X)为6,按15 倍计算,考虑上报不规范和错误数据,将样本量扩大20%,计算出样本量为108 例。本研究共调查201 例,收集调查表201 份,有效率为100%,排除电脑胎儿监护仪2 例,最终纳入199 例。
1.2 调查工具
根据国家医疗器械不良事件监测信息系统的调查项目,结合已发表的文献自行设计调查问卷。调查内容主要包括:病区、患者姓名、预期治疗疾病及作用、器械故障表现、主要伤害、事件后果、事件陈述、医疗器械注册证号、生产企业名称、型号规格、产品编号、事件初步处理情况、患者性别、患者年龄、器械生产日期、曾用注册证编号上报情况、产地、管理类别。
1.3 资料收集方法
镇江市药品不良反应监测中心与我院联合组成领导小组,小组成员包括副院长、设备科科长、护理部主任等,各病区护士长任监测员,负责上报不良事件。设备科专职监测员当日核对、确认数据,定期通过国家医疗器械不良事件监测信息系统向市药品不良反应监测中心上报相关数据。为避免因上报人员不同而产生差异,由护理部与设备科联合,在全院进行调查内容、注意事项等培训。对数据收集过程中的问题及时沟通协调,确保规范上报,保证调查质量。
1.4 统计学方法
使用Excel 2016 进行双人录入,确保信息准确。采用SPSS 23.0 软件进行分析。呈正态分布的计量资料采用均数± 标准差表示,进行两样本比较t检验;非正态分布的计数资料以率(%)表示,进行χ² 检验。本研究中,因变量为二分类,故采用二元Logistic回归分析,P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料
共收集199 例数据,男101 例,女98 例;国产134 例,进口65 例;Ⅱ类83 例,Ⅲ类116 例;曾用注册证编号上报79 例,曾用注册证编号未上报120 例;年龄1 ~95 岁,平均年龄(43.36±27.574)岁;生产日期2012—2023 年。
2.2 不良事件发生情况的单因素分析
本研究中共有97 例发生不良事件,85 例为一般不良事件,12 例为严重不良事件。单因素分析结果显示,未发生多参数监护仪不良事件组与发生多参数监护仪不良事件组多参数监护仪曾用注册证编号上报情况、多参数监护仪生产日期、患者年龄的差异有统计学意义(P<0.05)。未发生多参数监护仪不良事件组与发生多参数监护仪不良事件组患者性别、多参数监护仪产地、多参数监护仪管理类别的差异无统计学意义(P>0.05)。见表1。
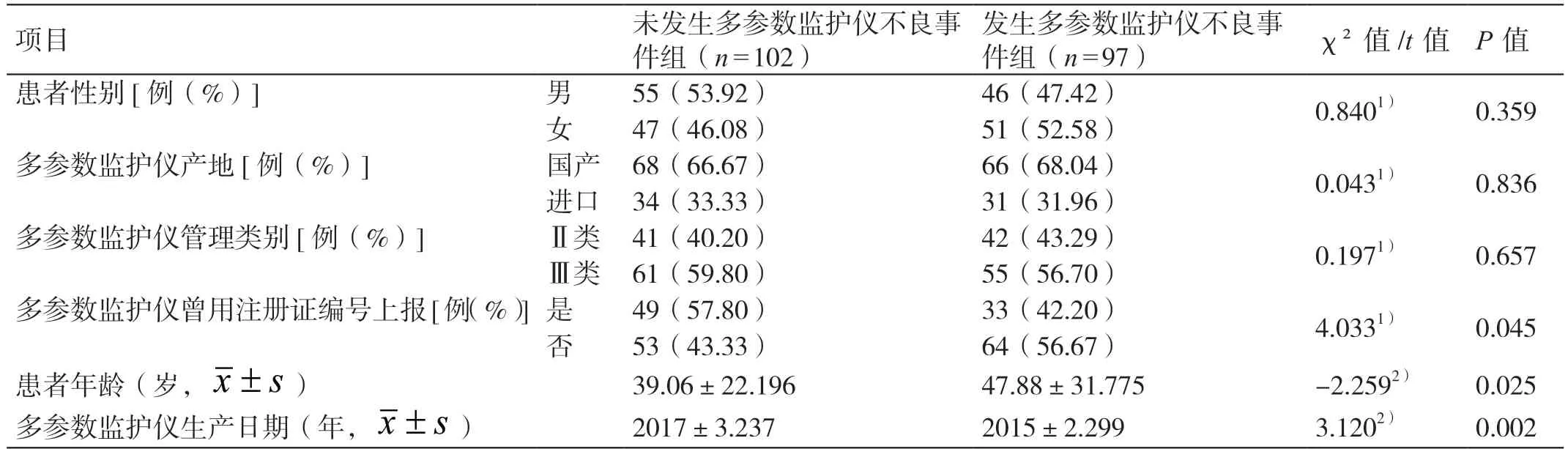
表1 发生不良事件单因素分析
2.3 不良事件发生情况二元Logistic 回归分析
逐步回归法结合了前进法和后退法两种,既考虑引入变量又考虑剔除变量[5],因此本研究采用逐步回归法,将患者性别、多参数监护仪产地、多参数监护仪管理类别、多参数监护仪曾用注册证编号上报情况、患者年龄、多参数监护仪生产日期作为自变量,以是否发生不良事件为因变量进行二元Logistic 回归分析,结果发现,多参数监护仪生产日期、患者年龄、多参数监护仪曾用注册证编号上报情况是多参数监护仪不良事件的影响因素。见表2。
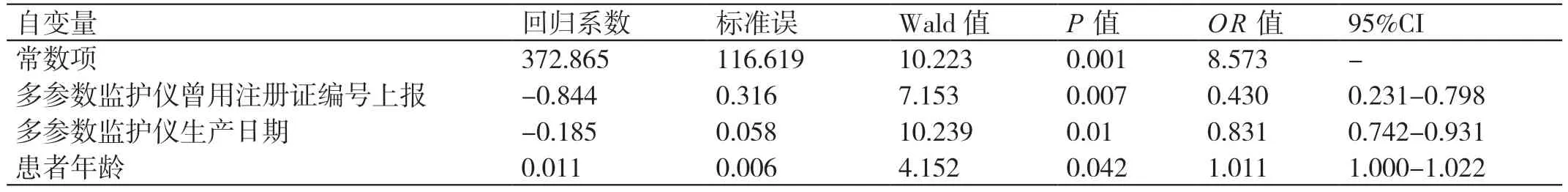
表2 不良事件发生情况的Logistic 回归分析
3 讨论
3.1 多参数监护仪不良事件影响因素的实用价值及意义
多参数监护仪是目前医院常用的医疗器械之一,一旦发生不良事件可能会影响患者生命体征的监测,甚至会威胁患者的生命安全[6-7]。推进多参数监护仪不良事件监测不仅可以挖掘潜在风险信号,降低使用医疗器械相关风险,保障公众用械安全,而且符合中国医院协会发布的《中国医院协会患者安全目标(2022版)》[8]、市场监督管理总局发布的《医疗器械使用质量监督管理办法》[9]、国家卫健委发布的《多参数监护仪安全管理》[10]等政策。此外,由设备科专员在国家医疗器械不良事件监测信息系统上报不良事件,可促进使用多参数监护仪的医务人员与国内外生产厂家的沟通联系,实现信息交换。综上所述,调查多参数监护仪不良事件影响因素具有较强的实用价值及意义。
3.2 多参数监护仪不良事件的发生情况
本研究共收集多参数监护仪不良事件97 例,其中85 例为一般不良事件,12 例为严重不良事件。赵亚丽等[11]调查的长沙市第四医院近六年348 例医疗器械不良事件中,多参数监护仪不良事件仅50 例,其中严重不良事件0 例。蔡权周等[12]通过对多参数监护仪不良事件进行上报、处理、分析和改进干预减少了多参数监护仪不良事件的发生。本院上报的多参数监护仪不良事件的数量较多,这主要是由于本院推行“护理安全(不良)事件报告”制度,实行非惩罚性上报,并予以对应奖励。
3.3 多参数监护仪不良事件的影响因素分析
本研究结果显示,患者年龄是多参数监护仪不良事件的影响因素。进入老年期后,患者的机体老化,组织器官功能衰退,高血压、食管癌等疾病的患病率增加[13-15]。因此,在对年龄较大的患者采用多参数监护仪进行监护时,应注意多观察,以准确采集患者的生命体征,及时识别不良事件。此外,有曾用注册证编号上报情况的多参数监护仪、生产日期较早的多参数监护仪其不良事件的发生率较高。可见,多参数监护仪不良事件与仪器本身有关[16-17]。故在使用有曾用注册证编号上报情况的多参数监护仪、生产日期较早的多参数监护仪时,应加强不良事件的监测。
4 小结
推行多参数监护仪不良事件监测具有较强的实用价值及意义,可降低使用医疗器械相关风险,且符合当前国家政策。多参数监护仪有曾用注册证编号上报情况、多参数监护仪的生产日期早、患者年龄大是多参数监护仪不良事件的影响因素。多参数监护仪不良事件是多种因素共同作用的结果,科室应重视对使用时间较长的、有曾用注册证编号上报情况的多参数监护仪的监测。同时,应提高对使用多参数监护仪高龄患者的重视程度。本研究仅选择一家医院,样本代表性有限,且样本量较少。因此,今后需扩大样本量,进一步研究影响多参数监护仪不良事件的因素。
