不同碱源对合成MgAl-LDHs 的结构及除氯性能的影响
2023-12-22易春健刘淑贤聂轶苗
易春健 刘淑贤 黄 宏 聂轶苗 王 玲 王 龙
(1.华北理工大学矿业工程学院,河北 唐山 063210;2.河北省矿业开发与安全技术重点实验室,河北 唐山 063210)
随着采矿、石油化工、冶金、化学制药等行业的快速发展,工业废水排放量逐年升高,对人类生存环境造成潜在威胁[1]。 目前,在工业废水处理领域,废水处理的关键就在于高盐废水的处理。 而其中最突出的问题之一就是氯离子浓度过高,现有处理工艺较难去除[2]。 水体中的高浓度氯离子的危害主要有影响动植物和微生物的生长、腐蚀金属工业设备、缩短建筑材料的服役寿命等,因此含氯废水的处理一直是国内外学者关注的热点。 吸附法是去除废水中氯离子的有效方法,尽管在以往的研究中开发了几种吸附剂,包括沸石[3]、改性粉煤灰[4]、壳聚糖[5]、树脂[6]等,但由于这些材料的吸附容量低、吸附反应时间长,仍需要开发具有高吸附性能的材料。
类水滑石具有二价和三价阳离子与阴离子夹层的独特层状结构,相比于沸石、改性粉煤灰等吸附剂,不但具有优异的化学稳定性与阴离子交换能力,而且还可通过其“记忆效应”回收重复利用,因此可作为水中阴离子的极佳吸附剂[7]。 此外,类水滑石的制备过程可以完美调控,这一特性对其在含氯废水处理中具有重要意义[8]。 类水滑石的制备方法有共沉淀法[9]、水热法[10]、成核晶化法[11]等,其中共沉淀法使用最为广泛,江晓[12]采用共沉淀法制备了镁铝类水滑石,其中硝酸根插层的镁铝类水滑石对氯离子吸附容量达到32.32 mg/g。 张万有等[13]通过共沉淀法制备了镁铝铁三元类水滑石,并将其负载于斜发沸石上,焙烧后的类水滑石对氯离子吸附容量可达36.8 mg/g。 然而,有研究发现[14-15],水热法合成的晶体结晶度和比表面积均高于共沉淀法,归因于水热法在封闭条件下进行反应,不会引入杂质离子,因此采用水热法制备类水滑石除氯具有较好的可行性[16],而采用水热法制备类水滑石对其结构及除氯性能的影响研究十分有限。 水热法最常用的碱源为尿素和氢氧化钠,其中尿素受热易分解,可能会对合成的类水滑石结构及除氯性能有影响,因此研究这2 种碱源对合成类水滑石结构及除氯性能的影响很有必要。
为了探究不同碱源对水热法制备类水滑石结构及除氯性能的影响,本文以尿素、氢氧化钠为碱源,通过水热法制备了2 种类水滑石,采用XRD、SEM、N2吸附-脱附、傅立叶变换红外光谱等分析方法对2 种类水滑石的微观形貌进行了表征;通过吸附动力学方程、吸附等温模型和吸附前后的XRD 和傅立叶变换红外光谱对比考察了2 种类水滑石对氯离子的吸附性能和除氯机理。 研究表明,以氢氧化钠为碱源,通过水热法制备的类水滑石吸附容量可达67. 58 mg/g,远超过共沉淀法制备的类水滑石。
1 试验材料及方法
1.1 试剂和仪器
Mg(NO3)2·6H2O、Al(NO3)3·9H2O、CO(NH2)2、NaOH、NaCl、HNO3,均为购于麦克林公司的分析纯试剂。 D/MAX2500PC 型X 射线衍射仪,日本理学株式会社;JW-BK112 型比表面积及孔径分析仪,北京精微高博仪器有限公司;Scios 型聚焦离子束场发射扫描电子显微镜,FEI 捷克有限公司;Thermo Scientific Nicolet iS20 傅里叶变换红外光谱仪,美国赛默飞世尔公司;PCL-1 型氯离子浓度计,上海盛磁仪器有限公司;PHS-25 型pH 计,上海仪电科学仪器股份有限公司。 含氯模拟废水:采用NaCl 配制。
1.2 类水滑石的制备
采用水热法分别制备不同碱源的类水滑石,具体步骤为:按n(Mg2+)∶n(Al3+)= 3 ∶1(Mg2+浓度为0.5 mol/L)将Mg(NO3)2·6H2O、Al(NO3)3·9H2O 混合溶于50 mL 去离子水中得到溶液A。 按n(尿素) ∶n(NO-3)= 2 ∶1 将尿素溶于50 mL 去离子水中得到溶液B1,按n(NaOH):n(NO-3)= 2 ∶1 将NaOH 溶于50 mL 去离子水中得到溶液B2。 将溶液A 与溶液B1、B2分别混合后加入到烧杯中,在60 ℃下磁力搅拌30 min,将搅拌好的溶液转移到内衬为聚四氟乙烯的反应釜中,放入烘箱,在100 ℃下恒温晶化18 h,将反应釜取出并冷却至室温。 将所得沉淀抽滤,同时用去离子水冲洗至中性,在80 ℃下干燥8 h 得到2 种产物,以尿素为碱源记作LDHs-A,以NaOH 为碱源记作LDHs-B。
1.3 类水滑石的表征
采用XRD、SEM、N2吸附-脱附、傅立叶变换红外光谱等分析方法对类水滑石进行表征。
1.4 氯离子吸附试验
在2 个盛有100 mL 一定浓度氯化钠溶液的锥形瓶中,分别加入一定质量的LDHs-A 和LDHs-B。 将上述锥形瓶放在磁力搅拌器上,在30 ℃下以200 r/min 的搅拌速率搅拌一定时间后过滤,取上清液,用氯离子浓度测定仪测定上清液氯离子质量浓度,并分别按式(1)、式(2)计算得到氯离子吸附量和氯离子去除率。
式中,q为单位质量类水滑石对氯离子的吸附量,mg/g;C0为氯离子的初始质量浓度,mg/L;Ce为吸附后氯离子的质量浓度,mg/L;V为溶液体积,L;m为类水滑石质量,g;Y为氯离子去除率,%。
2 试验结果与讨论
2.1 类水滑石的表征
2.1.1 XRD 分析
图1 为LDHs-A 和LDHs-B 的XRD 图谱。
由图1 可知,2 种类水滑石的衍射峰基线都比较平稳,峰形较窄且尖锐,无明显杂峰,代表类水滑石层状结构的特征衍射峰(003)峰形尖锐,强度较强,说明2 种类水滑石的结晶度较高,结晶相单一,晶体结构完整。 其中,LDHs-A 在(003)衍射峰处的强度比LDHs-B 的强,说明以尿素为碱源得到的类水滑石具有更好的结晶度,晶体发育更好。 分析认为尿素受热分解缓慢释放氨,使得溶液内部pH 值保持恒定,有利于晶体的生长[17]。 从图1 可以看出,LDHs-A 在2θ=11. 67°、23. 51°、34. 92°、39. 48°、47. 06°、60. 87°、62.21°左右出现7 个相对强度较大的特征衍射峰,分别对应(003)、(006)、(012)、(015)、(018)、(110)、(113)晶面,而LDHs-B 在2θ=11.14°、22.42°、34.12°左右出现3 个相对强度较大的特征衍射峰,分别对应(003)、(006)、(009)晶面。
可以发现,LDHs-B 的特征衍射峰比LDHs-A 整体均往低角度偏移,其中特征峰(003)代表着类水滑石的层间距,根据布拉格(公式(3)),计算得到LDHs-B 的层间距为0.794 nm,而LDHs-A 的层间距为0.762 nm。
式中,d为晶面间距;θ为入射线,°;λ为波长,0.154 056 nm;n为反射级数,一般取1。
硝酸根插层镁铝类水滑石层间距为0.80 nm 左右[18],而碳酸根插层镁铝类水滑石层间距为0. 76 nm 左右[19-20]。 将LDHs-A 与碳酸根插层类水滑石标准PDF 卡片(#89-0460)对比,LDHs-B 与硝酸根插层类水滑石标准PDF 卡片(#50-1892)对比,特征衍射峰位置一致。 因此,分析认为LDHs-A 为碳酸根插层镁铝类水滑石,LDHs-B 为硝酸根插层镁铝类水滑石,LDHs-A 的碳酸根来源是尿素分解产生的二氧化碳。
2.1.2 SEM 分析
图2 为LDHs-A 和LDHs-B 的扫描电镜图。
从图2 可以看出,2 种材料均有明显的层状结构,LDHs-A 为花瓣状片层堆积的结构(图2(a)),LDHs-B 为松散堆砌的蜂窝状结构(图2(c)),LDHs-A 的颗粒形状近似于六边形(图2(b)),而LDHs-B的颗粒形状则更接近椭圆形(图2(d))。 LDHs-A 和LDHs-B 晶粒尺寸分别为1 000~2 000 nm、200~400 nm,LDHs-A 的晶粒尺寸明显比LDHs-B 的晶粒尺寸大,这进一步说明,以尿素为碱源可以获得结晶度更高、晶粒尺寸更大的类水滑石。
2.1.3 N2 吸附-脱附等温线和孔径分布
图3 为2 种样品的N2吸附-脱附等温线和孔径分布图。
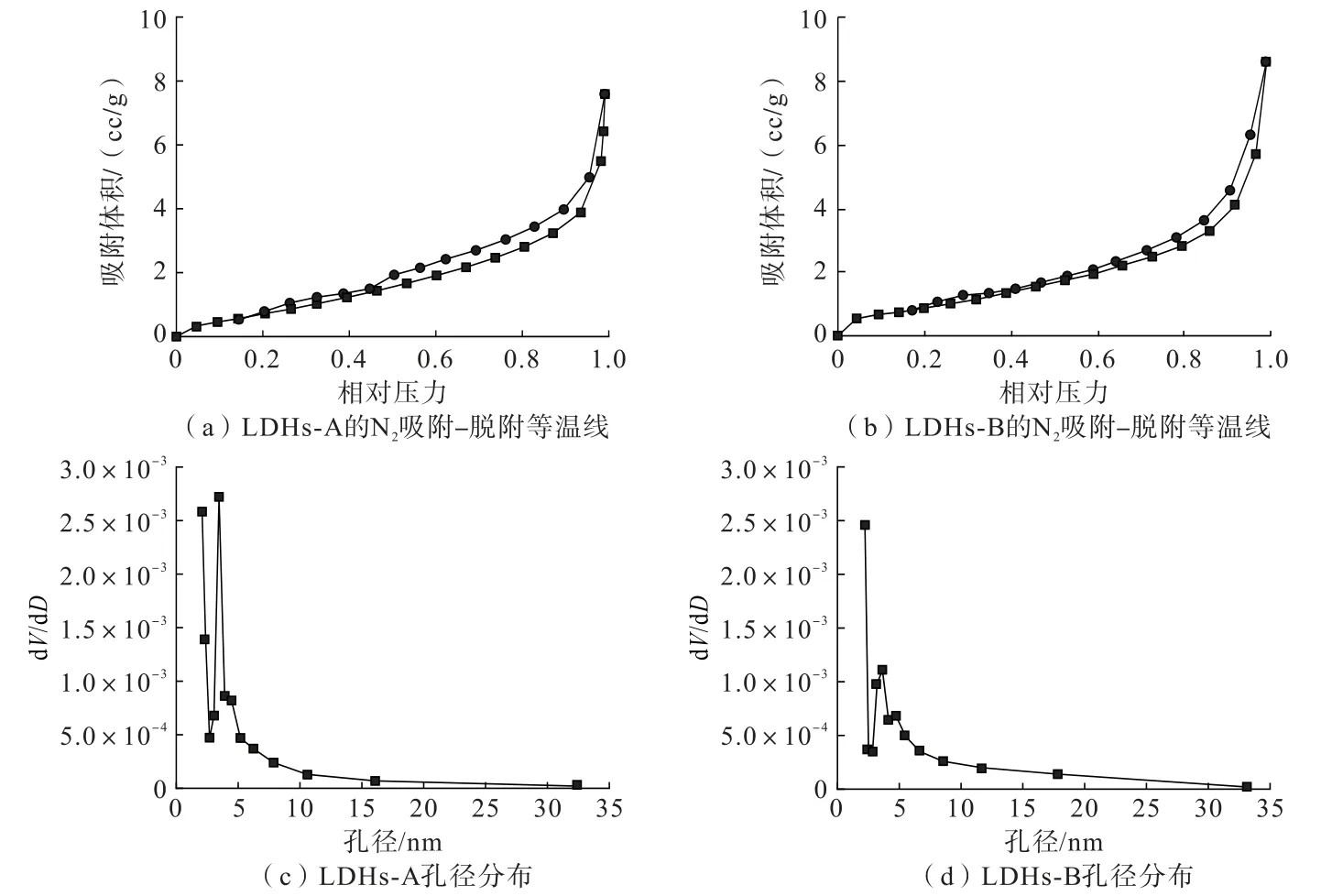
图3 LDHs-A 及LDHs-B 的N2 吸附-脱附等温线和孔径分布图Fig.3 N2 adsorption-desorption isotherm and pore size distribution of LDHs-A and LDHs-B
由图3 可以看出,LDHs-A 和LDHs-B 的吸附等温线都属于Ⅳ型带有H3 型的滞后环,分析认为2 种材料均为介孔材料[21]。 通过BET 测得LDHs-A 和LDHs-B 的比表面积分别为40.804、62.609 m2/g,其中LDHs-B 的比表面积更大,归因于LDHs-B 晶粒尺寸更小,小的晶粒使晶粒间堆积的孔隙密度增多,从而导致比表面积增大[22]。 由孔径分析图可以看出,2种类水滑石孔径都较小,分布在2~35 nm 之间。LDHs-A 的孔径分析图有2 个峰,说明孔径主要分布有2 个尺寸,分别为3.45 nm 和2.08 nm,最可几孔径为3.45 nm,而LDHs-B 的孔径主要分布在2.22 nm,最可几孔径为2.22 nm。
2.1.4 FTIR 分析
采用傅里叶变换红外光谱分析了LDHs-A 和LDHs-B 的表面官能团,测试结果如图4 所示。
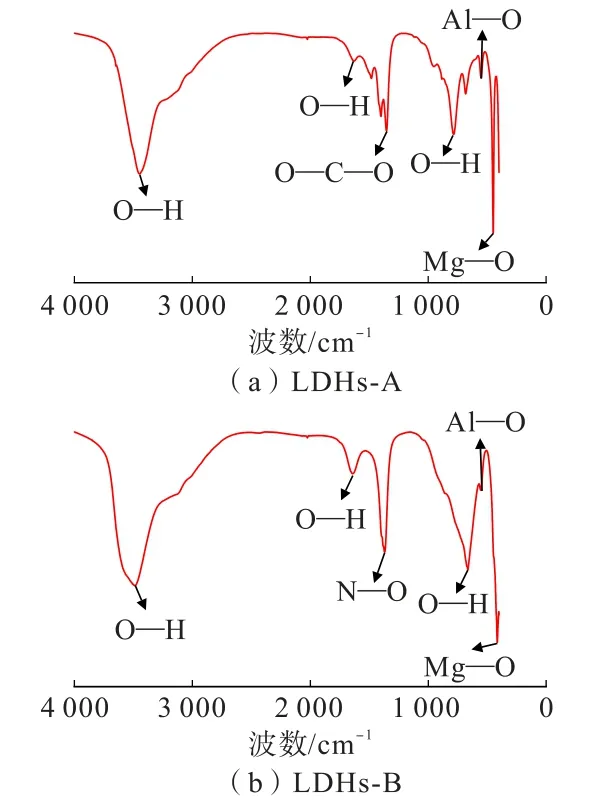
图4 LDHs-A、LDHs-B 的傅立叶变换红外图谱Fig.4 Fourier transform infrared spectra of LDHs-A and LDHs-B
分析图4 可知,750~400 cm-1范围内的吸收峰归因于类水滑石层板阳离子(Mg—O、Al—O)的晶格振动和层板金属阳离子与氧原子之间化学键的弯曲和伸缩振动吸收峰。 LDHs-A 在3 447、1 633、784 cm-1处,LDHs-B 在3 483、1 641、665 cm-1处均出现较宽的吸收峰,是由H2O 分子中—OH 的伸缩振动引起的,这表明晶粒表面富含羟基,且层间存在H2O 分子[23]。 由于层间阴离子不同,层间H2O 分子和层间阴离子与金属层板上羟基的氢键作用力大小的不同,导致2 种样品羟基的伸缩振动峰位置不同。 LDHs-A在1 353 cm-1处的峰归属于CO2-3 伸缩振动峰,表明了层间碳酸根离子的存在。 LDHs-B 在1 370 cm-1处的峰归属于层间硝酸根的振动吸收峰,证明了其层间阴离子为硝酸根离子。
2.2 类水滑石的除氯性能及作用机理
2.2.1 类水滑石投加量对氯离子去除效果的影响
分别取一定质量的LDHs-A 和LDHs-B,放入100 mL 初始氯离子质量浓度为500 mg/L 的氯化钠溶液中,在反应温度为30 ℃、振荡时间为6 h 的条件下,类水滑石投加量对氯离子去除效果的影响见图5。
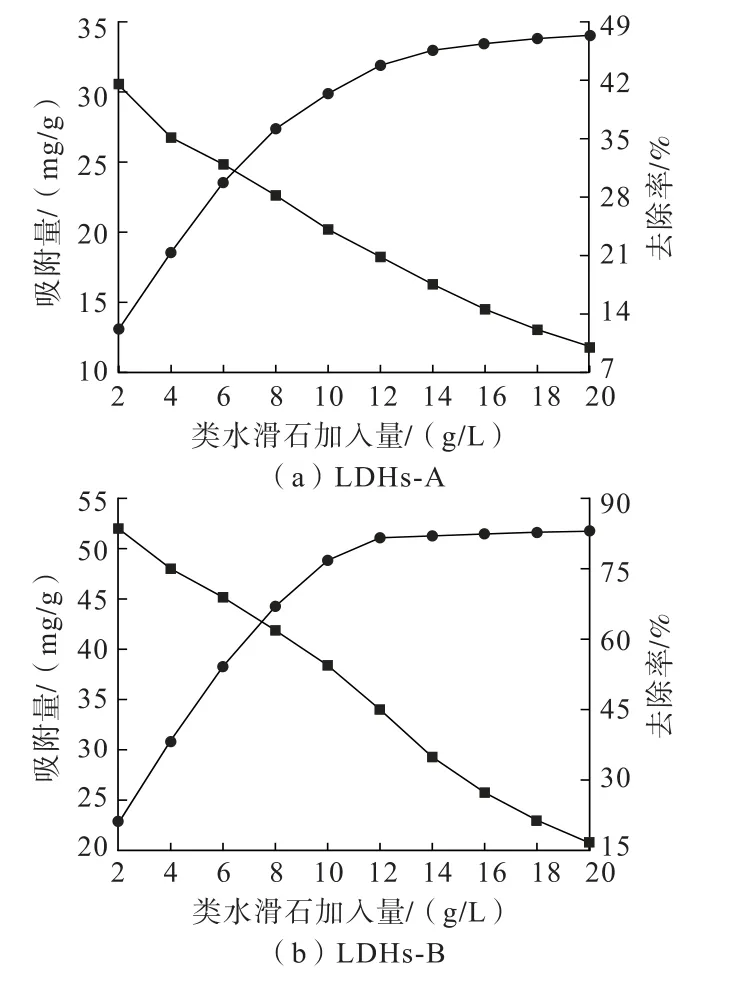
图5 LDHs-A、LDHs-B 加入量对氯离子去除效果的影响Fig.5 Influence of LDHs-A and LDHs-B dosage on chloride ions removal effect
从图5 可以看出,LDHs-B 的除氯效果较LDHs-A的除氯效果好,LDHs-A 到达平衡时对氯离子的去除率为43.8%,而LDHs-B 到达平衡时对氯离子的去除率为81.6%。 随着类水滑石投入量的增加,氯离子去除率逐渐增加,当类水滑石加入量超过12 g/L 时,增加速率减缓,而氯离子的吸附量一直在下降。 这是因为随着类水滑石投入量的增加,总吸附点位也逐渐增加,所以氯离子去除率逐渐增加,但溶液中氯离子的总量是有限的,更多的吸附位点未被氯离子占据,导致氯离子吸附量降低[24]。 继续增加类水滑石投入量,氯离子去除率增加趋缓同时氯离子吸附量仍快速降低,因此后续试验选定类水滑石加入量为12 g/L。
2.2.2 溶液初始pH 对氯离子去除率的影响
分别取1.2 g 的LDHs-A 和LDHs-B,放入100 mL初始氯离子质量浓度为500 mg/L 的氯化钠溶液中,在反应温度为30 ℃、振荡时间为6 h 的条件下,通过稀HNO3和NaOH 溶液调节溶液初始pH,溶液初始pH 对氯离子去除率的影响见图6。
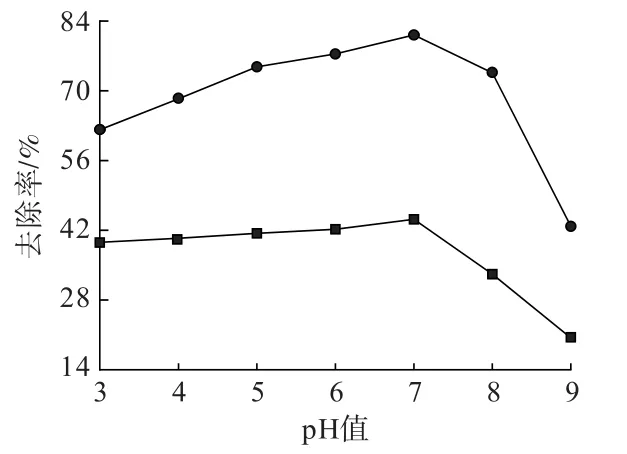
图6 溶液初始pH 对氯离子去除效果的影响Fig.6 Influence of initial pH of solution on chloride ion removal effect
由图6 可知,当pH=7 时,LDHs-A 和LDHs-B 对溶液中氯离子的去除率最大,分别为44.2%、81.2%。当pH<7 时,类水滑石对氯离子的去除率下降,分析认为是类水滑石层板在酸性环境下发生部分溶解导致,而LDHs-B 较LDHs-A 受影响更大,这是因为加入的稀HNO3使得溶液中NO-3增多,抑制了层间NO-3将Cl-从溶液中交换出来。 当pH>7 时,类水滑石对氯离子的去除率骤降,分析认为溶液中的OH-与Cl-形成了竞争吸附,因此后续试验中不需要调节pH。
2.2.3 吸附动力学
分别取1. 2 g 的LDHs-A 和LDHs-B,放入100 mL 初始氯离子质量浓度为500 mg/L 的氯化钠溶液中,控制反应温度为30 ℃,测定不同吸附时间溶液中的氯离子质量浓度并计算吸附量,得到吸附动力学曲线,如图7 所示。
由图7 可以看出,LDHs-A 在60min 时已经达到吸附平衡,而LDHs-B 在350 min 时才达到吸附平衡。
为了深入探究LDHs-A 和LDHs-B 吸附氯离子的动力学特征,采用准一级动力学方程(式(4))和准二级动力学方程(式(5))分别对LDHs-A 和LDHs-B 吸附溶液中氯离子的试验数据进行拟合,拟合结果如图7 及表1 所示。
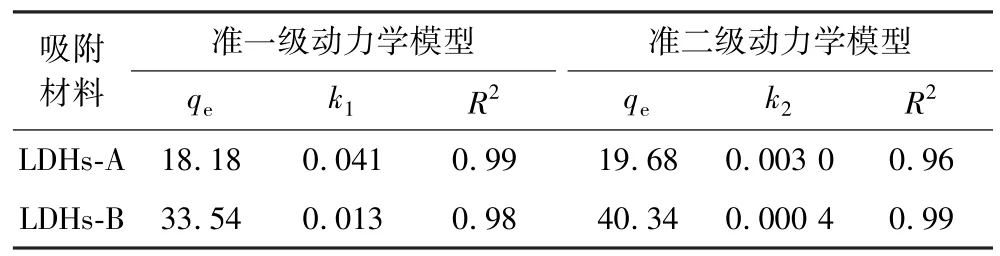
表1 吸附动力学模型参数Table 1 Adsorption kinetics model parameters
式中,k1为准一级动力学速率常数,min-1;k2为准二级动力学速率常数,g/(mg·min);qe、qt分别是平衡时和反应时LDHs-A 和LDHs-B 对氯离子的吸附量,mg/g;t为反应时间,min。
结果表明,LDHs-A 对溶液中氯离子的吸附过程更符合准一级动力学模型,说明LDHs-A 的吸附速率主要受物理吸附控制;LDHs-B 对溶液中氯离子的吸附过程更符合准二级动力学模型,说明LDHs-B 的吸附速率主要受化学吸附控制[25]。 分析认为氯离子比碳酸根离子更容易被交换,因此LDHs-A 对氯离子的去除主要是表面物理吸附,而硝酸根离子比氯离子更容易被交换,因此LDHs-B 对氯离子的去除主要是层间离子交换,主要为化学吸附。
2.2.4 吸附等温线
分别取10 组质量为1.2 g 的LDHs-A 和LDHs-B,配制氯离子初始质量浓度为20、50、100、200、300、500、800、1 000、1 200、1 500 mg/L 的氯化钠溶液各100 mL,控制反应温度为30 ℃、反应时间为350 min,进行吸附试验,得到吸附等温线,对所得数据分别用Langmuir 吸附等温模型(式(6))和Freundlich 吸附等温模型(式(7))进行拟合,结果如图8 及表2所示。
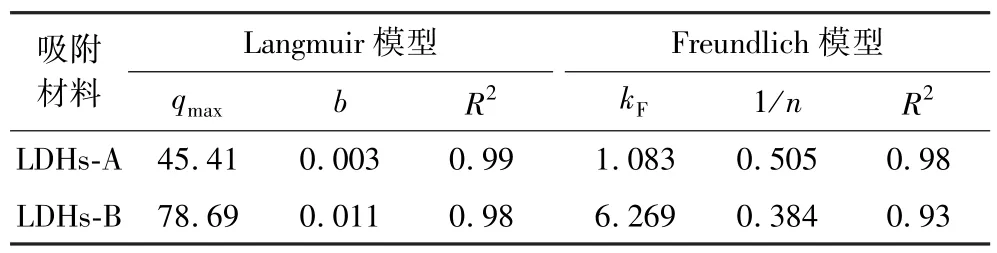
表2 吸附等温模型参数Table 2 Adsorption isothermal model parameters
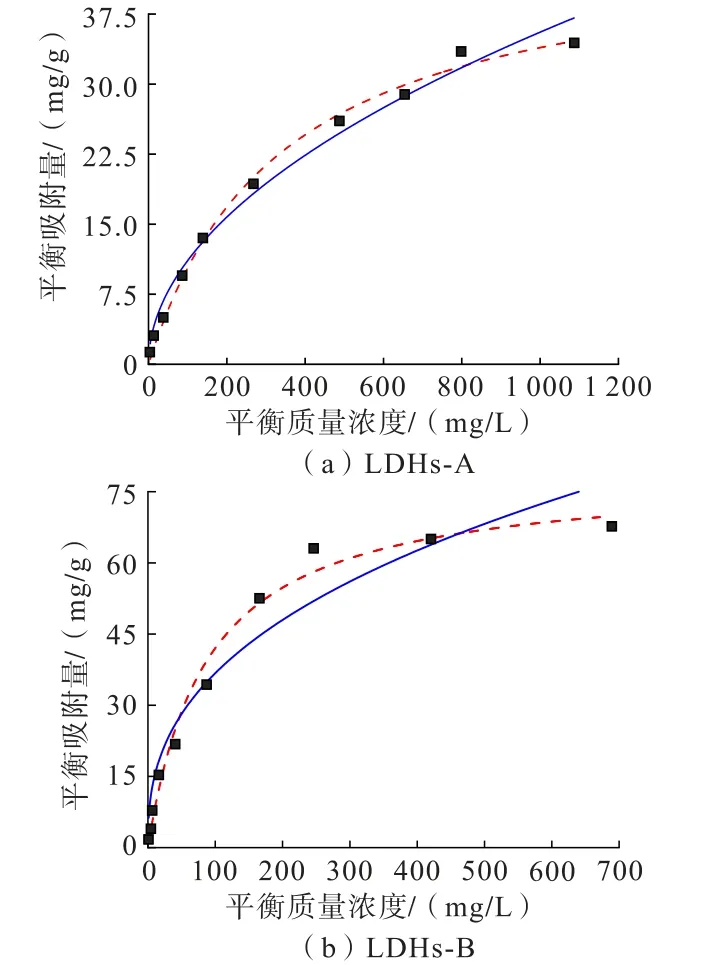
图8 LDHs-A、LDHs-B 对氯离子的吸附等温线Fig.8 Adsorption isotherms curves of LDHs-A and LDHs-B for chloride ions
式中,qe为平衡吸附量,mg/g;Ce为吸附平衡时溶液浓度,mg/L;kF为Freundlich 吸附常数,mg/g;qmax为饱和吸附量,mg/g;b为Langmuir 吸附常数,L/mg。
结果表明,LDHs-A 和LDHs-B 的Langmuir 模型相关系数R2分别为0.99 和0.98,均大于Freundlich模型的相关系数R2,表明这2 种材料的吸附过程主要为单层吸附。 Freundlich 模型的相关系数也比较高,1/n介于0.1~0.5 之间,说明2 种材料都容易发生吸附[26],且LDHs-B 的1/n为0.384,比LDHs-A 的0.505 小,说明LDHs-B 比LDHs-A 更容易发生吸附。分析认为LDHs-B 的晶粒尺寸更小,比表面积更大,所以更易于吸附。 LDHs-B 对氯离子的饱和吸附量为78.69 mg/g,远大于LDHs-A 的45.41 mg/g,这也再次证明了硝酸根插层的镁铝类水滑石比碳酸根插层的镁铝类水滑石吸附效果好。
2.2.5 类水滑石除氯机理探究
为了进一步探究LDHs-A 和LDHs-B 的除氯机理,采用XRD 测试吸附后的LDHs-A 和LDHs-B,分析类水滑石在吸附氯离子前后晶格结构及参数是否发生变化及变化程度。 采用傅里叶变换红外光谱测试吸附后的LDHs-A 和LDHs-B,分析类水滑石在吸附氯离子前后表面官能团是否发生变化及变化程度。吸附后的样品分别记为LDHs-A-Cl 和LDHs-B-Cl,图9 为吸附前后类水滑石的XRD 图谱,图10 为吸附前后类水滑石的傅里叶变换红外光谱图。 表3 为吸附前后类水滑石的晶格参数。
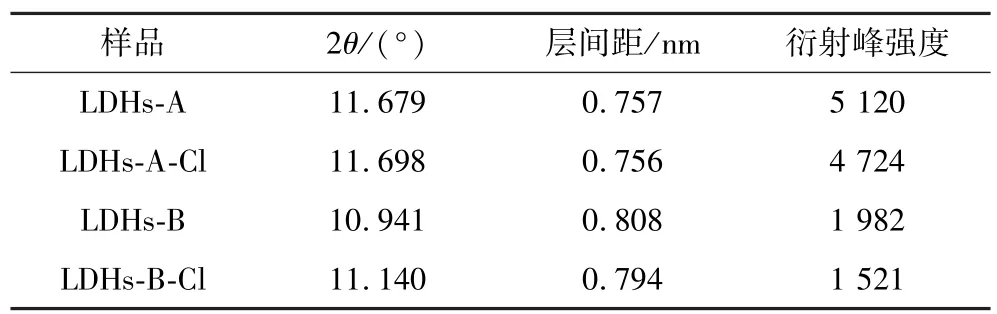
表3 LDHs-A、LDHs-B 吸附氯离子前后的晶格参数Table 3 Lattice parameters of LDHs-A and LDHs-B before and after adsorption of chloride ions
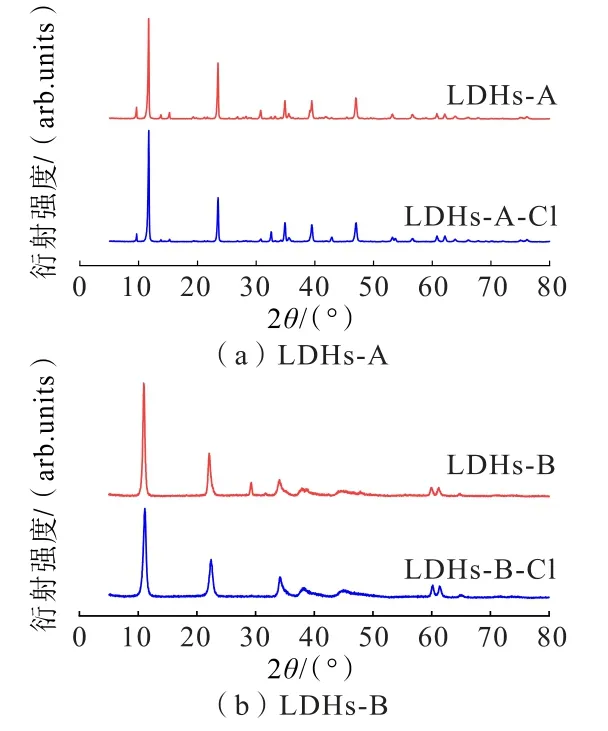
图9 LDHs-A、LDHs-B 吸附氯离子前后的XRD 图谱Fig.9 XRD patterns of LDHs-A and LDHs-B before and after chloride ion adsorption
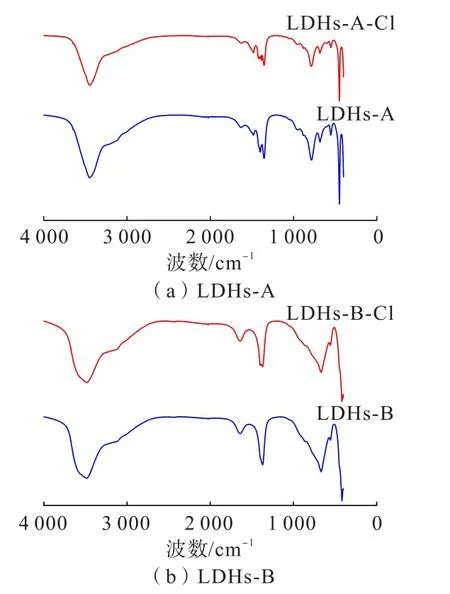
图10 LDHs-A、LDHs-B 吸附氯离子前后的傅里叶变换红外光谱图Fig.10 Fourier transform infrared spectra of LDHs-A and LDHs-B before and after chloride ion adsorption
由图9 及表3 可知,在吸附氯离子后,LDHs-A-Cl和LDHs-B-Cl 的X 射线衍射图谱仍具有代表类水滑石层状结构的特征衍射峰。 其中LDHs-A 的(003)衍射峰对应的衍射角从11.679°增加到11.698°,层间距从0.757 nm 减小到0.756 nm,衍射峰强度从5 120减小到4 724;LDHs-B 的(003)衍射峰对应的衍射角从10.941°增加到11.140°,层间距从0.808 nm 减小为0.794 nm,衍射峰强度从1 982 减小到1 521。 分析认为LDHs-A 吸附氯离子的过程发生了离子交换,离子半径为0. 270 nm 的碳酸根离子与离子半径为0.168 nm 的氯离子交换导致层间距减小,但层间距变化程度很小,说明碳酸根离子较难与氯离子发生交换。 LDHs-B 吸附氯离子的过程也发生了离子交换,离子半径为0.200 nm 的硝酸根离子与离子半径为0.168 nm 的氯离子交换导致层间距减小且层间距变化程度较大,说明硝酸根离子较易与氯离子发生交换。 进一步证明硝酸根插层的镁铝类水滑石比碳酸根插层的镁铝类水滑石除氯效果好。
分析图10 可知,LDHs-A 和LDHs-B 吸附氯离子前后傅里叶变换红外光谱图基本相同,仅有若干吸收振动峰发生变化,LDHs-A 位于784 cm-1处的与层板上羟基对应的伸缩振动峰蓝移2 cm-1,位于1 353 cm-1处的伸缩振动峰蓝移了0.2 cm-1,并且吸收峰强度都发生减弱,分析认为LDHs-A 层板上的羟基与氯离子发生反应,小部分层间的与氯离子发生离子交换。LDHs-B 位于1370cm-1处的NO-3振动吸收峰蓝移0.7cm-1,位于3483cm-1处的与层间羟基对应的伸缩振动峰红移0.4 cm-1,并且吸收峰强度都发生减弱,分析认为LDHs-B 层间的羧基和NO-3与氯离子发生反应。
3 结 论
(1)以尿素和氢氧化钠为碱源,采用水热法分别制备出的LDHs-A 和LDHs-B 两种镁铝类水滑石均具有典型的类水滑石层状结构特征,结晶度高且晶型完整,层间阴离子分别为和NO-3,层间间距分别为0.76 nm 和0.80 nm,结果表明层间间距大对氯离子吸附有利;LDHs-A 的颗粒形状近似于六边形,而LDHs-B 的则更接近椭圆形,LDHs-A 和LDHs-B 晶粒尺寸分别为1 000~2 000 nm、200~400 nm;LDHs-A和LDHs-B 的比表面积分别为40.804、62.609 m2/g,前者孔径集中在3.45 nm 和2.08 nm 左右,后者孔径集中在2.22 nm 左右,均为介孔材料。
(2)类水滑石加入量为12 g/L,初始溶液pH=7为最佳条件。 LDHs-A 初始阶段的吸附速率非常快,吸附平衡时间为60 min,而LDHs-B 在吸附初始阶段的吸附速率较慢,吸附平衡时间为350 min;随着溶液初始浓度的增大,氯离子的去除率呈不断下降的趋势,吸附量呈上升趋势,最大吸附量分别达到34.42 mg/g 和67.58 mg/g。
(3)动力学方程的拟合结果表明,LDHs-A 对溶液中氯离子的吸附过程主要为物理吸附,而LDHs-B的吸附过程主要为化学吸附。 LDHs-A 和LDHs-B 对溶液中氯离子的吸附过程更符合Langmuir 吸附等温模型,表明吸附过程属于单分子层吸附。 LDHs-A 和LDHs-B 经Langmuir 吸附等温模型拟合所得饱和吸附量分别为45. 41 mg/g 和78. 69 mg/g。 吸附后LDHs-A 和LDHs-B 的层间距均有不同程度的减小且LDHs-B 层间距减小程度更大,说明硝酸根离子较碳酸根离子更易与氯离子发生离子交换。
