矿物材料在燃料电池质子导体中的研究进展
2023-12-22李俊升黄鸿鑫杨园园陈佳淇
李俊升 黄鸿鑫 杨园园 陈佳淇
(武汉理工大学化学化工与生命科学学院,湖北 武汉 430070)
从能源危机到双碳目标的提出,无一不预示着以传统矿石燃料为主的能源消费结构将会引起国家能源安全隐患以及社会经济体系不可持续发展。 新型绿色能源的开发利用是促进社会经济发展、保障国家能源安全以及保护生态环境的重要途径。 氢气(H2)得益于其极小的分子量而表现出高达120 MJ/kg 的质量比能量密度,同时由于氢气具有清洁无污染、资源丰富、来源广泛、利用形式多样、可再生性等特性,使其成为目前最为理想的一种绿色能源。 因此,氢能的开发利用是保障国家能源安全、更快实现“碳中和”目标以及更快完成能源低碳化转型的重要途径。燃料电池作为氢能的主要应用载体,其通过电化学反应将H2与O2中所含的化学能转化为电能,具有极高的能量利用率,广泛应用在交通运输、集中式发电站以及便携式设备等领域。 燃料电池根据离子传导种类可以划分为不同的类型,如通过质子(H+)在电池内部进行传导的质子交换膜燃料电池(PEMFC)和磷酸燃料电池(PAFC);通过氧离子(O-2)进行传导的固体氧化物燃料电池(SOFC) 以及通过碳酸根()进行传导的熔融碳酸盐燃料电池(MCFC)。其中PEMFC 和SOFC 由于其全固态结构不会发生电解液泄漏具有优异的安全性能,是目前燃料电池主要的发展方向[1]。 PEMFC 具有工作温度低、启动速度快、能量密度高以及噪声低等特点,在交通工具、便携式电源、潜艇动力源等领域备受青睐[2]。 然而,PEMFC 受限于高昂的成本以及储氢运氢技术的不完善等因素,PEMFC 的广泛应用仍然面临着巨大的挑战。
质子交换膜是PEMFC 的核心组件,目前主要采用全氟磺酸树脂类有机聚合物作为质子交换膜材料。但是昂贵的原材料、复杂的生产工艺以及较高的能源消耗,使得全氟磺酸膜的成本每平米超711 美元[3]。同时,全氟磺酸膜对使用要求较高且存在热稳定性较差、高温下易发生化学降解等问题,使得PEMFC 在实际应用过程中受温度、湿度以及燃料纯度等因素的限制。 为了降低质子交换膜成本,部分氟化聚合物膜、非氟聚合物膜以及复合膜被广泛研究[1]。 但这些有机聚合物质子交换膜在稳定性、机械性能、质子传导性能以及生产成本等方面仍然面临诸多挑战。而对矿物材料加工制得的无机质子导体成本低廉、合成工艺简单,相较于传统的有机聚合物质子交换膜有着更好的物理耐久性,更有利于电池的长期运行,在PEMFC 中有着良好的应用前景。 同时无机质子导体的开发有利于矿物材料的高附加值化,并且拓宽了矿物材料的发展空间。 然而,新型无机质子导体的开发仍然需要克服质子传导性能以及稳定性上的挑战。因此,本文着重概述了不同类型无机质子导体的研究现状,为新型无机质子导体的开发提供借鉴。
1 PEMFC 概述
PEMFC 以聚合物薄膜作为电解质,因此也被称为聚合物电解质膜燃料电池,由通用电气公司的化学研究员GRUBB 和NIEDRACH 在20 世纪50 年代发明[4]。 随后在20 世纪60 年代被美国国家航空航天局应用在太空任务中,作为电力供应装置为宇宙飞船、人造卫星、探测器等设备提供电力。 随着能源危机的出现以及社会对清洁能源的需求,PEMFC 得到快速发展,尤其是在电动汽车领域。 丰田在2020 年推出的第二代Mirai 燃料电池汽车续航里程高达850 km,电堆的功率密度达到了5.4 kW/L,相较于1995年的0.11 kW/L,25 年间功率密度提高了约50 倍。新型高性能、低成本材料的开发是加速PEMFC 发展的关键。 PEMFC 作为一种由多种金属材料与非金属材料组合而成的能量转换装置,需要的材料种类复杂多样。 而我国作为矿产资源总量丰富,矿物种类最齐全的国家,拥有54 种金属矿产以及91 种非金属矿产,为燃料电池用新型材料的开发提供了强有力的支撑。 同时新材料的开发也有利于传统矿产资源利用效率的提高。
1.1 PEMFC 的结构组成
PEMFC 作为不同矿物材料高值化后的集成,主要由双极板、气体扩散层、催化剂层以及质子交换膜组成,结构如图1 所示。
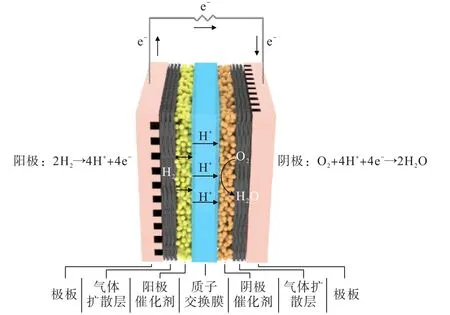
图1 质子交换膜燃料电池工作原理及结构示意Fig.1 Working principle and structural diagram of proton exchange membrane fuel cells
双极板是PEMFC 的关键功能部件之一,其表面刻有流场,因此也称为流场板。 双极板主要起着传输反应气体、支撑电池结构、收集电流以及输送冷却剂等作用[5]。 为了满足双极板的功能,要求双极板材料具有高导热性、高导电性、优异的耐腐蚀性、与气体扩散层具有良好化学和机械兼容性、良好的可加工性以及高表面平滑度等特点[6]。 根据应用领域的不同,双极板所采用的材料也有所区别,主要有石墨双极板、金属双极板以及复合双极板三大类。 石墨双极板是最早的一类双极板,主要是以天然的鳞片石墨为原料,通过高温石墨化、化学氧化、化学插层以及高温膨胀制得膨胀石墨,然后通过对膨胀石墨进一步加工处理得到。 石墨双极板具有优异的耐腐蚀性、良好的导热性和导电性以及较高的化学稳定性等特点,但是易碎和多孔的特点使得石墨双极板可加工性差、整体质量和体积较大、整体成本较高,难以满足市场需求[7]。 以铁矿石、钛矿、铝土矿为原材料,制备得到的不锈钢、钛合金、铝合金等金属双极板具有优越的机械性能、良好的阻气性能以及较低的生产成本等优点,是传统石墨双极板的有效替代品[8-10]。 然而金属双极板的耐腐蚀性较差,需要通过表面处理改性来提高金属基材料的耐腐蚀性以及降低表面接触电阻。复合双极板将石墨和金属材料进行复合,同时兼顾了石墨材料的耐腐性以及金属材料的高机械性能,但复杂的制备工艺使其在大规模生产上仍然面临巨大挑战。
气体扩散层作为PEMFC 核心部件之一,位于双极板和催化层之间并将二者连接,起着促进反应气体传输到电催化剂位点、改善水管理、支撑催化剂层以及收集产生的电流等作用[11]。 气体扩散层材料的选择需要满足高透气性、高导电性、高导热性、良好的机械强度、良好的化学稳定性和热稳定性以及耐腐蚀性等要求[12]。 为了满足使用要求,气体扩散层主要采用经过憎水处理的碳纸、碳布、炭黑纸或者无纺布作为多孔碳纤维基底,随后使用导电炭黑和疏水剂在碳纤维基底上制备一层微孔层得到[13]。 此外,不锈钢网、钛毡、镍网等金属基材也可以作为PEMFC 的气体扩散层[14-16]。
催化剂层作为PEMFC 核心部分,是进行氢氧化和氧还原的电化学反应场所。 精心设计的催化剂层需要具有优异的电子传导能力、H+传导能力、催化能力、耐腐蚀能力以及长的使用寿命[17]。 为了满足上述要求,催化剂层一般由贵金属催化剂与离聚物制备而成。 与其他贵金属金属相比,铂(Pt)具有促进解离途径反应、提高反应速率和降低吉布斯活化能的优异能力,常作为催化氢氧化和氧还原的材料[18]。 催化剂通常是先以铂矿(自然铂、硫化铜镍铂矿、硫铂矿等)为原料,经过富集、精炼、溶解、纳米化等流程制备得到3~5 nm 的Pt 纳米颗粒,随后将Pt 纳米颗粒分散在高比表面积碳载体上,最后得到Pt/C 催化剂。 由于贵金属Pt 的使用,催化剂层的成本占据了燃料电池总成本的55%[19]。 降低催化剂层的成本,可以通过优化催化剂层制备工艺和降低贵金属 Pt 的使用量来实现。 根据涂层基底的类型和实验步骤,两种薄膜制备方法广泛用于催化剂层的制备,分别是在气体扩散层衬底上涂覆催化剂的催化剂涂层基底(CCS)工艺和在质子交换膜上涂覆催化剂的催化剂涂层膜(CCM)工艺[20]。 为了制备出更薄的催化剂层厚度、提高催化剂利用率以及建立更好的三相催化界面,催化剂主要通过CCM 工艺涂覆到质子交换膜两侧,然后与气体扩散层通过热压制备得到PEMFC 核心组件“膜电极”[21]。 常用的CCM 工艺主要有干式喷涂法、转印法、丝网印刷法、磁控溅射法等,其中转印法是制备膜电极最为常用的方法之一。 降低贵金属Pt 的使用量是降低催化剂成本的有效手段之一。如将Pt 与Co、Cr、Ni、Mn、Ru 等形成二元、三元甚至是四元Pt-M 合金来降低Pt 用量;以非Pt 材料为核,以Pt 或Pt-M 为壳,形成核壳结构能够有效提高Pt 的利用率;或者将单个Pt 原子分散在载体材料上形成Pt单原子催化剂,最大程度上利用Pt 的催化能力[22-25]。
质子交换膜作为PEMFC 关键部件,在燃料电池运行中起着分隔燃料(H2)与氧化剂(空气或者O2)、选择性传导H+并对电子绝缘、支撑催化剂层等作用。因此,质子交换膜需要具有优异的质子传导性能、强大的阻气能力、优异的化学稳定性和热稳定性、良好的机械性能以及较低的生产成本等特点[26]。 目前商业化的质子交换膜主要是含氟有机聚合物,如美国DuPont 公司生产的全氟磺酸型质子交换膜,Nafion 系列膜;加拿大Ballard 公司生产的部分氟化型质子交换膜,BAM3G 膜以及美国Gore 公司生产的复合型质子交换膜,Gore-select-PTFE 增强膜等。 天然矿物材料萤石作为上游原材料,为含氟质子交换膜的生产奠定了坚实基础。 但是由于氟化工艺复杂,含氟质子交换膜的价格居高不下,一些基于碳氢聚合物的非氟化质子交换膜如聚芳醚砜、聚苯并咪唑、聚芳醚酮、聚酰亚胺等,正在被积极研究。 这类质子交换膜具有良好的热稳定性,环境友好且成本低,但在化学稳定性、质子传导性能以及膜的使用寿命上还需要进一步优化改善[3]。
1.2 PEMFC 的工作原理
PEMFC 在工作时,H2经极板上的流场达到气体扩散层,随后通过扩散作用到达阳极侧的催化剂层。在阳极催化层中,H2首先在Pt 纳米颗粒表面发生解离吸附,而后吸附在Pt 表面的氢失去一个电子形成H+并脱离Pt 表面。 该过程称为氢氧化反应,可以通过Tafel-Volmer 机制或者Heyrovsky-Volmer 机制进行,具体涉及到3 个基本反应步骤:只有吸附H2没有电子转移的Tafel 反应、吸附H2同时转移一个H+和一个电子的Heyrovsky 反应以及释放吸附氢产生H+和电子的Volmer 反应[27]。 而氢氧化形成的电子通过外电路到达阴极侧,H+则穿过质子交换膜到达阴极侧的催化剂层。 与此同时,O2也通过极板上的流场在气体扩散层的作用下到达阴极侧的催化剂层。在阴极催化层中,O2在Pt 的催化作用下被还原为H2O,该过程称为氧还原反应。 实际氧还原反应历程复杂,包含众多反应步骤,首先是O2吸附在Pt 纳米颗粒表面,然后与阳极侧传递过来的H+和电子以直接四电子反应或者以连续二电子反应生成H2O。 在直接四电子反应中根据O—O 断裂步骤可以分为解离机理和缔合机理。 对于解离机理,O2先形成O∗中间产物,O∗相继被还原成∗OH 和H2O;对于缔合机理,O2先被还原成∗OOH,而后∗OOH 被还原成H2O 和O∗,O∗接着被还原成∗OH 和H2O。 在连续二电子反应中O2先被还原成H2O2,而后H2O2再被还原成H2O[28]。 PEMFC 在运行时涉及的反应如下所示(式中∗表示催化剂中的活性位点):
阳极氢氧化反应:
Tafel 反应:
Heyrovsky 反应:
Volmer 反应:
阴极氧还原反应:
解离机理:
缔合机理:
连续二电子反应:
总反应:
1.3 传统聚合物质子交换膜所面临的挑战
分析PEMFC 的工作原理可以发现,H+在质子交换膜中的顺利迁移是PEMFC 能够高效运作的关键。质子交换膜性能的好坏决定着PEMFC 的放电功率以及使用寿命。 目前,Dupont 研发的Nafion 系列质子交换膜,如Nafion-115、Nafion-117 等占据着PEMFC 电解质膜的主要市场。 作为一种全氟磺酸树脂类聚合物质子交换膜,Nafion 膜以聚四氟乙烯作为疏水主链,以含有磺酸基团的醚支链作为亲水侧链。 高度疏水的碳氟主链可以为聚合物膜提供优异的化学稳定性、良好的水稳定性以及良好的机械强度。 侧链上亲水的磺酸基团相互聚集形成彼此连通的富离子区域,为H+的快速传导提供通道,使得Nafion 膜在80℃完全水合状态下质子电导率可以达到0. 1 S/cm[29-30]。 然而Nafion 膜在扩大应用规模上还面临着以下挑战:
(1)质子交换膜的制备涉及全氟离子交换树脂前驱体的合成以及溶液成膜工艺,整个制备工艺过程复杂、合成困难而且最终的成膜率较低,导致Nafion膜成本高昂。
(2)Nafion 膜对使用温度和含水量要求高,最佳的使用温度在80 ℃左右。 温度过高会导致膜的含水量迅速下降,质子传导性能急剧降低,同时在较高温度下Nafion 的化学稳定性差,容易老化降解。 而较低的使用温度一方面导致阴极氧还原反应动力学过程缓慢,需要更多的Pt/C 催化剂去促进反应进行,使得成本上升。 另一方面较低的温度导致Pt/C 催化剂对CO、SO2等杂质气体具有较差的耐受性,容易被杂质气体占据活性位点,导致催化剂的活性降低甚至是失去催化活性,从而对燃料的纯度有着严格要求,难以使用成本较低的重整氢[1]。 此外,低温、高含水量的使用要求导致电池水管理复杂化,引起整个电池成本的上升。
(3)为了获得更高的电池性能,目前膜电极的制备主要通过CCM 工艺将Pt/C 催化剂涂覆在Nafion膜的两侧。 然而,Nafion 膜在吸水和脱水的过程中会有10%~20%的尺寸变化,较差的尺寸稳定性容易造成催化剂从质子交换膜表面剥离,从而导致电池性能以及使用寿命变差。
因此,开发新型质子导体,进一步提高质子交换膜的性能仍然是推进PEMFC 广泛商业化所面临的主要任务。
2 质子在电解质中的传导
2.1 质子传导机制
明确质子传导机制、了解质子传导过程、掌握质子传导机制判定对指导新型质子导体材料的设计至关重要。 目前质子传导机制主要有两种,一种是1806 年GROTTHUSS 提出的Grotthuss 机制,也称为旋转-跳跃机制,一种是1982 年KREUER、RABENAU和WEPPNER 提出的Vehicle 机制,也称为运载机制[31]。 在Grotthuss 机制中H+可以围绕氧原子快速转动和重新定向,通过与相邻的氧原子形成新的氢键而后断裂旧的氢键进行传导。 对于Vehicle 机制,H+以H2O 或NH3等分子为载体,以水合氢离子(H3O+、H5、H9)或N H+4等复合离子的形式通过扩散作用进行传导。
2.2 质子传导过程
对于不同性质的质子导体而言,虽然质子传导机制都是Grotthuss 机制和Vehicle 机制,但具体质子传导过程以及2 种传导机制的贡献程度存在明显区别。在传统全氟磺酸质子交换膜中,质子传导机制是基于1981 年GIERKE 等人提出的离子簇—网络模型[32]。该模型认为疏水的碳氟主链相互聚集形成疏水区域,亲水的磺酸基团水化后相互连接形成亲水性纳米结构域,以反胶束离子簇形式存在。 其中离子簇的直径为4 nm,2 个相邻离子簇距离为5 nm,彼此通过直径为1 nm 的通道网络相互连接,而水和离子通过该网络进行传导,模式如图2 所示。 温度和湿度在H+传输过程中起着重要作用,这2 个因素决定着膜的含水量,而质子传导机制又与膜含水量直接相关。 在全氟磺酸质子交换膜中质子在传导过程中会同时以Vehicle 机制和Grotthuss 机制进行,但是不同含水量情况下占据主导地位的传导机制不同,如图3 所示[33]。在高含水量情况下Vehicle 机制占据主导地位,H+以H3O+作为载体通过被H2O 填充的通道进行整体迁移。 随着含水量的降低,Grotthuss 机制逐渐占据主导地位,H2O 分子通过旋转运动使得氧原子、氧原子中的空轨道与H3O+中的H+到达合适位置,而后H3O+中的H+向该H2O 分子跳跃形成新的H3O+,以此往复从而实现H+在水分子之间传导。 当含水量进一步降低时,H+将通过离子簇表面的磺酸基团进行传导,而由于2 个相邻的磺酸基团距离较大,H+难以直接通过磺酸基进行传导,需要借助位于2 个相邻磺酸基团之间的H2O 分子以Grotthuss 机制进行传导,这种传导方式由EIKERLING 和KORNYSHEV 在2001 年提出,也被称为表面机制[34]。
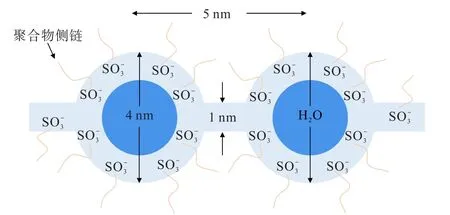
图2 全氟磺酸质子交换膜的离子簇—网络模型[32]Fig.2 Ion cluster network model of perfluorosulfonic acid proton exchange membrane[32]
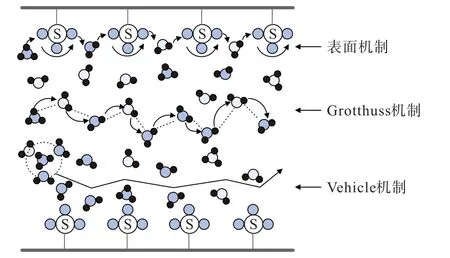
图3 全氟磺酸质子交换膜不同质子传导机制示意[33]Fig.3 Schematic diagram of different proton conduction mechanisms in perfluorosulfonic acid proton exchange membranes[33]
对于以矿物材料制备得到的无机质子导体,通常会存在体积内质子传导和表面质子传导。 体积内的质子传导主要依赖于氧空位的存在。 质子以Vehicle机制进行传导时,H+随着氧离子一起沿着氧空位进行迁移;质子以Grotthuss 机制进行传导时,H+首先围绕着氧原子进行旋转定位然后跳跃到相邻的氧原子上,重复上述行为实现H+的传导,2 种传导机制如图4 所示[35]。 而表面质子传导主要依赖于表面H2O 分子的吸附。 H2O 分子会与裸露的导体表面的末端金属阳离子结合形成化学吸附层,被吸附的水分子可能进一步解离,形成端羟基和多配位羟基,如图5 所示[36]。 当相对湿度从0 到30%,H2O 分子与导体表面的端羟基形成氢键,而后继续增长到三层,由于化学吸附层和第一物理吸附层中的强成键,它们在结构上是类似于冰的,因此前三层水分子称为“类冰态水”。 当相对湿度从30%增加到60%时,冰状结构继续增长至饱和,其中可能存在多聚物链水层,形成“冰”和“液体”结构之间的过渡区。 进一步将相对湿度提高到60%以上,吸附层厚度开始呈指数增加,最外层吸附的水分子结合更加松散,呈液态水结构[37-39]。 无机质子导体表面呈现出液态水时,H+能够以Vehicle 机制进行,当表面H2O 分子以氢键网络相互连接时,Grotthuss 机制成为H+传导方式的首选。
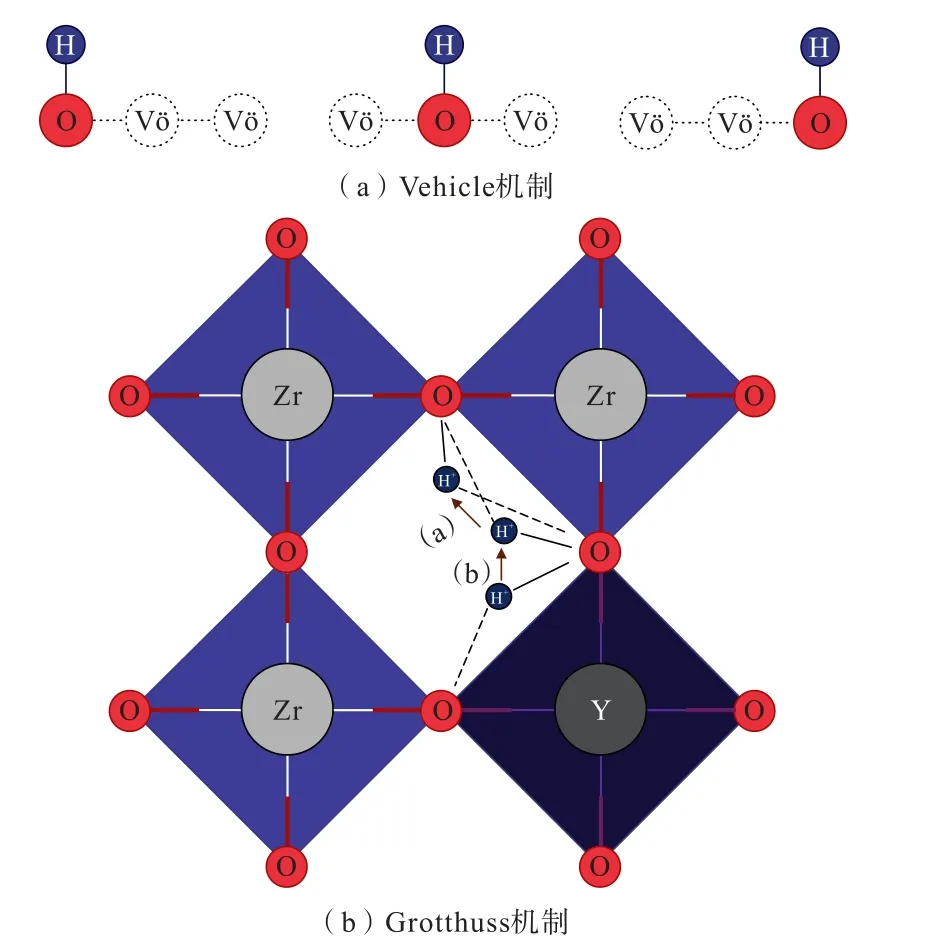
图4 体积内质子传导机制示意[35]Fig.4 Schematic diagram of proton conduction mechanism within the volume[35]
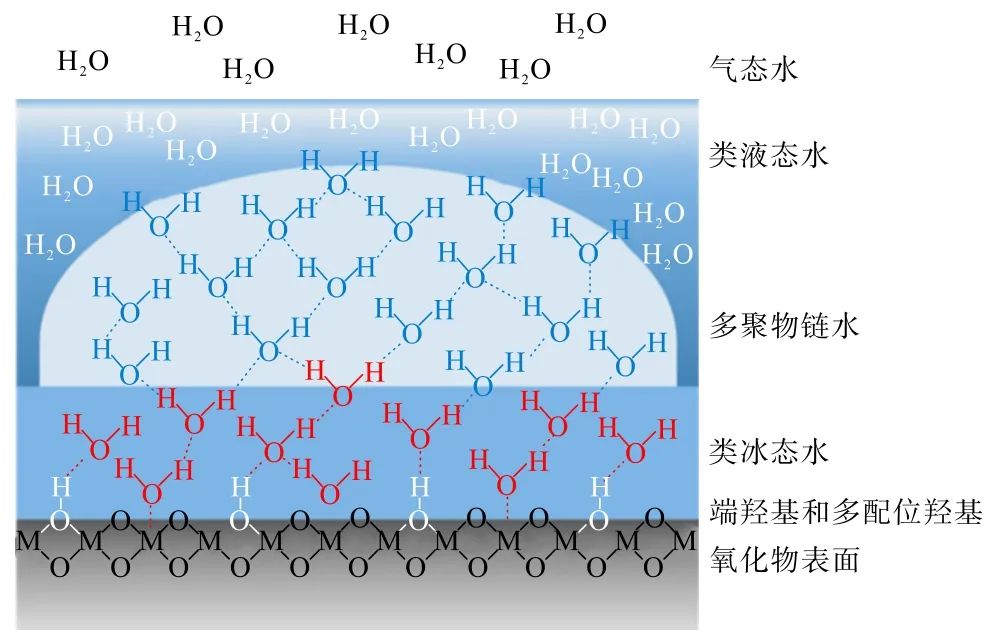
图5 无机质子导体表面吸附水层示意[36]Fig.5 Schematic diagram of inorganic proton conductor surface adsorbed water layer[36]
2.3 质子传导机制的判定
传导机制的确定主要可以通过2 种方式,一种是通过质子传导活化能的大小进行区分。 活化能可以通过测定不同温度下质子导体的电导率而后利用Arrhenius 方程进行拟合得到。 通过公式(16)求得的活化能称为表观活化能,主要反映了质子传输时所克服的自由能势垒。 当活化能在0.1~0.4 eV 时,Grotthuss 机制占据主导地位;活化能在0.5~0.9 eV 时,Vehicle 机制占据主导地位;活化能在0. 4~0. 5 eV时,通常考虑为2 种机制并行[40]。
式中,σ是质子电导率,S/cm;T是绝对温度,K;A是指前因子;Ea是活化能,eV;k是玻尔兹曼常数,通常为1.38×10-23J/K。
另一种则是通过利用同位素效应对比H 传导和H 同位素D 传导的区别。 H/D 以Grotthuss 机制进行传导时,O—H/O—D 键断裂,H/D 跃迁到相邻的氧上,形成新的O—H/O—D 键。 在经典理论模型中,质子跳跃速率跟O—H/O—D 的伸缩频率成正比,而伸缩频率又与根号质量分之一成正比,且活化能Ea与同位素无关,由此可得σH/σD理论值为1. 4[41]。一般来说,同位素效应数值的大小可以反映质子的传导机制,当σH/σD数值在1.4 及以上时,质子以Grotthuss 机制进行传导,σH/σD数值在1 左右时,质子以Vehicle 机制进行传导。 但是在实际过程中由于同位素质量不同,H/D 物种在其所在势阱中的零点能E0不同,因此H 和D 传导的活化能不同,从而σH/σD的数值会出现偏离理论值1.4 较多的情况。
3 矿物材料在质子导体中的应用
PEMFC 的发展在一定程度上受限于质子交换膜的发展。 目前,广泛应用在PEMFC 中的有机聚合物质子交换膜存在成本高昂、生产工艺复杂且热稳定性差等问题。 而无机质子导体具有优良的稳定性以及可调控的质子传导行为,被认为是理想的PEMFC 电解质材料。 无机质子导体的设计合成离不开矿物材料的支持,在目前已经开发的无机质子导体中主要有氧化物、固体酸、金属盐三大类,涉及到众多种类的矿物材料,其中稀土矿、钡矿、锆矿以及磷矿是无机质子导体的主体材料来源。 同时一种无机质子导体会涉及多种元素,与多种矿物材料相关,本文以其共同涉及的某一元素进行分类,将目前的无机质子导体分为稀土矿衍生的质子导体、钡矿衍生的质子导体、锆矿衍生的质子导体以及磷矿衍生的质子导体四大类。各种质子导体材料的性能见表1。
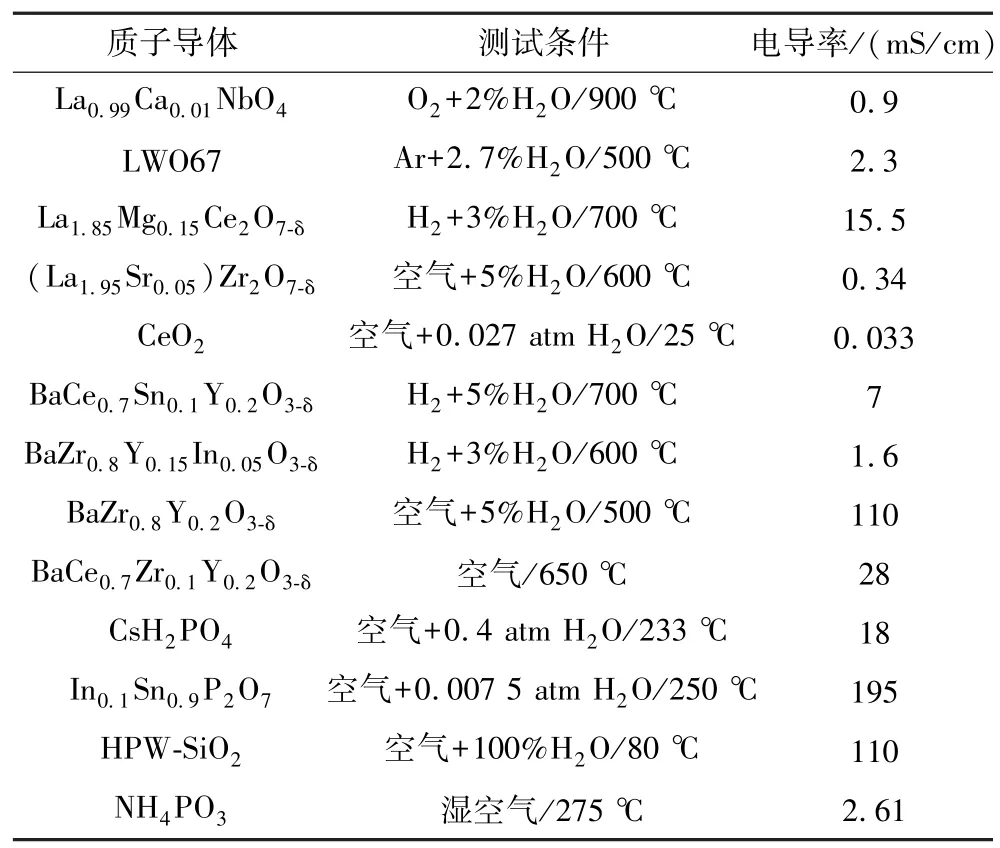
表1 各种质子导体材料不同测试条件下的质子电导率Table 1 Proton conductivity of various proton conductor materials under different test conditions
3.1 稀土矿衍生的质子导体
稀土矿是一种战略资源,目前氟碳铈矿、独居石矿、磷钇矿以及风化壳淋积型矿是工业提取稀土元素的主要矿物,稀土元素具有优异的光、电、磁等物理特性,在航空航天、石油化工、新能源、农业、纺织等领域具有不可替代的地位。 稀土元素活泼的化学性质使其能够生成极稳定的氧化物,该氧化物具有优异的化学稳定性和热稳定性,能够在高温和极端环境下保持结构的稳定性,这种稳定性对于电解质材料来说至关重要。 在17 种稀土元素中,镧的氧化物和铈的氧化物可以作为电解质材料用来传导H+或者O2-,而钇、钪、钐、铕、钆、镱等稀土元素常作为电解质的掺杂剂,用于提高电解质的整体性能。
3.1.1 镧基质子导体
在氧化物型质子导体中质子的传导主要依赖H2O 分子与氧空位结合形成质子缺陷,或者H2还原晶格氧形成质子缺陷。 因此氧化物型质子导体需要本身具有晶格氧缺陷,或者能够通过低价元素掺杂产生氧空位。 萤石结构和烧绿石结构具有开放式结构,能够接受低价元素的掺杂而保持结构稳定性,是较为理想的氧化物晶型。 镧基质子导体主要有两大类一种是基于萤石结构的铌酸镧(LaNbO4)、钨酸镧(La6WO12)、铈酸镧(La2Ce2O7),还一类是基于烧绿石结构的锆酸镧(La2Zr2O7)。
3.1.1.1 铌酸镧
铌酸镧(LaNbO4)作为一种质子导体,其在490℃到520 ℃之间会发生相变,从单斜相转变为四方相[42]。 这2 种晶体结构的LaNbO4均表现出质子传导性能,但是相比于四方晶型,质子在单斜晶型中具有更高的各向异性,表现出更高的质子传导活化能[43]。 2006 年HAUGSRUD 等人研究LaNbO4和掺杂LaNbO4的质子传导性能,纯的LaNbO4在950 ℃时电导率约为0.3 mS/cm,而性能最好的1.0 % Ca掺杂的LaNbO4在900 ℃下电导率也仅约为0. 9 mS/cm[44]。 因此,LaNbO4材料的研究主要聚焦于如何进一步提高其质子传导性能。 目前主要的策略就是通过掺杂取代部分La、Nb 或者两者同时部分取代,以增加氧空位浓度的形式来提高其质子电导率。Ca、Sr、Zn、Mg、Ba、Gd 等元素常用来取代La 位点,Ga、Ge、Si、B、Ti、Zr、P、Al、Sn 等元素常用取代Nb 位点,然而这些掺杂的LaNbO4并没有观察到明显增强的质子传导性能,甚至有的质子电导率反而下降[45-49]。 这是由于掺杂元素溶解度的限制,La 位点上掺杂元素的溶解度仅为0.5%~2%,Nb 位点上的掺杂元素溶解度最高为3%,如此低的掺杂浓度使得氧空位浓度的提高并不理想。 因此提出新的改性策略是提高LaNbO4质子传导性能的关键。
3.1.1.2 钨酸镧
钨酸镧(LWO)是一种混合导体,同时具有质子传导性能和电子电导性能。 LWO 电导率特性的研究首次报道是在2001 年, SHIMURA 等人研究了La5.8WO11.7的电导率特性,发现其在湿润H2氛围下表现出混合质子电子电导,在800 ℃下总电导率高达50 mS/cm[50]。 2007 年,HAUGSRUD 通过交流阻抗研究了LWO 在湿H2和湿D2氛围下的电导率,在800 ℃以下时,湿H2下的电导率高于湿D2下的电导率,表现出明显的同位素效应,说明当温度低于800℃且在潮湿氛围下LWO 的电导率主要受质子传导控制[51]。 研究表明未掺杂LWO 在800 ℃潮湿氛围下质子电导率为5 mS/cm,而在干燥氛围下LWO 表现出一定的氧离子传导,在高温下LWO 以电子导电为主,高温氧化氛围下以p 型空穴传导,高温还原氛围下以n 型电子传导[52-53]。
为了提高LWO 的质子传导性能,传统的掺杂方式被广泛研究。 然而无论是使用Ce、Ca、Sr 等元素对La 位点进行掺杂,还是Mo、Nb、Cr 等元素对W 位点进行掺杂,均未显著提升LWO 质子传导性能[54-57]。同时W 位点的掺入还会导致LWO 材料电子传导性能的提高。 通过增加La/W 比来增加LWO 氧空位浓度,从而增加其质子传导性能是一种有效手段。 在LWO 晶体结构中,当La/W 小于7.0 时,W 起施主掺杂作用部分La3+位点被W6+占据,W 原子取代La 位点提高了LWO 的结构稳定性,但是电荷中和降低了晶体结构中的本征氧空位浓度。 而LWO 中的La/W可以通过合成过程进行控制。 在此之前,MAGRASÓ等人通过冷冻干燥的方法合成了La/W 5.3~5.7 的单相LWO 样品,并对其晶相和质子电导率进行了研究。 研究发现LWO 的质子传导性能随着La/W 的增加而增加,但是当La/W 小于5.3 时观察到La6W2O15的形成,而当La/W 大于5.7 时观察到了La2O3的形成[58]。 在2017 年之前由于制备工艺的原因,La/W最大被限制在了5.7。 2017 年KOJO 等人通过1 700℃的高温烧结获得了La/W 在6.3~6.7 范围内的单相LWO,当La/W 在6.7 时LWO 性能最佳,CO2氛围下具有良好的化学稳定性,在500 ℃时质子电导率达到了2.3 mS/cm,同时700 ℃以下时电子电导和空穴电导被充分抑制[59]。 上述研究结果表明LWO 有望通过改进制备方法来提高其应用价值。
3.1.1.3 铈酸镧
铈酸镧(La2Ce2O7)可以认为是50%的La2O3掺杂的CeO2,因此在成相过程中会发生缺陷反应,使得La2Ce2O7本身就含有氧空位,从而能够在不掺杂的情况下传导质子。 SUN 等人研究表明纯La2Ce2O7在湿空气(3% H2O)550 ℃下质子电导率可以达到66.8 μS/cm,同时发现总电导率随水蒸气分压的增加而显著增加[60]。 由于Ce4+在还原氛围下会被还原成Ce3+从而产生电子电导,因此La2Ce2O7是混合质子电子导体。 而且随着温度的升高La2Ce2O7中电子电导占据主导地位,在2.5% H2O 湿空气800 ℃时总电导率便高达14.1 mS/cm[61]。 而纯La2Ce2O7质子电导率偏低,难以应用,研究表明在La 位点上掺杂Li、Na、K、Rb、Cs 等碱金属能够显著提高La2Ce2O7的质子传导性能,且电导率随掺杂碱元素离子半径的增大而增大,而随铯掺杂而减小,La1.85Rb0.15Ce2O7-δ性能最佳,在800 ℃的湿H2中表现出6.21 mS/cm 的电导率,且以La1.85Rb0.15Ce2O7-δ基的单电池,在700℃下表现出高达1 031 mW/cm2的峰值功率,稳定放电时间超过200 h[62]。 当使用碱土金属Mg 对La2Ce2O7进行掺杂时,不仅可以增加La2Ce2O7电导率,还能作为烧结助剂降低La2Ce2O7烧结温度。 WU等人在1 300 ℃烧结5 h 的条件下成功制备出全致密的La1.85Mg0.15Ce2O7-δ电解质膜[63]。 此外,在700℃的湿H2(3% H2O)中La1.85Mg0.15Ce2O7-δ的电导率最高为15.5 mS/cm,并且对CO2和H2O 保持优异的化学稳定性,同时基于La1.85Mg0.15Ce2O7-δ的燃料电池在700 ℃时表现出高达897 mW/cm2的峰值功率密度[63]。 对La2Ce2O7的La 位点进行掺杂是提高La2Ce2O7整体性能至关重要的手段,而进一步降低La2Ce2O7使用温度是提高其应用价值的必经之路。
3.1.1.4 锆酸镧
早在1997 年LABRINCHA 等人就报道了纯相的La2Zr2O7具有质子传导性能,但是其质子导电性较差,在900 ℃下仅有4.2 μS/cm[64]。 TAKAHISA 等人研究发现纯相的La2Zr2O7不能溶解H2O 蒸气,从而导致质子传导性能较差,而使用Ca2+掺杂的La2Zr2O7具有较好的H2O 蒸气溶解能力[65]。 电动势测试结果表明, 在 200 ~ 800 ℃ 范围, ( La1.98Ca0.02)(Zr1.98Ca0.02)O7-δ是纯离子导体,而且在600 ℃以下是纯质子导体,在600 ℃以上开始出现O2-传导,但是O2-传导较弱,在800 ℃时O2-的转移数也仅为0.18,质子传导占据主导地位。 通过对La 位点和Zr位点使用碱土金属进行掺杂取代,能够显著增加La2Zr2O7的质子传导性能。 TAKAHISA 等人的研究表明,由于La2Zr2O7烧绿石相的特殊结构,导致仅被La 原子包围氧原子显示出高碱度,因此La 位点掺杂的(La2-xMx)Zr2O7-δ中质子溶解度要比Zr 位点掺杂的La2(Zr2-xMx)O7-δ(M=Mg、Ca、Sr、Ba)高出3 倍[66]。同时掺杂碱土金属的种类对La2Zr2O7的质子传导性能也有所影响,BJÖRKETUN 等人研究发现Ca 和Sr与质子的相互作用较弱,对质子的传导起促进作用,而Mg 和Ba 的存在对质子的迁移有着负面影响[67]。此外,晶粒尺寸对La2Zr2O7基材料的电导率也有一定影响,在(La1.95Sr0.05)Zr2O7-δ中总电导率随着晶粒尺寸的增加而单调增加[68]。 总体而言,烧绿石结构的La2Zr2O7质子传导性相较于萤石结构的La 基材料偏低,但是其具有良好的烧结特性[69]。
3.1.2 铈基质子导体
铈基质子导体主要有三类,分别是上文介绍过的萤石结构La2Ce2O7、钙钛矿结构的铈酸钡(BaCeO3)以及氧化铈(CeO2)。 BaCeO3将会在下一节进行详细介绍,本节主要是介绍CeO2在质子导体中的研究进展。 CeO2具有萤石结构,因其优越的储存和释放O2的能力而被广泛用作催化领域的催化剂、载体或促进剂。 此外CeO2还是SOFC 中一种主要用来传导O2-的电解质。
将材料纳米化时,由于扩散长度短以及界面密度高而表现出显著的尺寸效应。 作为高温氧离子导体的CeO2通常情况下认为是不良质子导体,但是在湿润氛围中CeO2的纳米晶在中低温下表现出可观的质子传导性。 2010 年,AVILA-PAREDES 等人通过放电等离子烧结技术制备了平均晶粒尺寸约为15 nm的Ce1-xGdxO2-δ(x=0.5、10 和20%)纳米晶陶瓷,研究了其在30~200 ℃温度范围内质子传导与Gd 掺杂水平之间的关系[70]。 研究结果表明,在低于200 ℃的温度下,电导率与Gd 掺杂水平无关,当温度高于200℃后,离子电导率随着Gd 掺入量的增加而增大,这得益于较高的Gd 掺杂水平引起的较大浓度的氧空位。 基于上述结果,AVILA-PAREDES 等人认为在纳米晶萤石结构材料中质子的传导与体相缺陷无关,质子可能沿着晶界进行传导。 然而,2011 年SHIRPOUR 等人研究了晶粒尺寸在40 nm 的纳米晶和晶粒尺寸在300~500 nm 的微晶的导电性能[71]。 研究发现微晶样品的电导率在潮湿和干燥氛围下没有变化,而纳米晶样品在潮湿氛围下表现出明显比干燥氛围下更高的电导率,热重分析进一步表明纳米晶CeO2在200 ℃以下表现出明显的吸水性,结果表明晶界和开放性空隙均有可能对质子的传导起积极促进作用。随后,GREGORI 等人通过脉冲激光沉积(PLD)生长制备了全致密外延纳米晶CeO2薄膜,以及利用旋涂法制备了多孔纳米晶CeO2薄膜,探讨了孔隙率对表面质子传导的影响。 研究结果显示全致密外延纳米晶CeO2薄膜的电导率在干湿条件下差异不大,但多孔纳米晶薄膜的电导率在暴露于300 ℃以下的潮湿大气中时显著增加[72]。 这些结果表明,开放性空隙或者裂缝是影响质子在中低温下通过金属氧化物传输的核心因素,而不是大的晶界密度。
2018 年,MANABE 等人利用电化学阻抗谱研究了潮湿条件下多孔CeO2的表面传输特性。 对于相对密度为60%的低致密度样品,通过等效并联电路可以很好地提取晶粒和晶界的内部和表面电导率[73]。 研究结果显示在潮湿条件下的表面质子电导率随着温度的降低而增加,表明吸附水在CeO2表面的质子传输中起着重要作用。 400 ℃时颗粒体表面(内部)的电导率对水分压的依赖性表明,促进表面质子传输的是水分子而不是离解的水。 上述这些工作清楚地表明,吸附水在CeO2的表面质子传导中起着重要作用,特别是在低温下。 最近,SIMONS 等人利用喷涂法制备了CeO2薄膜,通过对比退火前后CeO2薄膜的电导率发现,退火后的薄膜具有更高的电导率[74]。 他们认为薄膜退火后增加了晶态CeO2的比例以及晶粒尺寸,从而增加了高导电路径,表明晶界实际上是有助于质子的传导。 同时,作者证明由于CeO2缓慢的水合动力学过程,室温下潮湿大气中获得稳定电导率所需的时间长达76 h,这意味着动力学可能在之前的研究中抑制了质子传导,从而解释了迄今为止报告中CeO2电导率的强烈波动。
3.2 钡矿衍生的质子导体
钡的化学性质相当活泼,能与大多数非金属反应,在自然界中难以以单质形式存在,主要以矿物形式存在。 钡矿主要成分是钡的盐类,主要产出于岩浆岩、变质岩中。 钡矿可以分为重晶石(BaSO4)、毒重石(BaCO3)和天青石(BaSO4)3 种。 我国的钡矿资源丰富,拥有全球29%重晶石的储量,钡矿储量和产量目前均居世界首位,因此钡矿的开发利用对我国矿物产业的发展起着重要作用。 而钡基材料的用途十分广泛,玻璃、陶瓷、涂料、医药、新能源等行业均离不开钡基材料。 钡矿衍生的质子导体主要是钙钛矿材料,钙钛矿最初是指在1839 年发现的钛酸钙(CaTiO3)矿物,后来泛指与CaTiO3具有相同结构的材料。 理想的钙钛矿通式为ABO3,结构可以认为是面心立方晶格,角原子为A 原子,面上为O 原子,B 原子最终确定了位于晶格中心的结构。 其中A 位点为半径较大的低价态金属阳离子,如一价的Na+、K+,二价的Ca2+、Sr2+、Ba2+,三价的Fe3+、Gd3+、La3+;B 位点为半径较小的高价态金属阳离子,如W5+、Nb5+、Ce4+、Zr4+、Co3+等[75]。 A、B 位点不同金属离子组合得到的钙钛矿材料表现不同的绝缘性、光学性能、铁电性、催化性能以及离子传导性[76]。 从1981 年IWAHARA等人发现SrCe1-xMxO3-δ(M=Yb、Y、Sc)在600~1 000℃的H2或湿空气氛围下表现出大于10-4S/cm 的质子传导性能开始,具有质子传导性能的钙钛矿得到了广泛研究,其中BaCeO3以及锆酸钡(BaZrO3)因其良好的化学稳定性、优异的质子导电性和简单的制备工艺而备受关注[77]。
3.2.1 铈酸钡基质子导体
BaCeO3是钙钛矿结构,Ba 在A 位点,Ce 在B 位点,具有较高的质子电导率,在中温下比铈酸锶(Sr-CeO3)的质子电导率高出一个数量级[78]。 这是由于影响质子导电性的化学和结构参数决定的。 未掺杂的BaCeO3具有Pnma空间群,在高温下表现出理想的立方结构。 低温BaCeO3中存在的2 个结晶学上不同的氧位点在高温下变得能量等价[79]。 一般而言,能量不相等的氧位点会使得水化行为更加复杂,而BaCeO3在高温下克服了这一点,从而导致电导率的增加。 尽管SrCeO3与BaCeO3具有相同构型,但与BaCeO3相比,SrCeO3的晶体结构表现出较大的立方对称性扭曲,从而在加热到1 000 ℃时仍保持正交结构,存在2 个能量不相等的氧位点,导致导电性下降[80]。
优秀的电解质材料应满足3 个要求,分别是高离子电导率、强化学稳定性和良好的烧结性。 BaCeO3基质子导体普遍拥有较高的离子电导率(在600 ℃时电导率≥0.01 S/cm),而且具有良好的烧结性,但是由于BaCeO3具有天然的碱性,很容易与酸性气体如CO2、 SO2以及水反应生成BaCO3、 BaSO4和Ba(OH)2,阻碍质子的迁移,导致材料发生较大的热膨胀,从而降低燃料电池的性能[81]。 BaCeO3在较低温度下的分解,严重阻碍了其在实际中的应用,比如在1 041 ℃以下与CO2发生反应,在403 ℃以下与水蒸气发生反应[82]。 以20% Gd 掺杂的BaCeO3(BCG20)为电解质组装而成的燃料电池在600 和700 ℃、含50%水蒸气环境中可以稳定运行1 000 h[83]。 但是BHIDE 和VIRKAR 的研究结果显示,在400 ℃以下,以BCG20 为电解质的燃料电池仅运行168 h,BCG20 就会与水蒸气发生反应而分解[84]。
MATSUMOTO 等人将不同的三价稀土离子掺入BaCeO3中,用以改变BaCeO3的性能。 研究发现掺杂BaCeO3的电导率和化学稳定性由掺杂离子半径决定,掺杂离子半径越大,离子电导率越高,但化学稳定性降低[82]。 因此,掺Y3+的BaCeO3表现出最佳的电导率性能,掺Sc3+的BaCeO3表现出最佳的化学稳定性,然而Sc 昂贵的价格阻碍了其广泛应用。 对于化学稳定性的增强,很难找到比Sc3+半径更小的三价稀土阳离子,而Al3+的半径仅为54 pm,远小于Sc3+的半径(75 pm),且Al 来源广泛价格低廉。 SHIN 等人的研究表明Al3+掺杂的BaCeO3表现出良好的化学稳定性,且当Al3+掺杂量超过20%时Al3+发生溶出,但其在400~470 ℃的电导率接近Y 掺杂的BaCeO3[85]。对Ce 位点进行双金属掺杂, 在BaCe0.8Y0.2O3-δ(BCY20)的基础上引入具有更高电负性的金属元素,能够有效降低BCY20 的碱性,从而使BaCeO3基材料对CO2和H2O 表现出更高的化学稳定性。 BI等人将Ta 和Y 共掺杂到BaCeO3的Ce 位点中形成BaCe0.7Ta0.1Y0.2O3-δ,该材料在沸水中煮6 h 能够保持结构的稳定性,且700 ℃时在100% CO2氛围下表现出足够的化学稳定性,同时以BaCe0.7Ta0.1Y0.2O3-δ作为电解质组装的燃料电池在700 ℃的功率密度可达142 mW/cm2[86]。 XIE 等人利用固相反应法制备了Sn、Y 共掺杂的BaCe0.7Sn0.1Y0.2O3-δ,对H2O 和CO2均有很好的化学稳定性,在700 ℃湿H2氛围下电导率可以达到7 mS/cm。 同时由于Sn 的掺入提高了电解质的可烧结性,相比于BCY20 在1 400 ℃烧结后仅有83.3%的相对密度,BaCe0.7Sn0.1Y0.2O3-δ烧结后的相对密度可以达到 96. 0%。 而且以BaCe0.7Sn0.1Y0.2O3-δ为电解质的燃料电池在700 ℃功率密度达到了470 mW/cm2,界面电阻也仅为0. 13 Ωcm2,表明该电解质材料与电极之间具有良好的相容性[87]。 除了采用金属离子进行掺杂改性外,还可以通过在BCY20 电解质表面脉冲激光沉积一层BaZr0.8Y0.2O3-δ(BZY20),在保护BCY20 的同时不会显著影响其导电性[88]。 寻找合适的途径来提高BaCeO3基电解质的化学稳定性,同时保持较高的质子电导率,是实现质子传导燃料电池在低温下运行的关键。
3.2.2 锆酸钡基质子导体
BaZrO3具有优异的物理性能和高导热性能,与BaCeO3相比具有更低的热膨胀值、更好的稳定性以及更高的机械强度,能够在CO2和H2O 氛围下稳定存在[89]。 但是较差的烧结性能使BaZrO3作为电解质面临着低相对密度以及高晶界电阻等问题。 而较高的烧结温度或者较长的热处理时间会导致BaO 的蒸发,从而引起A 位点占有率的降低,导致氧空位的浓度下降,从而对整体的导电性性能产生不利影响[90]。 因此,BaZrO3基电解质的研究方向主要是提高BaZrO3基的电导率以及烧结性能。 为了提高Ba-ZrO3基电解质的电导率,一般采用低价元素进行掺杂来提高氧空位浓度。 由于三价稀土元素Y3+的掺入不会改变质子缺陷的水化热和迁移率,因此Y3+被认为是BaZrO3中B 位点最好的掺杂剂。 20% Y3+掺杂的BaZrO3具有较高的化学稳定性和体相质子电导率,当Y3+掺杂量超过20%时将会导致激活能增加从而引起电导率下降,因此BZY20 是目前BaZrO3基材料的主要研究对象[80]。
为了获得高性能BaZrO3电解质,一般从使用烧结助剂、金属离子共掺杂以及探索新的制备工艺3 个方面提高BaZrO3的烧结性能。 在BZY20 中添加1%的ZnO 作为烧结助剂,焙烧时Zn 进入晶格与BZY20形成固溶体,从而使得BZY20 的烧结温度从1 700 ℃降低至1 325 ℃,致密度达到96%,在600 ℃以上时,总电导率可以达到1 mS/cm,明显高于未加ZnO 的BZY20[91]。 然而,最近的研究表明,在BZY20 中使用烧结助剂,虽然可以提高BZY20 的烧结性,但是质子掺入能力和质子传导能力显著降低,同时空穴传导增强,总体是不利于BZY20 的导电性能[92]。 掺杂通常涉及晶格缺陷,通过增加氧空位浓度来提高质子电导率,同时由于掺杂剂的影响,可以实现烧结性能的改善。 研究表明,使用In、Pr、Sn 与Y 对BaZrO3进行共掺杂能够有效地提高BaZrO3的烧结性能同时不损害BaZrO3的化学稳定性[93-95]。 SUN 等人研究了Y 和In 共掺杂的BaZrO3,BaZr0.8Y0.2-xInxO3-δ。 随着In 浓度的增加,BaZr0.8Y0.2-xInxO3-δ的烧结活性显著提高,在湿H2中(3% H2O)600 ℃时BaZr0.8Y0.15In0.05O3-δ的总电导率最高可以达到1.6 mS/cm,对CO2、H2O 蒸气和H2还原也表现出很高的化学稳定性[95]。 同时,SUN 等人以简单的滴涂技术,于1 400 ℃空气中反应5 h,在阳极衬底上成功地制备出了完全致密的BZYI5 电解质薄膜,BaZr0.8Y0.15In0.05O3-δ基单电池的功率密度在700 ℃时最高可达379 mW/cm2。 此外,一些新的制备工艺能够有效地降低BaZrO3的烧结温度,提高BaZrO3的性能。 KHANI 等人通过微乳液法以及丙烯酸酯水凝胶法制备了高度均匀的超细BaZr0.9Y0.1O2.95粉末,在1 500 ℃焙烧10 h 后致密度达到93%,600 ℃时的电导率为2 mS/cm[96]。 除了采用传统的高温烧结技术外,先进的薄膜制备技术对BaZrO3基电解质性能的提高起着重要作用。 PERGOLESI 等人采用PLD 在(100)取向的MgO 衬底上获得了高度织构外延取向的BZY20 薄膜,由于没有晶界的阻碍,BZY20 薄膜在500 ℃时质子电导率高达0.11 S/cm[97]。 2017 年,BAE 等人通过PLD 制备的BaZr0.85Y0.15O3-δ薄膜在组装成单电池后,600 ℃时燃料电池的最大功率密度达到了740 mW/cm2[98]。 虽然通过PLD 能够制备得到性能优异的BaZrO3基电解质,然而高昂的制造成本使其目前还无法大规模应用。
3.2.3 锆酸钡-铈酸钡基质子导体
BaCeO3具有优异的离子电导率以及良好的烧结性,BaZrO3具有良好的化学稳定性, 通过形成BaCexZr1-xO3固溶体能够有效地整合二者的优点同时规避其缺点。 通过对BaCe0.9-xZrxY0.1O3-δ(BCZY)系统地研究发现,Zr 含量的增加可以提高BCZY 的化学稳定性,而Ce 含量的增加则提高了BCZY 的导电性以及可烧结性[99]。 为了改善BCZY 烧结性能,一般采用过渡金属作为烧结助剂,NIKODEMSKI 等人研究了NiO、Fe2O3、WO3、PdO 等15 种金属氧化物烧结助剂对BCZY 体系相形成和致密化的影响[100]。 研究结果表明,当添加的金属离子半径与Zr4+离子半径相近而且具有稳定的+2 价时,能够有效增加BCZY 的烧结性能,同时产生大量缺陷,对离子的传导起着积极的促进作用;当金属离子具有多种状态,但是离子半径与Zr4+离子半径相近时,可以通过形成具有有限晶粒尺寸的机械稳定的高孔隙微结构来导致部分烧结;当金属离子半径远离Zr4+离子半径或者是稳定价态大于+2 价时,由于不能与BaZrO3形成固溶体,对烧结行为没有改善作用。 因此常用的烧结助剂主要是NiO、ZnO、CuO 和CoO 四种。 NASANI 等人研究了NiO、ZnO 和CuO 作为烧结助剂对BCZY 性能的影响,相比于不添加烧结助剂,在1 400 ℃煅烧的BCZY的相对密度仅为86%,使用烧结助剂后相对密度提高到了95%以上,但是在所有情况下,添加烧结助剂均会显著降低整体电导率,而晶界电导率相对不受影响[101]。
相比于使用烧结助剂会对BCZY 电解质的性能产生影响,一些特殊的烧结方式正在被积极研究。 比如WANG 等人通过微波烧结法制备得到晶粒尺寸仅为25 nm 的BCZY 粉末,在1 300 ℃烧结5 h 后相对密度达到了96%,而且以该电解质膜组装的燃料电池在700 ℃功率密度达到了791 mW/cm2[102]。 此外,通过改进BCZY 粉体的制备方法也能有效提高电解质的性能。 FAN 等人以Tween-80 为表面活性剂,采用碳酸盐共沉淀法制备了粒径在150~300 nm 的BCZY 粉末,在1 400 ℃、无烧结助剂的情况下,BCZY粉末与阳极基板共烧结后,电解质高度致密化。 电解质厚度为20 μm、使用湿H2(3%H2O)作为燃料和环境空气作为氧化剂的燃料电池700 ℃时的峰值功率密度高达1 050 mW/cm2[103]。
总体而言,BaCexZr1-xO3基质子导体表现出巨大的应用潜力,但是在电导率与稳定性之间的平衡仍然需要进一步研究。
3.3 锆矿衍生的质子导体
由于独立矿床较少,锆矿是一种稀有金属矿产资源。 目前锆石、斜锆石、异性石、钠锆石以及锆钽矿等是工业提取锆的主要矿物。 由锆矿加工而成的锆产品应用广泛,如碳酸锆是纺织、造纸、涂料、化妆品行业的重要原料;氯氧化锆可以用于纺织、皮革、橡胶添加剂、金属表面处理剂、涂料干燥剂、耐火材料等;氧化锆(ZrO2)适用于精密陶瓷、电子陶瓷、光学透镜、玻璃添加剂、人造宝石、耐火材料、研磨抛光等行业;而金属锆更是重要的战略金属,主要用于核动力航空母舰、核潜艇和民用发电反应堆的结构材料、铀燃料元件的包壳等。 然而我国作为全球最大的锆资源消费国,2022 年锆金属储量仅有7.16 万t,需要大量依赖海外进口,因此锆矿资源的高效利用是缓解锆资源紧张的有效手段。 锆基质子导体主要有3 类,分别是上文介绍过的萤石结构La2Zr2O7、钙钛矿结构的BaZrO3以及ZrO2,前2 种已经在上文进行了详细介绍,这里就不在赘述。
ZrO2表现为萤石结构,Y 掺杂的ZrO2(YSZ)常作为SOFC 中的电解质,用以传导O2-,随后发现具有纳米结构的YSZ 存在质子传导而被广泛研究。 在早期工作中,KIM 等人在潮湿环境下观察到YSZ 纳米晶中质子的传导,且随着YSZ 晶粒尺寸的减小质子电导率增加,室温下,当晶粒尺寸从100 nm 减小到13 nm,质子电导率增加3 个数量级[104]。 他们认为晶界是质子传输路径,并将导电性归因于烧结时产生的高晶界密度。 2013 年,SCHERRER 等人研究了多孔YSZ 薄膜和致密YSZ 薄膜在低温下的质子传导[105]。 他们制备了具有不同微观结构和晶粒尺寸的薄膜和块状样品,以探索质子是否通过多孔表面或晶界传输。 在多孔膜中,室温下发现了相当高的电导率,室温至120 ℃,主要发生的是质子沿着YSZ 内表面物理吸附水进行传导,由于其高度依赖于周围大气的湿度,因此随着温度的升高电导率降低。 在120~400 ℃的温度范围内,导电性被热激活,活化能在0.4 eV 到1.1 eV 之间,导电是由O2-和H+所贡献,H+传导是由多孔膜内表面的羟基引起的。 大于400 ℃时,活性能为0.9 eV 至1.3 eV,O2-导电率占主导地位。在纳米多孔体陶瓷YSZ 中也可以观察到相同的行为,与纳米多孔YSZ 相比,完全致密的纳米晶体薄膜仅显示出O2-导电性。 由于多孔膜和致密膜的主要区别在于孔隙率或者开孔的体积,而不是晶粒尺寸,因此可以得出结论,质子是沿着内部开孔的表面而不是晶界传导的。 MIYOSHI 等人的研究也支持了这一结论,他们采用纳米粉末合成与室温超高压压实(4 GPa)相结合的新制备方法,制备了具有不同热稳定性和迁移率的羟基和水分子分级结构的YSZ 致密纳米晶颗粒[38]。 YSZ 样品分别在中温和低温区域显示出基于Grotthuss 机制和Vehicle 机制的高质子电导率。 表面终止羟基、氢键水分子和自由H2O 分子构成纳米结构氧化物内的分级界面水合层,具有热稳定性和同位素交换动力学的特征,这表明界面水合层在作为表面质子传导途径方面发挥着重要作用。 2017年,STUB 等人在较宽的相对湿度(RH)和温度(25~400 ℃)范围内研究了多孔YSZ 陶瓷样品的电性能和载流子机制[39]。 多孔YSZ 在低于150 ℃时表现出纯H+传导,当相对湿度超过60%时,质子传导机制从Grotthuss 机制向Vehicle 机制变化,与吸附水层从“类冰”结构向“类水”结构的变化同时发生。 同时吸附水层的厚度也会影响带电物种的形成焓和迁移焓,当相对湿度从20%增加到84%时,质子传输的活化能从0.43 eV 降低到0.28 eV。 而SUN 等人的研究工作表明不同烧结温度引起的结晶和优选晶面的差异可能对表面质子传导产生重大影响[106]。 较低的烧结温度使样品形成相对圆形的非晶晶粒表面,从而有利于分子化学吸附,而高烧结温度诱导形成优选的表面取向,导致强烈的解离化学吸附,从而导致高的活化能。
3.4 磷矿衍生的质子导体
磷矿石作为磷化工的重要原材料,其在工业上的应用已经超过100 a,我国磷矿石全球储量第二,拥有36.90 亿t 的储量,其相关产品已经深入工业、农业、食品、医药、新能源等领域。 而通过磷化工加工得到的磷酸盐是一类结构多样的酸性固体,根据不同的金属阳离子与磷酸根阴离子组合以及采用不同合成方法,制备得到的磷酸盐结构可以从三维开放骨架到二维层状网络结构再到一维聚合物[107]。 磷酸盐含有酸性磷酸基团(H2PO-4或),水分子可以在磷酸盐骨架内形成氢键,因此磷酸盐可作为质子导体。此外,磷酸盐成本低廉,具有亲水性、良好的热稳定性、结构可设计性等优点。 磷酸二氢铯(CsH2PO4)、焦磷酸盐、杂多酸、聚磷酸盐等因具有优异的质子电导率而被广泛研究。
3.4.1 磷酸二氢铯基质子导体
酸式盐由碱金属阳离子(Li+、K+、Rb+、Cs+)或者铵根离子与不完全电离的多元酸根阴离子组成,表现出介于正酸和盐之间的性质。 酸式盐在室温下表现出较低的质子传导性,但是当温度升高到一定程度时,酸式盐可以发生超质子相变,形成动态无序的氢键网络,从而使得质子电导率提高4 ~ 5 个数量级[108]。 同时,由于酸式盐本身可以形成氢键网络,能够在无水条件下传导质子,而且具有良好的抗H2和O2渗透性能,可以提高PEMFC 的开路电压,这些性质有助于PEMFC 在较高温度下的运行[109]。 酸式盐作为质子导体研究最多是硫酸氢铯(CsHSO4)、硒酸氢铯(CsHSeO4)以及CsH2PO4。
CsHSO4和CsHSeO4受热会分解,被H2还原成H2S 或H2Se 气体从而毒害催化剂,因此,CsH2PO4是研究最广泛的一种酸式盐。 CsH2PO4在230 ℃时发生超质子相变,相变后质子电导率从223 ℃时的8.5 μS/cm 提高到233 ℃时的18 mS/cm,同时在氧化/还原气氛下表现出良好的稳定性,在Pt 催化作用下也没有HxP 物种的生成[110]。 UDA 和HAILE 在不锈钢气体扩散电极上采用悬浮液沉积法制备了CsH2PO4厚度为25 μm 的燃料电池,开路电压为0.98 V,240℃时功率密度达到了415 mW/cm2[111]。 然而CsH2PO4在250 ℃以上会脱水失重形成焦磷酸氢盐和多磷酸盐,直至完全分解成CsPO3[112]。 但是CsH2PO4的分解是可逆的,OTOMO 等人的研究表明,当环境中水分压在0. 3 atm 及以上时能够抑制CsH2PO4的分解并使CsH2PO4保持高的质子电导率[113]。
酸式盐虽然发生超质子相变时具有高的质子电导率,但是酸式盐的水溶性以及较差的机械性能使其在实际应用中仍然面临困难。 通过在酸式盐中加入SiO2、Al2O3、ZrO2等氧化物颗粒形成复合材料,酸式盐与氧化物颗粒之间的相互作用可以产生非晶相,增加复合材料机械强度的同时在超质子相变温度以下增强质子传导[114-116]。 LEAL 等人通过机械研磨将CsH2PO4与SiO2进行复合,SiO2的加入提高了材料的稳定性,在270 ℃时添加SiO2的CsH2PO4比纯CsH2PO4电导率高出一个数量级[116]。
3.4.2 焦磷酸盐基质子导体
MP2O7(M=Sn、Ce、Ti、Zr)在100~300 ℃、低湿度或者干燥条件下具有优异的质子导电性(10-3~10-2S/cm),是最具潜力的中温质子导体之一。 低价金属离子(如In3+、Sc3+、Al3+、Mg2+)的掺入能够有效地提高焦磷酸盐的质子电导率,In0.1Sn0.9P2O7在250℃下的电导率高达0. 195S/cm,Mg2+的掺入将CeP2O7的电导率从 30 mS/cm 提高到 40 mS/cm[117-118]。 关于焦磷酸盐高质子电导率的原因目前还存在争议。 JIN 等人认为焦磷酸盐中质子的掺入是H2O 与电子空穴作用形成,但是并未得到广泛认同[119]。 此外,还有研究指出焦磷酸盐高质子电导率可能与晶界或气孔中次生的无定形相或吸水相有关,或者是合成过程使用过量的H3PO4前驱体和不充分的热处理温度,导致H3PO4在焦磷酸盐表面残留等[120-121]。
由于焦磷酸盐难以形成致密的颗粒,因此以其组装的燃料电池难以获得较高的开路电压,而且存在较大的气体交叉[108]。 为了解决致密性问题,通常将焦磷酸盐与聚合物进行复合,从而获得较好的电池性能。 HEO 等人通过将90%的In0.1Sn0.9P2O7与有机磺酸进行混合制备出复合In0.1Sn0.9P2O7电解质材料,组装成燃料电池后开路电压为0.97 V,200 ℃下的功率密度可以达到187 mW/cm2[122]。 LEE 等人通过将SnP2O7与Nafion 混合制备出复合膜,通过在催化剂中加入季铵盐系聚苯乙烯离聚体粘结剂,在240℃下获得了870 mW/cm2的优异电池性能[123]。
3.4.3 磷钨酸基质子导体
杂多酸也称为多金属氧酸,总共有6 种结构,其中Keggin 类型的杂多酸酸性更强,且结构稳定,化学式为HnXM12O40,X 为杂原子(P、Si),M 为多原子(W、Mo、V)。 其结构为中心的杂原子与氧形成四面体,多原子与氧形成八面体,12 个八面体围绕在一个四面体周围组成杂多酸阴离子[124]。 杂多酸分子通过形成H+、H3O+、H5O2+等离子来桥接水分子,这种水合的水分子结合松散,因此杂多酸表现出高质子传导性[125]。 磷钨酸、磷钼酸在室温下完全水合时,质子电导率可以达到0.18 S/cm。 然而杂多酸易溶于水,导致纯杂多酸质子导体膜失效,可以通过浸渍法或是自组装将杂多酸负载到介孔SiO2载体上[126-127]。与简单的杂多酸与介孔SiO2共混相比,由于杂多酸阴离子锚定在介孔SiO2通道内,杂多酸的耐水性显著提高,且随着杂多酸含量的增加,杂多酸纳米团簇之间的平均间距减小,降低了质子迁移的能垒,从而提高了质子的传导性能。 通过将磷钨酸真空浸渍到介孔SiO2上制备的复合电解质膜,25~90 ℃时质子电导率为0.07~0.11 S/cm,且降低了磷钨酸对水的敏感性[128]。 而以磷钨酸/介孔SiO2组装的燃料电池在150 ℃下,没有外部加湿的情况下功率密度达到372.1 mW/cm2,且电池运行8 d 输出功率几乎恒定[129]。
3.4.4 聚磷酸盐基质子导体
聚磷酸铵(简写为NH4PO3)本身是不良质子导体,在干燥氛围下250 ℃时,电导率仅为10-7S/cm,随着温度的升高,NH4PO3开始部分分解生成HPO3,电导率随之急剧增加,300 ℃时质子电导率达到5 mS/cm[130]。 NH4PO3在湿润气氛下也表现出较高的质子电导率,在湿润的空气中,50~275 ℃温度范围内质子电导率可达0.012~2.61 mS/cm[131]。 为了提高NH4PO3的热稳定性以及力学性能,通常将NH4PO3与(NH4)2MP4O13(M=Si、Ti、Sn)、焦磷酸盐、氧化物(SiO2、TiO2、P2O5-SiO2)进行复合[132-135]。
4 结论与展望
矿物材料的开发利用为无机质子导体的发展提供了坚实的基础。 同时无机质子导体的开发,拓宽了矿物材料的应用领域,提高了矿物材料的利用效率。在众多类型的无机质子导体中,具有萤石结构、烧绿石结构以及钙钛矿结构的氧化物,拥有优异的质子传导性能、良好的稳定性以及简单的制备工艺,是目前无机质子导体的主要研究对象。 氧化物型质子导体主要面临质子传导性能和可烧结性的挑战。 采用不同金属离子对氧化物进行掺杂,通过增加氧空位浓度的方式来增加质子缺陷浓度,是提高氧化物质子传导性能的关键。 掺杂离子的半径和浓度影响着氧化物的整体性能,掺杂离子半径过大或是过小均难以取代氧化物中活性位点上的离子产生氧空位。 掺杂浓度过低,氧空位产生较少,质子传导性能提高不明显;掺杂浓度过高,将会引起氧化物结构的不稳定。 因此,金属离子掺杂存在最佳掺杂离子和掺杂浓度,从而导致离子掺杂对氧化物性能的提高存在上限。 为了提高氧化物的可烧结性,通常的策略就是添加烧结助剂,但是烧结助剂的加入会对氧化物的质子传导性能产生不利的影响,如生成不导质子的杂相、导致掺杂离子的偏析等。 基于目前的研究现状,在后续氧化物型质子导体的研究中可以从以下几个方面考虑:
(1)氧化物界面工程的研究,界面作为质子在氧化物上传导的重要路径,通过对氧化物表面进行功能化改性是提高电解质性能的重要手段。
(2)复合型氧化物质子导体的研发,将氧化物与其他组分进行复合,通过调控不同组分之间的相互作用,从而获得高性能质子导体。 如将氧化物与低温熔盐进行复合,利用熔盐的高温熔融的特性,在增强电解质致密性的同时构筑超质子传导界面。
(3)新的低成本烧结技术的开发,放电等离子烧结、PLD、微波烧结等非常规烧结技术在提高烧结效率、降低能源消耗、改善材料性能等方面表现出巨大的潜力,人工智能的引入、新型烧结介质的开发以及先进的控制系统能够有效降低这些烧结技术的成本。
