磷石膏/固硫灰渣复合材料对铀(Ⅵ)的吸附行为及机理研究
2023-12-22杨国辉廖志慧聂小琴董发勤
夏 雪 周 磊 杨国辉 廖志慧 聂小琴 董发勤,4
(1.西南科技大学环境与资源学院,四川 绵阳 621010;2.核废物与环境安全国防重点学科实验室,四川 绵阳 621010;3.西南科技大学国防科技学院,四川 绵阳 621010;4.固体废物处理与资源化教育部重点实验室,四川 绵阳 621010)
铀是一种高能清洁核燃料,在核能工业发展中起着重要的作用[1]。 铀矿开采、提炼和核燃料循环过程中,会产生大量的含铀低放废水[2]。 这些含铀废水可能通过与核工业有关的活动进入环境,污染地表水和地下水,对人类健康造成潜在威胁[3-4]。 因此,需要采用经济、高效的方法对含铀废水进行处理,达标排放。 吸附法具有吸附能力强、生产成本低、操作方便和可重复使用等特点[5],被认为是从水溶液中提取铀的有效方法。 吸附法的关键是吸附材料的选择,寻找和开发高效低廉的天然吸附材料对于含铀废水的污染防治具有重要的意义。
磷石膏(PG)是湿法磷酸工艺中产生的工业固体废弃物[6],对磷石膏进行资源化利用具有重要的现实意义[7-8]。 磷石膏的主要成分为硫酸钙以及少量的磷酸盐、磷酸和氟化物等[9],其中磷酸主要以H3PO4、H2PO-4、和等形式存在于水溶液中,可溶性磷容易与钙离子和铀离子形成不溶性的钙盐,可用于含铀废水的处理[10-11]。 SYCZEWSKI 等[12]分析了磷石膏和黏土矿物基陶瓷复合材料的吸附能力,其对铀(Ⅵ) 的最大吸附量约0. 09 mol/kg。HAGAG 等[13]以磷石膏和氢氧化铝为主要原料合成了复合吸附材料,其理论吸附容量可达477 mg/g,吸附性能受体系中共存元素的影响较小,使用2 mol/L的盐酸可实现材料上铀的洗脱。
1 试验材料、仪器及方法
1.1 试验材料与设备
本试验所用磷石膏(PG)和固硫灰渣(SFA)均取自绵阳安洲区路林磷化工有限公司,磷石膏和固硫灰渣的主要成分如表1、表2 所示。
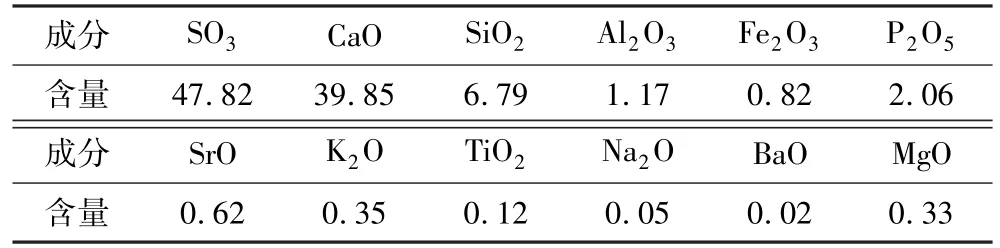
表1 磷石膏主要成分分析结果Table 1 Results of main components analysis of PG%
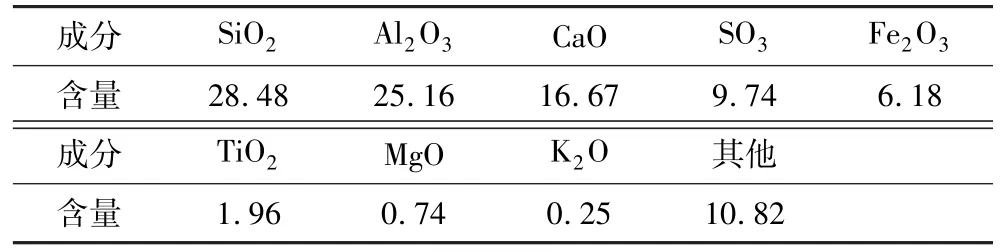
表2 固硫灰渣主要成分分析结果Table 2 Results of main components analysis of SFA%
所用药剂包括Na2CO3、HCl、Na3PO4·12H2O、Na2SO4、 NaF、 NaNO3、 NaCl、 NaOH、 FeCl3·6H2O、SrCl2·6H2O、CaCl2、 BaCl2·2H2O、 NiCl2·6H2O 和UO2(NO3)2·6H2O,除UO2(NO3)2·6H2O(中国西安鼎盛有限公司)外,均购自成都金山化学试剂有限公司,所有试剂均为分析纯。
本试验所用仪器包括场发射扫描电子显微镜(SEM/EDS,Ultra 55,德国蔡司仪器公司),傅里叶变换红外光谱仪(FTIR,PerkinElmer Spectrum One,美国PE 仪器公司),X 射线光电子能谱仪(XPS,Thermo Escalab 250 electron spectrometer,美国ThermoFisher科技公司)和X 射线衍射仪(XRD,X′Pert PRO,荷兰帕纳科公司),微量铀分析仪(WGJ-III,杭州大吉光电仪器公司),电感耦合等离子体原子发射光谱仪(ICP-OES, iCA P6500, 美国 ThermoFisher 科技公司)。
1.2 PG/SFA 复合粉体的制备
将磷石膏与固硫灰渣分别研磨成细粉,并烘干。按照磷石膏与固硫灰渣的质量比0 ∶1、0. 5 ∶1、1 ∶1、2 ∶1、3 ∶1、4 ∶1、5 ∶1 分别混合均匀,置于马弗炉内800℃下煅烧1 h,取出煅烧产品,冷却至室温后研磨筛选得到PG/SFA 复合粉体,粒度小于0.074 mm。
1.3 批次吸附试验
1.3.1 吸附试验
将50mL 一定浓度的铀溶液加入锥形瓶中,随后加入一定质量的PG/SFA 复合材料,用1.0 mol/L 盐酸或碳酸钠调整溶液的pH 值,在一定温度下反应一段时间后,测量溶液中剩余铀浓度,计算PG/SFA 复合材料对铀的吸附量和去除率。
1.3.2 共存离子体系中PG/SFA 对铀的吸附
配制混合溶液1:铀浓度10. 0 mg/L,NO-3、F-、Cl-、SO24-、PO34-浓度5. 0 mg/L;混合溶液2:铀浓度10.0 mg/L,Ca2+、Ba2+、Sr2+、Ni2+、Fe3+浓度5.0 mg/L。用1.0 mol/L 碳酸钠或盐酸调节溶液pH 至6.0,加入0.02 g PG/SFA 反应60 min,取上清液测定剩余铀的浓度,分析各种阴离子和阳离子对PG/SFA 吸附铀的影响。
1.3.3 实际铀矿坑水的吸附试验
采集中国若尔盖铀矿区的铀矿坑水进行吸附试验,研究PG/SFA 对实际含铀废水的处理效果。 将50 mL 的铀矿坑水加入锥形瓶中,通过1.0 mol/L 盐酸和碳酸钠将溶液的pH 调整到6.0。 将0.02 g PG/SFA 加入50 mL 铀矿坑水中,在室温恒温振荡浴中振荡12 h。 吸附平衡后测定溶液中铀等金属离子的浓度,计算PG/SFA 对铀的去除率和吸附量[18-19]。
2 试验结果与讨论
2.1 PG/SFA 质量比的影响
在铀初始浓度为10 mg/L,PG/SFA 投加量0.02 g,溶液pH=6.0,吸附时间60 min,吸附温度25 ℃的条件下,考察PG/SFA 质量比对铀吸附效果的影响,结果见图1。
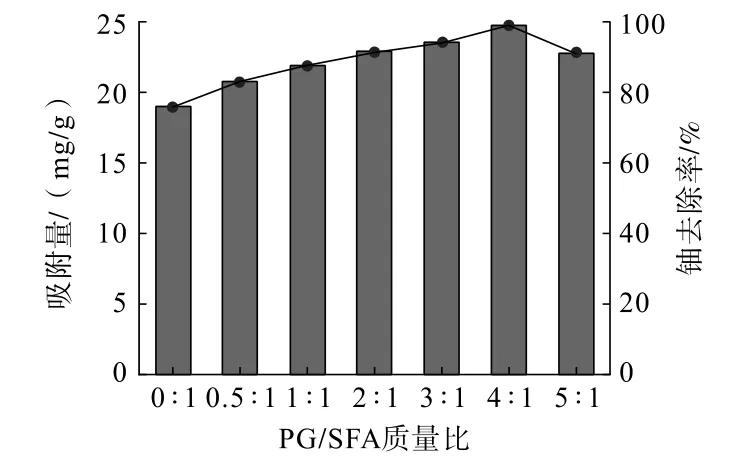
图1 PG/SFA 质量比对铀吸附效果的影响Fig.1 Influence of mass ratio of PG/SFA on uranium adsorption effect
分析图1 可知,随着磷石膏掺量的增加,PG/SFA复合材料对铀的吸附能力先上升后降低。 当磷石膏与固硫灰渣质量比为4 ∶1 时,PG/SFA 复合材料对铀的吸附效果最好,吸附量和去除率分别达24.7 mg/g和98.88%。
2.2 PG/SFA 投加量的影响
在铀初始浓度为10 mg/L,PG/SFA 质量比为4 ∶1,溶液pH=6.0,吸附时间60 min,吸附温度25 ℃的条件下,考察PG/SFA 投加量对铀吸附效果的影响,结果见图2。
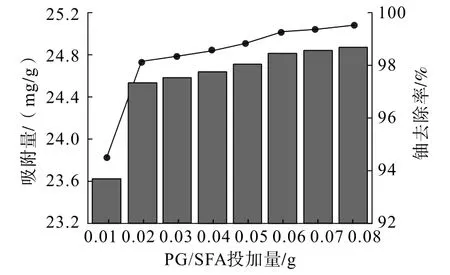
图2 PG/SFA 投加量对铀吸附效果的影响Fig.2 Influence of dosage of PG/SFA on uranium adsorption effect
分析图2 可知,随着PG/SFA 投加量的增加,PG/SFA 复合材料对铀的吸附能力逐渐增大后趋于稳定。 当PG/SFA 复合材料的投加量为0.02 g 时,PG/SFA 对铀的吸附量为24. 5 mg/g,铀去除率为99.13%;进一步增加PG/SFA 投加量,铀去除率的提升不明显。 综合考虑,选择PG/SFA 投加量0. 02 g进行后续试验。
2.3 溶液pH 的影响
在铀初始浓度为10 mg/L,PG/SFA 质量比为4 ∶1,PG/SFA 投加量0.02 g,吸附时间60 min,吸附温度25 ℃的条件下,考察溶液pH 对铀吸附效果的影响,结果见图3。
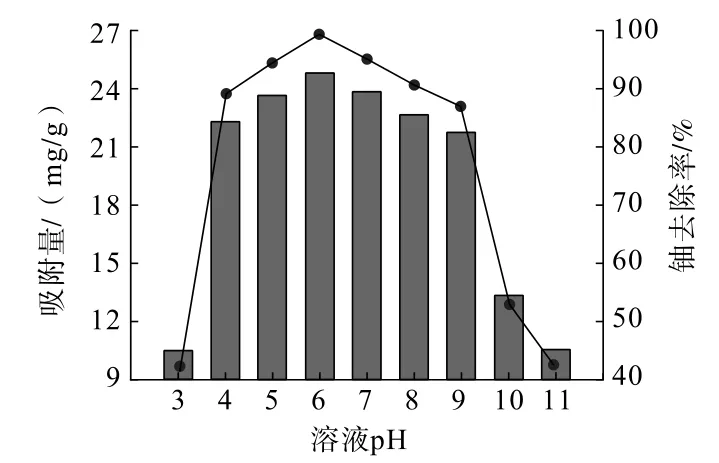
图3 溶液pH 对铀吸附效果的影响Fig.3 Influence of pH of solution on uranium adsorption effect
分析图3 可知,随着溶液pH 值的增加,PG/SFA复合材料对铀的吸附能力先上升后降低。 较宽的pH范围(4.0~9.0),PG/SFA 复合材料对铀的去除率均能保持在90%以上,且在pH=6.0 时表现出最大的吸附能力,吸附量和去除率分别达24. 8 mg/g 和99.2%。
结合Visual MINTEQ 3.1 数据库数据,计算铀在不同pH 值溶液中形态分布,如图4 所示。 结合PG/SFA 复合材料的Zeta 电位分析结果(图5)可知,当pH 为2.0~5.0 时,铀主要以的形式存在,此时PG/SFA 表面电荷为正,与之间电子排斥力较大,吸附量较低[20]。当pH 为5.0~9.0 时,铀主要以UO2CO3(OH)23-的形式存在,此时PG/SFA 与其结合能力最强。 当pH>9 时,铀主要以UO2(OH)24-和UO2(OH)-3的形式存在,但此时PG/SFA 表面电荷为负,同样也会与铀产生电子排斥作用[21]。
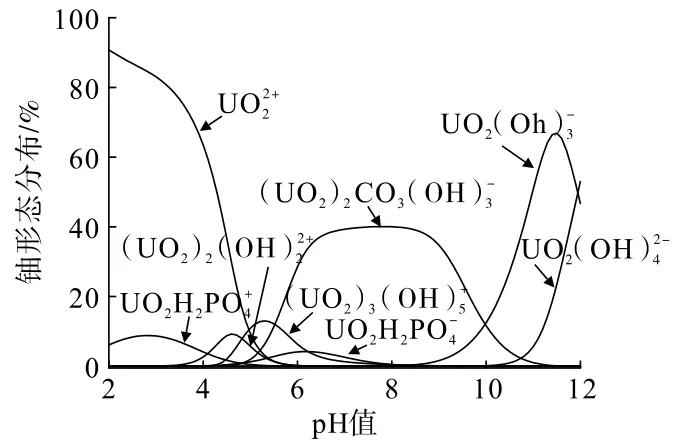
图4 不同pH 条件下铀形态分布Fig.4 Uranium morphology distribution under different pH conditions
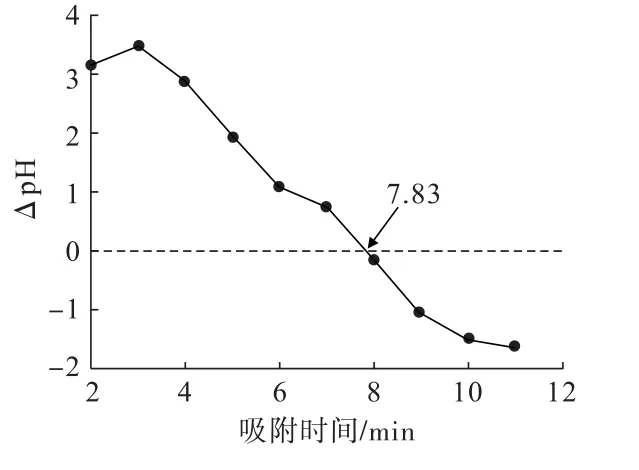
图5 PG/SFA 复合材料零电荷点分析Fig.5 Point of zero charge analysis of PG/SFA composites
2.4 吸附动力学研究
在铀初始浓度为10mg/L,PG/SFA 质量比为4 ∶1,PG/SFA 投加量0.02 g,溶液pH 为6.0 的条件下,不同吸附温度下吸附时间与铀吸附量的关系见图6。
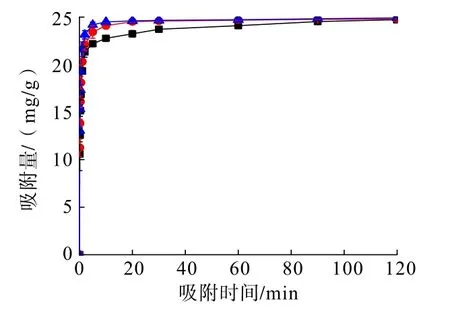
图6 不同吸附温度下吸附时间与铀吸附量的关系Fig.6 The relationship between adsorption time and uranium adsorption capacity at different adsorption temperatures
分析图6 可知,对于3 种吸附温度,PG/SFA 复合材料对铀的吸附在前10 min 内迅速增加,大量的活性位点迅速捕获溶液中的铀酰离子。 随着吸附反应的进行,活性基团被占据,最终在60 min 左右达到吸附平衡。 吸附温度越高,达到吸附平衡的时间越早,这表明适当地提高反应温度有利于铀的吸附。
采用准一级、准二级、粒子内扩散和Elovich 这4 种吸附动力学模型进行数据拟合[22],用于揭示PG/SFA 吸附过程中的速率控制步骤,动力学模型如下:
式中,qe为平衡时的吸附量,mg/g;qt为t时刻的吸附量,mg/g;k1为准一级动力学模型的吸附速率常数,min-1;k2为准二级动力学模型的吸附速率常数,(g·(mg·min)-1);k3为粒子内扩散动力学模型的吸附速率常数,mg·min-0.5·g-1;a、b均为Elovich 模型吸附动力学常数。
图7 为动力学模型拟合曲线,表3 及表4 为动力学模型拟合参数。 分析可知,准二级动力学模型更适用于描述PG/SFA 吸附铀的过程,其R2>0. 99[23]。同时,理论计算值qe与实验值qe接近,吸附过程主要是PG/SFA 固有的磷酸基团与铀之间的化学吸附作用[24]。
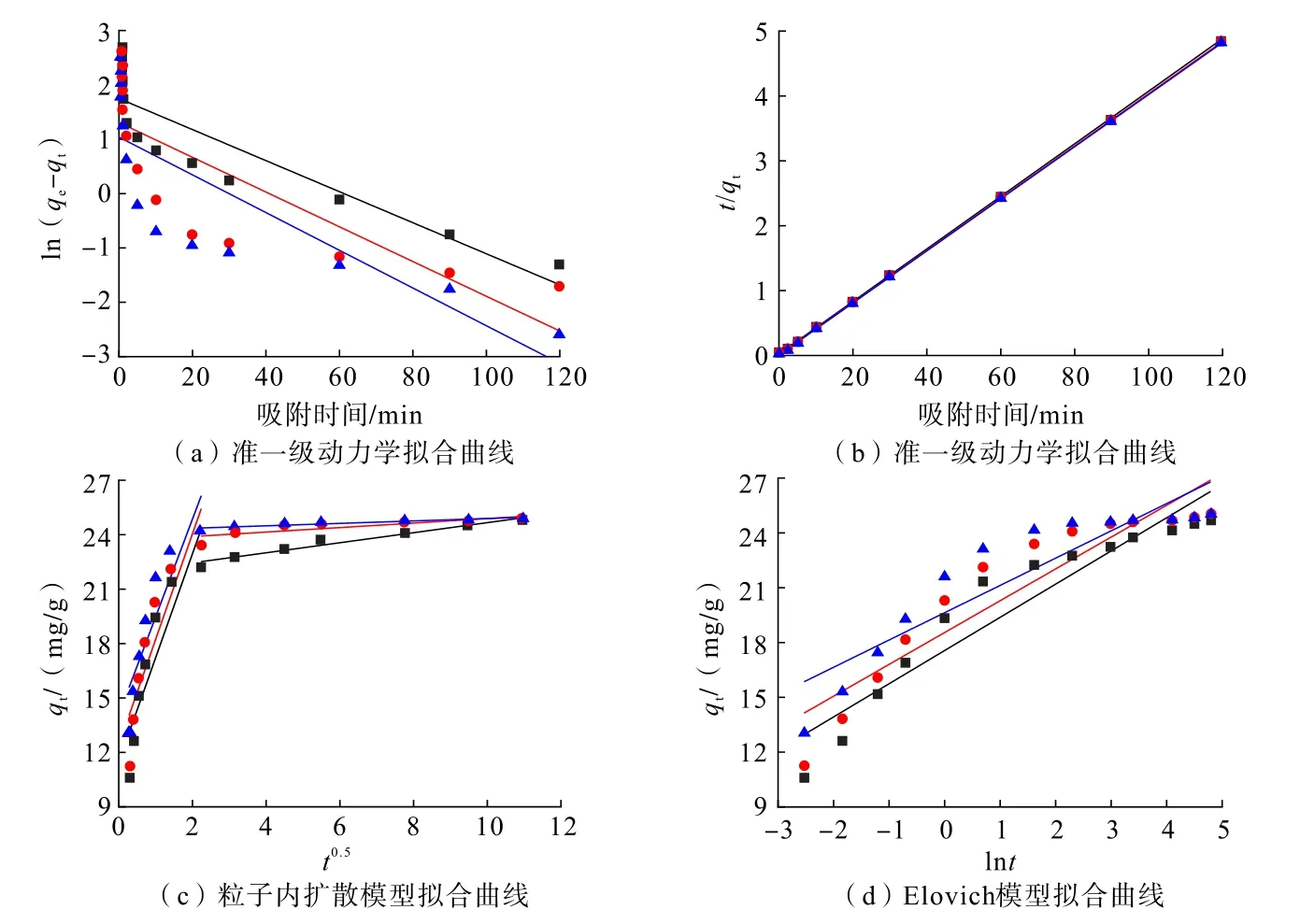
图7 动力学模型拟合曲线Fig.7 Fitting curves of dynamics models
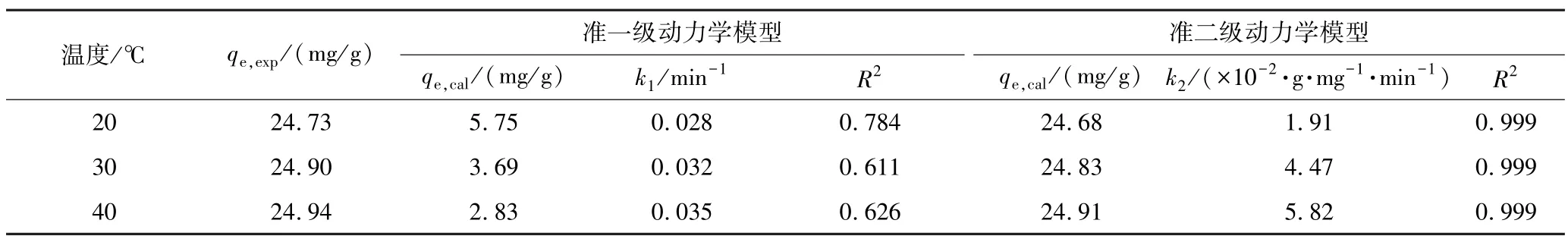
表3 准一级及准二级动力学模型拟合参数Table 3 Fitting parameters of dynamics models of pseudo-first-order and pseudo-second-order
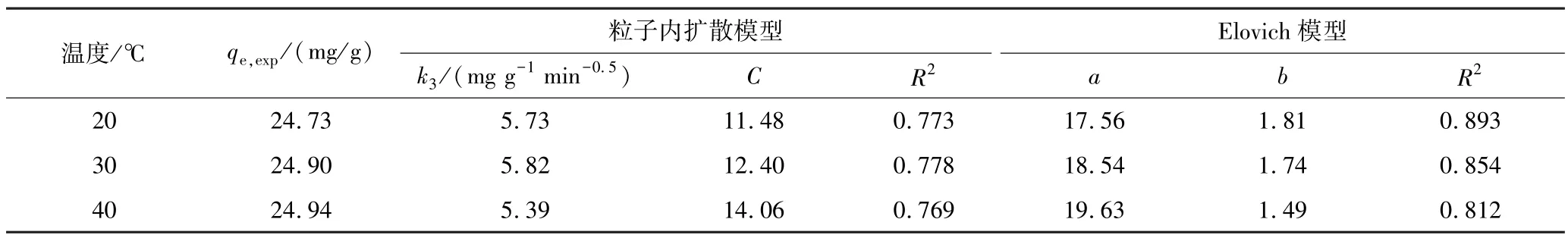
表4 粒子内扩散模型及Elovich 模型动力学模型拟合参数Table 4 Fitting parameters of dynamics models of intra-particle diffusion model and Elovich model
2.5 吸附等温模型研究
在PG/SFA 质量比为4 ∶1,PG/SFA 投加量0.02 g,溶液pH 为6.0,吸附时间为60 min 的条件下,不同吸附温度下铀初始浓度与铀吸附量的关系见图8。
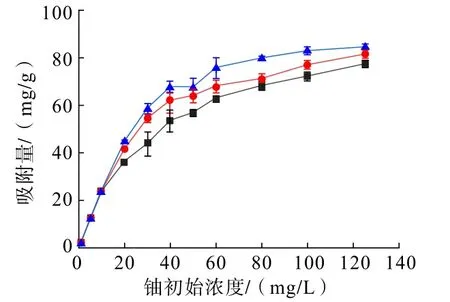
图8 不同吸附温度下铀初始浓度与铀吸附量的关系Fig.8 The relationship between uranium initial concentration and uranium adsorption capacity at different adsorption temperatures
分析图8 可知,对于3 种吸附温度,PG/SFA 复合材料对铀的吸附量随铀初始浓度的增大而逐渐增加,最大吸附容量达到84.6 mg/g。 在低铀浓度条件下,PG/SFA 固有的大量磷酸基团与铀作用,基本实现铀的全捕获,而高铀浓度条件下铀的吸附量趋于平衡。 PG/SFA 复合材料的最大吸附能力随吸附温度的升高而增强。
利用Langmuir、Freundlich 和Dubinin-Radushkevich(D-R)等温模型对吸附数据进行拟合,Langmuir等温模型如下[25]:
式中,Ce为平衡浓度,mg/L;qm为理论饱和吸附量,mg/g;kL为平衡常数,L/mg。
Freundlich 等温模型如下[26]:
式中,kF为吸附量,mg/g;n为吸附强度的常数。
D-R 等温模型如下[27]:
式中,qDR为单层饱和吸附容量,mol/L;β为与吸附自由能有关的常数,mol2/kJ2;E为平均自由能,kJ/mol。
图9 为等温吸附模型拟合曲线,表5 为等温吸附模型拟合参数。 分析可知,PG/SFA 复合材料吸附铀的过程更适合采用Langmuir 模型描述,其理论吸附容量与实验吸附容量接近,吸附过程属于单分子层吸附[28],铀与PG/SFA 之间主要受化学吸附机制的控制[29]。
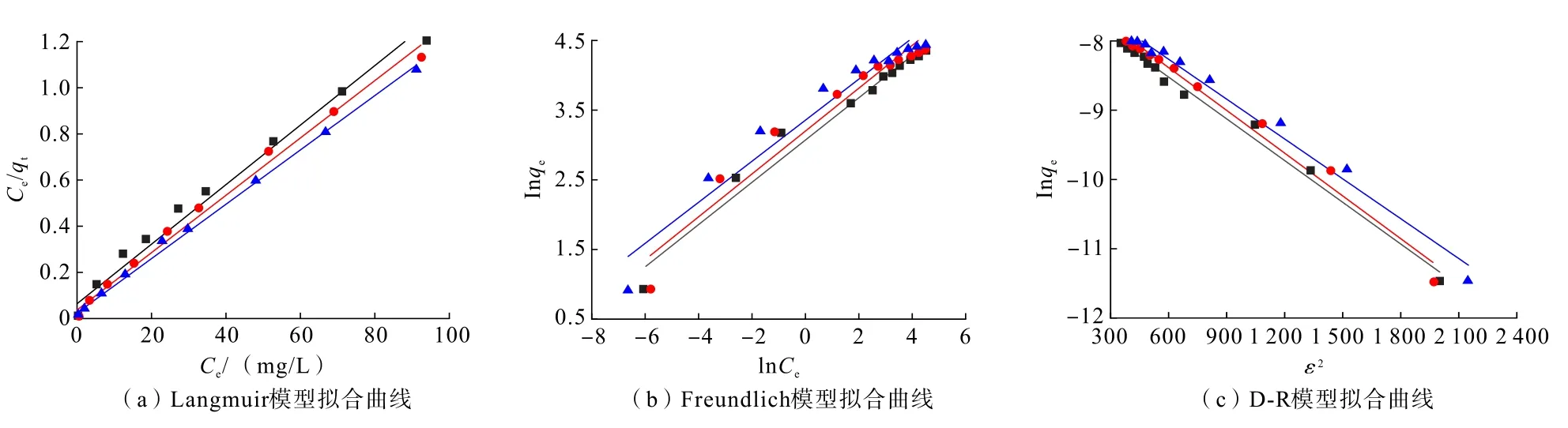
图9 等温吸附模型拟合曲线Fig.9 Fitting curves of isotherm adsorptionmodels
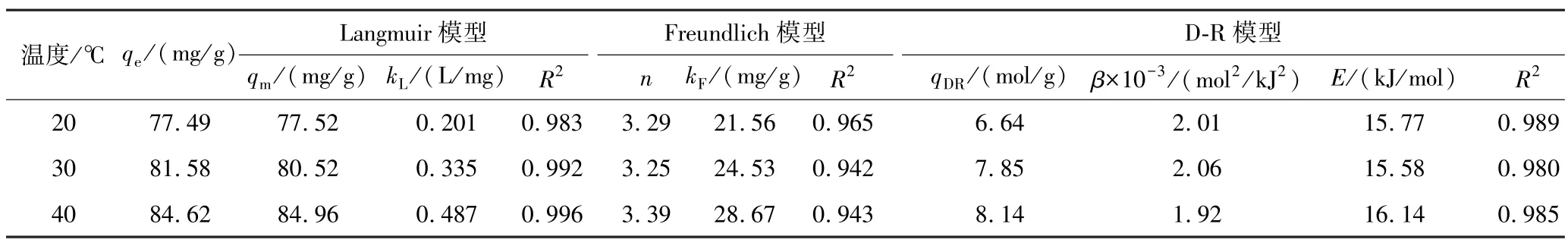
表5 等温吸附模型拟合参数Table 5 Fitting parameter of isotherm adsorption models
2.6 吸附热力学研究
根据Vander Hoff 方程[30]计算PG/SFA 吸附铀的吸附热效应,不同温度下的qmax值如图10 所示,热力学参数ΔG、ΔS和ΔH如表6 所示。 结果表明,PG/SFA 复合材料对铀的最大吸附能力随温度的升高而显著增加;PG/SFA 复合材料和铀的结合过程是自发的(ΔG随温度升高而降低,ΔG<0),且是吸热反应(ΔH=34.93 kJ/mol),吸附过程中的随机性增加(ΔS=152.31 J/(mol·K))。
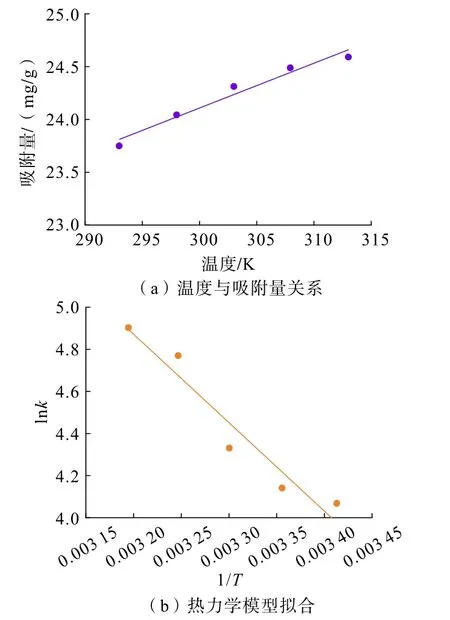
图10 PG/SFA 复合材料对铀吸附的热力学分析Fig.10 Thermodynamics analysis of uranium adsorption by PG/SFA composite

表6 PG/SFA 复合材料对铀的吸附热力学参数Table 6 Thermodynamic parameters of uranium adsorption by PG/SFA composite
2.7 离子种类对PG/SFA 复合材料吸附铀的影响
为探究离子种类对PG/SFA 复合材料吸附铀的影响,分别设置了不同阴离子与铀共存溶液体系和不同阳离子与铀共存溶液体系,分析各类阴离子和阳离子对PG/SFA 复合材料吸附铀的影响,结果见图11。
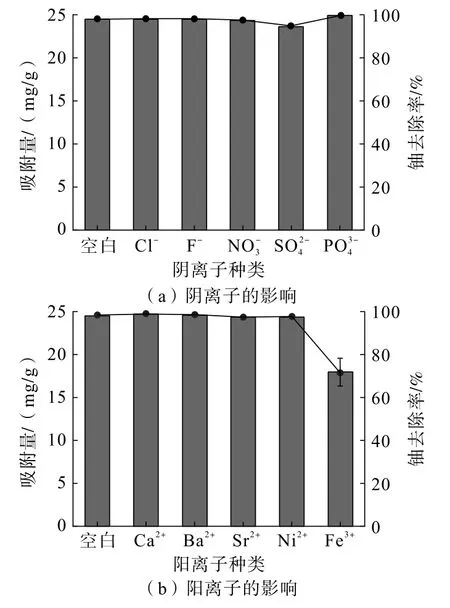
图11 离子种类对PG/SFA 复合材料吸附铀的影响Fig.11 Influence of ion type on adsorption of uranium by PG/SFA composites
分析图11(a)可知,在各类阴离子存在的情况下,PG/SFA 复合材料对铀的吸附能力均能达到90%以上,其对含SO24-铀溶液中铀的吸附容量略低于含Cl-、F-、NO-3、的铀溶液。 Cl-、NO-3、F-可与溶液中的铀离子形成UO2Cl+、UO2NO+3、UO2F-3等可溶性配合物,而SO24-与铀离子具有较强的络合能力,从而影响了复合材料对铀的吸附[31-33]。的存在对PG/SFA 复合材料吸附铀具有促进作用,加入后更有利于生成矿化物Ca(UO2)2(PO4)2·3H2O[34]。
分析图11(b)可知,在各类阳离子存在的情况下,含Ca2+、Ba2+、Sr2+、Ni2+溶液中铀的吸附容量基本不受影响,然而Fe3+存在的铀溶液中,铀的吸附量明显下降。 由于在含Fe3+的铀溶液中,Fe3+与铀存在竞争关系,Fe3+会优先抢占PG/SFA 复合材料的表面活性位点,致使材料的吸附容量降低[35]。
2.8 PG/SFA 复合材料在铀矿坑水中的应用研究
为考察PG/SFA 复合材料的实际应用性能,开展若尔盖铀矿场含铀废水的除铀试验研究,结果见图12。
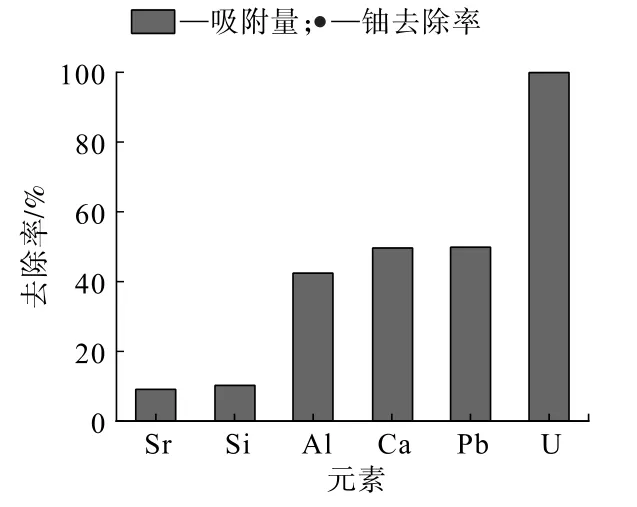
图12 PG/SFA 复合材料对铀矿坑水的处理效果Fig.12 Treatment effect of PG/SFA composites on uranium mine water
分析图12 可知,在众多离子共存体系下,PG/SFA 复合材料对铀的吸附率最高,达99.8%。 根据下式计算PG/SFA 复合材料对各离子的分配系数(Kd)和选择性系数(SU)[24],结果列于表7。
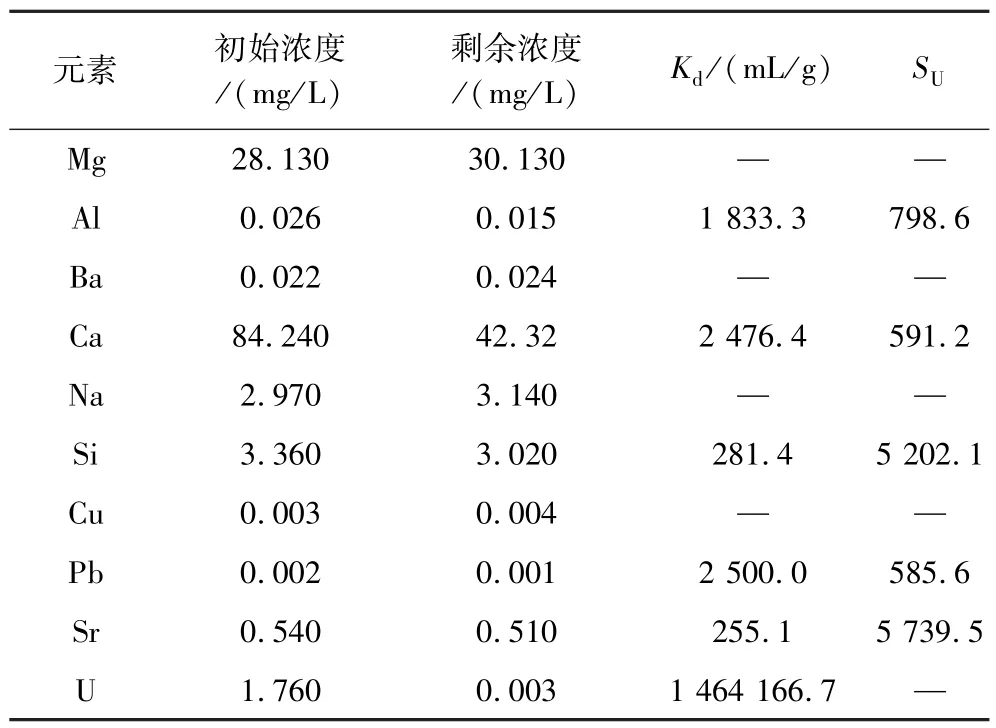
表7 PG/SFA 复合材料对各离子的分配系数(Kd)和选择性系数(SU)Table 7 Distribution coefficient (Kd) and selectivity coefficient (SU) of PG/SFA composites
式中,Kd表示吸附剂对吸附质的结合亲合力,mL/g;和分别为铀离子和其他竞争离子在吸附剂和溶液中的分配比。
分析表7 可知,PG/SFA 复合材料的Kd值最高,达1.46×106mL/g;同时,铀离子和其他竞争离子相比的选择性系数(SU)较高,说明与其他共存的离子相比,铀的吸附具有明显的优势。
2.9 机理分析
2.9.1 SEM-EDS 分析
图13 为PG 及PG/SFA 复合材料吸附铀前后的SEM-EDS 分析结果。
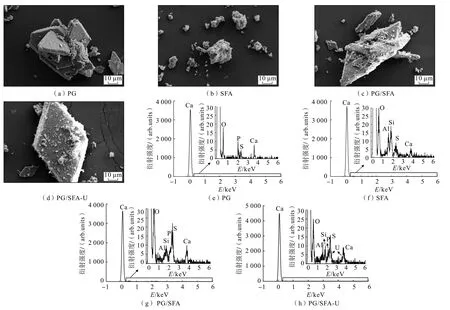
图13 SEM-EDS 分析结果Fig.13 Results of SEM-EDS analysis
由图13(a)可知,PG 以斜晶体柱为主,晶体结构主要为菱形,晶体表面有少许细小的矿物颗粒[36]。EDS 分析表明PG 主要由Ca、O、P、S 这4 种元素组成的(图13(e)),也证明了磷石膏中主要成分为生石膏。 图13(b)显示SFA 呈现不规则粉末,主要元素有Ca、O、Al、Si 和S(图13(f));图13(c)显示PG/SFA 复合材料以斜晶体为主,晶体结构依然为菱形,掺入固硫灰渣后表面附着的粉体增多。 吸附铀后(图13(d)),PG/SFA 复合材料表面有晶体附着,EDS 分析图谱(图13(h))中发现了铀的存在,表明PG/SFA 复合材料对铀具有很高的亲和力且铀成功被吸附/矿化在PG/SFA 表面。
2.9.2 FTIR 分析
PG、SFA 及PG/SFA 吸附铀前后的红外光谱如图14 所示。
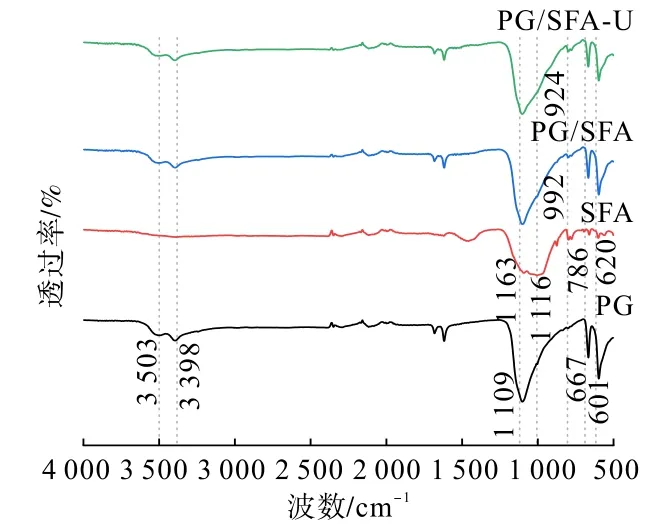
图14 红外光谱分析结果Fig.14 Results of FTIR analysis
由图14 可知,对于PG,3 503 cm-1和3 398 cm-1处为PG 结晶水的—OH 伸缩振动吸收峰,1 109 cm-1处为SO24-的γ3伸缩振动吸收峰,667cm-1和601 cm-1处为SO24-的γ4伸缩振动吸收峰[28]。对于SFA,1116cm-1处为Si—O与Al—O基团的伸缩与弯曲振动[37],620 cm-1处为硬石膏的特征峰,786 c m-1为石灰石(CaCO3) 的特征峰[38]。 对于PG/SFA,呈现明显的PG特征峰,在786cm-1出现明显的SFA特征峰,说明该复合材料制备成功。PG/SFA吸附铀后,992 cm-1处出现了P—O 的拉伸振动峰,在924 cm-1还出现U—O 的不对称拉伸振动新峰[39]。 P—O 的出现表明磷基团是参与铀吸附的有效官能团,与铀之间形成了配位键。
2.9.3 XRD 分析
PG/SFA 复合材料吸附铀前后的XRD 表征结果如图15 所示。
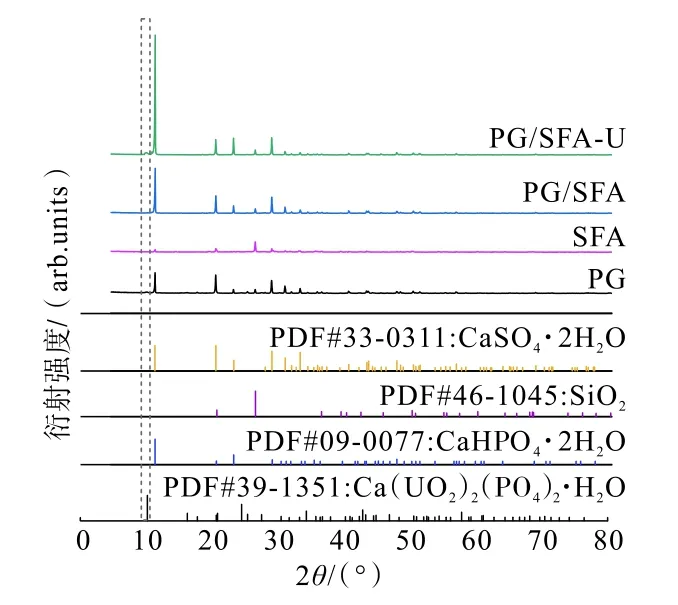
图15 PG、SFA、PG/SFA 吸附铀前后的XRD 图谱Fig.15 XRD patterns of PG,SFA and PG/SFA before and after adsorption of uranium
从图15 可以看出,磷石膏中主要矿物为生石膏(CaSO4·2H2O),并含有少量未反应的CaHPO4·2H2O和SiO2[40];固硫灰渣的主要矿物为二氧化硅(SiO2),并含有部分生石膏矿相。 将磷石膏与固硫灰渣进行复合和煅烧后,主要成分变成了硫酸钙(CaSO4)和二氧化硅(SiO2),剩余的矿相均不溶于水中,可以证明该复合粉体材料制备成功。 从图15 还可以看出,PG/SFA 吸附铀后出现了少量的Ca(UO2)2(PO4)2·3H2O 的晶体,表明PG/SFA 的Ca2+和与发生沉淀反应,成功将溶液中的铀固化生成了钙铀云母Ca(UO2)2(PO4)2·3H2O。 结果表明,PG/SFA 表面与铀之间可能存在表面物理吸附和化学络合[41]。
3 结 论
(1)在pH=6.0、PG/SFA 投加量0.02 g、平衡吸附时间60 min、铀初始浓度125 mg/L、吸附温度40℃的条件下,PG/SFA 对铀的最大吸附容量为84. 6 mg/g。
(2)PG/SFA 对铀的吸附服从准二级动力学模型和Langmuir 模型,为化学吸附过程,属于单分子层吸附方式。
(3)PG/SFA 对实际铀矿坑水中铀的去除率为99.8%,铀的分配系数达1.46×106mL/g,表现出好的铀净化效果。
(4)吸附铀后,铀在PG/SFA 上主要是以钙铀云母Ca(UO2)2(PO4)2·3H2O 矿相结构形式存在,这归因于PG/SFA 中存在的Ca2+和PO34-与UO22+发生了表面沉淀反应。
