喹诺酮配合物材料的制备及其抗菌性能研究*
2023-11-09夏姣云李潇潇
夏姣云,李潇潇,徐 彤,杨 灿
(长沙理工大学 化学化工学院,长沙 410114)
0 引 言
癌症是现代致死率最高的流行病之一。据研究,所有癌症中有近1/5的感染源都是微生物感染,因其感染而导致的各种疾病,都严重威胁着人类健康[1-5]。细菌感染可以用抗生素治愈,这对癌症的预防也具有重要意义。金属配合物作为有效药物的广泛使用,例如癌症治疗药物[6]、抗炎药[7]、降糖药或抗菌剂和诊断剂[8-9],表明金属离子的细胞毒性可以通过适当的配体选择得到很好的控制。喹诺酮类是具有优异配合特性的合成化合物,可作为双齿配体、单齿配体和桥联配体与金属离子结合形成配合物[10-12]。喹诺酮类药物与金属离子的相互作用,可以获得许多与母体喹诺酮类化合物具有同等或更强的抗菌活性的金属配合物[13-15]。铂、钌、钴、钯、铜和其他d-嵌段金属离子的配合物已在医学上广泛应用。但是铂类抗癌药物有很强的副作用,如周围神经病变、脱发和患者的骨髓毒性等。因此研究人员致力于开发可提供不同作用模式和改善抗癌活性的替代金属药物,而铜离子异于铂类化合物的特殊生物活性使其脱颖而出,铜很容易在还原态Cu(Ⅰ)和氧化态Cu(Ⅱ)之间循环,是生物系统、生命活动甚至生物细胞成分中不可或缺的重要元素[16-17]。铜配合物的抗肿瘤活性早在几十年前就已被报道,许多新的配合物已显示出巨大的抗菌、抗肿瘤潜力[18-20]。铜配合物可能比铂类药物的副作用相对较低,并被认为能够克服顺铂的遗传和获得性耐药性。本文选用喹诺酮类抗生素环丙沙星作为第一配体,苯并咪唑类化合物作为第二配体,通过微波辅助合成法合成新型三元铜配合物,并将铜配合物用于对大肠杆菌、金黄色葡萄球菌的抗菌活性测试。研究结果表明,配合物与单一的喹诺酮类抗生素具有更强的抗菌活性。
1 实 验
1.1 实验原材料
5-甲基-2-(2′-吡啶基)苯并咪唑按照文献[21]合成;牛肉膏蛋白胨培养基、牛肉膏蛋白胨琼脂培养基、牛血清白蛋白(BSA)、溴化乙锭(EB)均为生化试剂,生工生物工程(上海)股份有限公司;小牛胸腺DNA:生化试剂,索莱宝生物技术有限公司;三羟甲基氨基甲烷(Tris):生化试剂,上海阿拉丁生化科技股份有限公司;噻唑蓝(MTT):生化试剂,上海麦克林生化科技有限公司;环丙沙星、高氯酸铜六水合物,上海麦克林生化科技有限公司;其他试剂为市售的分析试剂,实验用水为去离子水。研究配合物与牛血清白蛋白作用时,底液为含0.05 mol/L NaCl的pH值=7.2的Tris-HCl 缓冲溶液,配制的EB溶液和牛血清蛋白溶液浓度分别为1×10-3、3×10-6mol/L;研究配合物与牛血清白蛋白作用时,底液为含0.05 mol/L NaCl的pH值=7.2的Tris-HCl 缓冲溶液,配制的EB溶液和牛血清蛋白溶液浓度分别为1×10-3、3×10-6mol/L。
1.2 配合物的合成
取0.3313 g(1 mmol)环丙沙星溶于10 mL水中,并用等摩尔量的NaOH中和,再加入0.2416 g(1 mmol)Cu(NO3)2·3H2O,室温搅拌,混合均匀。再将溶有0.2091 g(1 mmol)HPBM用30 mL乙醇溶解,再用(0.2 mol/L)NaOH 调节pH值至5~6,将混合溶液转移至圆底烧瓶中,置于120 ℃油浴中,冷凝回流1.5 h,冷却过滤,弃去浅绿色固体。滤液在室温下放置,数周后有蓝绿色晶体析出,乙醇重结晶,空气中干燥后置于干燥器中保存。

图1 化合物SF-Cu-HPBM结构示意图Fig.1 Schematic diagram of the compound SF-Cu-HPBM structure
1.3 样品的性能及表征
1.3.1 傅里叶变换红外光谱仪(FT-IR)
通过FT-IR光谱仪分析样品的分子结构和化学组分,Nicolet iS20型,上海赛默飞世尔科技有限公司。
1.3.2 元素分析仪(EA)
通过元素分析仪分析环丙沙星和SF-Cu-HPBM的元素组成和含量,Elementar UNICUBE型,德国元素-艾力蒙塔贸易(上海)有限公司。
1.3.3 紫外分光光度计(UV-Vis)
通过紫外分光光度计分析环丙沙星和SF-Cu-HPBM的光吸收性能以及与小牛胸腺DNA的作用,F7000型,日本日立公司。
1.3.4 高分辨质谱仪(ESI-MS)
通过ESI-MS测试SF-Cu-HPBM的组成,Waters G2-XS Qtof型,沃特世科技(美国)有限公司。
1.3.5 精密电导率仪
通过电导率仪分析化合物的电解质类型,MP515-03型,上海三信仪表厂。
1.3.6 荧光分光光度计
通过荧光分光光度计分析配合物与DNA结合的方式,F7000型,美国Millipore System (Biocel) 公司。
1.3.7 乌氏粘度计
通过乌氏粘度计分析配合物与DNA的作用,PH-010A 型,上海一恒科学仪器有限公司。
2 结果与讨论
2.1 配合物表征
2.1.1 红外光谱分析
室温下,测定了配体环丙沙星、及配合物SF-Cu-HPBM在400~4 000 cm-1范围内的红外光谱。喹诺酮为第一配体,苯并咪唑类为第二配体的红外分析结果见表1,实验结果表明:(1)SF-Cu-HPBM配合物分别在3 474.39 cm-1出现吸收峰,而环丙沙星配体中未出现,这归因于配合物-NH2+的伸缩振动ν—NH2+及结合水的O-H伸缩振动峰ν—O—H。(2)环丙沙星在3 043.87 cm-1出现了吸收峰,这是哌嗪基上N—H的伸缩振动v—NH,而SF-Cu-HPBM配合物分别在2979.78 cm-1处出现了吸收峰,这是第二配体咪唑环上N-H的伸缩振动ν—NH。(3)环丙沙星在1 613.96 cm-1(νC=O)、1 498.28 cm-1(νC—OH)、1 372.60 cm-1(νas(COO—))三处表现强的吸收峰,这归因于羧基的C=O伸缩振动、C—OH的伸缩振动和COO-的对称伸缩振动。在配合物中并没有出现—COO—的3个特征吸收峰,由于形成配合物,羧基峰特征峰向低波数方向位移,SF-Cu-HPBM配合物在1 627.25,1 461.83,1 292.23 cm-1处分别表现3个强吸收峰,分别归属于C=O的伸缩振动(νC=O)、—COO—的不对称伸缩振动νas(COO—)和对称伸缩振动νas(COO—),这意味着第一配体环丙沙星中的羧酸基团脱去了H离子,并通过COO-阴离子单齿与中心铜离子配位。(4)另外,SF-Cu-HPBM配合物在511.52、429.20 cm-1处分别表现的两个吸收峰为Cu-O和Cu-N的伸缩振动,这进一步表明两种配体均与中心铜离子发生了配位。

表1 苯并咪唑类配合物与配体的红外特征峰Table 1 Infrared characteristic peaks of benzimidazole complexes and ligands
2.1.2 元素分析
元素分析是研究有机化合物中元素组成和含量的化学分析方法。根据比较理论与实际合成化合物中C、H、N 3种元素的百分含量,来分析化合物是否与预期一致。如表2所示,配合物中各元素的实验测定值与计算值较为吻合,百分含量相差不大,与预期实验结果一致。

表2 5种配合物的元素分析数据Table 2 Elemental analysis data of five complexes
2.1.3 紫外光谱分析
室温下,测定了配合物的DMSO溶液(1×10-2~1×10-5mol/L)在200~450 nm和450~800 nm范围内的紫外可见吸收光谱。如表3所示,配合物与配体的DMSO溶液在近紫外区283.00~284.50 nm和331.50~332.00 nm处均有2个较强的吸收峰,这是由于配体和配合物的π→π*跃迁。研究发现,配体和配合物最大吸收峰的位置并未发生改变,但吸收峰的强度却有所减弱,这是由于金属离子与配体配位后,氮原子的电子云密度的降低。其次,发现配合物在可见光区673.80 nm出现了配体中不含有的弱而宽的吸收峰,这是由于配合物分子中心Cu离子的d→d跃迁。

表3 配合物与配体的紫外光谱数据Table 3 UV spectral data of complexes and ligands
2.1.4 质谱分析
室温下,测定了配合物乙腈溶液(1×10-5mol/L)的电喷雾质谱(ESI-MS)。如图2,在SF-Cu-HPBM配合物的质谱图中显示,存在正离子峰m/z为604.39,推测配合物溶液中存在配离子[Cu(SF)(HPBM)]2+。

图2 配合物的质谱图Fig.2 Mass spectra of complexes
2.1.5 摩尔电导率
在室温25 ℃下,测定配合物在甲醇和DMSO溶液中(1×10-3mol/L)的摩尔电导率分别为172.3和72.3 S·cm2/mol,配合物为1:2型电解质。
2.2 新型三元铜配合物的抗菌性能
2.2.1 最小抑菌浓度实验
实验测定了配合物与配体对大肠杆菌、金黄色葡萄球菌的抑菌性能,它们的体外活性数据如表4所示。实验结果表明配合物的抗菌活性优于喹诺酮类抗生素配体的抑菌性能,第二配体HPBM的抑菌效果不是很明显,而Cu(ClO4)2·6H2O也表现出优异的抑菌性能。配合物SF-Cu-HPBM与环丙沙星相比,大肠杆菌(0.098 μg/mL<0.178 μg/mL)和对金黄色葡萄球菌(0.102 μg/mL<0.425 μg/mL)都有更好的活性。
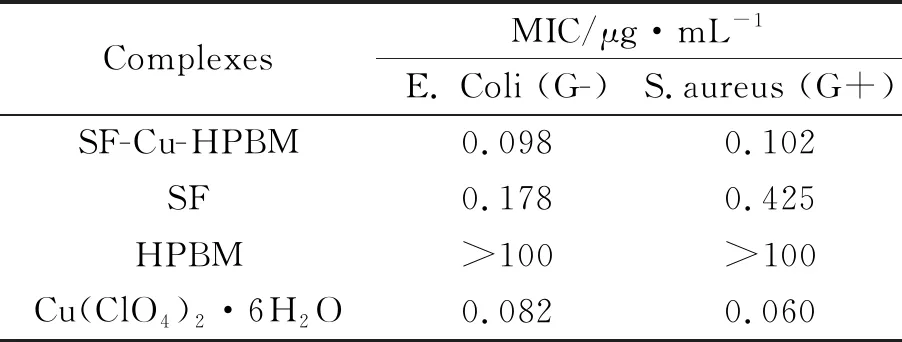
表4 配合物与配体的最小抑菌浓度MICTable 4 MIC of complexes and ligands
2.2.2 抑菌效果实验
(1)平板涂布法
将配体、配合物药液与菌液共同孵育4 h,平板涂布培养24 h后,各菌落的生长情况如图3所示。实验结果表明:(1)从图3中可以看出,相比于空白组和阴性对照组,第一配体环丙沙星组的大肠杆菌菌落明显减少,但是仍有一些菌落分布于固体培养基的四周,说明第一配体对于大肠杆菌具备一定的杀菌效果,且杀菌效果良好。第二配体HPBM没有明显的杀菌效果。而相较于第一配体,配合物SF-Cu-HPBM将所有细菌都杀死了,未长出任何菌落。因此喹诺酮类为第一配体、苯并咪唑类为第二配体的新型三元铜配合物对大肠肝菌的抑菌性能明显高于单一的喹诺酮抗生素;(2)从图4中可以看出,相比于空白组和阴性对照组,环丙沙星组金黄色葡萄球菌菌落有所减弱,但抑菌效果不是很完全,HPBM配体也几乎未显现出抑菌性能,而合成的SF-Cu-HPBM配合物抑制了所有菌落的生长。因此喹诺酮类为第一配体、苯并咪唑类为第二配体的新型三元铜配合物对金黄色葡萄球菌也达到了很好的抑菌效果。

图3 喹诺酮-铜-苯并咪唑类配合物、配体对大肠杆菌的生长情况的影响图:(a)为空白对照组;(b)为阴性对照组;(c)为配体HPBM组;(d)为环丙沙星(SF)组;(e)为喹诺酮-铜-苯并咪唑类(SF-Cu-HPBM)组Fig.3 Effect of quinolone-copper-benzimidazolium complexes and ligands on the growth of E.coli Figure:(a) blank control group;(b) negative control group;(c) ligand HPBM group;(d) ciprofloxacin (SF) group;(e) quinolone-copper-benzimidazolium complex (SF-Cu-HPBM) group
(2)抑菌圈
采用滤纸片法研究了各配体及铜配合物(20 μg/mL)对大肠杆菌和金黄色葡萄球菌的抑菌效果,结果以抑菌圈直径来表示。每个培养皿都放置了相应的配体与配合物,更直观的比较配合这一作用方式,是否能够在喹诺酮抗生素抗菌活性的基础上得到提高。如图5(a)和 (b)所示,明显看出,配合物4位上的抑菌圈直径明显大于1位上的,抑菌效果明显提高,与上述实验结果一致。
2.3 新型三元铜配合物与DNA的相互作用
2.3.1 DNA紫外滴定分析
紫外滴定分析法应用广泛,操作简便,是探究生物大分子(DNA/蛋白质)与过渡金属离子之间的相互作用的有力手段,不仅能够判断两者之间的作用模式,还能够准确地表征作用强度。当配合物与DNA作用,双螺旋结构被破坏,则会产生增色效应;若配合物与DNA作用,而导致分子构象变化,则会产生红移和减色效应,作用越强减色效果越明显。
由图6可知,配合物、配体与DNA作用均产生明显的红移和减色效应。这可能归因于配合物插入DNA碱基对中,发生电子堆积,配合物作用配体的π*空轨道与碱基的π电子轨道发生耦合,能级下降,产生π→π*跃迁。如图6(a)所示,随着DNA浓度的升高,苯并咪唑类为第二配体的配合物SF-Cu-HPBM在277 nm处产生了33.66%的减色;如图6(b)所示,环丙沙星在273.5 nm处产生了8.03%的减色效应。新型三元铜配合与DNA的作用明显高于单一的喹诺酮类化合物。配合物、配体与DNA作用的大小为SF-Cu-HPBM>环丙沙星。配合物、配体与DNA作用的紫外光谱数据见表5。

图6 配合物、配体与DNA相互作用的紫外光谱图:(a)为SF-Cu-HPBM与的DNA相互作用的紫外光谱图;(b)为SF与的DNA相互作用的紫外光谱图;(a)(b)两图中,曲线1为游离的待测样品的吸收曲线,曲线2-12为不同DNA浓度下的吸收光谱Fig.6 UV spectra of the interaction between the complexes,ligands and DNA:(a) the UV spectra of the interaction between SF-Cu-HPBM and the DNA;(b) the UV spectra of the interaction between SF and the DNA;(a) (b) in both figures,curve 1 is the absorption curve of the free sample to be tested,and curves 2-12 are the absorption spectra at different DNA concentrations
2.3.2 EB竞争实验分析
溴化乙锭(EB)是一种因其物理性质和生物活性而被广泛应用于分子生物学的荧光化合物。它是一种具有抗病毒特性的锥虫染料,可插入核酸双螺旋区域的相邻碱基对之间。通过嵌入,EB的荧光量子产率显著提高,它与DNA形成的体系在可见光区显示出光学活性。当DNA-EB体系被DNA-待测物体系所替代,EB从DNA双螺旋结构中游离出来,荧光被猝灭。利用这种方法进一步研究两者之间的相互作用。
由图7可知,在仅有待测样品或DNA时,在332 nm的激发光下,580~600 nm处都没有荧光产生。而DNA-EB体系在580~600 nm处显示出荧光,这说明EB已经嵌入DNA的双螺旋结构中。随着待测样品的不断加入,DNA-EB体系的荧光强度明显减弱,这说明了DNA-EB体系被DNA-待测物体系所替代,待测样品与DNA很可能是通过经典插入模式相结合。
2.3.3 牛血清蛋白实验分析
荧光分析是评价金属配合物与牛血清白蛋白相互作用的一种有效方法。许多蛋白质的特征荧光都主要由色氨酸贡献。在牛血清白蛋白中,荧光发射强度取决于两个色氨酸侧链134和212在极性溶剂中的暴露程度。铜配合物的加入能够使BSA体系荧光产生规律性猝灭,观察BSA最大发射峰的红移或蓝移现象,可以进一步分析待测样品与BSA的作用关系。从图8中可以看出,随着配合物与配体的加入,BSA的荧光强度都发生了不同程度的猝灭。

图8 配合物、配体与BSA作用的荧光谱图:(a)为SF-Cu-HPBM与BSA作用的荧光谱图,曲线1为BSA的荧光曲线,曲线2-8为向BSA中逐次加入等量DMSO溶解的配合物待测样品浓度(浓度控制为10~150 μmol/L)的吸收曲线;(b)为SF与BSA作用的荧光谱图,曲线1为BSA的荧光曲线,曲线2-8为向BSA中逐次加入等量DMSO溶解的配体待测样品浓度(浓度控制为10-150 μmol/L)的吸收曲线Fig.8 Fluorescence spectra of the interaction between the ligands and BSA:(a) shows the fluorescence spectra of SF-Cu-HPBM with BSA,curve 1 shows the fluorescence curve of BSA,curves 2-8 show the absorption curves of the concentration of the ligand to be tested (concentration control 10-150 μmol/L) by adding equal amount of DMSO to BSA one at a time;(b) shows the fluorescence spectra of SF with BSA fluorescence spectra,curve 1 is the fluorescence curve of BSA,and curves 2-8 are the absorption curves of the concentration of the ligand to be tested (concentration controlled as 10-150 μmol/L) by adding equal amount of DMSO to BSA one at a time
图9和表6是配合物、配体与BSA相互作用的荧光变化趋势和光谱数据,更直观的阐明了各种化合物与BSA的作用强度。根据Stern-Volmer方程计算得出各种配合物、配体与BSA作用的Ksv,配合物与牛血清白蛋白的结合常数Ksv为2.36×105M-1,明显高出第一配体环丙沙星与BSA的结合力3.85×103M-1,表明BSA在承担药物分子血液运输等过程中,更易与配合物产生作用,抵达靶细胞。

表6 配合物、配体与BSA相互作用的荧光光谱数据Table 6 Fluorescence spectrum data of complexes,ligands and BSA interactions

图9 不同浓度化合物下BSA体系荧光的变化趋势Fig.9 Variation trend of fluorescence in BSA system under different concentrations of compounds
3 结 论
(1)成功合成了喹诺酮类抗生素环丙沙星为第一配体、苯并咪唑类化合物为第二配体的铜离子配合物。配合物可能的分子式为:[Cu(SF)(HPBM)](NO3)2·1.5H2O。
(2)结合红外光谱、紫外光谱、电喷雾质谱、元素分析以及摩尔电导率的测试结果表明,喹诺酮类配体是通过4-位羰基氧原子、3-位羧基氧原子与铜离子配位,苯并咪唑类配体是通过芳香杂环上的两个氮原子与铜离子配位,配合物性质稳定、性能优异。
(3)将新型三元铜配合物,用于对大肠杆菌、金黄色葡萄球菌的抗菌活性测试,发现配合物比单一的喹诺酮类抗生素具有更强的抗菌活性。
(4)通过研究新型三元铜配合物与小牛胸腺DNA的作用及DNA-EB竞争实验,证明了配合物以经典插入模式与DNA结合。并且在牛血清蛋白实验中,发现配合物与牛血清白蛋白(BSA)的结合常数为2.36×105M-1,第一配体环丙沙星与BSA的结常数为3.85×103M-1,明显看出配合物与BSA的结合能力高于与配体与BSA的结合能力,表明BSA在承担药物分子血液运输等过程中,更易与配合物产生作用,抵达靶细胞。
