(001)/(101)晶面暴露TiO2光催化氧化甘油制备甲酸研究*
2023-11-09侯浩强徐俪菲马春慧刘守新
侯浩强,杨 峥,徐俪菲,马春慧,李 伟,罗 沙,刘守新
(东北林业大学 材料科学与工程学院,生物质材料科学与技术教育部重点实验室,哈尔滨 150040)
0 引 言
光催化反应发生在催化剂表面或近表面区域,催化剂不同的暴露晶面具有不同的原子构型和配位,对光催化活性具有重要影响[1-2]。锐钛矿TiO2具有较高的光催化活性和化学稳定性,一直是研究者关注的热点[3]。锐钛矿TiO2主要暴露(001)、(100)和(101)晶面,平均表面自由能分别为0.90、0.53和0.44 J/m2[4-5]。由于表面能的最小化,传统合成路线制备的TiO2优先暴露热力学稳定的(101)晶面,高能(001)晶面通常在TiO2晶体生长过程中迅速消失。Yang等利用HF作为形貌调控剂首次制备了富含 (001)晶面的锐钛矿TiO2微晶[6],研究发现F离子在(001)晶面的表面吸附会降低其表面活化能,促进(001)晶面择优生长[7]。Murakami等研究发现锐钛矿TiO2的(001)和(101)晶面分别是光催化过程中氧化和还原活性位点[8]。Li等证明了光生空穴(h+)和电子(e-)主要并分别分布于TiO2的(001)和(101)晶面[9]。因此,高活性TiO2并非单独暴露(001)或(101)晶面,而是同时暴露(001)/(101)晶面,形成表面异质结,促进e-向(101)晶面以及h+向(001)晶面的定向转移[10-12]。由于表面原子结构(配位不饱和位点)和电子结构(表面异质结)的协同作用,(001)/(101)晶面暴露的TiO2在生物质光重整反应中表现出高催化活性[13-15],但是关于不同晶面对生物质光催化选择性的影响研究较少。Yang等在甘油光催化氧化过程中发现TiO2(001)晶面的配位不饱和活性位点(O2c-Ti5c-O2c)有利于醛基向羧酸的深度氧化[16]。Wang等以甲酸脱水为探针反应,发现TiO2(101)晶面的光激电子浅阱有利于甲酸脱水生成CO,而(001)晶面的光激电子深阱有利于甲酸的稳定存在[17]。因此,研究TiO2不同晶面对生物质衍生物光催化氧化活性和选择性的影响对生物质资源利用具有指导意义。
甘油是生物柴油工业衍生的过剩副产品,是生物质多元醇光催化转化的理想模型分子[18-19]。甲酸是生物质光催化重整的重要中间体,可以在温和的条件下(光/电/低热)脱氢或脱水生成H2或CO,被认为是一种理想的液体燃料载体[20-22]。本文以甘油选择性氧化制备甲酸为探针反应,以钛酸异丙酯(titanium tetraisopropanolate,TTIP)为钛源,以氢氟酸(hydrofluoric acid,HF)为形貌控制剂,通过水热法合成不同暴露晶面的锐钛矿TiO2,在不添加碱和其他氧化剂条件下,研究不同暴露晶面TiO2在紫外光下光重整甘油制备甲酸的催化性能和反应过程。
1 实 验
1.1 实验原材料
钛酸异丙酯、氢氟酸、氢氧化钠、甘油、甲酸、二羟基丙酮、甘油醛、甘油酸、乙醇醛、乙二酸、异丙醇((isopropyl alcohol,IPA)、对苯醌(p-Benzoquinone,BQ)、草酸铵(Ammonium oxalate,AO)、溴酸钾(potassium bromate,PB)购自上海阿拉丁试剂公司;去离子水,自制;实验所用试剂均为分析级。
1.2 不同晶面暴露催化剂的制备
如图1所示,通过控制HF加入量,制备不同主要暴露晶面的TiO2。将2 mL去离子水、2 mL HF和5 mL HF分别加入20 mL钛酸异丙酯中,然后将混合物转移到100 mL聚四氟乙烯内衬的高压釜中,在180 ℃下保持24 h。待高压釜自然冷却至室温后,用0.1 mol/L NaOH和去离子水清洗白色沉淀物,直至pH为7,在60 ℃烘箱中干燥。最后,将白色粉末在管式炉中450 ℃煅烧2 h,去除催化剂中残留的有机物和氟原子。得到的3个样品分别记为TiO2、TiO2-2F和TiO2-5F。
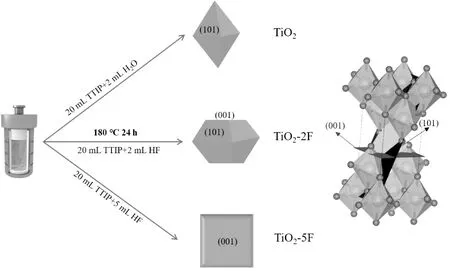
图1 光催化剂制备流程图Fig.1 Schematic illustration for the preparation ofphotocatalyst
1.3 催化剂表征
采用X射线衍射仪(XRD)测试了样品的晶体结构,D/MAX 2200型,日本株式会社;通过扫描电子显微镜(SEM)观察样品的表面形貌,Apreo S Hivac型,美国Thermo Scientific公司;采用透射电子显微镜(TEM)观察样品的微观形貌,JEM-2100型,日本株式会社;采用X射线光电子能谱仪(XPS)对样品表面元素和结合方式进行分析,K-Alpha 型,美国Thermo Scientific公司;使用拉曼光谱仪进行晶相和表面成分分析,Lab RAM HR型,法国HORIBA Jobin Yvon公司;采用电子顺磁共振波谱仪(EPR)测试了样品的离子价态、空位和衍生的自由基,Bruker Emxplus型,德国Bruker公司;采用紫外-可见分光光度计测试了样品的紫外可见漫反射光谱(UV-Vis DRS),TU-1901型,北京普析仪器公司;采用荧光分光光度计测试样品在室温下的光致发光(PL)光谱,LS 55型,美国Perkin-Elmer公司。
1.4 光催化重整甘油制备甲酸
甘油光催化重整实验使用300 W氙灯光源,配备紫外反射片(波长300~400 nm,光功率密度为200 mW/cm2),在自制40 mL石英反应器中进行。标准反应条件下,向反应器中加入10 mL甘油水溶液(10 mmol/L)和10 mg催化剂,超声5 min使其分散均匀,用N2(O2/空气)鼓泡30 min替换系统气氛,光反应4 h并持续搅拌,风冷装置控温在40 ℃以下。反应结束后将液体产物经0.22 μm有机滤膜过滤,利用配备RID和VWD检测器的Agilent 1260高效液相色谱(HPLC)对反应物甘油和产物甲酸进行定量分析,选用Agilent Hi-Plex H(300×7.8 mm)色谱柱,柱温30 ℃,流动相为5 mmol/L的硫酸溶液,流速为0.6 mL/min,光学设备温度30 ℃,紫外检测波长210 nm。通过外标法得到甘油和甲酸的标准浓度曲线来确定反应产物中甘油和甲酸的浓度,甘油转化率和甲酸选择性按下式计算:
(1)
(2)
式中:c为甘油转化率,%;y为甲酸选择性,%;C0为甘油初始浓度,mmol/L;C为反应结束甘油浓度,mmol/L;CFA为反应结束甲酸浓度,mmol/L。
2 结果与讨论
2.1 催化剂结构与组成分析
图2为TiO2、TiO2-2F和TiO2-5F的XRD谱图,3种催化剂在25.3°、37.9°、48.1°、53.9°、55.2°、63.0°、69.2°、70.4°和75.0°处出现了衍射峰,分别对应锐钛矿TiO2的(101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)和(215)晶面(JCPDS No.21-1272),说明3种样品均为锐钛矿相。TiO2、TiO2-2F和TiO2-5F衍射峰强度依次增强,表明HF能够提高TiO2的结晶度。随着HF的加入,(004)衍射峰强度增强,(200)衍射峰峰宽变窄,说明TiO2晶体沿着[001]方向厚度减小,[100]方向长度增加,(001)晶面暴露比例增大[16,23]。

图2 TiO2、TiO2-2F和TiO2-5F的XRD谱图Fig.2 XRD patterns of TiO2,TiO2-2F and TiO2-5F
图3(a)-(c)分别为TiO2、TiO2-2F和TiO2-5F的扫描电镜图。常见的(001)晶面暴露锐钛矿TiO2是截断的八面体双棱锥结构,上下两个面原子暴露情况等效于锐钛矿的(001)晶面,8个侧面原子暴露情况等效于锐钛矿的(101)晶面[9,11]。TiO2是粒径较小的纳米颗粒,TiO2-2F显露出截断的八面体双棱锥纳米结构,TiO2-5F主要以纳米片的形式存在。随着HF的加入,3种催化剂的粒径逐渐增大。

图3 (a) TiO2;(b) TiO2-2F;(c) TiO2-5F的SEM图Fig.3 SEM image of TiO2,TiO2-2F and TiO2-5F
通过TEM进一步观察TiO2、TiO2-2F和TiO2-5F的表面结构。图4(a)-(c)为TiO2的TEM、HRTEM和粒径分布图,TiO2为5~13 nm的纳米颗粒,形貌主要为八面体双棱锥,晶格条纹间距为0.352 nm,表明TiO2主要暴露(101)晶面[24]。TiO2-2F的TEM、HRTEM和粒径分布图如图4(d)-(f)所示,样品主要为20~40 nm的截断八面体双棱锥结构,上、下截面为正方形,截面间厚度约为6~10 nm。在TiO2-2F表面发现间距为0.235和0.352 nm两种晶格条纹,两者夹角为68.0°,与TiO2(001)和(101)晶面晶格间距及其理论夹角度数吻合,证明TiO2-2F共同暴露(001)和(101)晶面[12,25]。如图4(g)-(i)所示,TiO2-5F主要以纳米片的形式存在,纳米片粒径分布在30~70 nm,晶格条纹间距为0.235 nm,是典型的TiO2(001)晶面[26]。根据文献报道,化学吸附的F原子能够有效降低(001)晶面表面能[6-7,12],随着HF加入量的增加,锐钛矿八面体双棱锥两侧顶点沿[001]方向生长,(001)晶面以截面形式暴露在TiO2表面。

图4 (a)-(c) TiO2;(d)-(f) TiO2-2F;(g)-(i) TiO2-5F的TEM、HRTEM和粒径分布图Fig.4 TEM,HRTEM and particle size distribution image of TiO2 (a)-(c),TiO2-2F (d)-(f) and TiO2-5F (g)-(i)
通过XPS分析TiO2、TiO2-2F和TiO2-5F的表面元素状态,Ti 2p和O 1s的XPS谱图分别见图5a和5b。TiO2、TiO2-2F和TiO2-5F在458.3和464.2 eV处出现典型Ti4+特征峰,529.4 eV处为O 1s特征峰,随着(001)晶面暴露比例的增大,Ti4+谱峰结合能逐渐向低能方向移动,O 1s特征峰向高能方向移动,是由于Ti3+和氧空位(VO)出现[27]。

图5 TiO2、TiO2-2F和TiO2-5F的 (a) XPS Ti 2p谱图;(b) XPS O 1s谱图Fig.5 (a) XPS Ti 2p spectra;(b) XPS O 1s spectra of TiO2,TiO2-2F and TiO2-5F


图6 TiO2、TiO2-2F和TiO2-5F的(a) EPR谱图;(b)拉曼光谱图Fig.6 (a) EPR spectra;(b) Ranman specta of TiO2,TiO2-2F and TiO2-5F
2.2 催化剂光学性能分析
不同催化剂的漫反射光谱如图7(a)所示,3种催化剂的吸收边均在380.0 nm左右,TiO2-2F和TiO2-5F在400~500 nm出现微弱的吸收,可能是由于氧空位存在[28]。图7(b)是根据Tauc plot法得到的TiO2、TiO2-2F和TiO2-5F带隙宽度,分别为3.22、3.24和3.27 eV。结合XPS价带谱(图7(c))计算,TiO2、TiO2-2F和TiO2-5F价带能(相对于标准氢电极)分别为2.56,2.49和2.43 eV。不同暴露晶面存在表面电势差,TiO2-2F同时暴露(001)和(101)晶面,其激发产生的光生电子和空穴更易迁移到(101)和(001)晶面,形成表面异质结(图7d)[28,33],有效抑制电子与空穴的重组。
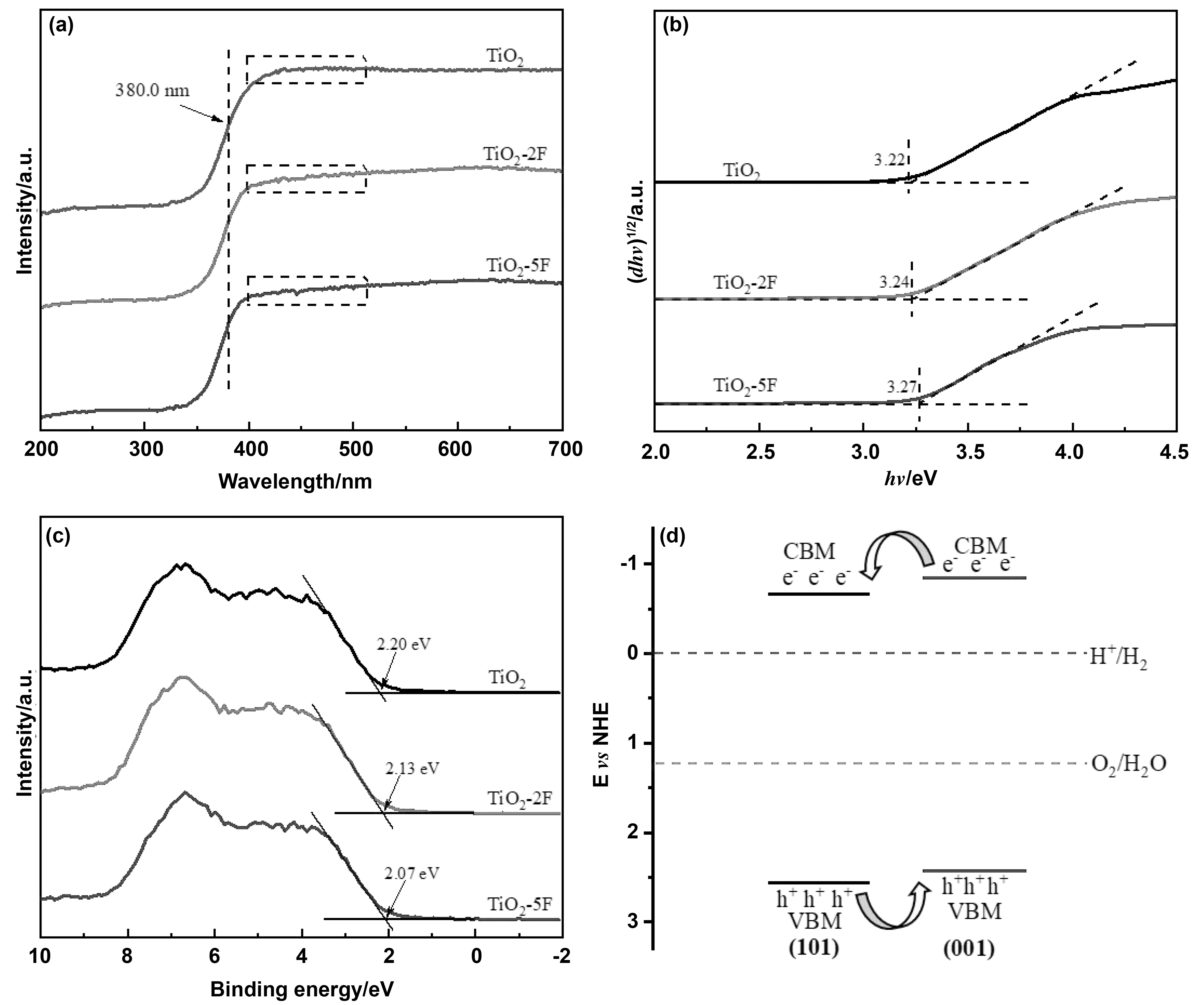
图7 TiO2、TiO2-2F和TiO2-5F的 (a)紫外可见漫反射光谱;(b)Tauc plot禁带宽度图;(c)XPS价带谱图;(d) TiO2-2F表面异质结示意图Fig.7 (a) UV-Vis DRS;(b) band gap analysis through Tauc plot method;(c) XPS valence band spectra of TiO2,TiO2-2F and TiO2-5F;(d) schematic diagram of surface heterogeneous junction of TiO2-2F
图8是TiO2、TiO2-2F和TiO2-5F在350~600 nm波长范围内的荧光光谱。350~440 nm荧光信号属于带带激发,440~550 nm归因于激子激发[34]。TiO2-2F和TiO2-5F在350~440 nm和440~550 nm的荧光信号明显减弱,表明(001)晶面暴露降低了电子和空穴对的重组率,可能是由表面氧空位和Ti3+缺陷对光生载流子的捕获所致[34]。TiO2-2F峰强度最低,证明(001)和(101)接触界面形成的表面异质结进一步降低了光生电子和空穴对的复合率[35]。

图8 TiO2、TiO2-2F和TiO2-5F的光致发光光谱Fig.8 Steady-state PL emission spectra of TiO2,TiO2-2F and TiO2-5F
2.3 光催化性能分析
图9(a)和(b)是3种催化剂在空气气氛下光催化氧化甘油制备甲酸的转化率和选择性。随着反应时间的增加,TiO2、TiO2-2F和TiO2-5F光催化氧化甘油转化率逐渐升高,8 h后分别达到63.4%、70.5%和62.0%。TiO2-2F较高的反应活性可能是由于催化剂表面(001)-(101)异质结的形成促进了光生电子-空穴的迁移和分离[28]。随着反应时间延长,TiO2、TiO2-2F和TiO2-5F催化剂上甲酸选择性先升高后降低,在反应4 h左右达到最高,分别为37.7%、55.6%和52.4%。与TiO2相比,存在(001)暴露晶面的TiO2-2F和TiO2-5F具有更高的甲酸选择性,是由于(001)晶面富含氧空位和O2c-Ti5c-O2c配位不饱和位点利于醛类向甲酸的演化[16]。随着反应时间超过4 h,甲酸发生过度氧化生成CO2或CO[36-37],三种催化剂的选择性均出现下降趋势。

图9 TiO2、TiO2-2F和TiO2-5F光催化重整甘油制备甲酸的转化率(a)和选择性(b);不同气氛下TiO2-2F光催化重整甘油制备甲酸的转化率(c)和选择性(d)Fig.9 (a) Conversion and (b) selectivity of photocatalytic reforming glycerol to formic acid of TiO2,TiO2-2F and TiO2-5F;(c) conversion and (d) selectivity of photocatalytic reforming glycerol to formic acid of TiO2-2F under different atmospheres



表1 自由基猝灭实验Table 1 Free radical quenching experiment

图10 TiO2-2F光催化重整甘油 (a)不同反应时间中间产物液相谱图-VWD;(b)DMPO-·OH EPR谱图;谱图Fig.10 (a)Liqiud chromatography of the intermediates for glycerol photocatalytic reforming under different reaction time-VWD detector;(b) EPR spectrum of DMPO-·OH;(c) EPR spectrum of
结合以上分析结果,提出TiO2-2F光催化氧化甘油制备甲酸的反应过程(图11)。TiO2-2F在紫外光激发下产生e--h+对,(001)-(101)表面异质结的存在使e-从(001)晶面转移到(101)晶面,h+从(101)晶面迁移到(001)晶面,促进了e--h+的有效分离。氧空位和不饱和O2c-Ti5c-O2c键合方式使吸附在(001)晶面的甘油及其中间产物深度氧化为甲酸[16],主要中间产物包括甘油醛、二羟基丙酮和乙醇醛。

图11 TiO2-2F光催化重整甘油制备甲酸机理图Fig.11 Reaction mechanism of TiO2-2F photocatalytic reforming glycerol to formic acid
3 结 论
(1)以钛酸异丙酯为钛源,氢氟酸为形貌控制剂,采用水热法制备了具有不同暴露晶面的锐钛矿TiO2。结果表明,随着HF加入量的增加,(001)晶面以截面形式暴露在TiO2表面。TiO2主要暴露(101)晶面,TiO2-5F主要暴露(001)晶面,TiO2-5F同时暴露(001)和(101)晶面。随着(001)晶面的暴露,TiO2出现更多的表面缺陷(Ti3+和VO)。
(2)以甘油选择性氧化制备甲酸为探针反应,研究发现同时暴露(001)和(101)晶面的TiO2-2F表现出最高的光催化活性和选择性。在温和条件下(无碱、低温、常压、空气)紫外光照射4 h,TiO2-2F催化剂上甘油转化率为49.0%,甲酸选择性为55.6%。

