铋/锌对铅酸蓄电池性能的影响
2023-08-21梁天宝牛玉辉杨成斌陈亚利刘亮孙茂汉
梁天宝,牛玉辉,杨成斌,陈亚利,刘亮,孙茂汉
(河南超威正效电源有限公司,河南 沁阳 454550)
0 引言
铅酸蓄电池是目前为止使用最广泛的二次电池。铅酸蓄电池最大缺点是比能量低。例如:镍氢电池的比能量是铅酸蓄电池的 2 倍,锂离子电池的比能量则是铅酸蓄电池的 3 倍[1-2]。但是,相较于其他二次电池来说,铅酸蓄电池也具有很多优点。例如:原材料丰富;生产技术成熟;电池性能稳定安全;价格便宜;回收再利用率高等[3]。随着铅酸蓄电池应用领域逐步扩大,对诸如水损耗、充电接受能力、低温容量、循环寿命等电性能的要求也越来越高。若要提高铅酸蓄电池的性能,在铅膏中使用添加剂是最有效的途径之一[4-5]。
许多研究文献中提到,无论在板栅合金中掺入铋,还是在铅膏中掺入铋对蓄电池都是有益的[6]。铅与铋的性质极其相似,因此在精炼铅时极难将铋除去。若要除去铋,就会使铅酸蓄电池的成本增加[7]。有关铋对铅酸蓄电池性能的影响报道层出不穷,但得到的结论很不一致,甚至有相反的结论出现[8-11]。先进铅酸蓄电池组织的文献显示,添加锌和铋,使其在铅膏中所占的质量分数为 5×10-4,可以提高电池的电化学性能[12]。并且,Pavlov D 也提到,铅膏中含有质量分数为 0.5 ‰ 的铋的化合物能提高 VRLA 电池的容量和充电接受能力[13]。
本文中,笔者针对锌和铋两种金属元素展开研究,探究锌的化合物和铋的化合物对铅酸蓄电池电化学性能的影响。实验中,手工制作样品电极,并用电化学工作站扫描。得出初步结论后,制备 12 V富液电池进一步验证。
1 实验
1.1 制备实验电极
现行负极铅膏配方的基础上,添加锌和铋的化合物。按表1 所示配方在烧杯中将电极 A、B、C、D 所需的物料搅拌均匀,成为实验铅膏。将胶圈与板栅筋条连接,做成电极载体(参见图1 中的 ①)。胶圈的尺寸参数:内径 10 mm;外径 14 mm;厚 3 mm。内面积约为 0.785 cm2。将制得的铅膏分别均匀的涂到相应的电极载体上,保证涂膏量相同。自然固化 4 d,并记录固化后电极的质量(参见图1的 ②)。将胶圈周围多余的铅膏去除后,称量干铅膏的质量。在小型充放电机上对实验电极进行化成,得到实验负电极(参见图1 中的 ③)。
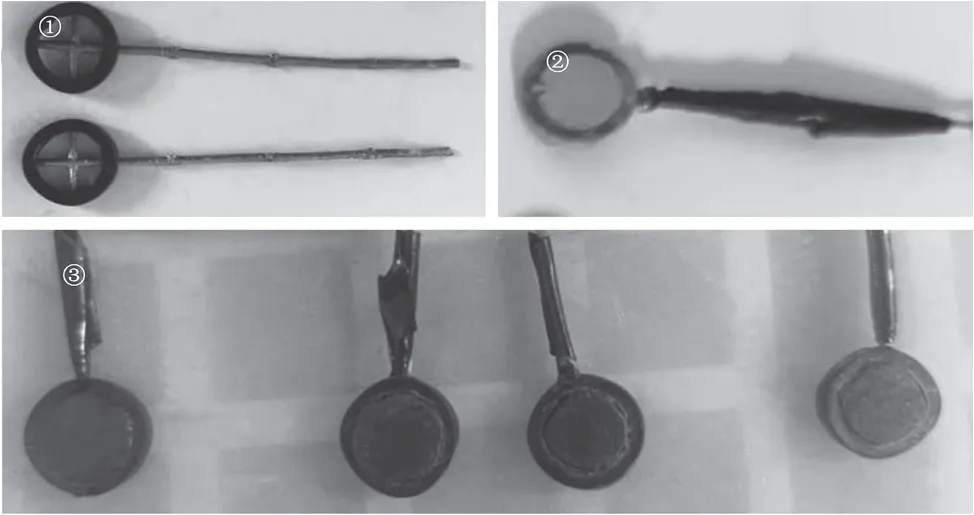
图1 实验电极
1.2 制备实验电池
按常规配方称取铅粉、硫酸、水,并按表2中设计方案称取添加剂(锌的化合物、铋的化合物),在和膏机中将物料搅拌均匀,制成电池 A、B、C、D 所需实验铅膏。为了保证电池的性能,将电池 B、C 中锌的化合物或铋的化合物的添加量减少到y。涂板过程中保证各负极板的涂膏量相同。将极板放到固化室内,固化 48 h。按表2 中方案,以 8 片正极板和 8 片负极板的极群方式,经包封、铸焊等工序,将正、负生极板组装成 12 V“绿”电池。在“绿”电池中加入相同密度的硫酸溶液,按照相同的化成工艺进行化成,制成实验用富液“黑”电池。
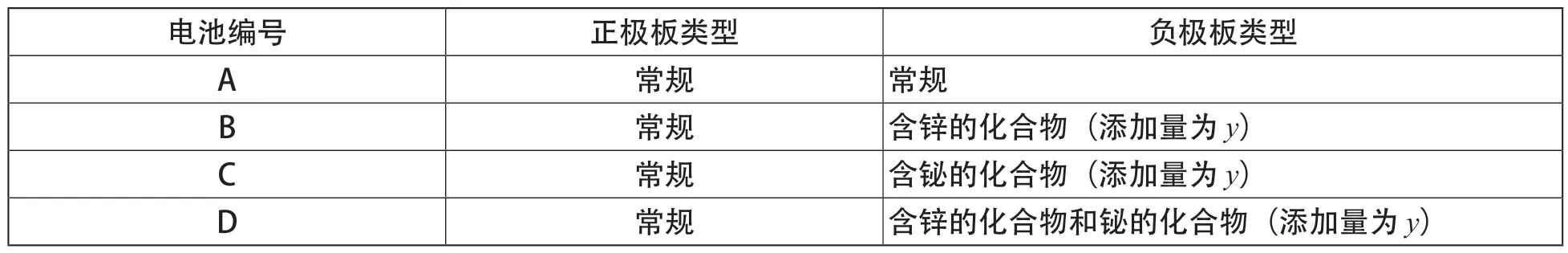
表2 电池设计方案
2 电极的电化学测试
以实验负电极为工作电极,1 cm2Pt 片为对电极,Hg/Hg2SO4电极为参比电极,1.29 g/cm3的H2SO4溶液为电解液,在 25 ℃ 下测试负极的析氢性能。先通过循环伏安扫描(扫描范围 -1~-2 V,扫描速率 10 mV/s) 20 圈,使电极达到稳定状态,然后通过线性扫描伏安曲线和线性拟合计算,来评价负极的析氢性能。
图2 所示为电极 A、B、C、D 的线性伏安曲线。电流相同的条件下,负极的电位越负,则其析氢过电位越大,析氢效果越弱。电位相同的条件下,负极的电流越小,则其析氢电流越小,析氢效果越弱。从图中的线性循环伏安曲线可以看出:整体上负极 B 的析氢电位最负,析氢电流最小;与负极 B 相比,负极 A(空白样)的析氢电位升高一些,析氢电流变大一点;与负极 A 相比,负极 C的析氢电位又升高一些,析氢电流变得更大;负极 D的析氢电位最高,析氢电流最大。以上结果可以说明,铅膏添加锌的化合物(铅膏中锌的化合物的质量分数为x)使负极减少了析氢,添加铋的化合物(铅膏中铋的化合物的质量分数为x)使负极增加了析氢,而添加锌的化合物与铋的化合物的混合物(铅膏中铋和锌的化合物的质量分数均为y)使负极析氢最严重。
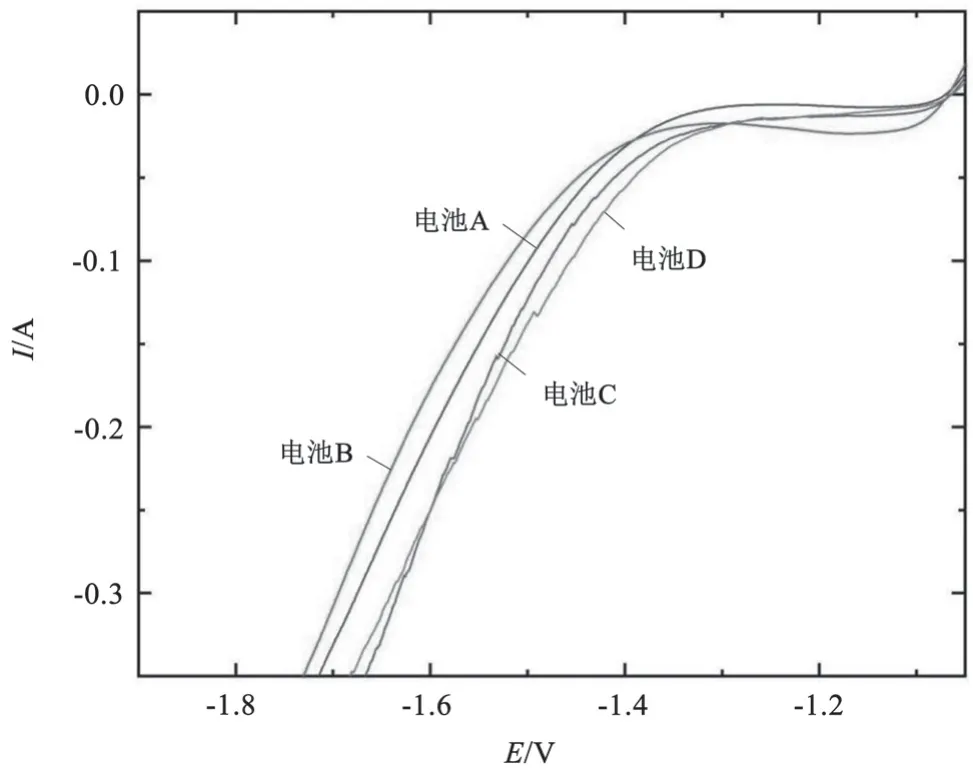
图2 实验电极的线性伏安曲线
对图2 中线性伏安曲线进行线性拟合,得到图3 和表3 的拟合结果。残差平方和越小,以及R2越接近 1,都说明趋势线估计值与实际值之间的差异越小,线性拟合程度越好,趋势线的可靠性越高。当析氢电流I趋近于 0 A 时的电位即为析氢电位。负极 B 的析氢电位最负,为 -1.467 V;负极 A 的析氢电位为 -1.439 V;负极 C 的析氢电位为-1.406 V,会促进析氢;负极 D 的析氢电位最高,为 -1.377 V,说明析氢最严重。拟合结果说明,铅膏添加锌的化合物(铅膏中锌的化合物的质量分数为x)降低了析氢电位,添加铋的化合物(铅膏中铋的化合物的质量分数为x)使负极增加了析氢,而添加锌的化合物与铋的化合物的混合物(铅膏中铋和锌的化合物的质量分数均为y)使负极的析氢电位最高。
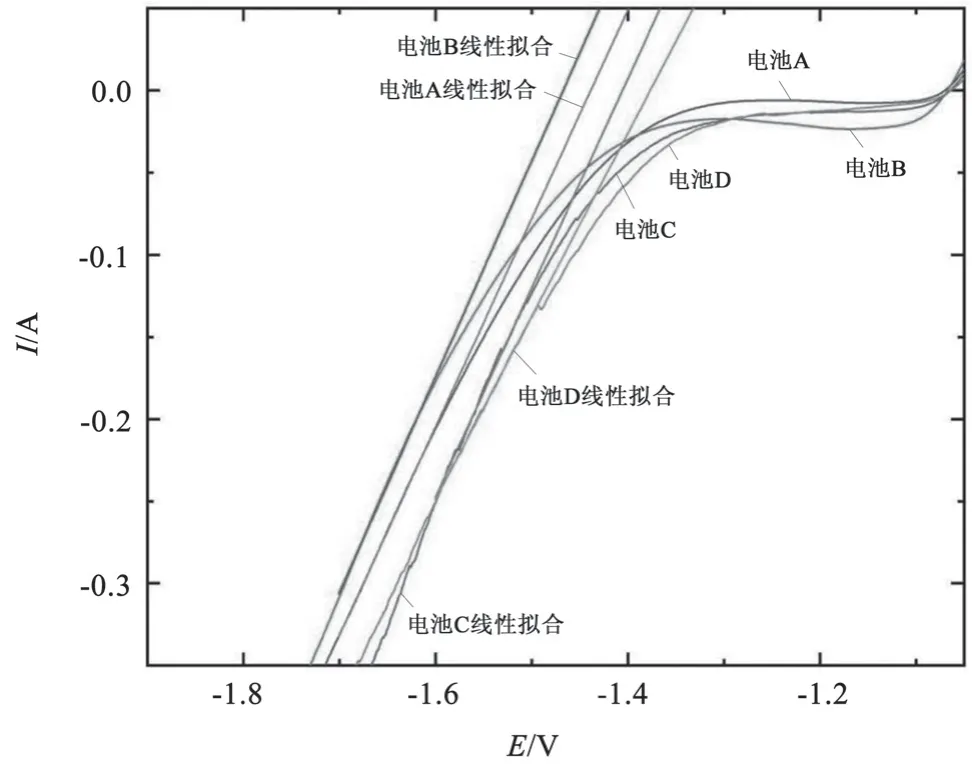
图3 实验电极线性伏安曲线拟合图
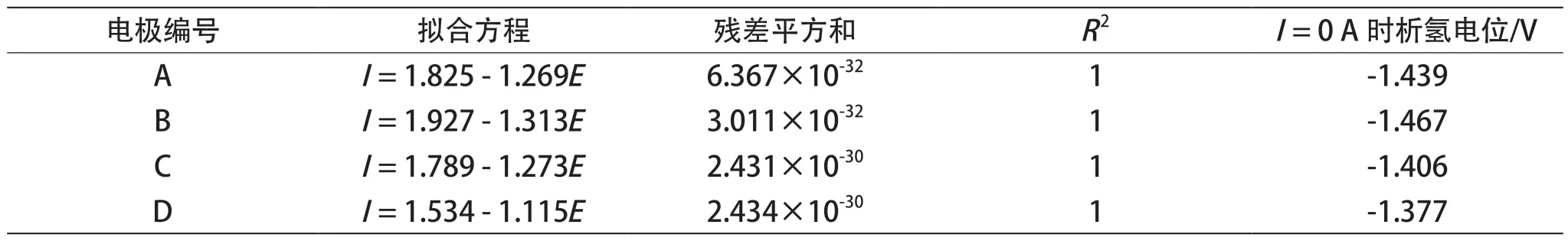
表3 线性伏安拟合数据
3 电池性能测试
试验电池的性能均按照大众标准(VW 750730 Issue 2019-10)进行测试。
3.1 初期容量
由表4 可见,电池 A、B、C、D 的初期 20 小时率容量C20均超过了 70 Ah,且彼此之间的容量差异不大。
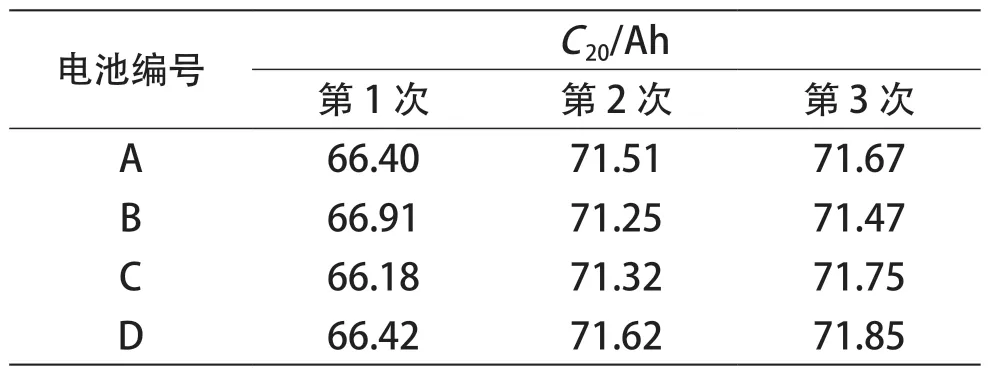
表4 电池的初期容量
3.2 -18 ℃ 低温起动能力
电池 A、B、C、D 在 -18 ℃ 下的低温起动放电时间均合格(标准要求t≥ 103 s)如图4 所示。电池 B 的低温起动性能最差,即相较于空白电池 A其低温起动放电时间减少了 10 s 左右。电池 C 与 D的低温起动放电时间相差不大,相较于空白电池 A增加了 5 s 左右。以上数据表明,析氢电位越负,低温起动放电时间越短,也就是二者呈现负相关。
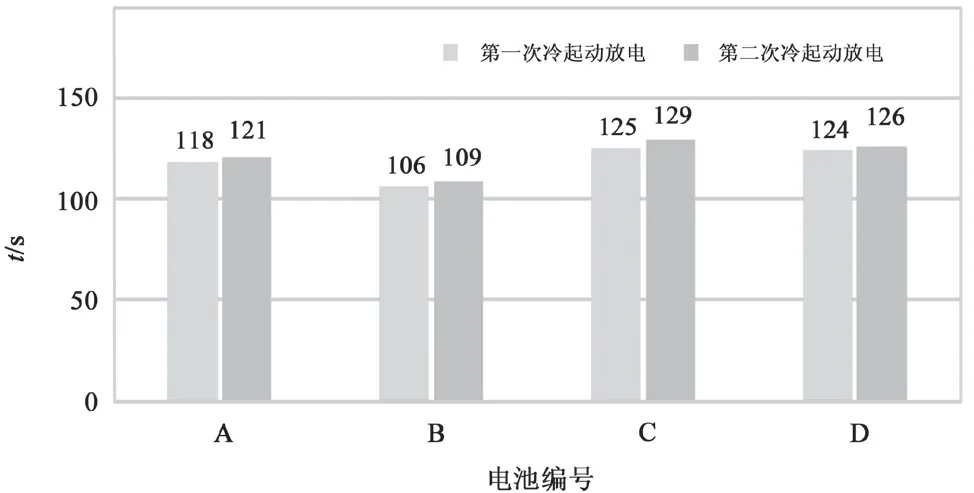
图4 -18 ℃ 低温起动放电时间
3.3 动态充电接受能力
电池 A、B、C、D 在 90 % SoC(荷电状态)下的充电接受能力如图5 所示。90 % SoC 下,电池B 与电池 C 的充电接受能力相差不大。若按充电接受能力大小排序,那么电池 B 最高,电池 C 次之,空白电池 A 再次,电池 D 最差。以上说明,与空白电池 A 相比,铅膏中只添加锌的化合物(铅膏中锌的化合物的质量分数为y)的电池 B 和铅膏中只添加铋的化合物(铅膏中铋的化合物的质量分数为y)的电池 C 的充电接受能力都提高了,而同时添加锌化合物和铋化合物(铅膏中铋和锌的化合物的质量分数均为y)的电池 D 的充电接受能力降低了。
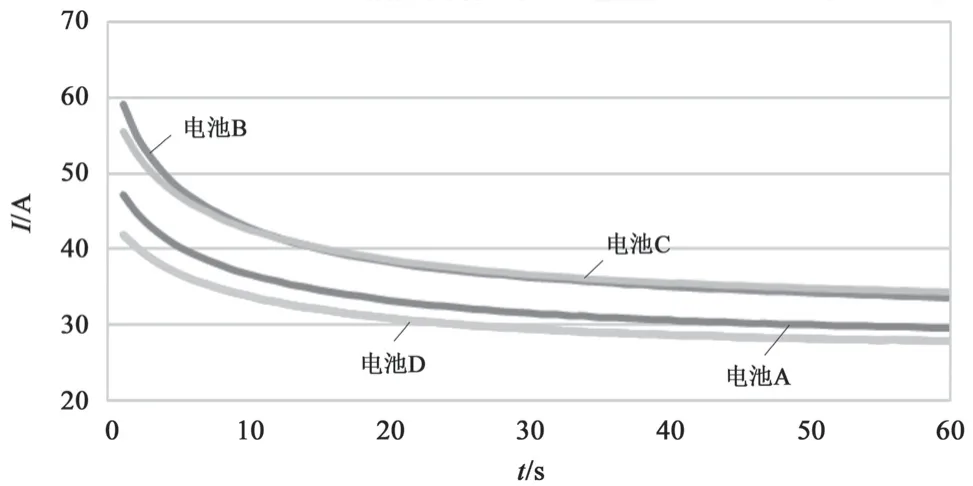
图5 90 % SoC 下充电接受能力
电池 A、B、C、D 在 60 % SoC 下的充电接受能力如图6 所示。60 % SoC 下,电池 B 与电池 C的充电接受能力依旧相差不大,还是电池 B 略高。但是,电池 D 的充电接受能力提高了,相较之下空白电池 A 的充电接受能力最差。以上说明,90 % SoC 与60 % SoC 下电池 B、C 的充电接受能力均优于空白电池 A,而电池 D 的充电接受能力在低荷电状态60 % SoC 下有所提高。
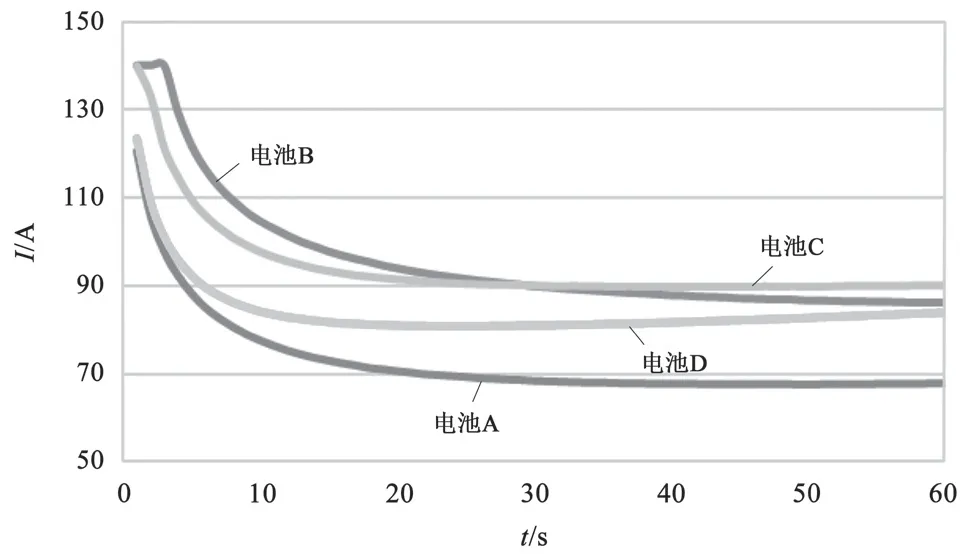
图6 60 % SoC 下充电接受能力
3.4 能量回收
电池 A、B、C、D 的能量回收情况如图7 所示。能量回收与动态接受能力所反映的电池性能是一致的。电池 B、C 的能量回收差异不大。若按能量回收多少排序,那么电池 B 最多,电池 C 次之,空白电池 A 再次,电池 D 最少。
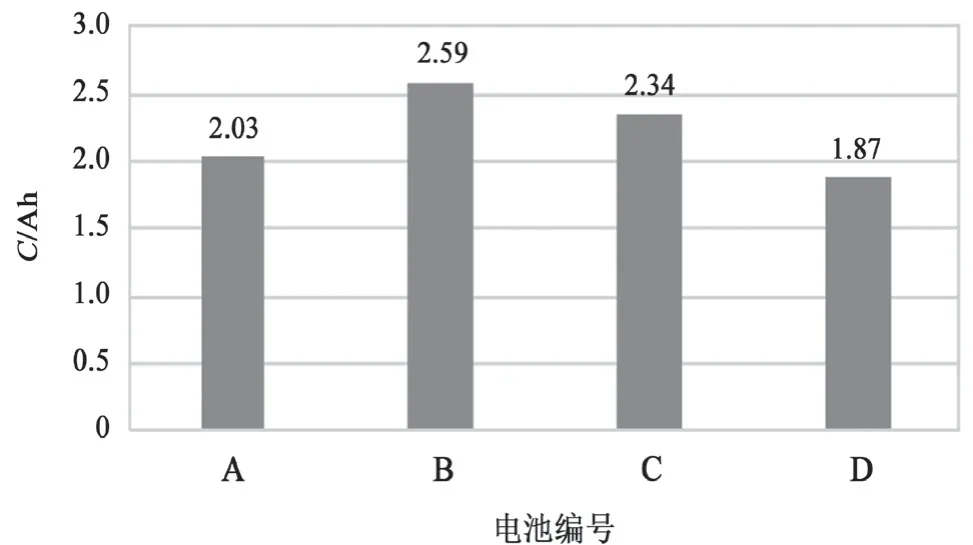
图7 能量回收
3.5 60 ℃ 水损耗
电池 A、B、C、D 在 60 ℃ 下水损耗测试结果如图8 和表5 所示。在 60 ℃ 下测试 21 d 的结果是,相较于空白电池 A,电池 B 的失水量减少,电池 C 的失水量增多,电池 D 的失水量最多。60 ℃下 21 d 水损耗测试结果与线性伏安扫描的结果较为一致。实验表明,电池的水损耗与其末期电流有关,即末期电流越大,水损耗越大。铅膏中只添加锌的化合物减少了电池失水,而只添加铋的化合物或者共同添加锌、铋的化合物会使电池失水量增加。
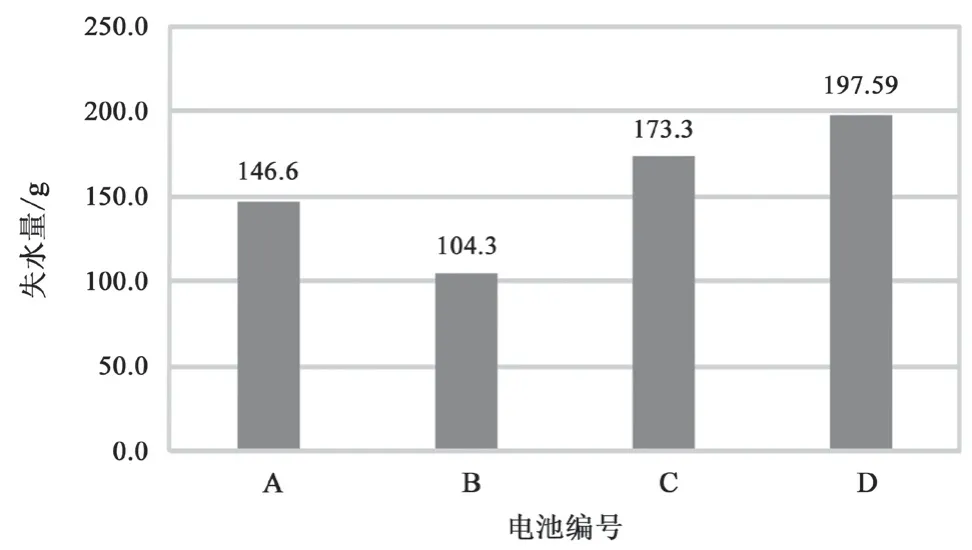
图8 电池水损耗
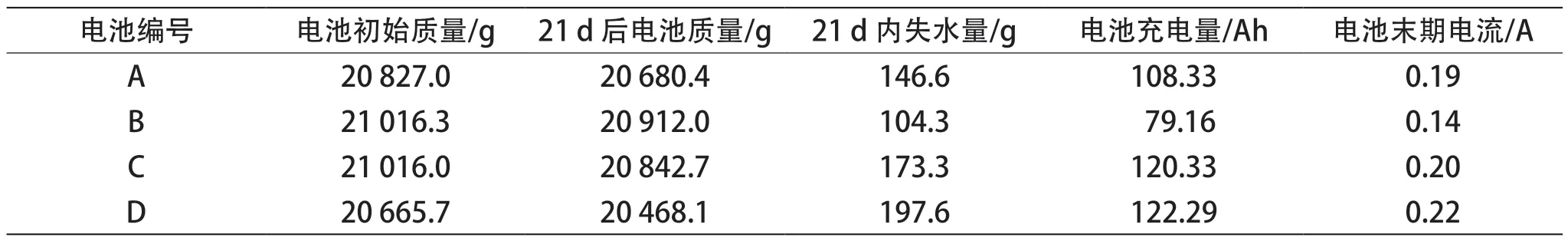
表5 60 ℃ 下 21 d 水损耗测试结果
3.6 加速循环
在水损耗实验结束后,继续进行 17.5 % DoD持续循环测试。电池 A、B、C、D 的 17.5 % DoD持续循环曲线以及充/放比曲线(即充电量与放电量之比)见图9 和图10。循环过程中电池 D 的终止电压与充/放比出现较大波动,可能是锌与铋在电池中互相影响的结果。并且,电池 D 的循环寿命最短,仅有 334 次。循环结果表明,添加锌的化合物的电池 B 的循环寿命最长,为 427 次;空白电池A 与电池 C 循环寿命接近,分别为 365 与 372 次;而电池 D 循环寿命最差,仅为 334 次。
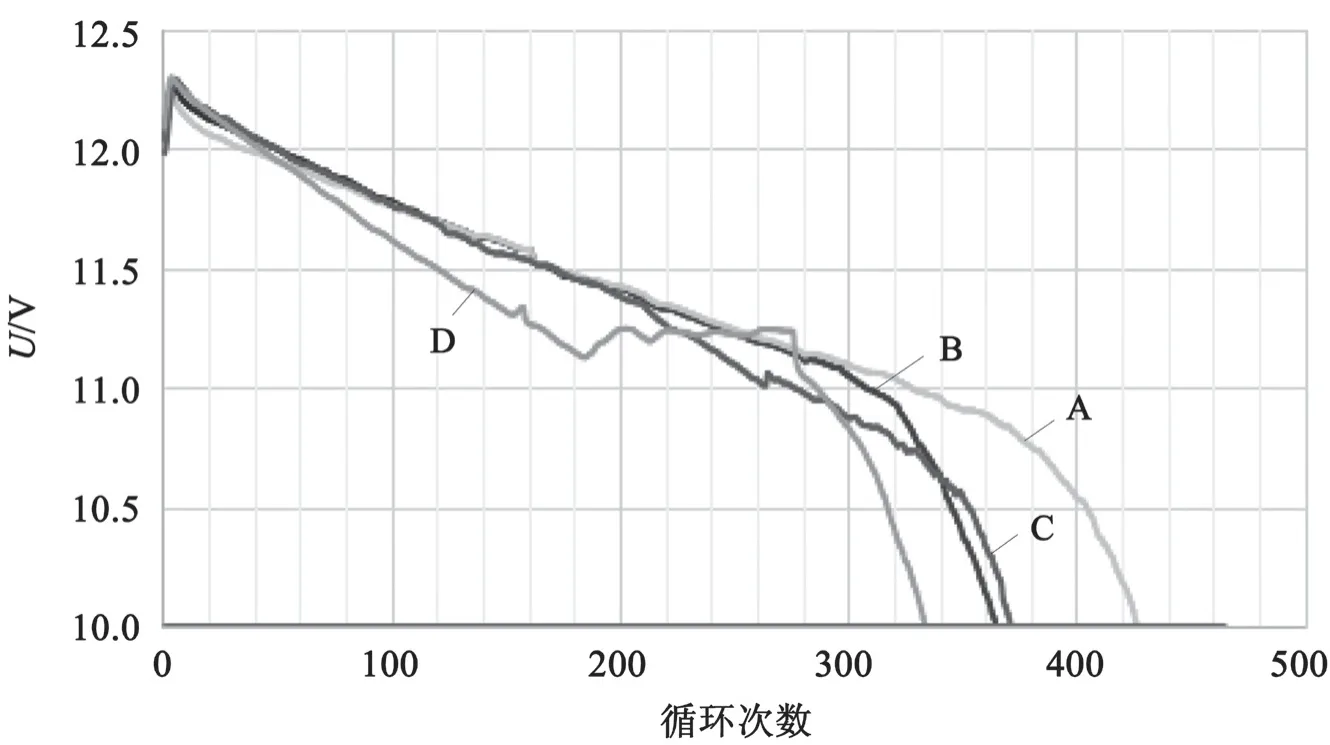
图9 17.5 % DoD 持续循环曲线
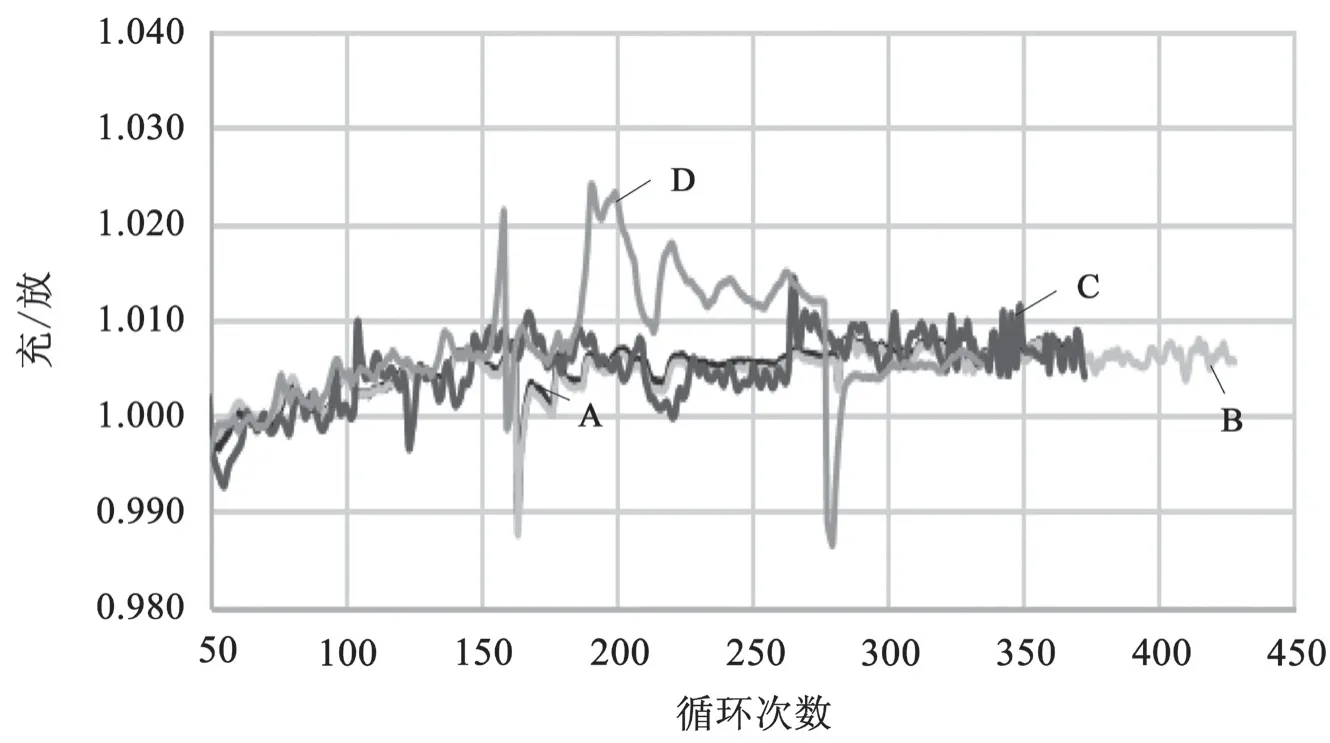
图10 17.5 % DoD 持续循环充/放比曲线
4 电池失效模式分析
4.1 电池解剖
图11 所示电池解剖后取出的极板。解剖电池后发现:电池 D 失水最严重,隔板上层已无电解液;电池 C 中电解液也比较少;电池 A 中电解液较多;电池 B 电解液最多,说明失水最少。正极板表面轻微泥化,负极板中部摩擦后依旧有银白色金属铅,但负极板底部硫酸盐化严重,且有大面积铅膏脱落。初步判断,电池的电解液干涸以及分层使负极板底部严重硫酸盐化,导致电池寿命终止。

图11 被解剖电池的极板
4.2 电解液分层现象
测量循环寿命终止的电池内上、下位置的硫酸电解液密度。表6 中数据说明:失水严重的电池 D 内,由于氢气和氧气产生的气泡起到了搅拌电解液的作用,电解液分层的程度最轻,上、下位置的硫酸电解液密度差仅为 0.018 g/cm3;电池 A、C内电解液分层程度次之,上、下位置的硫酸电解液密度差约为 0.040 g/cm3;失水最少的电池 D 内电解液分层最严重,上、下位置的硫酸电解液密度差为 0.092 g/cm3。分析的结果说明,电池失效原因是失水严重和电解液分层。
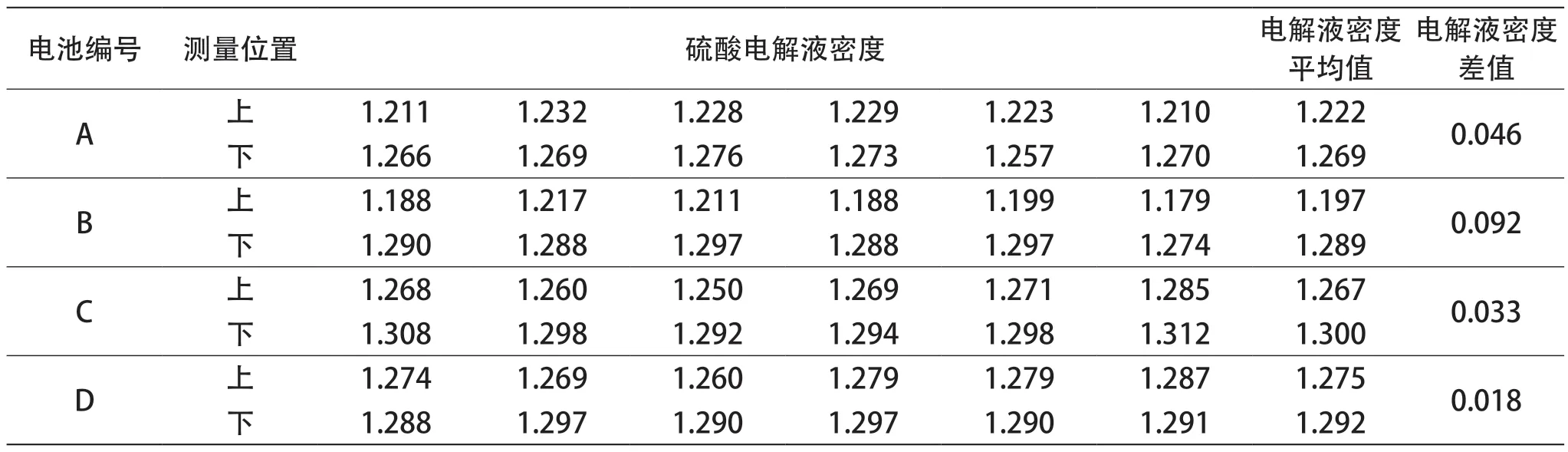
表6 电池酸液分层数据 g/cm3
5 总结
通过电化学工作站探究了铅膏中添加锌的化合物与铋的化合物时,负极的析氢过电位。线性伏安曲线以及拟合结果表明:添加锌的化合物降低了负极的析氢电位;添加铋的化合物提高了负极的析氢电位,而混合添加锌、铋的化合物使负极的析氢电位提高更明显。
电池性能检测结果表明:铅膏中添加锌的化合物使电池的水损耗、动态充电接受能力、17.5 %DoD 持续循环性能都有所提高,但是使低温起动能力降低;铅膏添加铋的化合物使电池的低温起动能力和充电接受能力有所上升,且能保持寿命不变,但是会使电池的水损耗增加;混合添加铋的化合物和锌的化合物可使电池的低温起动能力和低荷电状态下的充电接受能力有所升高,但是会使电池的水损耗加剧,以及缩短电池的寿命。
最后,此次实验表明:添加锌的化合物降低了析氢电位,抑制了析氢;添加铋的化合物,或者混合添加锌的化合物和铋的化合物提高了析氢电位,促进了析氢。
