搭起脊髓再生的希望之桥
2023-08-17李佳音戴建武
李佳音 戴建武
人的中枢神经系统包括脑和脊髓两部分,是神经系统的最主体结构,它就像一根电缆,通过接收躯干、脏器和四肢的信息,传达指令,调控身体的各项感觉和运动功能。成人脊髓两侧连有31对脊神经,每对脊神经连接一段脊髓,共分为31个节段,包括8个颈节,12个胸节,5个腰节、5个骶节和1个尾节。
脊髓在受到创伤或由疾病导致的严重损伤后,“电缆”的通路中断,致使损伤节段以下的感觉和运动功能部分或完全丧失。而压疮、痉挛、疼痛及泌尿系统、呼吸系统等的并发症则严重影响了患者的康复治疗及生活质量。据统计,全世界每年新发脊髓损伤病例13.3万~22.6万例,美国脊髓损伤患者一生的治疗康复费用平均达75万美元以上, 每年脊髓损伤患者的花费总计超过60亿美元[1]。随着康复医学的发展,目前脊髓损伤已不会显著影响患者寿命,但其导致的生理及心理问题,以及高昂的治疗和康复费用,给家庭和社会带来了沉重负担。
脊髓损伤后难以再生的原因
动物体内细胞间质(细胞之间的空间和物质)及其中体液的各种成分,组成了细胞生存及组织器官正常运行的“微环境”。其中,细胞外基质及结构蛋白可以支撑细胞的位置,而再生因子及信号分子支持细胞的生长、增殖和分化。
人体的一些组织器官,如皮肤、骨等在损伤后会形成有利于再生的微环境,促使组织自发修复,并在一定程度上恢复其功能。但是,脊髓损伤后局部神经组织缺失、形成瘢痕或空洞,同时产生一些神经再生抑制因子,使得局部形成不利于神经再生的微环境,导致神经再生非常困难。

首先,脊髓中的细胞包括神经元和神经胶质。神经元通过其长长的轴突来传递信号,而神经胶质细胞(包括星形胶质细胞、小胶质细胞、少突胶质细胞等)负责维持神经元稳态、清除病原体、循环脑脊液等,保护神经元发挥其功能。脊髓损伤后,局部的创伤会引发一系列病理反应,导致损伤部位神经细胞死亡及局部促进再生的营养因子缺乏。
其次,脊髓损伤后,胶质细胞被激活,在损伤部位周围形成胶质瘢痕,并在中心形成纤维化瘢痕。笔者团队发现,瘢痕组织的组分在急性期(损伤后7天内)到陈旧期(损伤14天后)的过程中是动态变化的。急性期的胶质瘢痕可能具有一定的引导感觉神经纤维再生的作用,而陈旧期的瘢痕组织及其分泌的分子则主要发挥抑制神经再生的作用[2]。此外,这些参与瘢痕形成的胶质细胞还会产生一种叫做硫酸软骨素聚糖的物质,激活神经元中抑制轴突生长的信号通路,进而抑制神经再生。
再次,损伤部位还存在一类髓鞘相关蛋白,可抑制神经元轴突的生长以及神经干细胞向神经元的定向分化。髓鞘是包裹在神经细胞轴突外面的一层膜,在中枢神经系统由少突胶质细胞产生。在髓鞘中,至今已发现至少3种典型的髓鞘相关蛋白,它们被认为是髓鞘再生抑制因子,与细胞中的配体结合后,会引起细胞骨架重排,最终抑制轴突的生长。
最后,与胚胎或新生儿不同,成年人的脊髓神经元内许多与再生相关的基因处于沉默状态,再生信号无法激活,导致中枢神经无法自主再生。
在以上因素的共同作用下,脊髓损伤后神经再生非常困难。因此,如何改善这种抑制微环境并促进神经再生是脊髓损伤再生修复研究中的关键问题。
再生医学助力脊髓损伤再生修复
再生医学研究的发展,为攻破脊髓损伤这一世界医学难题提供了新的方向。作为一个前沿交叉学科,再生医学应用生命科学、材料科学、临床医学、工程学等学科的原理和方法,研究和开发用于替代、修复、重建或再生人体各种组织器官的理论和技术,其三个重要组成部分为生物材料、生长因子及干细胞。
神经营养因子是引导神经元生长发育以及损伤后重建的关键。脊髓损伤后内源性再生因子的不足严重影响神经再生,因此,外源性再生因子的补充尤为重要。目前已发现神经营养因子—3、脑源性神经营养因子、神经生长因子、碱性成纤维细胞生长因子、胶质细胞源性神经营养因子等可促进细胞存活,刺激轴突生长,促进实验动物的脊髓损伤修复[3]。
干细胞是再生医学研究的重要组成部分,具有自我更新,并可分化为特定组织中功能细胞的能力,可以作为种子细胞,应用于多种组织器官的再生修复。在中枢神经系统的再生修复中,间充质干细胞和神经干细胞是最为常用的两种干细胞,在动物实验中显示了一定的脊髓修复效果。
但是,干细胞移植目前仍存在许多问题,限制其进一步发挥作用。首先,由于脊髓中脑脊液不断流动, 移植的干细胞很难定植于损伤部位,这样不仅会降低细胞治疗效果,还会带来细胞异位扩散的风险。其次,无论是移植的干细胞还是内源动员的干细胞,在到达成年动物的脊髓损伤处后,都很难分化為神经元,而更多地会分化为胶质细胞,难以起到神经再生的作用。
神经再生胶原支架
在神经再生的基础及临床研究中,已有的支架材料主要包括合成材料和天然材料。其中,天然材料,如天然高分子蛋白质、胶原、纤维蛋白等细胞外基质及透明质酸、壳聚糖等天然高分子,由于其来源方便、免疫源性低而更受青睐。如能以生物材料作为支架,改善微环境,促进内源或移植干细胞的定植和分化,就有望为脊髓损伤提供可能的治疗策略。

笔者团队经过多年的探索,创新研发出了具有自主知识产权的神经再生胶原支架。其基于胶原的力学特性及有序的结构可以为神经轴突的生长提供支撑,并引导神经纤维有序再生。此外,还研制了能与胶原特异结合的再生因子,使用这些再生因子对支架进行功能化改进,在减少用量、降低副作用的同时,既可以改善损伤的微环境,在损伤局部聚集促进内源或移植的干细胞,使其定向分化为神经元,又可以诱导干细胞向损伤部位迁移,在支架材料上定植与富集,使得神经胶原支架具有双重功能性,有效地引导脊髓损伤的再生与修复。
脊髓损伤研究中的动物模型
新的治疗方案、医疗器械产品或药品在获批应用到临床之前,必须要进行大量的动物实验和临床试验,以确保其安全性及有效性。脊髓损伤动物模型是研究脊髓损伤的病理、治疗效果及机制的重要工具。其中,小鼠和大鼠因性情温顺,易于饲养、操作和观察而被广泛应用于机理或毒性研究;而比格犬、恒河猴等大动物则更多应用于临床前研究。目前研究中常见的脊髓损伤模型包括挫伤、压迫伤、半横断和完全横断脊髓损伤动物模型。其中,完全性横断损伤切断了上下行的神经纤维束,排除了残存组织的干扰,虽然给手术及护理带来了更大的挑战,但更适合于作为研究脊髓损伤再生和运动功能恢复机制的动物模型。
啮齿动物全横断脊髓损伤模型
自2009年起,笔者团队先后建立了胸段脊髓缺损3~10毫米不等的大鼠全横断脊髓损伤模型,并利用该模型完成了多批次再生因子或干细胞结合神经再生胶原支架移植修复脊髓损伤的研究。利用这些急性或陈旧性全横断脊髓损伤大鼠模型,证实了手术清除瘢痕组织的安全性,以及功能神经胶原支架对神经再生及运动功能恢复的有效性,并提出和验证了脊髓再生修复的主要机制是形成新的神经桥接。
比格犬全横断脊髓损伤模型
比格犬是国际上公认的最理想的实验动物之一,已被广泛应用于医学、生物学、病理学、肿瘤学、药理学、生物化学等生命科学领域。笔者团队首次建立了胸段脊髓缺损5~40毫米不等的比格犬全横断脊髓损伤模型,并建立了一套行之有效的术后护理系统,最大限度防止犬的尿路和皮肤感染,以及褥疮、压力溃疡等的发生。通过多批次300余只犬的动物实验,证实神经再生胶原支架可与神经营养因子、再生抑制因子的拮抗剂或间充质干细胞结合,有效促进损伤部位的神经再生和运动功能的恢复。
恒河猴全横断脊髓损伤模型
非人灵长类动物进化程度高,有许多与人类相似的生物学特征。其中,恒河猴(猕猴)与人类的遗传物质有75%~98.5%的同源性,是人类疾病研究理想的动物模型,已被广泛用于遗传学疾病、行为学、神经生物学、生殖生理学、肿瘤学等领域的研究。笔者团队率先建立了恒河猴全横断脊髓损伤模型,并评估了神经营养因子—3功能化神经再生胶原支架移植治疗的效果。结果显示,移植后恒河猴的脊髓损伤部位空腔形成显著减少,具有更多的神经纤维再生、再髓鞘化和突触形成[4]。
经过多年的探索,笔者团队成功建立了不同类型的大鼠、犬和非人灵长类全横断脊髓损伤模型,并应用于脊髓损伤再生修复研究,助力我国在该领域的研究走在国际前列,为脊髓再生修复产品的临床转化提供了可靠的大动物评价体系。
脊髓损伤后功能恢复的主要机制
在脊髓中,下行神经传导束主要由皮质脊髓束(corticospinal tract, CST)、中缝核脊髓束、网状脊髓束和红核脊髓束等长的神经轴突组成,负责将大脑的运动指令传递给肌肉。其中,CST因其在自主运动功能控制中的关键作用而备受关注,许多研究也致力于诱导CST的生长以恢复肢体的运动功能。

脊髓损伤根据其损伤程度的不同,分为不完全性损伤和完全性损伤。通过回顾近10年来脊髓损伤再生修复的研究可以发现,利用人工构建神经支架或基质,同时结合药物、蛋白因子、各种外源性细胞等进行移植修复,均可以促进某些截断的轴突在损伤后继续生长。但是,这些研究几乎没能发现在完全性截断后的脊髓中有 CST 轴突延伸或穿过损伤区。而对于脊髓挤压伤或半橫切损伤模型,通过残存的完整神经纤维芽生则可以实现部分功能恢复,但其再生距离和数量非常有限,难以支持其再生穿过损伤区并恢复运动功能,因此CST轴突再生的机制备受争议。
损伤区功能神经元形成神经桥接
对于完全性损伤后的功能恢复机制,目前研究认为可能有3种:神经长轴突再生通过损伤区域;损伤区新生的神经元将损伤的两个断端连接起来,形成桥接;前两种机制同时存在。
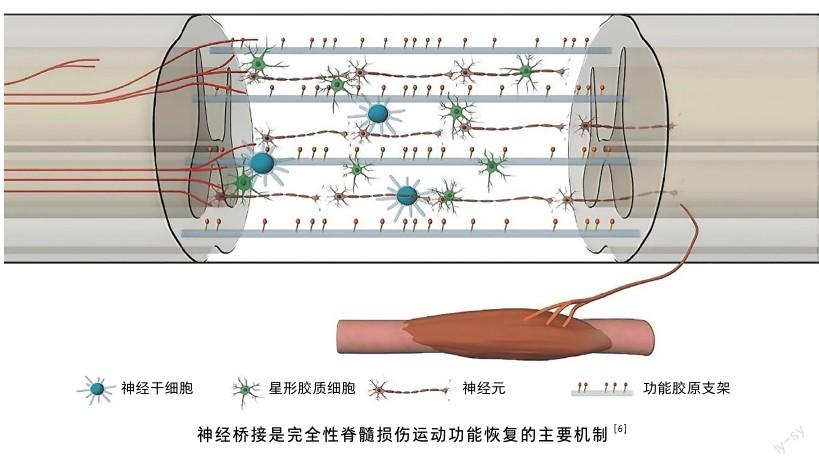
笔者团队在通过多种策略实现完全性脊髓损伤动物运动功能恢复的研究过程中,提出并证实神经桥接是完全性脊髓损伤后功能恢复的主要机制,即通过改善脊髓损伤后再生抑制的微环境,内源神经干细胞或移植的干细胞可在损伤部位形成新的功能神经元,连接两个断端形成新的神经桥接,促进完全性脊髓损伤后的功能恢复[5]。这种神经元桥接的一个重要特征是在损伤部位产生新的神经元,新生神经元与宿主神经元或宿主轴突形成新的突触,并产生适当的神经递质进行神经传导。然而,由于脊髓组织中损伤后的抑制微环境以及脑脊液的流动性,仅通过干细胞或神经细胞移植很难使其在损伤部位定植、分化,并形成神经桥接。因此,笔者团队另辟蹊径,通过创新研发的功能性神经再生胶原支架来改善抑制微环境,结合外源及内源的神经干细胞,实现了完全性脊髓损伤动物运动功能恢复的突破。

神经再生胶原支架引导外源神经干细胞定向分化
髓鞘蛋白是一类抑制神经干细胞定向分化为神经元的再生抑制分子。研究发现,脊髓损伤后,髓鞘相关蛋白会激活细胞表皮生长因子受体(EGFR),通过EGFR的信号通路来抑制轴突再生。为了拮抗这一信号传导途径,笔者团队制备了可以与胶原特异结合的EGFR抗体,它可以复合在神经再生胶原支架上,并将外源神经干细胞与支架一起移植到完全性脊髓损伤大鼠的损伤部位。功能化的神经再生支架可与神经干细胞表面的EGFR受体特异结合,使细胞最大限度地保留在损伤区域,并定向分化为神经元,在损伤部位形成新的神经桥接,促进大鼠的神经传导和运动功能恢复[7]。
脊髓损伤激活内源神经干细胞
位于成体动物脊髓中央管中的室管膜细胞,被认为是内源神经干细胞的潜在来源。这些细胞在正常组织中并不活动,但在损伤后的脊髓组织中会被激活并迁移至损伤部位。笔者团队发现,虽然室管膜细胞在损伤后会被激活,但在损伤部位更倾向于分化为星形胶质细胞,并形成密集的胶质瘢痕,阻碍神经再生。而神经胶原支架结合神经营养因子、间充质干细胞或神经再生抑制因子拮抗剂,都可以重建脊髓损伤后神经抑制微环境,促进损伤激活的内源性神经干细胞更多地自发分化为功能神经元并形成神经桥接,明显改善实验动物的运动功能,充分证实了神经桥接是完全性脊髓损伤后运动功能恢复的主要机制。今后,需进一步阐明这些新生神经元如何与脊髓组织整合并形成神经网络,促进运动功能更好地恢复[8]。
神经再生胶原支架为脊髓损伤患者搭起“希望之桥”
在完成系列临床前研究的基础上,笔者团队从2015年1月16日起,开展了首例神经再生胶原支架结合自体骨髓细胞修复陈旧性完全性脊髓损伤的临床研究。通过一年的随访,证实了采用神经电生理方法进行瘢痕清理是安全可行的,神经再生胶原支架联合细胞移植可改善完全性脊髓损伤患者的感觉平面或运动诱发电位, 自主神经功能也得到一定程度的恢复, 部分颈段损伤患者的运动功能也得到了改善[9]。
在急性脊髓损伤的临床研究中,建立了综合ASIA分级、影像学、神经电生理和术后运动功能恢复时间相结合的更严格判定完全性脊髓损伤的方法。随访一年后, 两名患者的感觉和运动功能明显改善, 一例胸段损伤患者可以借助支架行走,另一例颈部损伤患者可以移动腿和脚趾。感觉诱发电位和运动诱发电位可以跨损伤区传导, 患者损伤状态由A级完全损伤改善为C级不完全损伤, 显示了良好的修复效果[10]。
到目前为止,笔者团队已完成了15例急性完全性脊髓损伤患者和51例陈旧性完全性脊髓损伤患者2~5年长期的随访,结果表明,神经再生胶原支架移植治疗急性和陈旧性完全性脊髓损伤是安全的,部分急性患者的大小便感觉和下肢活动能力恢复明显。目前,神经再生胶原支架相关技术已实现企业转化,正在进行以获得产品注册证为目的的临床试验,其最终形成产品将造福于更多的患者。
新的探索——脊髓移植与脊髓制造
神经再生支架的临床转化取得初步成果后,鉴于单一细胞移植很难完全替代脊髓损伤区的细胞功能,难以满足功能完全重建的更高要求,因此,笔者团队近年来还尝试通过新的途径和再生医学技术来助力脊髓损伤的再生修复,并已在成体脊髓组织移植和脊髓组织体外制造方面取得了进展。
首次开展大鼠及犬的成体脊髓组织移植
组织器官移植是通过外科手段,将他人具有活力的器官移植给病人,以代替其病损的器官使其迅速恢复功能的手术。目前,皮肤、骨、心脏、肝、肾等组织器官都可以成功移植,但成人的脊髓组织异体移植仍未能实现。笔者团队在2019年首次报道了利用成年大鼠脊髓的完整脊髓组织异体移植治疗完全性脊髓损伤的研究成果,在移植时联合再生因子“鸡尾酒”,营造出有利于神经细胞存活的微环境,提高异体成体脊髓组织以及神经细胞移植后的存活率。该研究是国际上首次对成年脊髓组织移植的可行性进行探索,受到广泛关注。
之后,团队利用犬的全横断脊髓损伤模型进一步研究了成年完整脊髓组织移植的长期治疗效果,在术后半年发现其同样促进了犬的运动功能恢复,移植的成体脊髓组织和神经细胞术后半年在体内可以存活,表明成年脊髓组织移植具有可行性。像心臟、肝脏、肾等成功的器官移植一样,该研究为未来的异体脊髓组织移植治疗脊髓损伤这一不治之症开启了希望之门。
脊髓组织体外制造
近年来,随着干细胞研究及3D生物打印、单细胞测序、谱系失踪和组学等技术的迅速发展,人们对组织器官的发育、构造及损伤后不同类型细胞的变化有了深入了解,促使科幻小说中的体外器官组织制造日渐变为可能。
一个可用于体内移植的组织单元至少要包括两个重要的部分:与体内结构类似的细胞基质,以及一种或多种可以定植并发挥作用的组织特定功能细胞。根据脊髓组织制造的需求,笔者团队通过单细胞测序等技术阐明了人胚胎脊髓神经细胞的发育过程,建立了人脊髓神经前体细胞及胶质细胞的培养体系和细胞及有序生物材料纤维的产品标准,实现了复合2种人脊髓功能细胞的脊髓功能单元的构建。在全横断脊髓损伤动物模型中,证实了这种体外制造的脊髓组织在损伤区能够存活,并进一步分化为成熟的脊髓背腹侧神经元,其可与移植物与宿主的运动或感觉轴突形成靶向连接,脊髓损伤动物的运动诱发电位和后肢功能也得到改善。该研究也即将开始向临床转化,为脊髓组织单元移植修复脊髓损伤研究提供了一种治疗策略。
雄关漫道真如铁,笔者团队通过20年的辛勤耕耘,取得了突破性成果,使我国在脊髓损伤再生修复这一世界医学难题的研究领域达到世界领先水平,并仍在不断进取,力争为数百万脊髓损伤患者重燃自主站立和康复的希望。
[1]Lee B B, Cripps R A, Fitzharris M, et al. The global map for traumatic spinal cord injury epidemiology: update 2011, global incidence rate. Spinal Cord, 2014, 52(2): 110-116.
[2]Li X, Yang B, Xiao Z, et al. Comparison of subacute and chronic scar tissues after complete spinal cord transection. Experimental Neurology, 2018, 306: 132-137.
[3]Boyce V S, Mendell L M. Neurotrophic factors in spinal cord injury. Handbook of Experimental Pharmacology, 2014, 220: 443-460.
[4]Han S, Yin W, Li X, et al. Pre-clinical evaluation of CBD-NT3 modified collagen scaffolds in completely spinal cord transected non-human primates. Journal of Neurotrauma, 2019, 36(15): 2316-2324.
[5]Li X, Liu D, Xiao Z, et al. Scaffold-facilitated locomotor improvement post complete spinal cord injury: Motor axon regeneration versus endogenous neuronal relay formation. Biomaterials, 2019, 197: 20-31.
[6]肖志峰, 赵燕南, 李佳音, 等. 脊髓损伤再生研究进展——搭建脊髓损伤修复的希望之桥. 中国科学: 生命科学, 2019(49): 1395.
[7]Xu B, Zhao Y, Xiao Z, et al. A dual functional scaffold tethered with EGFR antibody promotes neural stem cell retention and neuronal differentiation for spinal cord injury repair. Advanced Healthcare Materials, 2017, 6(9).
[8]Li X, Zhao Y, Cheng S, et al. Cetuximab modified collagen scaffold directs neurogenesis of injury-activated endogenous neural stem cells for acute spinal cord injury repair. Biomaterials, 2017, 137: 73-86.
[9]Zhao Y, Tang F, Xiao Z, et al. Clinical study of NeuroRegen scaffold combined with human mesenchymal stem cells for the repair of chronic complete spinal cord injury. Cell Transplant, 2017, 26(5): 891-900.
[10]Xiao Z, Tang F, Zhao Y, et al. Significant improvement of acute complete spinal cord injury patients diagnosed by a combined criteria implanted with NeuroRegen scaffolds and mesenchymal stem cells. Cell Transplant, 2018, 27(6): 907-915.
關键词:脊髓损伤 再生医学 神经再生 胶原支架 ■
