基于径向基函数神经网络的肺部加权频差电阻抗成像方法*
2023-07-19白世展李文胜林海军李建闽张甫杨宇祥
白世展 李文胜 林海军 李建闽 张甫 杨宇祥
(湖南师范大学工程与设计学院,长沙 410081)
电阻抗成像(electrical impedance tomography,EIT)旨在通过附着于目标表面阵列电极给予受试者微弱的安全电流激励,循环测量表面电压响应,重建目标内部的电导率分布(变化)[1-2],进而反映不同目标组织或器官的功能和结构信息[3-4]。EIT具有无创、便携、成本低、可连续监测等优点,近些年已被广泛应用于人体肺部损伤的诊断[5]和机械通气的实时监测[6-7],以及气胸的检测[8]等。
通过对肺部进行EIT成像来监测呼吸是EIT技术最重要的医学应用,肺部EIT已经用于机械通气患者的管理,它可以指导机械通气压力、容量和呼吸频率的设置[9]。肺部充气时由于肺泡间隔变薄和延长,肺部内区域与周围组织之间的电导率差异较大,将会损害电流的通过。安静呼吸时肺组织阻抗变化约5%,而在深呼吸时(从残余容量到总肺容量)阻抗变化可达300%[2],阻抗值大小与肺内含气量有着密切关系。肺部EIT图像重建技术基于对呼吸时肺部电阻率变化的估计[10],而肺部呼吸气时气体容量不断发生变化,导致其电导率分布处于持续变化的状态,因此为EIT成像技术在肺通气分布监测提供了天然的基础条件,从而能够动态、实时监测随着呼吸运动肺内气体分布及其动态变化[11]。
传统EIT成像采用基于单一频率下阻抗测量的绝对成像方法[12],测量组织或器官阻抗绝对值Z重建图像虽然可行,但其对EIT正演模型中的待测域几何建模误差非常敏感[13],给胸腔肺部成像带来一定困难。差分成像通过两个测量状态之间的阻抗差异容忍几何建模误差,重建胸腔内部电导率变化[14],主要分为时差电阻抗成像(time difference EIT,td-EIT)和频差电阻抗成像(frequency difference EIT,fd-EIT)。td-EIT方法通过不同时刻线性阻抗差对肺部通气分布进行可视化描述[6],有效减少重建图像伪影。然而,针对于生物应用,随着时间的改变、温度变化以及细胞活动而导致背景电导率不断改变[15],以及在发病或者急诊状态进入治疗的患者往往缺乏健康状态的时间阻抗基线参考数据,都将阻止检测到临床相关变化而耽误治疗诊断[16-17]。因此,td-EIT仅适用于短期监测。
fd-EIT方法使用多个激励频率同时刻阻抗数据来反映电导率相应变化[18]。fd-EIT不仅能够像td-EIT一样有效地消除常见边界几何误差,而且允许在数据收集速度较快情况下消除由身体运动引起的伪影,同时降低逆问题的自由度和病态性,可获得增强的重构图像[19]。与td-EIT算法相比,fd-EIT算法利用宽频激励信号一次获取多个频率点的瞬时生物电阻抗信息[20],可准确记录生命时变系统某时刻的瞬时阻抗谱信息,分析生物的频率相关行为[21-22]。同时,fd-EIT不需要过去时刻阻抗参考,能够解决实际临床环境中胸腔参考阻抗难以获得的限制[23]。在fd-EIT中使用两个频率之间的加权阻抗差来生成内部电导率分布随频率变化的加权频差电阻抗图像(the weighted fd-EIT,wfd-EIT),使得背景物质的电导率变化被抑制,而目标组织的电导率变化大小被增强[18]。wfd-EIT在实际临床应用中成为肺部EIT研究的一个重要转变,允许在没有时间变化的情况下重建目标组织,其更能满足医疗急诊救护所需[23]。
胸腔EIT可视化的实质是解决逆问题,即图像重建。由于未知量(即空间电导率的数量)远多于测量的阻抗数量,导致图像重建成为一个严重的非线性、不适定和病态问题[24]。传统的图像重建算法[25]分为非迭代算法(反投影法、敏感矩阵法和正则化法)以及迭代算法(高斯-牛顿算法及改进算法),通过最小化惩罚函数来获得逆问题的近似最优解。然而,传统图像重建方法对正问题建模有着高度依赖性,并且对其他复杂的建模因素(如电极位置、边界形状和接触阻抗)极其敏感[24],根据线性近似来重建图像所得的空间分辨率很难达到高精度,不能直接应用于具有明显个体差异的医学可视化任务[26]。近年来,在计算机视觉领域得到广泛应用的神经网络学习,为解决逆问题的非线性化联系提供了新的思路。神经网络中非线性模式下的特征提取和参数重建可以为EIT提供更好的成像求解方法,避免正问题中的敏感矩阵计算和图像重建逆问题线性化,通常采用反向传播、Hopfield和径向基函数等有效可靠的神经网络建立网络模型。而相比于其他神经网络,径向基函数神经网络(radial basis function neural network,RBFNN)的优势在于对EIT逆问题求解的非线性模型拥有强大的全局逼近能力,可以很好地逼近任意连续函数[27]。通过边界加权频差阻抗矩阵直接重建肺部wfd-EIT图像,能够满足图像重建的要求。
鉴于RBFNN的上述优势,本文提出基于RBFNN的肺部wfd-EIT方法,用于重建肺部呼吸的多个wfd-EIT帧图像,在保证成像速度基础上进一步提高图像重建质量。首先通过COMSOL和MATLAB联合仿真建立了2 028个数据仿真样本集,分为互不重叠的训练集和测试集。利用训练集训练网络模型,使用测试集验证所提出方法的可行性并比较Tikhonov-Noser和RBFNN方法的准确性。其次,通过所建立胸腔模型中具有不同电学模型的生物组织来模拟肺部图像组织电导率分布,进行16电极wfd-EIT系统成像实验,测量所得数据用于比较Tikhonov-Noser和RBFNN方法的成像准确性。
1 数值分析与方法
1.1 wfd-EIT数学模型
EIT正问题中,根据已知电流和电导率分布计算得到胸腔分布阻抗值。从电磁场理论出发,EIT正演模型从麦克斯韦电磁方程组的一个子集的低频近似和一些混合Dirichlet/Neumann边界条件数学上建立[28],胸腔边界阻抗测量可表示为以下边值问题:
式中Ω表示场域,σx,y表示场域内部的电导率分布,ux,y表示场域内电位分布函数。
待测场生物组织可视为离子导电体,内部单元电导率σx,y和可测参数边界电极间电位ϕ的函数关系为:
式中∂Ω表示场域边界,n表示场域Ω的外法向单位向量,jx,y表示流入场域Ω的激励电流密度。
wfd-EIT测量基于四电极测量策略,采用相邻电流驱动方法。边界电流激励I采用作者前期所优化的等幅值低波峰因数(CF,峰值/有效值)多频正弦(multisine)信号[20],能够提供更多能量来保障多个频率阻抗测量精度。离散的multisine激励信号I(n):
式中Am,fm,φm分别表示multisine信号以基波周期f0为1 kHz的第m次谐波幅值、模拟频率和初相位,m为正整数。fs为系统采样频率,N为采样点数。使用multisine激励信号在一个基波周期内即可完成各个频率点阻抗矢量Z的测量:
其中ε(σ)为背景电导率的变化影响,e为测量噪声。
采用wfd-EIT成像方法,使用两个频率之间的加权阻抗差来生成内部电导率分布随频率变化的图像,可避免难以准确获取时间阻抗基线参考数据的问题,并抑制背景阻抗ε(σ)和测量噪声e对测量结果影响,增强肺部通气区域的阻抗变化。由式(4)可得在不同频率(f1,f2)下加权阻抗变化矢量:
其中系数α为两个不同频率阻抗矢量之间的内积比,为计算内积符号。
wfd-EIT图像重建的目的是通过给定电流密度,研究加权频差阻抗数据ΔZ对复杂电导率分布变化Δσ的敏感性:
其中,J为灵敏度矩阵。
1.2 径向基网络方法
RBFNN是一种性能良好的前馈式神经网络,其基本结构由输入层、隐含层和预测层组成(图1)。其中,输入层到预测层的非线性变换能够逼近任意非线性函数,加快学习收敛速度和避免局部极小问题。

Fig. 1 Network framework of radial basis function neural network

Fig. 2 The parameter learning process of the RBFNN network algorithm
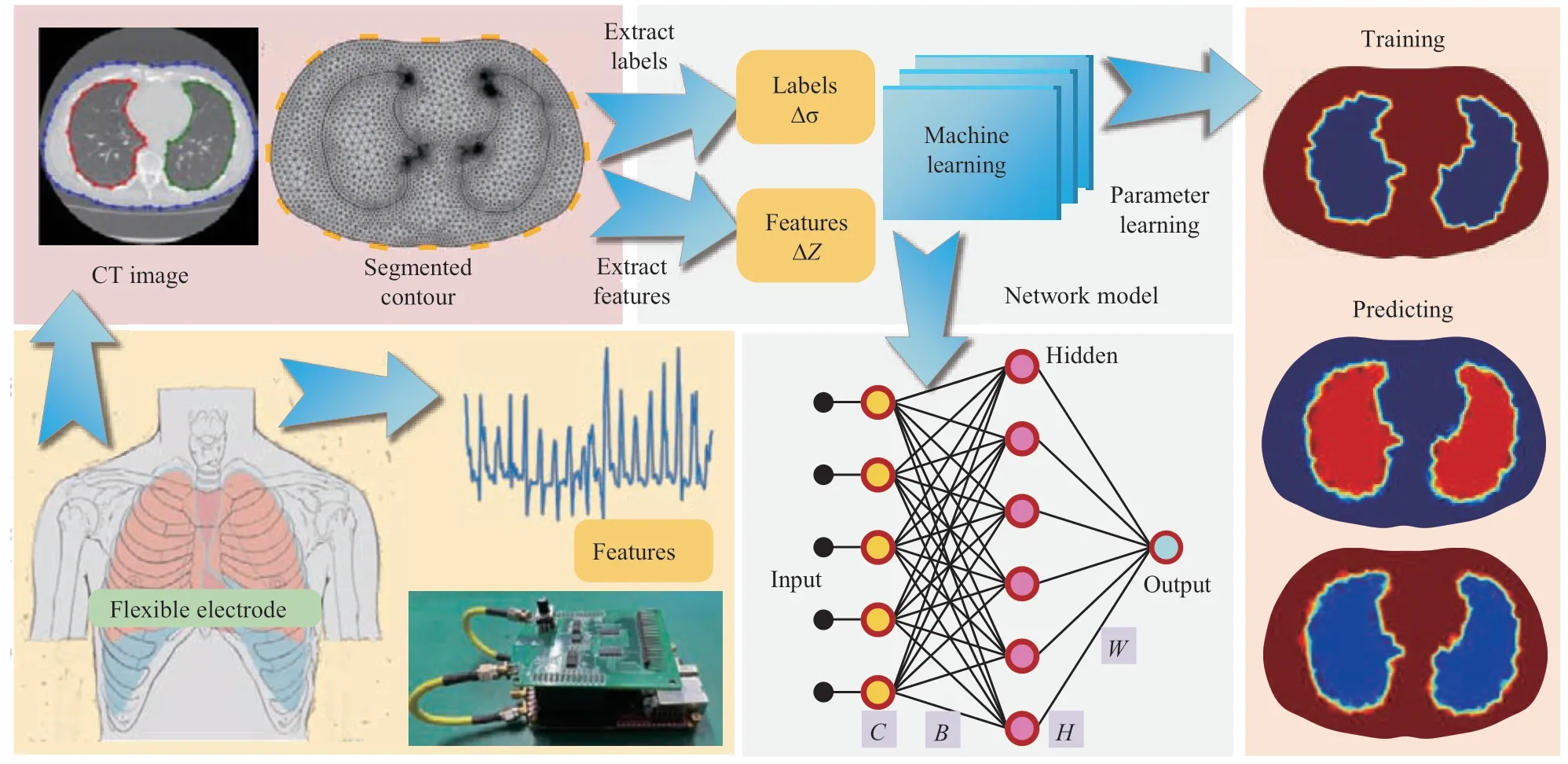
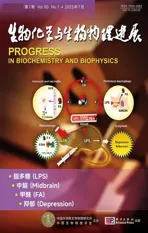
Fig. 3 The mapping model of image reconstruction for wfd-EIT based on RBFNN

Fig. 4 Partial sample distribution

Fig. 5 Reconstructions of lung phantoms from modeling with different methods
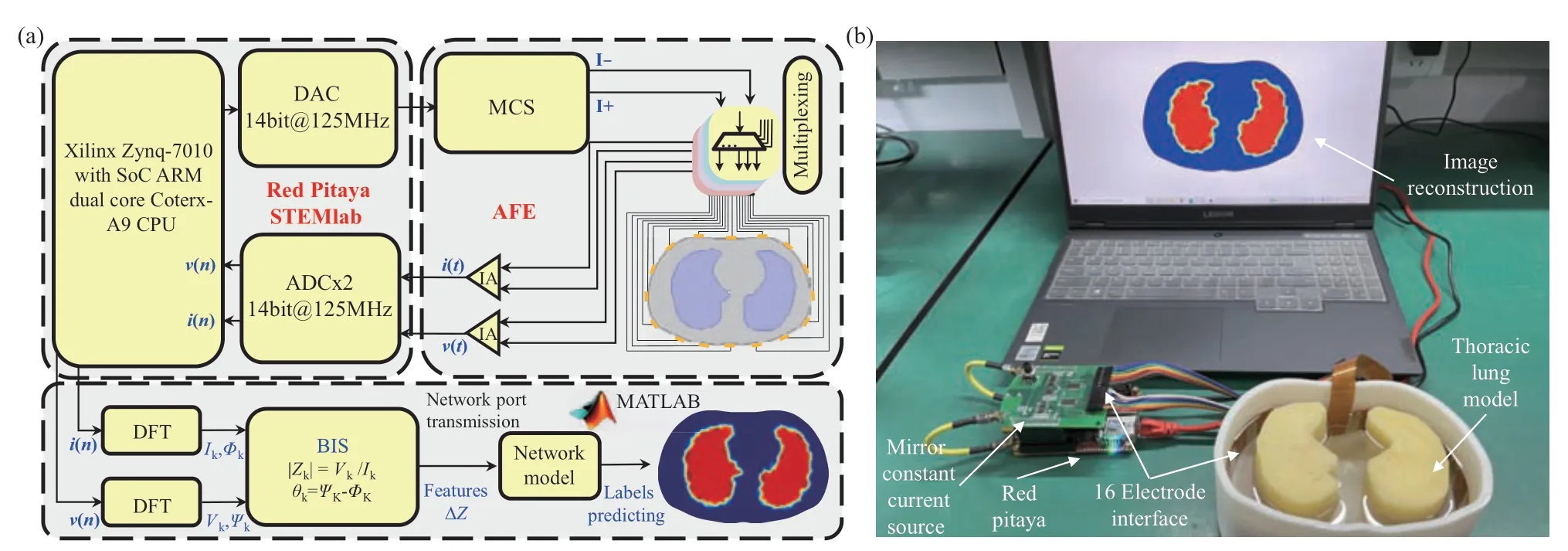
Fig. 6 Experimental equipment hardware system
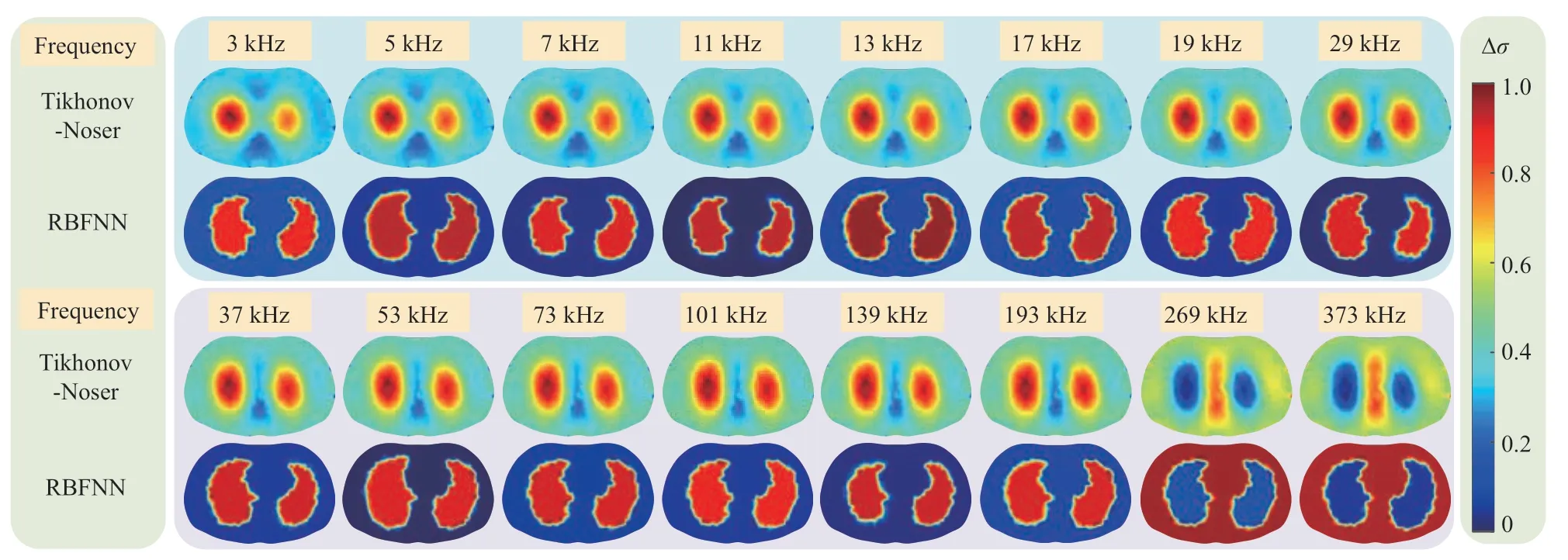
Fig. 7 Experimental reconstruction results of wfd-EIT based on Tikhonov-Noser or RBFNN
在网络运算结构中,输入层为加权频差阻抗ΔZ=[Δz1,Δz2,…,Δzi]T,隐含层选取高斯函H=[h1,h2,…,hj]T。
其中,B=[b1,b2,…,bj]T为基宽向量,C=[c1,c2,…,cj]T为中心向量。假设隐含层到预测层之间的连接权值向量为W=[w1,w2,…,wj]T,则RBFNN期望输出电导率ΔσP=[Δσ1,Δσ2,…,Δσi]T计算为:
网络结构中的中心向量C,基宽向量B和权值向量W均需要训练学习。
a.利用K-Means聚类算法初始化i个聚类中心确定中心向量C,可由下式调整中心cj:
b.利用K最近邻(K-Nearest Neighbor,KNN)分类算法确定基宽向量B,可由下式调整中心bj:
式中:dj为所选聚类中心之间最大距离。
c.利用粒子群优化算法(particle swarm optimization,PSO)优化权值向量W,确定粒子群规模即随机生成粒子群的(速度矩阵V和位置矩阵P),通过迭代找到最优解。每次迭代,粒子通过跟踪局部极值pbest和全局极值来自主更新。位置矩阵P(权值向量W)初始值为:W=H,·Δσ。
使用均方根误差(root mean square error,RMSE)作为PSO的适应度函数,来度量粒子空间位置的优劣。
式中:ΔσP为期望输出值,ΔσT为训练样本值,N为训练样本元素总数。
粒子通过自己的经验和同伴中最好的经验来决定下一步的运动,不断更新自身速度Vij和位置Pij:
满足结束条件,停止迭代,粒子群的全局极值gbest即是RBFNN连接权值的最优解。RBFNN全局网络流程如图2所示。
1.3 评价标准
为了比较EIT加权频差图像重建质量,使用图像相关系数(image correlation coefficient,ICC)来衡量重建图像和真实模型之间的误差和相似性。计算肺区域比(lung regional ratio,LRR)作为衡量重建图像的形状性能。
图像相关系数ICC表示预测重建图像和实际之间的非线性改变,定义为:
式中:N为节点数,为实际测试和仿真计算所得的各节点电导率变化值及其平均值。ICC范围为[0,1],数值越接近于1则重建图像与真实图像误差越小,图像结构更相似,重建方法更精确。
为了对图像形状度量,首先定义SRV为目标区域的形状总面积,SΔ(i)表示第i个剖分网格三角面积,j为SΔ(i)为节点坐标下标值,SGT为剖分网格中目标区域面积,其对应关系为:SRV=∑SGT(i)。定义电导率变化振幅平均值作为计算SGT的阈值,SGT可计算得:
肺区域比LRR为截面下肺部通气区域相对于胸腔总区域的占比,定义为:
式中:SSV表示胸部截面除肺部以外区域的面积,SRV即为肺部通气面积。LRR代表肺通气区域面积比,可用数值表示肺通气扩张功能状况,实验中所用模型占比最大为0.383。
2 模型仿真验证
2.1 数据集模型
Gabriel等[29]研究人体组织及器官在10 Hz~20 GHz频率范围内的介电特性,为研究生物阻抗谱提供重要参考标准。空气电导率恒为0 S/m,本文仿真样本中的正常肺组织、肌肉以及其他组织电导率值均来自于该数据库。人体胸腔相关器官组织在部分频率下的电导率和相对介电常数如表1所示。

Table 1 Electrical characteristics data of some human tissues
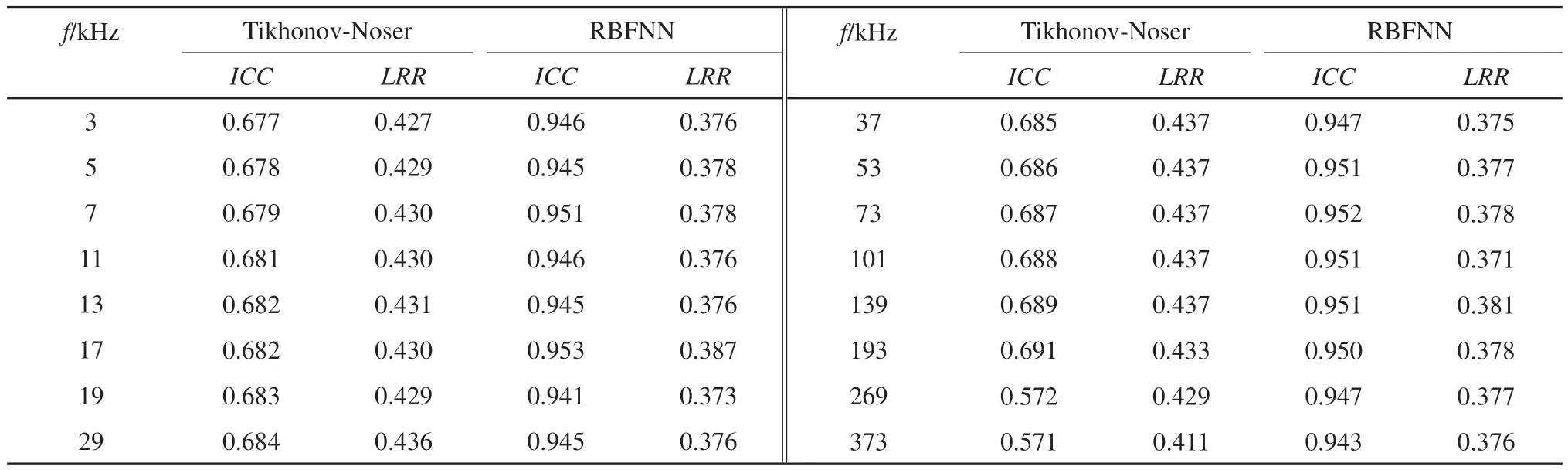
Table 2 Average ICC values of reconstructed images at different excitation frequencies and LRR values under maximal ventilation in the test set
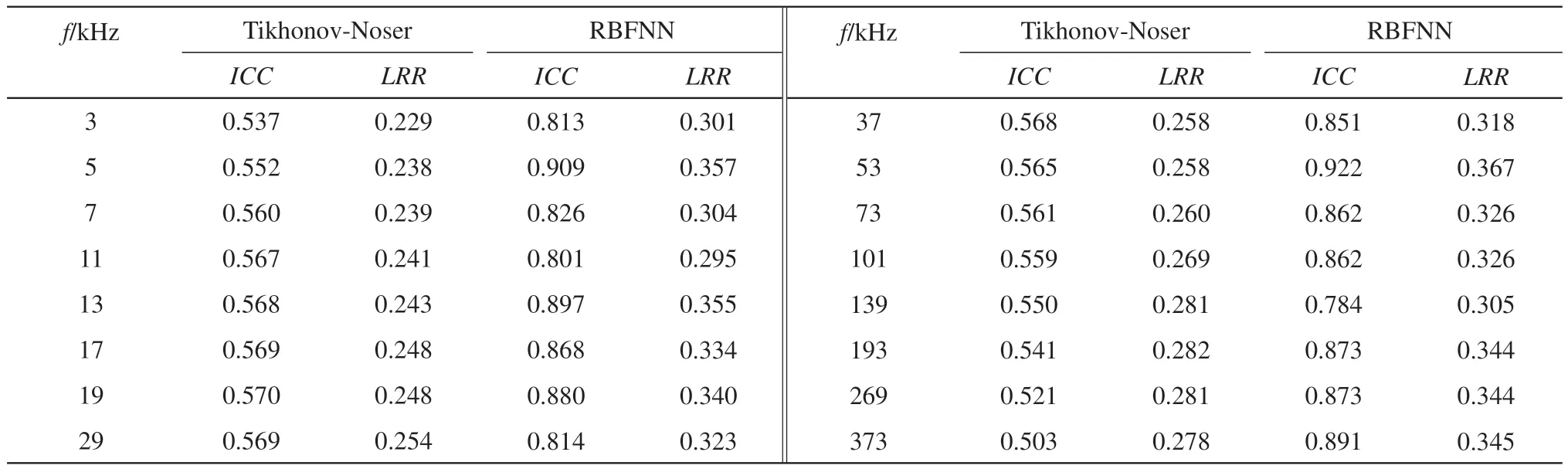
Table 3 ICC and LRR values of experimental reconstructed images
基于胸腔CT扫描图片,提取人体真实胸部轮廓与肺部轮廓组合为二维胸腔肺部模型。为了研究肺部在不同频率下的EIT运动,使用COMSOL和MATLAB联合仿真,在研究频域电流场中对生物组织构建不同频率仿真数据集进行有限元网格剖分计算。仿真模拟通过均匀分布在胸腔第4~5肋骨间的16个电极片采集胸腔表面阻抗数据,模拟重建场域内部电导率分布,使用相邻法测量模式,激励电流为3 mA,测量激励频率分量为2、3、5、7、11、13、17、19、29、37、53、101、139、193、269、373 kHz。数据集需要包括边界加权阻抗差值矩阵(参考频率f1统一选择为2 kHz)以及相对应的内部节点电导率变化分布矩阵,输入如图3所示的神经网络工作框图进行训练及预测。
图4所示为仿真中不同样本的分布情况。按照构造肺部不同通气状态大小目标,共计进行2 028次数值仿真计算,以获得不同电导率分布在不同频率下的电导率变化和边界阻抗加权变化。其中,随机选择1 800个数值样本用于训练,剩余228个样本用于测试。
针对图4中所示的每个实验样本仿真得到的数据集都包括1 304个电导率分布变化值和相对应208个边界阻抗加权变化值,且分别归一化处理到[0,1]的范围。其中边界阻抗加权变化值是在不同频率下测得的阻抗数据进行加权相减所得,用作网络模型特征输入,相对应场域电导率分布变化值作为网络模型标签输出。
2.2 数据仿真结果
本文分别采用Tikhonov-Noser和RBFNN方法进行加权频差图像重建实验。选取图4中测试集样本模型在部分频率下的加权频差阻抗重建图像(图5)。表2为测试集重建结果图像相关参数ICC在不同频率下对应的平均值,并计算当肺部达到最大扩张时所对应的LRR参数。
基于传统的Tikhonov-Noser重建方法重构所得图像边缘模糊,且图像存在伪影(图5)。Tikhonov-Noser重建方法在各个频率下图像ICC值均不超过0.70,LRR比样本实际占比大。与Tikhonov-Noser重建方法相比,基于RBFNN的频差成像方法重影的图像伪影更少,更加准确地表现出图像轮廓信息。不仅准确反映出不同肺部模型在任意激励下的目标位置,所得图像具有更好的ICC(平均达到0.940以上)。基于RBFNN的wfd-EIT不仅能够满足瞬时成像的需求,并且进一步提高重建图像质量,更为准确重建得到目标图像的空间位置与大小分布。
3 加权频差成像实验
3.1 系统设备
针对前文所述的检测成像方法,采用16电极wfd-EIT系统对待测物进行测量采集,开发出wfd-EIT系统硬件设备实物,系统各频率点的SNR较为均衡,平均SNR为55.3 dB,平均标准差为±6.2 dB。图6a给出了设备原理图,包括现场可编程门阵列(FPGA)模块、双通道14位125 Msps的DAC与ADC模块、模拟前端与电极阵列(含恒流源、差分放大电路、电极切换电路等)以及计算机和一个胸腔肺部模型(长15.8 cm,宽10.0 cm)。胸腔肺部模型是根据仿真中的胸腔肺部轮廓等比例所建立的,采用16个弧形铜质电极,宽度与之间间隔呈1∶1.5的比例均匀围绕于模型。
3.2 实验方法
如图6b,制作高度6 cm、内长半轴长15.80 cm、短半轴长10.00 cm的不规则胸腔轮廓用作wfd-EIT实验测量几何模型。实验设置模型内溶液电导率为0.02 S/m,采用的土豆材料(按等比例修成形似肺部的生物模型),电导率范围为:0.10~0.20 S/m,含水量65%~76%。所选取的生物组织的电导率差异比真实胸腔肺部内组织与气体的差异小得多,用于模拟肺部通气状态,并对其进行图像重建。
本文利用相位迭代优化的multisine合成算法[30]合成了一种包含16个等幅值质数伪对数频谱分布的多频正弦multisine激励信号,其中各个频率分量的归一化幅值均为0.316 2,基波周期f0为1 kHz。拥有较低的波峰因素(CF,峰值/有效值)提供更多的能量注入待测模型,以获得最大的阻抗测量精度。16电极的wfd-EIT系统采用相邻测量模式,将一个基波周期的multisine信号离散化成4 096个点预先存储在FPGA的ROM中,DAC在锁相环(PLL)控制下顺序读取ROM中的波形值生成模拟multisine信号,经过测量前端注入被测生物模型中,循环对(16-3)×16个通道在一个基波周期内(1 ms)进行单次测量即可完成全频阻抗测量,得到全频16个频率点的阻抗数据Zf(16×208)。
wfd-EIT系统以2 kHz激励下的边界阻抗数据作为基础参考数据,计算得到加权频差阻抗数据ΔZf:
其中,f为激励频率,Zf为待测模型在频率为f时的阻抗数据。将ΔZf送入预先训练好参数B、C、W的神经网络框架中计算场内电导率变化分布Δσf:
3.3 成像结果
根据仿真结果,wfd-EIT选择同时刻在2 kHz激励下的边界阻抗数据作为基础参考数据,利用式(16)与(17)计算瞬时时刻的多频加权频差阻抗重建图像(图7)。表3为各个频率下图像重建结果与仿真模型相关度(即式(12)表示的图像评价指标ICC),ICC越接近于1则表示成像结果相关度越高,成像质量更佳;肺区域比LRR则表示重建图像中的肺部通气区域相对于胸腔区域的占比。
对实验所建的胸腔肺部实物模型进行测量,wfd-EIT成像方法利用多频阻抗谱同步测量实现目标区域的快速可视化,能够快速得到多个频率下的肺部wfd-EIT图像(图7)。Tikhonov-Noser方法图像仅能呈现待测物的位置信息,其轮廓边缘模糊,图像依然存在伪影干扰,且拥有较低的ICC值和LRR值。而RBFNN方法能精确识别到模型中待测物位置轮廓信息,得到更为准确的成像效果。在53 kHz时wfd-EIT图像呈现最高的ICC值(最高可达0.922),LRR值为0.367最接近仿真模型面积占比。在不同频率下图像重建效果不同,考虑是受基础参考频率选定与实验目标电特性影响,而图像在193 kHz和269 kHz频率之间成像结果背景与目标颜色发生转变则是因为,在基于2 kHz参考频率阻抗时,胸腔和肺部的阻抗相对变化大小发生了转变。后续考虑改进multisine激励信号谐波频率组合,寻找最佳基础频率以呈现更好的成像效果。实验数据测试结果表明,基于RBFNN的肺部wfd-EIT方法,能够在同一时刻呈现多个频率的阻抗图像,并且有更好的目标边界轮廓重建能力,可定量数据评估肺部通气分布状况。
4 结论
为了能够对肺部通气状况的EIT实时可视化,提高肺部EIT图像重建的准确性,本文提出一种基于RBFNN的肺部wfd-EIT成像方法。依据公开生物电特性数据构建不同频率下的wfd-EIT胸腔肺部仿真样本集,研究了该方法的可行性,并通过实验进行验证。测试集图像重建结果与16电极wfd-EIT系统实验测试结果表明,使用测量所得的阻抗数据作加权差分求解,不仅可以有效消除单次建模误差和系统测量误差的影响,而且有效避免了临床医学中时间阻抗基线参考数据难以准确获取的问题,大幅提高wfd-EIT成像时间分辨率,能够满足对肺部呼吸运动进行实时性检测成像的要求。同时wfd-EIT在瞬时时刻获取不同频率的阻抗图像,显现肺部呼吸时电特性的变化。与Tikhonov-Noser算法相比,基于RBFNN的wfd-EIT算法逼近任意非线性函数的优点,有效提高了网络模型的预测精度(测试集精度平均可达到0.940),进而提高wfd-EIT图像的空间分辨率,具有更好的图像重建效果和轮廓重建能力(实验重建图像精度高达0.922)。
在未来的研究中,将所提出的成像方法用作对肺部呼吸运动实时成像的监测,无创地测量胸部阻抗,以提供通气分布的实时成像。基于这些优势,wfd-EIT方法针对呼吸疾病患者实时监测有着重要意义。