配合物[Pd(EDTB)Cl2]·2HCl·3H2O的合成、晶体结构及其荧光性质
2023-07-13金光陈彦国
金光,陈彦国
(湖北工业大学材料与化学工程学院, 湖北 武汉 430068)
0 引言
贵金属钯(palladium,Pd)的配合物参与协同活化、细胞显影、增殖抑制等过程,在化学[1]、生命科学[2]、医学等领域[3]有着广泛的应用.钯的配合物对偶联反应Mizoroki-Heck[4]、Suzuki-Miyaura[5]、Sonogashira[6]等有显著的催化效果,一些钯配合物还具有光学活性[7],可用于探索生物机体,El-sayed[8]等合成的掺杂于溶胶-凝胶基质中的Pd(Ⅱ)-邻羟基苯乙酮嗪配合物,可用于分析唾液中的α-淀粉酶的活性;Milic等[9]合成的2-氨基噻唑衍生物的Pd(II)配合物,能够与CT-DNA(小牛胸腺DNA)以沟槽方式结合,分析结肠癌CT-26细胞系的毒活性;Ragab等[10]制备的一种含1,4-二(3-氨基丙基)哌嗪(BAPP)配体的Pd(II)配合物,可用于模拟与人类DNA结合亲和力,并预测评估了体外药代动力学.一些重金属离子与机体休戚相关,如Pb2+[11],Hg2+[12],Fe3+[13]等通过DNA损伤[14]、细胞转化[15]的作用方式对机体造成伤害,形成潜在的致癌危险.
本工作合成了一种新的含六齿配体N,N,N′,N′-四(2′-苯并咪唑甲基)乙二胺(EDTB)单核Pd(Ⅱ)配合物[Pd(EDTB)Cl2]·2HCl·3H2O,测定了其晶体结构,研究了常见的碱金属离子、碱土金属离子、过渡金属离子对该配合物荧光光谱的影响.
1 实验部分
1.1 实验试剂邻苯二胺、乙二胺四乙酸(EDTA)、乙醇、乙二醇、氯化钯(PdCl2)及无机金属盐试剂均为分析纯,所有试剂使用前均未进一步纯化,实验用水为蒸馏水.
1.2 实验仪器APEX-II CCD型X-单晶衍射仪(Bruker公司),荧光光谱测试使用LS-55型荧光分光光度计(Perkin Elmer公司),iS50红外分析仪(Nicolet公司).
1.3 配合物1的合成将0.29 g EDTB(0.5 mmol)溶于20 mL热乙醇(50 ℃)之中,配制含0.088 7 g PdCl2(0.5 mmol)10 mL的盐酸溶液,使用滴液漏斗将PdCl2的盐酸溶液缓慢滴加至EDTB的乙醇溶液中,反应温度控制在78~80 ℃之间,回流反应8 h.反应结束后,待混合物冷却至室温,进行抽滤.收集滤液,在室温条件下自然挥发两周后得到配合物1的黄色晶体.IR(KBr)v/cm-1:3 622~3 148(br,s),1 217(s),1 622(m),1 457(m),747(s).
1.4 配合物1晶体结构测定选取大小为0.3 mm×0.2 mm×0.1 mm的晶体置于单晶衍射仪上进行测试,在低温条件100.15 K,以Ga Kα(λ=0.134 138 nm)为入射线,在2.968°<θ<61.872°范围进行扫描,收集到44 137个衍射点,选择其中8 527个独立衍射点,使用SHELXM对偶空间法进行晶体结构解析,并使用最小二乘法进行精细修正.
配合物1属于正交晶系,Pccn空间群,化学式为C34H40Cl4N10O3Pd,a=2.901 5(5)nm,b=1.447 8(2)nm,c=1.741 1(3)nm,α=β=γ=90°,V=7.314(2)nm3,Z=8,F(000)=3 616,Dc=1.607 g/cm3,Mr=884.96,μ=4.841 mm-1.最终因子(I>2σ(I))R1=0.063,wR2=0.151 6;R(全部数据):R1=0.067 4,wR2=0.153 9,最终差值电子云图中最大残余正峰和最大残余负峰分别为(Δρ)max=2 519 e/nm3、(Δρ)min=-1 538 e/nm3.
1.5 配合物1荧光光谱的测定将1.0×10-4mol/L配合物1的乙醇溶液加入荧光比色皿中,在室温下,激发狭缝10 nm,发射狭缝10 nm,扫描范围220~500 nm,扫描速度500 nm/min,测得其荧光光谱.
配制1×10-2mol/L金属离子储备溶液(AlCl3,NaCl,KCl,CoCl2,MgCl2,CaCl2,HgCl2,NiCl2,CuCl2,FeCl2,FeCl3,Pb(NO3)2,AgNO3),每次使用移液枪量取10 μL金属离子储备液加至1 mL 1.0×10-4mol/L配合物1的乙醇溶液中,测量不同金属离子加入后的荧光强度IF.所有荧光强度均在室温条件下测得,且体系在6 min时获得稳定可信的检测结果.
2 结果与讨论
2.1 配合物1的晶体结构分析配合物1晶体的主要键长及键角列于表1,配合物1分子的氢键列于表2,图1、2分别是配合物1的分子结构图和晶胞堆积图.
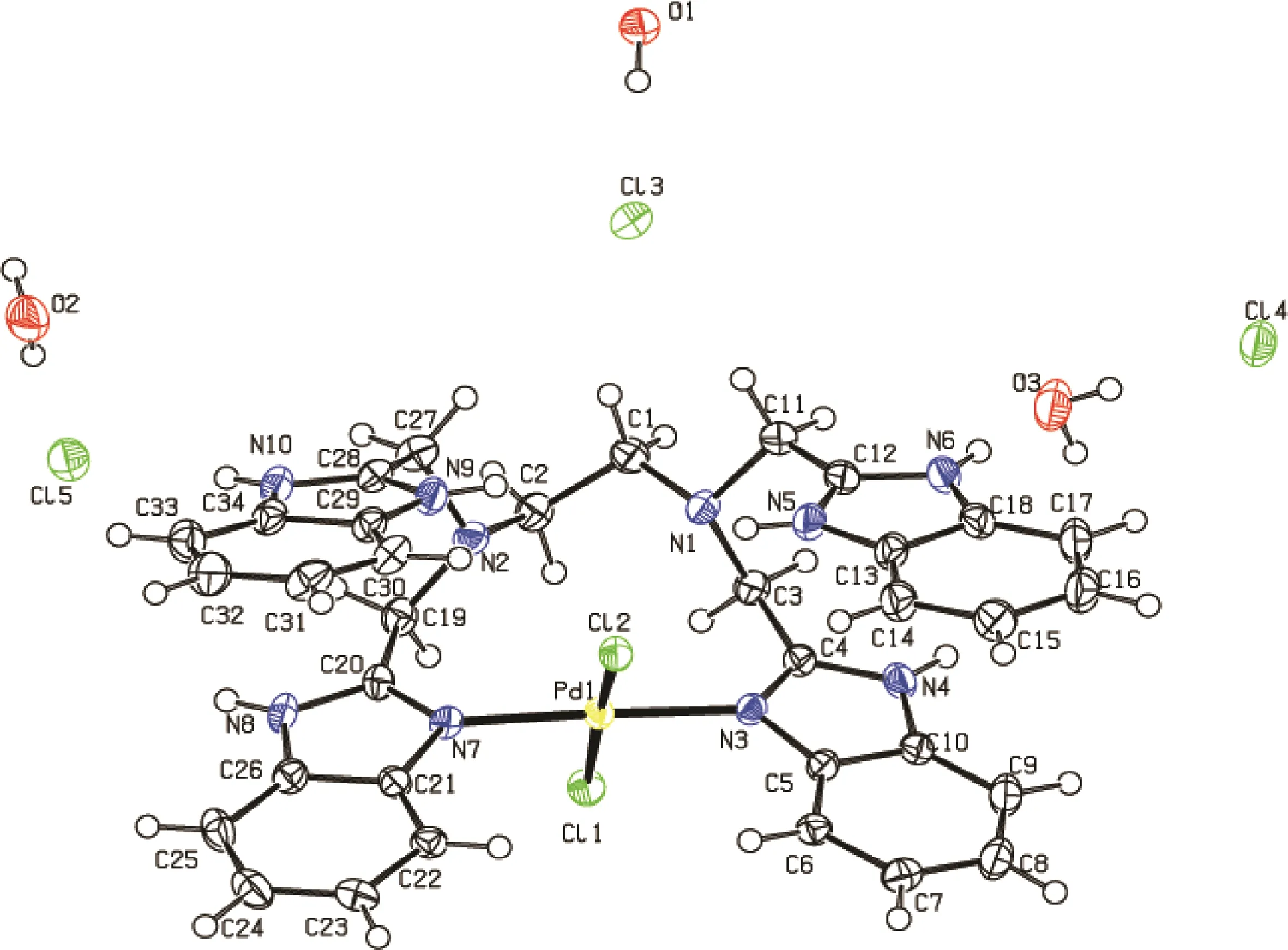
图1 配合物1的分子结构图
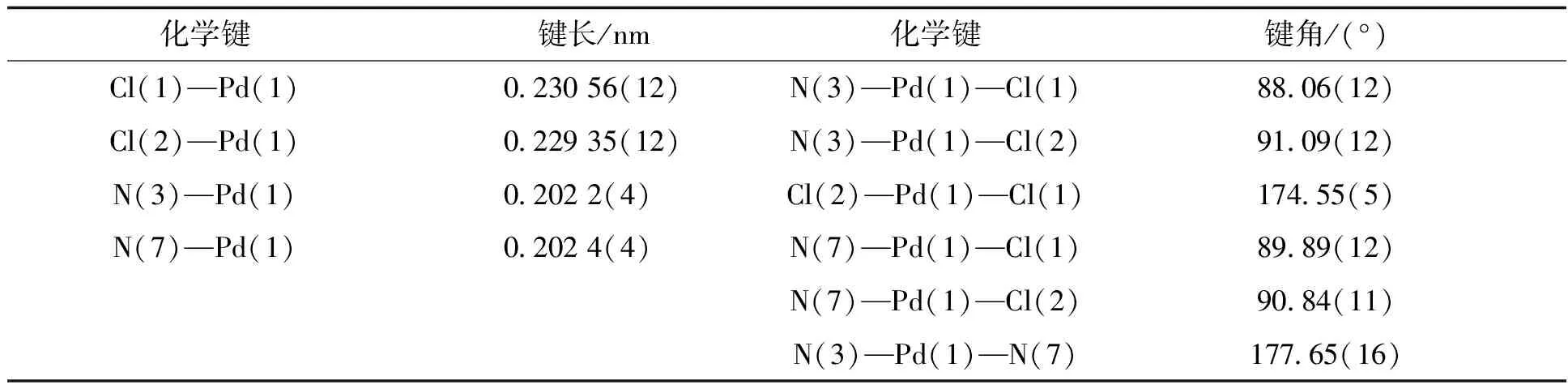
表1 配合物1的部分键长和键角数据

表2 配合物1分子的氢键键长和键角
配合物1的晶体结构分析表明(图1所示),Pd(1)离子与配体EDTB的苯并咪唑的2个N[N(3),N(7)]原子及2个Cl离子[Cl(1),Cl(2)]配位,N原子与Cl离子对角分布,形成四配位的平面结构.Pd(1)离子与配体EDTB苯并咪唑环上的N[N(3)、N(7)]原子配位,不与胺基N[N(1)、N(2)]原子配位,归因于胺基N原子与Pd(Ⅱ)配位的空间位阻较大,配位结构不稳定.分析表1可知,Cl(1)—Pd(1)和Cl(2)—Pd(1)键长都接近为0.23 nm,N(3)—Pd(1)和N(7)—Pd(1)键长都接近为0.202 nm,N(3)—Pd(1)—Cl(1)、N(3)—Pd(1)—Cl(2)、N(7)—Pd(1)—Cl(1)和N(7)—Pd(1)—Cl(2)的键角都接近90°,Cl(2)—Pd(1)—Cl(1)和N(3)—Pd(1)—N(7)键角分别为174.55(5)°和177.65(16)°,接近180°,证实配合物以Pd(Ⅱ)为中心形成了扭曲的四边形结构.晶体数据分析表明,配合物1中配位中心Pd(1)离子与N原子、Cl离子形成了四配位的扭曲平面结构.
图2是配合物1的晶胞堆积图,配合物中结构单元为[Pd(EDTB)Cl2]·2HCl·3H2O.依据图1、图2,结合表2可知,配体EDTB苯并咪唑环上的亚氨基N原子[N(4)、N(5)、N(6)、N(8)、N(9)、N(10)]、HCl中的Cl原子[Cl(3)、Cl(4)、Cl(5)]、H2O中的O原子[O(1)、O(2)、O(3)]彼此之间形成氢键.氢键种类有3种,分别是N—H…Cl,N—H…O和O—H…Cl.其中氢键N—H…Cl,即 N[N(5)、N(6)、N(8)、N(9)]—H…Cl,氯原子作为电子给予体;氢键N—H…O,即N[N(4)、N(10)]—H…O,氧原子为电子给予体;氢键O—H…Cl,即O[O(1)、O(2)、O(3)]—H…Cl,氯原子属于电子给予体.所有氢键D—H…A,d(D—H)近似于0.08 nm,d(H…A)近似于0.22 nm,d(D…A)近似于0.30 nm,表明氢键作用力均衡,使得配合物的分子结构更加稳定.
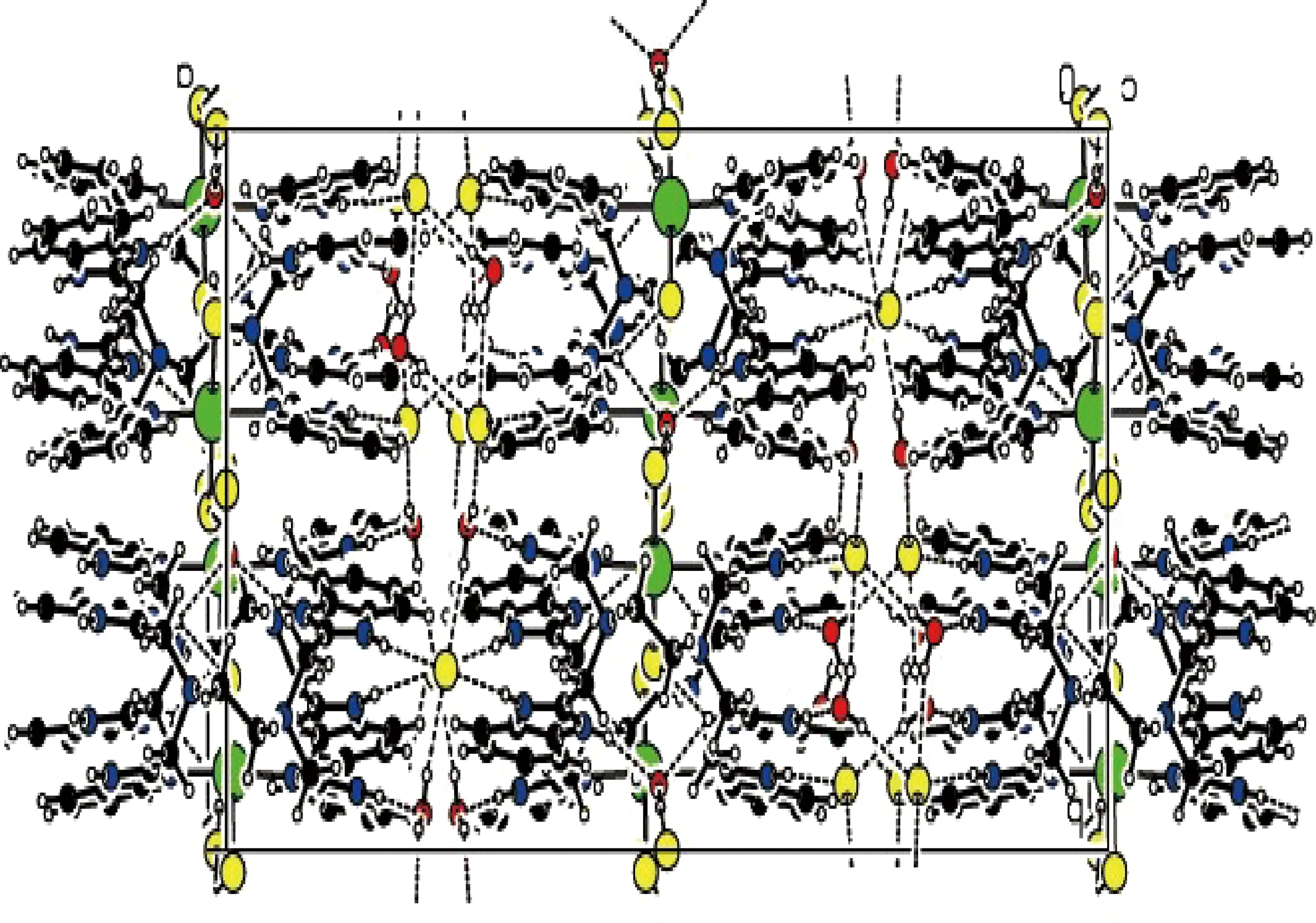
图2 配合物1的晶胞堆积图
2.2 配合物1的荧光特性研究
2.2.1 配合物1的荧光光谱 图3为1.0×10-4mol/L配合物1乙醇溶液的荧光光谱图,配合物的激发波长为300 nm,最大发射波长为366 nm.由配合物的晶体结构可知,苯并咪唑环上N原子与Pd(Ⅱ)以配位键形式连接,电子可通过配位键转移,受到特定能量激发后,N原子的孤对电子发生π-π*和n-π*跃迁[16],同时配合物分子中存在多种氢键,使得配合物在366 nm处具有较强的荧光发射峰.

图3 配合物1(1.0×10-4 mol/L)的荧光光谱
2.2.2 不同金属离子对配合物1荧光的影响 进行一系列实验探讨不同金属离子对配合物1荧光的影响.不同金属离子加入配合物1后其荧光强度变化不同,如图4、5所示,加入Al3+后,配合物1的荧光强度有较小的增强;分别加入碱金属离子Na+,K+后,配合物1的荧光发生了微小的猝灭;分别加入碱土金属离子Mg2+,Ca2+后,配合物1的荧光猝灭的程度较大;分别加入过渡金属离子Hg2+、Ag+、Co2+、Ni2+、Pb2+、Cu2+、Fe2+、Fe3+后,配合物1的荧光发生了较强的猝灭,其中Fe3+的荧光猝灭效率最高.
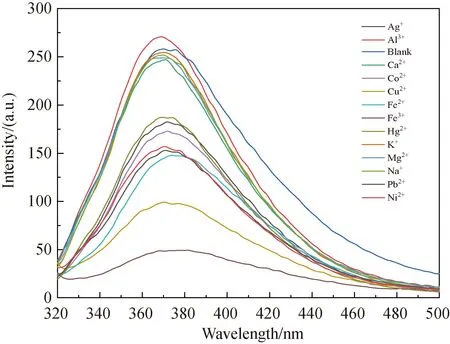
图4 加入不同金属离子6 min后配合物1的荧光光谱

图5 不同金属离子对配合物1荧光的影响
不同金属离子对配合物1的荧光影响不同,其荧光猝灭机理也不同[17-18],Al3+对配合物表现出荧光增强作用,可能是由于Al3+与配合物中的N-H的作用,形成了N-H…Al,使得共轭体系更加稳定[19-20],电子跃迁能量降低,使得荧光强度增强;而K+、Na+、Mg2+、Ca2+这些金属离子与配位中心Pd2+发生了自由碰撞,从而导致了荧光猝灭[21-22];多数过渡金属离子对配合物的荧光表现出较强的猝灭,这些金属离子可以提供空的4 d轨道,具有较强的容纳孤对电子能力,也可与配体EDTB进行配位,而含Fe配合物[23]、Co配合物[24]、Ni配合物[25]、Cu配合物[26]的报道证实金属离子存在与Pd2+发生竞争反应,导致了荧光动态猝灭[27-28]现象.其中Fe3+较Fe2+表现出更明显的猝灭,归因于Fe3+核电荷更高,半径更小,更加容易接受配体EDTB的电子对[29],更易于形成稳定的配合物,因此其猝灭配合物荧光的能力更强.
不同浓度的Fe3+、Fe2+对配合物1荧光强度的影响见图6.随着Fe3+的加入浓度增大,配合物1的荧光猝灭程度也不断增大,而Fe3+的EDTB配合物,其配位中心是双核Fe3+,因此Fe3+与Pd2+竞争EDTB配位键更加剧烈,使得荧光猝灭程度更强.
3 结论
合成了一种新的含六齿配体N,N,N′,N′-四(2′-苯并咪唑甲基)乙二胺(EDTB)的Pd(Ⅱ)配合物,其晶体结构用X-单晶衍射进行解析,结果表明,配合物中心阳离子Pd2+分别与两个苯并咪唑N原子和两个Cl离子进行配位,形成四配位的扭曲平面结构,氢键作用使得配合物的分子结构更加稳定,利用荧光光谱法研究了配合物1与不同金属离子的相互作用,实验表明:碱金属离子(Na+,K+)和碱土金属离子(Mg2+,Ca2+)对配合物荧光影响较小(干扰小),过渡金属离子对配合物的荧光产生了较强猝灭效应,其中Fe3+荧光猝灭效率最高,并探讨了配合物荧光猝灭的机理.
铁离子作为人体血红蛋白的载体,人体细胞中含量低时,会导致人体贫血.铁离子与其他重金属离子如汞离子、铅离子含量的高低是人体造血功能的正常与否的标志,人体细胞中重金属离子如汞离子、铅离子超标,影响人体细胞对铁离子的吸收从而影响肝脏造血功能,将导致血红蛋白的合成障碍诱发肝癌或白血病.因此,建立一种快速检测人体细胞中铁离子、汞离子、铅离子含量的方法具有现实意义,利用Fe3+对配合物1的荧光猝灭效率高,将我们新合成的配合物1作为荧光分子探针快速检测人体细胞中铁离子含量有实际应用价值.
