HPLC-DAD法同时测定莪棱胶囊中5种活性成分含量
2023-06-16邓俊昆
邓俊昆
(广东省中医院 药学部 制剂科,广东 广州 510170)
莪棱胶囊由赤芍、丹参、郁金、醋鳌甲、蒸枳壳、浙贝母等十一味中药组成,是由广东省中医院老中医经验方结合临床实践研制的医院制剂,主要用于治疗子宫肌瘤和子宫内膜异位症等。目前,学界对其质量控制的文献报道仅有芍药苷单一成分的含量测定方法[1],以及丹参、枳壳、延胡索的薄层鉴别方法[2],缺乏多指标的含量检测和质量控制方法。为了更好、更全面地控制莪棱胶囊的内在质量,本研究采用高效液相色谱(HPLC)波长切换法同时测定莪棱胶囊中5种活性成分的含量,以确保其临床用药安全有效,为后续莪棱胶囊质量标准提高提供实验依据。
1 仪器与试药
1.1 仪器
Agilent 1260高效液相色谱仪,配二极管阵列检测器(Agilent公司);KQ5200E型超声波清洗器(昆山超声仪器公司);ME104E型电子天平(梅特勒-托利多)。
1.2 试药
莪棱胶囊(批号:21050601、21052202、21060402)及其阴性对照样品均为本院制剂;芍药苷对照品(批号:110736-201927,含量:98.2%)、柚皮苷对照品(批号:110722-202012,含量:94.6%)、橙皮苷对照品(批号:110721-202008,含量:97.8%)、丹酚酸B对照品(批号:111562-201926,含量:96.7%)和丹参酮ⅡA对照品(批号:110766-202011,含量:94.3%),均购自中国食品药品检定研究院。乙腈和甲醇为色谱纯,磷酸为分析纯。
2 方法与结果
2.1 色谱条件
Agilent C18色谱柱(250mm×4.6mm,5μm);流动相为乙腈(A)-0.1%磷酸溶液(B),切换检测波长进行梯度洗脱(230nm:0~15min 15%A;280nm:15~16min,15%A→21%A,16~32min,21%A,32~45min,21%A→55%A;270nm,45~68min,55%A→85%A);流速1.0mL/min;柱温30℃;进样体积10μL。
2.2 溶液制备
2.2.1 混合对照品溶液 分别精密称取适量5种待测组分对照品,先用甲醇溶解定容制得不同浓度的单一对照品溶液,再分别精密吸取适量体积的上述单一对照品溶液,置于同一容量瓶中,加甲醇稀释定容,制得质量浓度为芍药苷18.06mg/mL、柚皮苷7.41mg/mL、橙皮苷24.93mg/mL、丹酚酸B 3.74mg/mL、丹参酮ⅡA1.06mg/mL的混合对照品溶液。
2.2.2 供试品溶液 取莪棱胶囊适量,去掉胶囊后研细混匀,过80目筛,精密称取1.0g左右的细粉,加甲醇50mL,称定质量,超声提取(功率250W,频率50kHz)30min,放置室温,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液 根据莪棱胶囊处方工艺,制备不含赤芍、丹参、枳壳药材的阴性对照样品,并按“2.2.2”项下方法处理,制得阴性对照溶液。
2.3 专属性试验
取混合对照品溶液、供试品溶液和阴性对照溶液,按照“2.1”项下色谱条件进样,记录色谱图,结果见图1。
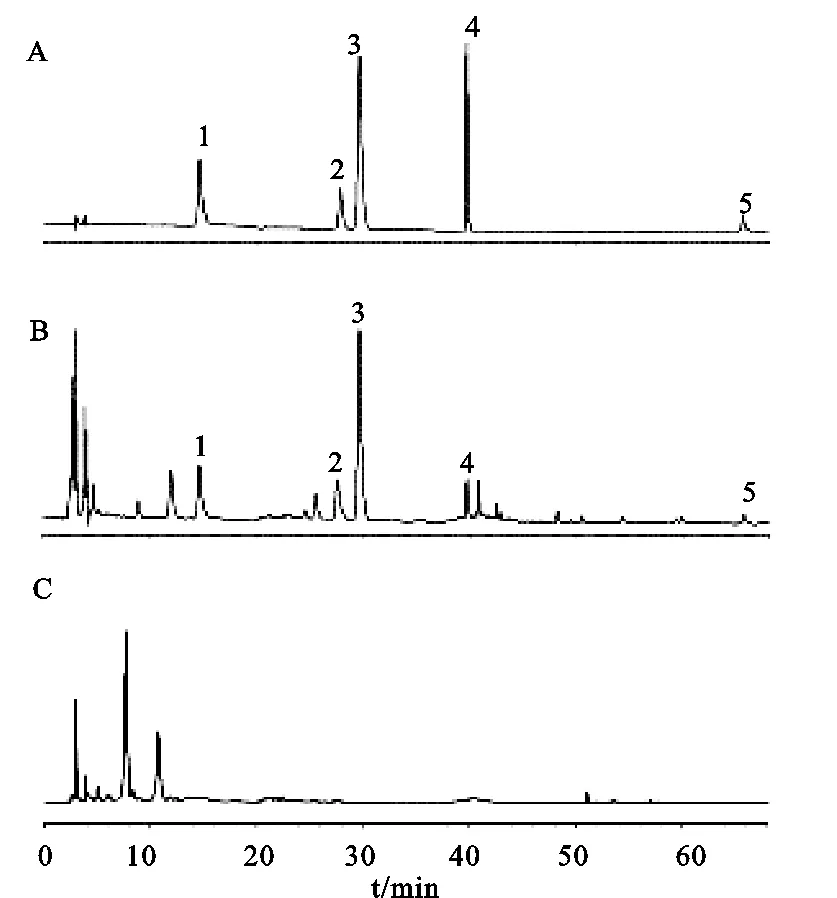
注:1.芍药苷;2.柚皮苷;3.橙皮苷;4.丹酚酸B;5.丹参酮ⅡA。
从图1可见,供试品溶液的色谱图和混合对照品溶液的色谱图有保留时间相同的色谱峰,而阴性对照溶液的色谱图在对应位置无色谱峰出现。此外,待测的5个成分与其相邻的峰之间均达到了基线分离,周边无杂质峰干扰。
2.4 线性关系考察
分别精密吸取“2.2.1”项下的混合对照品溶液2、5、10、15、20μL,按照“2.1”项下色谱条件进样,记录色谱峰面积。以进样质量(μg)为横坐标,峰面积A为纵坐标,进行线性回归,得回归方程,结果见表1。
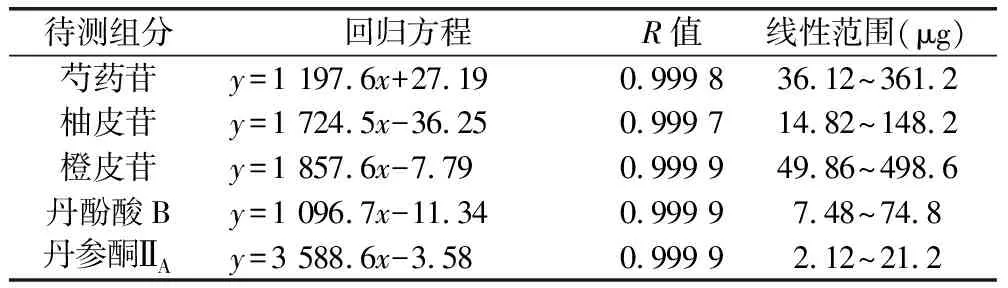
表1 线性关系考察结果
2.5 精密度实验
精密吸取“2.2.1”项下的混合对照品溶液10μL,注入液相色谱仪,连续6次进样测定峰面积,分别计算RSD。结果该方法的精密度良好,芍药苷、丹酚酸B、丹参酮ⅡA、柚皮苷和橙皮苷的RSD值分别为0.69%、0.57%、0.38%、0.40%和0.52%,均小于2%。
2.6 稳定性实验
取同一份供试品溶液,在制备后的第0、2、4、8、12、24h分别进样10μL,测定芍药苷、丹酚酸B、丹参酮ⅡA、柚皮苷和橙皮苷的峰面积,计算出RSD值分别是0.88%、1.12%、0.93%、0.69%和0.77%,表明在该检测条件下供试品溶液在24h内稳定。
2.7 重复性实验
取同一批次莪棱胶囊(批号:21050601),按照“2.2.2”项下供试品溶液制备方法制备,在相同的色谱条件下测定5种成分的含量和RSD值。结果显示,芍药苷、丹酚酸B、丹参酮ⅡA、柚皮苷和橙皮苷的含量分别为4.17、0.61、0.22、1.75和5.25mg/g,RSD值分别为0.98%、1.28%、1.64%、1.02%和1.23%,表明该方法重复性良好。
2.8 回收率试验
取已知含量的莪棱胶囊(批号:21050601)细粉约0.5g,平行6份,分别准确加入适量的混合对照品溶液,按照上述供试品制备方法和色谱条件进行检测。加样回收率的试验结果如表2所示。结果显示,芍药苷、柚皮苷、橙皮苷、丹酚酸B和丹参酮ⅡA的平均回收率分别为100.53%(RSD=0.41%)、98.91%(RSD=1.26%)、98.56%(RSD=0.53%)、100.03%(RSD=0.93%)和99.54%(RSD=0.99%),表明该方法回收率良好。
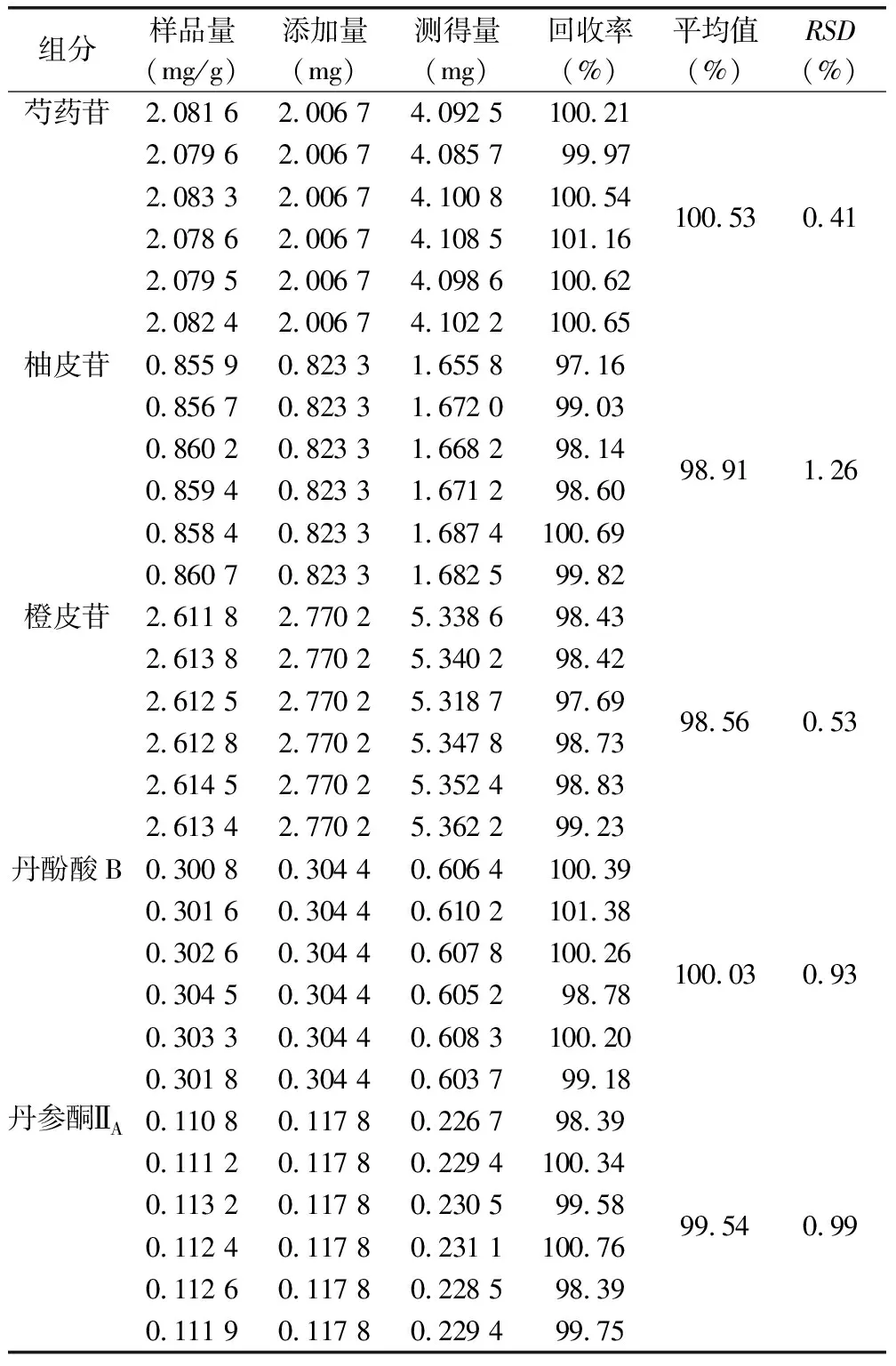
表2 五种成分的加样回收率试验结果 (n=6)
2.9 样品测定
取3批莪棱胶囊(批号:21050601、21052202、21060402),按照上述供试品制备方法和色谱条件进行检测,做3次平行,根据峰面积计算各待测组分的含量(mg/g),结果见表3。
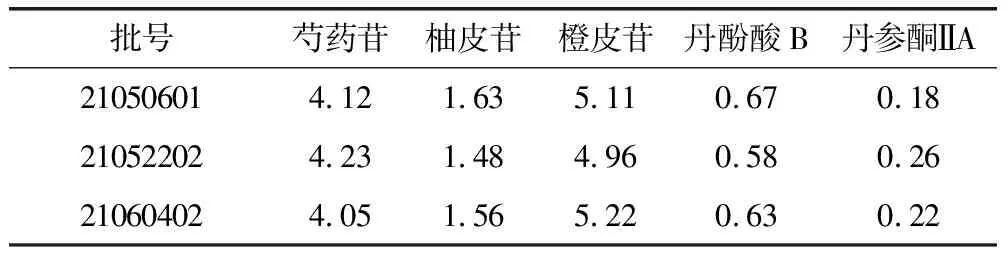
表3 莪棱胶囊各组分含量测定结果 (mg/g,n=3)
3 讨论
3.1 检测成分选择
莪棱胶囊包含十一味中药,前期预试验曾结合2020版《中华人民共和国药典》和相关文献报道[3-5]对其可能存在的活性成分进行检测,结果当归(阿魏酸)、郁金(姜黄素)和浙贝母(贝母素甲、贝母素乙)等药材中这些活性成分未见特征峰或峰分离效果不好,分析其原因可能有两个,一是各中药在莪棱胶囊处方中所占比例不同,二是不同中药之间存在相互作用或干扰。本研究根据前期实验结果并综合考虑各活性成分色谱峰情况、含量差异,以及制剂的综合评价,最终确定以芍药苷、柚皮苷、橙皮苷、丹酚酸B和丹参酮ⅡA这5种特征峰明显且分离较好的组分作为莪棱胶囊质量控制的检测指标。
3.2 检测波长确定
由于本研究检测的5种活性成分最大吸收波长并不相同,为了能够使莪棱胶囊中的这些成分在同一色谱条件下均可检测出。本实验采用HPLC波长切换法检测,根据莪棱胶囊中这5个待测组分的最大吸收波长或接近其最大吸收波长作为本实验的检测波长。通过二极管阵列检测器对各组分进行全波长扫描,并结合《中华人民共和国药典》和文献[6]中检测波长,最终确定了230nm(芍药苷)、280nm(橙皮苷、柚皮苷、丹酚酸B)和270nm(丹参酮ⅡA)三个检测波长,在实验中均取得了较好的检测效果。
3.3 色谱条件选择
莪棱胶囊作为由十一味药材组成的中药复方制剂,其包含的化学成分数量众多,不同类型的成分理化性质均不相同,为了让选择的检测组分实现较好的分离效果,本研究曾对乙腈-水、甲醇-水、乙腈-0.1%磷酸、甲醇-0.1%磷酸等不同流动相体系进行了考察,结果表明,最合适的溶剂体系是采用乙腈-0.1%磷酸溶液作为流动相进行梯度洗脱,在该色谱条件下,莪棱胶囊中的5个待测组分均表现出良好的分离效果,可以用于其含量测定。
3.4 供试品溶液制备方法选择
本研究曾根据莪棱胶囊中5种活性成分的理化性质,以理论板数、出峰情况和杂质干扰情况等作为评价指标,分别考察了不同提取溶剂(甲醇、稀乙醇、50%甲醇、70%乙醇、70%甲醇)、不同提取方法(超声提取、水浴回流)和不同提取时间(15、30、45、60min)下各待测组分的检测效果,最终确定“2.2.2”项下的制备方法。
4 结论
本研究建立了高效液相色谱(HPLC)波长切换法快速测定莪棱胶囊中5种活性成分的含量,并对其进行了方法学考察,结果表明,该方法稳定可行。运用此方法对三批样品的检验结果显示莪棱胶囊中芍药苷含量为4.05~4.23mg/g、柚皮苷含量为1.48~1.63mg/g、橙皮苷含量为4.96~5.22mg/g、丹酚酸B含量为0.58~0.67mg/g、丹参酮ⅡA含量为0.18~0.26mg/g。测定出不同批次莪棱胶囊各组分的含量波动范围较小,质量较稳定,可成为莪棱胶囊质量控制的一种有效方法。
