裂解温度对湿地植物基生物炭理化性质与镉吸附特性的影响
2023-03-20李心怡陆丽芳麻淳雅雷明婧
李心怡, 陆丽芳, 麻淳雅,2, 雷明婧, 朱 健
(1. 中南林业科技大学 环境科学与工程学院, 湖南 长沙 410004; 2. 衢州市生态环境局龙游分局, 浙江 衢州 324400;3. 中国石化股份有限公司 长岭分公司水务部, 湖南 岳阳 414000)
在全球范围内存在许多人工湿地和自然湿地系统, 为了使它们能够保持长期而高效的净化能力, 必须及时收割其中的湿地植物残体并进行科学的处理。 近年来, 许多研究发现生物炭在碳库增汇减排[1-2]、 土壤肥力改善[3-4]以及环境污染治理修复[5-6]等方面具有较大潜力, 因而引起全球土壤学和环境学领域专家学者的关注。 生物炭制备来源丰富, 目前主要集中于农林业废弃物、 畜禽粪便、 厨余废弃物等[7-8], 而对湿地植物的研究较少。 若将湿地植物制备成生物炭, 既可以维系湿地系统的稳定运行, 净化水质, 还可以通过生物炭还田来达到固碳、 减排作用。 此外, 热解温度是决定生物炭性质的关键因素之一。 已有研究表明, 生物炭最适裂解温度范围为300~700 ℃, 若裂解温度低于300 ℃, 生物炭结构不会发生明显改变, 若裂解温度高于700 ℃, 生物炭的微孔结构易于出现溶融[9-10]。 鉴于此, 本文中以美人蕉(MBC)、 再力花(ZBC)和旱伞草(HBC)为原料, 分别在低温(300 ℃)、 中温(500 ℃)和高温(700 ℃)裂解温度下制备湿地植物基生物炭,对其基本理化性质进行了分析,并以重金属镉(Cd)为目标污染物,研究湿地植物基生物炭对Cd的吸附特性,探究其潜在的吸附机制,为水土Cd污染治理与修复提供优质吸附材料及理论依据,实现湿地系统碳资源的高值化利用。
1 实验
1.1 主要材料和仪器设备
材料: 生物炭(制备原材料为MBC、 ZBC、 HBC, 2019年9月28日采自于湖南先导洋湖再生水有限公司人工湿地处理单元); 含Cd储备液(质量浓度为1 g·L-1), 将5.488 g的Cd(NO3)2溶解于2 L的容量瓶中, 用去离子水定容。
仪器设备: NCHS/O Flash Smart型全自动元素分析仪、 Axia Chemi型扫描电子显微镜(SEM)(美国赛默飞世尔科技公司);ALPHA II型傅里叶红外光谱仪(FTIR,美国布鲁克科技有限公司)。
1.2 方法
1.2.1 生物炭的制备
将HBC、 MBC、 ZBC地上部分洗净, 剪成小段后置于通风过道处自然晾晒2 d风干。 将风干植物置于温度为80 ℃的烘箱中烘制12 h, 剪碎磨成粉, 过筛(孔径为0.3 mm)后用密封袋保存。 称取一定质量的植物粉末放入坩埚中, 压实后封盖, 在马弗炉中加热。 先于温度为100 ℃条件下预热1 h, 然后以10 ℃·min-1的升温速率分别加热至300、 500、 700 ℃, 恒温加热2 h。 加热结束后先在炉内冷却30 min, 然后炉外继续冷却至常温, 研磨过筛(孔径为0.15 mm)后用密封袋保存并标记生物炭名称[11]。 将不同温度下制备的不同湿地植物基生物炭进行标记,MBC分别为M300、 M500、 M700, ZBC分别为Z300、 Z500、 Z700, HBC分别为H300、 H500、 H700。
1.2.2 静态吸附
将9种生物炭分别称取25、 50、 100、 150、 200 mg,放置于容积为50 mL的离心管中,再加入25 mL的含Cd溶液,将溶液pH调至设定值。预先设定摇床温度和转速(120 r·min-1),将离心管置于恒温摇床中振荡一段时间,在预设时间取出立即过滤至白色小方瓶中待测。分别探究不同吸附条件下(吸附时间t分别为5、 10、 20、 30、 60、 80、 120 min;投加的生物炭质量浓度ρ1分别为1、 2、 4、 6、 8 g·L-1; Cd2+初始质量浓度ρ0分别为10、 20、 50、 100、 200、 300、 500 mg·L-1; pH分别为3、 4、 5、 6、 7; 温度分别为15、 35、 55 ℃)生物炭对Cd2+的吸附能力与特性。吸附完成后,静置,取上清液采用原子吸收分光光度计测定Cd2+质量浓度,按式(1)计算吸附量。每个处理设置3次重复。在改变单因素的条件下,其他因素统一不变,即Cd2+初始质量浓度ρ0为100 mg·L-1,生物炭质量浓度ρ1为5 g·L-1, pH为7,温度为25 ℃, 吸附时间t为120 min。吸附量计算公式为
(1)
式中:qe为平衡时的吸附量, mg·g-1;ρ0为初始离子质量浓度, mg·L-1;ρe为平衡时的离子质量浓度, mg·L-1;V为Cd溶液体积, mL;m为生物炭投加质量,g。
利用Langmuir模型与Freundlich模型对湿地植物基生物炭在不同温度下对Cd2+的吸附量随其离子质量浓度的变化吸附等温线进行拟合,2个模型的线性表达式见式(2)、 (3)。
1/qe=1/(kL·qm)·1/ρe+1/qm,
(2)
(3)
式中:qm为吸附容量, mg·g-1;kL为Langmuir模型常数, L·mg-1;kF为Freundlich模型常数, mg·g-1;n为Freundlich模型常数。
采用拟一级动力学模型和拟二级动力学模型对湿地植物基生物炭吸附Cd2+的过程进行吸附性能考察,分别按式(4)和式(5)计算:
ln(qe-qt)=lnqe-k1t,
(4)
(5)
式中:qt为某时刻下的吸附量, mg·g-1;t为时间, min;k1为拟一级吸附反应的速率常数, min-1;k2为拟二级反应速率常数,g·mg-1·min-1。
1.2.3 样品分析与测试
采用差重法计算产率,利用文献[12]中提到的方法测定pH,生物炭灰分与挥发分的测定参照文献[13-14],采用比表面积物理测定仪测定比表面积和孔径分布[15],采用全自动元素分析仪测定元素含量,采用SEM表征观察生物炭的表面形貌,采用FTIR表征分析生物炭官能团的构成。
2 结果与讨论
2.1 湿地植物基生物炭理化特性
2.1.1 基本理化性质
裂解制备所得的9种湿地植物基生物炭的基本理化性质见表1所示。从表中可知,不同湿地植物制备的生物炭产率、灰分和挥发分差异性较为明显。就某一种湿地植物基生物炭而言,随着裂解温度的升高,生物炭的产率和挥发分含量均出现下降趋势,而灰分含量不断增加。9种湿地植物基生物炭中,Z300的产率最高,为45%,而H700的产率最低,为28.50%。同一裂解温度下ZBC的产率更高,说明选择ZBC作为基础材料,裂解制备得到的含碳产物更多。M700的挥发分含量最大,为35.72%,而H500的挥发分含量最少,为15.89%。
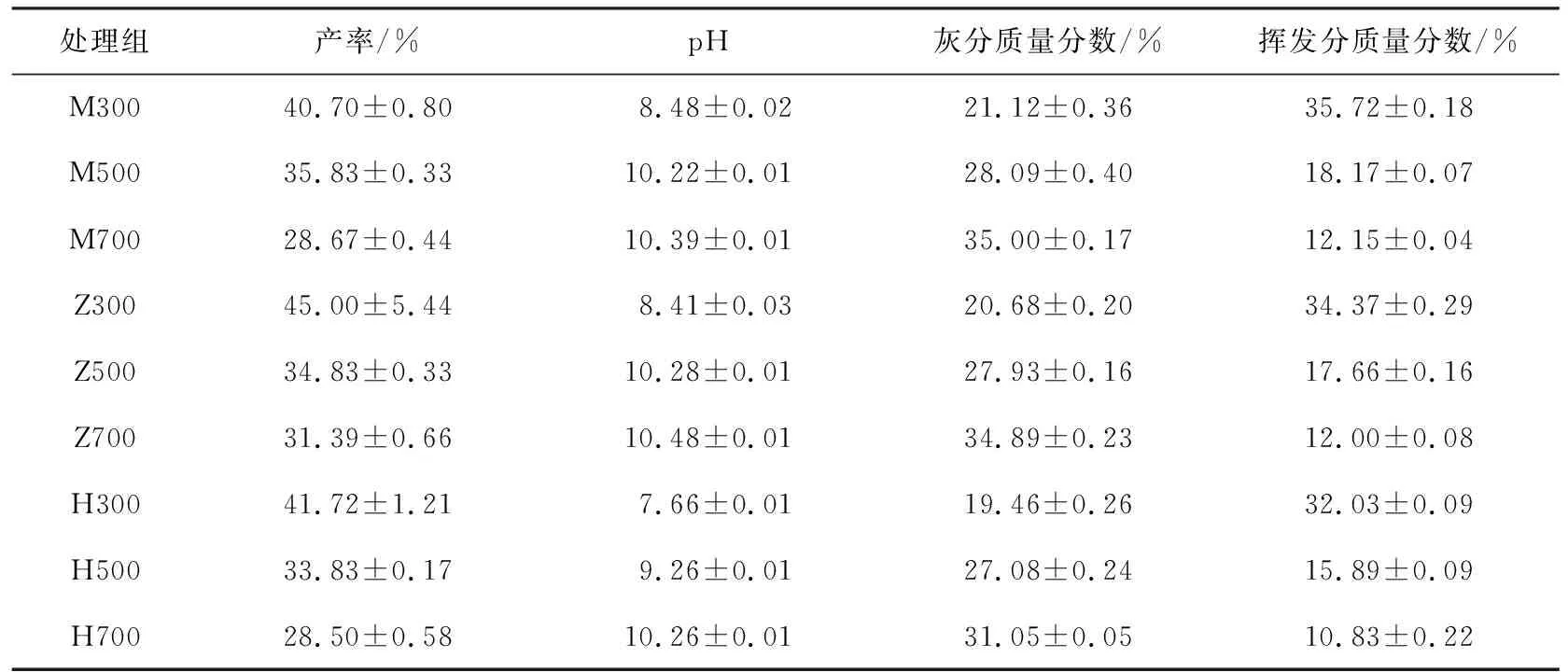
表1 湿地植物基生物炭的基本理化性质
9种湿地植物源生物炭的灰分含量从大到小的顺序为M300、 Z300、 H300、 M500、 Z500、 H500、 M700、 Z700、 H500,总体而言,MBC的灰分含量最高,其次是ZBC,最后是HBC。崔孝强[16]研究了在500 ℃下制备的22种湿地植物基生物炭,结果表明,相比于以秸秆或者木材为原料而裂解形成的生物炭,湿地植物源生物炭的产率、 灰分含量和阳离子交换量通常会更高,且pH大多数都在9~11之间。
2.1.2 理化结构特征分析
利用SEM对材料进行表征,得到了9种湿地植物基生物炭相同放大倍数下的表面形貌,如图1所示。由图可知,不同裂解温度下的生物炭材料表面形貌差异显著。各生物炭材料的表面粗糙,孔隙、颗粒较多,其中M700、 Z300、 H700的孔隙结构相比其他同植物基生物炭材料的特征更为明显,说明它们的比表面积相对更大。

(a)M300(b)M500(c)M700(d)H300(e)H500(f)H700(g)Z300(h)Z500(i)Z700图1 9种不同裂解温度下的湿地植物基生物炭的SEM图像Fig.1 SEM images of nine kinds of wetland plant-based biochar under different pyrolysis temperature
9种湿地植物基生物炭理化结构特征见表2所示。由表可知,随着裂解制备温度升高,9种湿地植物基生物炭中C和N、 C和H、 (O+H)和C的相对原子质量比值均明显减小,生物炭的BET比表面积、孔径和孔容积均有所增大(除了MBC的比表面积有所减小外)。热解温度是影响生物炭性能的重要条件之一。随着温度的升高,纤维素、半纤维素和木质素分解为小组分,包括小气体分子(如CO2、 H2O和CH4)以及随机释放的小挥发性有机物,从而降低了生物炭产率[17]。裂解温度越高,灰分含量越大[18],这是因为湿地植物中的绝大多数无机成分在裂解制备生物炭的过程中被浓缩存留在产物之中,碳化时生物炭内部热解激烈程度也在增加[19]。9种湿地植物基生物炭均呈碱性,随着温度的升高,其pH也随着灰分含量的增大而相应增大。pH的增大是因酸性有机官能团的丧失和碱性无机物的积累而引起的。

表2 湿地植物基生物炭理化结构特征
生物炭的理化结构也会随着热解温度的变化而变化。由元素组成分析结果可知,裂解制备温度越高,9种湿地植物基生物炭中碳元素所占比例越大,而氮、氢和氧元素质量分数越低,这与许多研究报道一致[20-21]。氮的减少是因氮的挥发以及氮随温度升高而损失[22]。此外,与以往的一些研究结论类似[23-24],制备过程中裂解温度越高,(O+N)和C、 H和C、 O和C的相对原子质量比值越低,这表明,高温能够促进生物炭中芳香结构的形成,提高生物炭的亲脂性能和稳定性能。以往研究表明,随着裂解温度升高,生物质分离、释放出更多挥发性物质,孔隙更多,比表面积增大[25]。在本研究中,Z700的BET比表面积却低于Z500的和Z300的,这可能是因为其灰分含量较高而堵塞部分生物炭孔隙所致,但是总体而言孔径尺寸的大小仍然随着制备温度的提升而增大。制备温度对生物质炭的理化性质、表面形貌和矿物成分有很大影响[26]。Chandra等[27]建议,稻草衍生生物炭的最佳热解温度为500~600 ℃,以获得高土壤养分含量、理想pH和低挥发性有机化合物含量。同时,生物炭可能携带原料中有害元素(如重金属和类金属)或热解过程中产生的意外致癌副产品(如二口恶英、多环芳烃)构成的污染物[28],因此,生物炭毒性与热解温度有关[29],在未来将生物炭应用于环境污染治理修复时,必须考虑固有毒性对生物的影响,谨慎选择热解温度以确保施用生物炭的安全性。
2.1.3 官能团构成分析

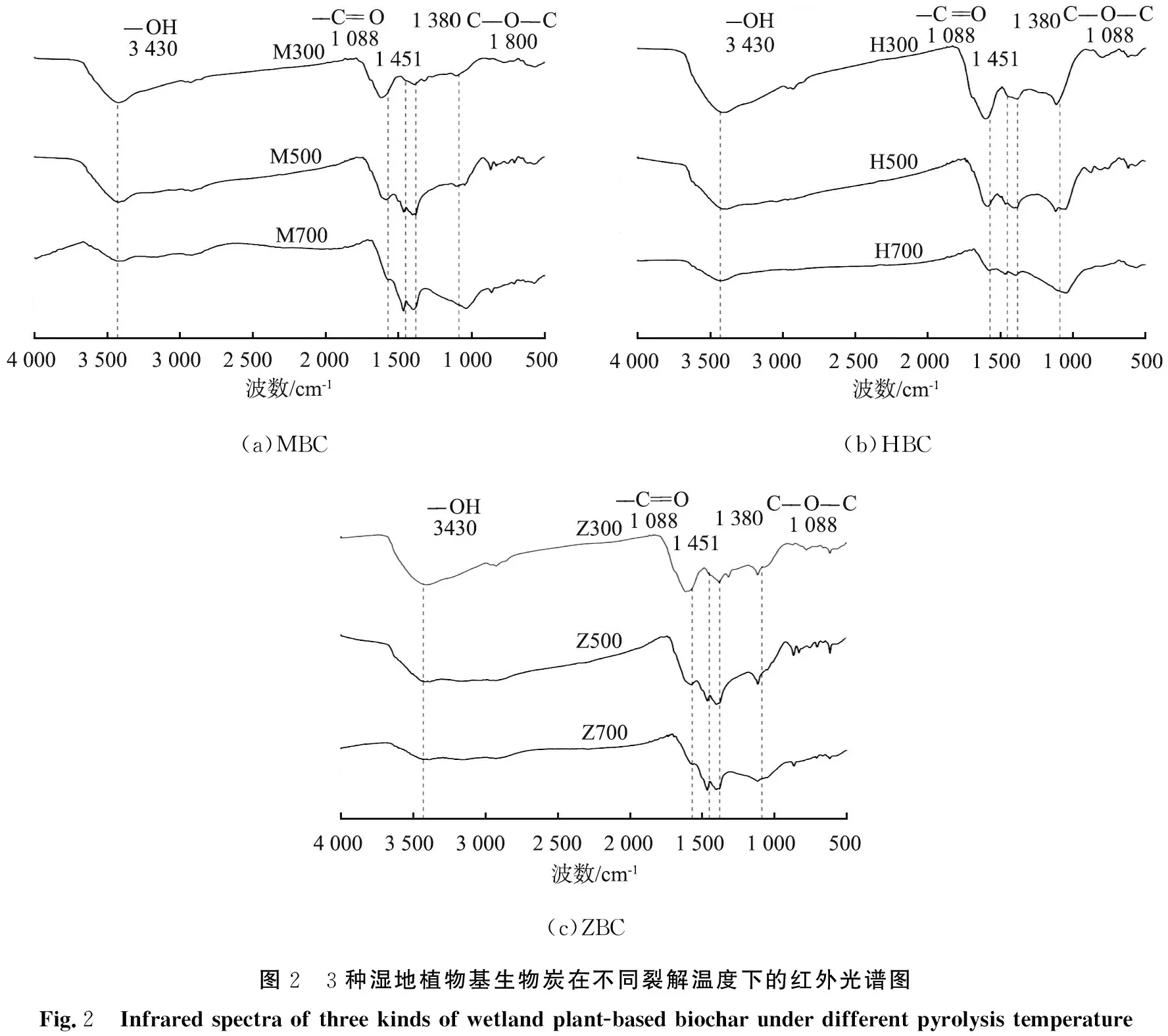
(a)MBC(b)HBC(c)ZBC图2 3种湿地植物基生物炭在不同裂解温度下的红外光谱图Fig.2 Infrared spectra of three kinds of wetland plant-based biochar under different pyrolysis temperature
2.2 湿地植物基生物炭对Cd的吸附特性
2.2.1 吸附时间的影响
图3所示为不同裂解温度下制备的湿地植物基生物炭在不同吸附时间下对Cd2+的去除情况。 在吸附前期, 随着反应时间的延长, 不同温度下制备的MBC、 ZBC和HBC对Cd2+的吸附量均有显著的增加, 而后吸附量增长幅度逐渐变得平缓, 吸附反应基本完成, 不同温度下吸附量的大小排序为: 500 ℃、 700 ℃、 300 ℃。M300、 M500和M700分别在吸附实验进行到75、 30、 30 min左右时达到吸附平衡,吸附量分别为20.69、 23.51、 21.41 mg·g-1;H300、 H500和H700分别在30、 80、 80 min左右达到吸附平衡,吸附量分别为18.15、 21.94、 20.88 mg·g-1;制备温度对ZBC的吸附反应速率无显著影响,吸附反应进行45 min左右后,Z300、 Z500和Z700对Cd2+的吸附基本完成,吸附量分别为22.72、 24.22、 23.03 mg·g-1。在吸附反应进行的伊始阶段,生物炭表面存在大量且充足的吸附位点,Cd2+能够快速地与生物炭表面的吸附位点进行结合,进而被吸附,故而反应速率较大。当吸附反应进行到一定程度时,溶液中的Cd2+已经占据了生物炭表面上绝大多数的活性位点,导致有效位点数量减少,所以吸附反应速率变缓,吸附量的变化逐渐变得平缓。整体而言,以不同湿地植物为原料制备的生物炭对Cd的吸附性能从大到小排序为ZBC、 MBC、 HBC。
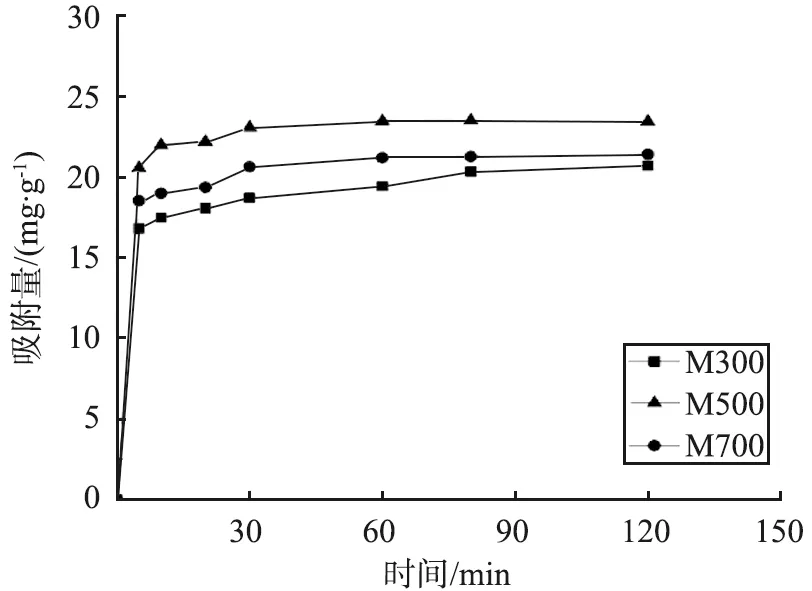
(a)MBC
2.2.2 溶液温度的影响
不同裂解温度下制备的湿地植物生物炭在不同温度下对Cd2+的去除情况见图4所示。由图可知,随着溶液温度的升高,分别在低温、中温、高温裂解制备的生物炭H300、 H500和H700对Cd的吸附量不断增加,且从大到小排序为H500、 H700、 H300。例如当溶液温度为55 ℃时,H300、 H500和H700的吸附量分别为21.47、 24.94、 22.98 mg·g-1;当温度从15 ℃升高至55 ℃时,H500的吸附量从21.12 mg·g-1增至24.94 mg·g-1, 提高了18.09%。 对于MBC和ZBC而言, 低温裂解制备的生物炭M300和Z300对Cd的吸附性能随着溶液温度的升高而增大, 但是溶液温度对中温、 高温裂解制备的生物炭M500、 M700、 Z500和Z700的吸附性能影响不大; 且当吸附温度为55 ℃时, 生物炭对Cd的吸附量由大到小排序为M700、 M300、 M500、 Z700、 Z300、 Z500, 这与生物炭原料和裂解温度有关。 以往多数研究表明, 随着反应温度的升高,溶液中重金属离子的活动程度更加剧烈, 处于激发态的离子数量增多,有利于反应的进行,但是也有研究指出吸附反应在很大程度上不会受到温度的影响, 这可能是由反应温度对吸附过程中各级控速步骤的影响方式不同所致。 一方面, 温度的升高增加了重金属离子活性, 加大了其与吸附材料的碰撞概率, 有助于重金属离子卸下表面自身携带的水膜扩散至吸附材料的孔道中; 另一方面, 温度的升高又不利于孔道中的活性基团与进入孔道的重金属离子发生吸附反应, 且温度对吸附过程的3个阶段的影响趋势不同, 有些是正影响, 有些是负影响, 因此温度对吸附反应的影响可能不会呈现出明显的规律性。
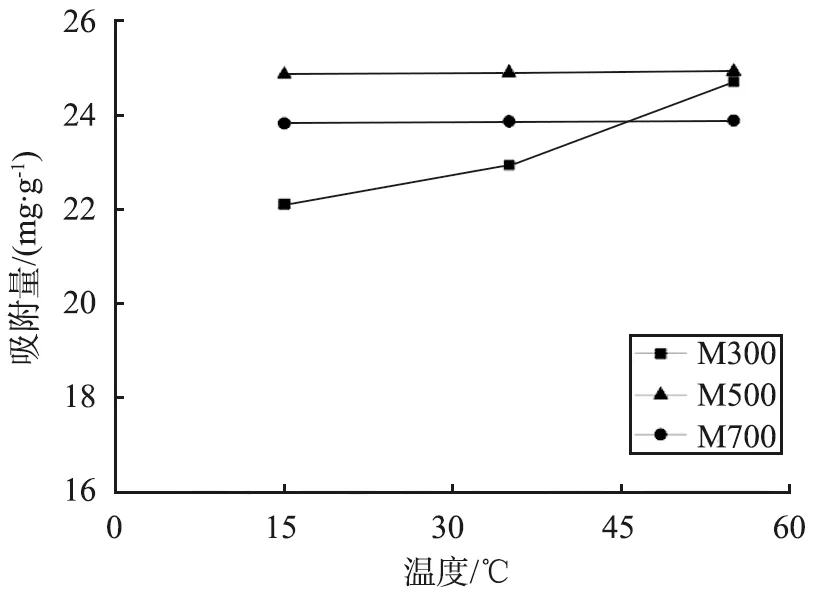
(a)MBC
2.2.3 溶液初始pH值的影响
溶液初始pH主要通过2个方面来影响生物炭对重金属离子的吸附性能: 一是改变溶液中重金属离子的赋存形态, 二是改变存在于生物炭表面的电荷数量以及官能团的去质子化(或质子化)程度。 图5所示为不同裂解温度下制备的湿地植物生物炭在不同pH下对Cd2+的去除情况。 由图可知, 裂解制备所得的生物炭对Cd的吸附量均随着pH的增大而增大, 裂解温度对生物炭吸附Cd的能力从大到小排序为700 ℃、 500 ℃、 300℃, 且pH对ZBC的影响更大。 例如, 当pH由3增至4时,M700、 H700和Z700对Cd的吸附量分别增加了35.76%、 16.15%、 50.45%;pH为7时,Cd2+开始与溶液中的OH-反应生成沉淀,所以此条件下吸附量出现显著的增加。在酸性条件下,溶液中H+数量较多,相比于Cd2+而言对吸附活性位点的竞争能力更强;除了H+之外,生物炭自身携带或者在制备过程中产生的大量2价阳离子(如Ca2+、 Mg2+和K2+)进入溶液后也会与Cd2+产生竞争关系,进而降低生物炭对Cd的吸附能力。此外,酸性溶液中静电排斥作用较强,Cd2+难以靠近生物炭表面与吸附活性位点相结合,进而抑制了吸附的进行。随着溶液碱性的增强,溶液中H+和生物炭所释放的2价阳离子数量显著减少,这会增大Cd2+结合生物炭表面活性点位而被吸附的概率;同时生物炭Zeta电位的减少(电负性增大),也能促进生物炭对Cd2+的吸附。
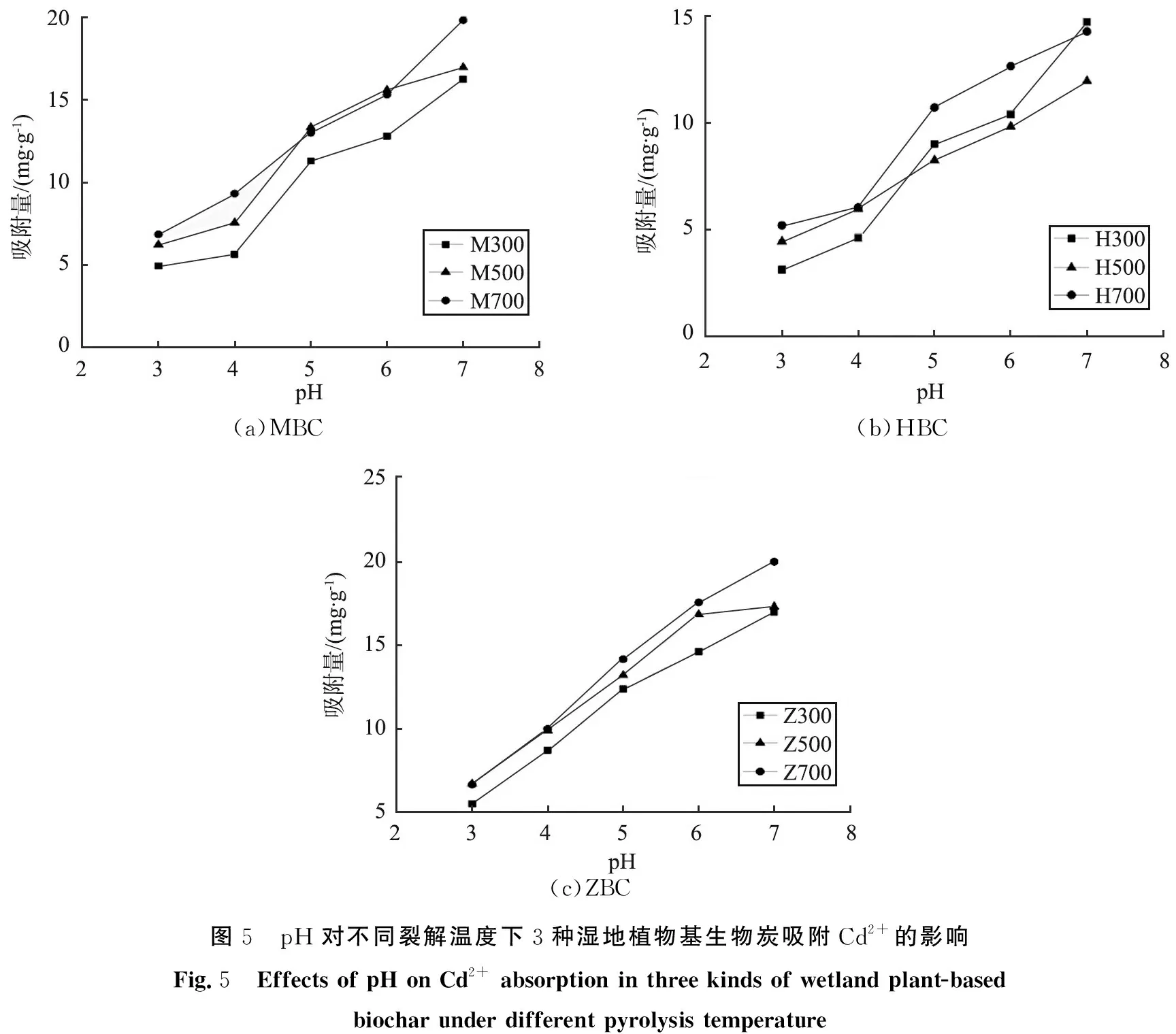
(a)MBC(b)HBC(c)ZBC图5 pH对不同裂解温度下3种湿地植物基生物炭吸附Cd2+的影响Fig.5 Effects of pH on Cd2+ absorption in three kinds of wetland plant-based biochar under different pyrolysis temperature
2.2.4 投加量的影响
图6所示为不同裂解温度下制备的湿地植物生物炭在不同投加量下对Cd2+的去除情况。 由图可知, 湿地植物基生物炭对Cd的吸附量均随着投加量的增加而不断减小, 不同裂解温度下制备的生物炭对Cd的吸附能力从大到小排序为500 ℃、 700 ℃、 300 ℃, 且MBC和ZBC对Cd的吸附效果较好, 优于HBC。 例如, 当投加量为1 g·L-1时, H300、 H500、 H700的吸附量分别为18.43、 63.08、 32.15 mg·g-1,而Z300、 Z500和Z700的吸附量分别为21.41、 99.34、 43.8 mg·g-1。 当投加量从1 g·L-1增加至8 g·L-1时, H300、 H500、 H700对Cd的吸附能力分别减小了47.96%、 88.22%、 77.01%,而Z300、 Z500、 Z700对Cd的吸附量分别减小了54.27%、 85.41%和71.53%。生物炭投加量与可提供的吸附位点数量有关。当离子初始质量浓度一定时,投入少量的生物炭,其表面具有的吸附位点可充分与溶液中的重金属离子相结合,因此吸附能力较高。投加的生物炭数量越多,吸附能力反而下降,这是因为过剩的生物炭颗粒在溶液中容易发生相互团聚现象,使得颗粒不均匀地覆盖在吸附位点表面,不利于金属离子以合适的比例与吸附位点相结合,进而吸附量有所减少。
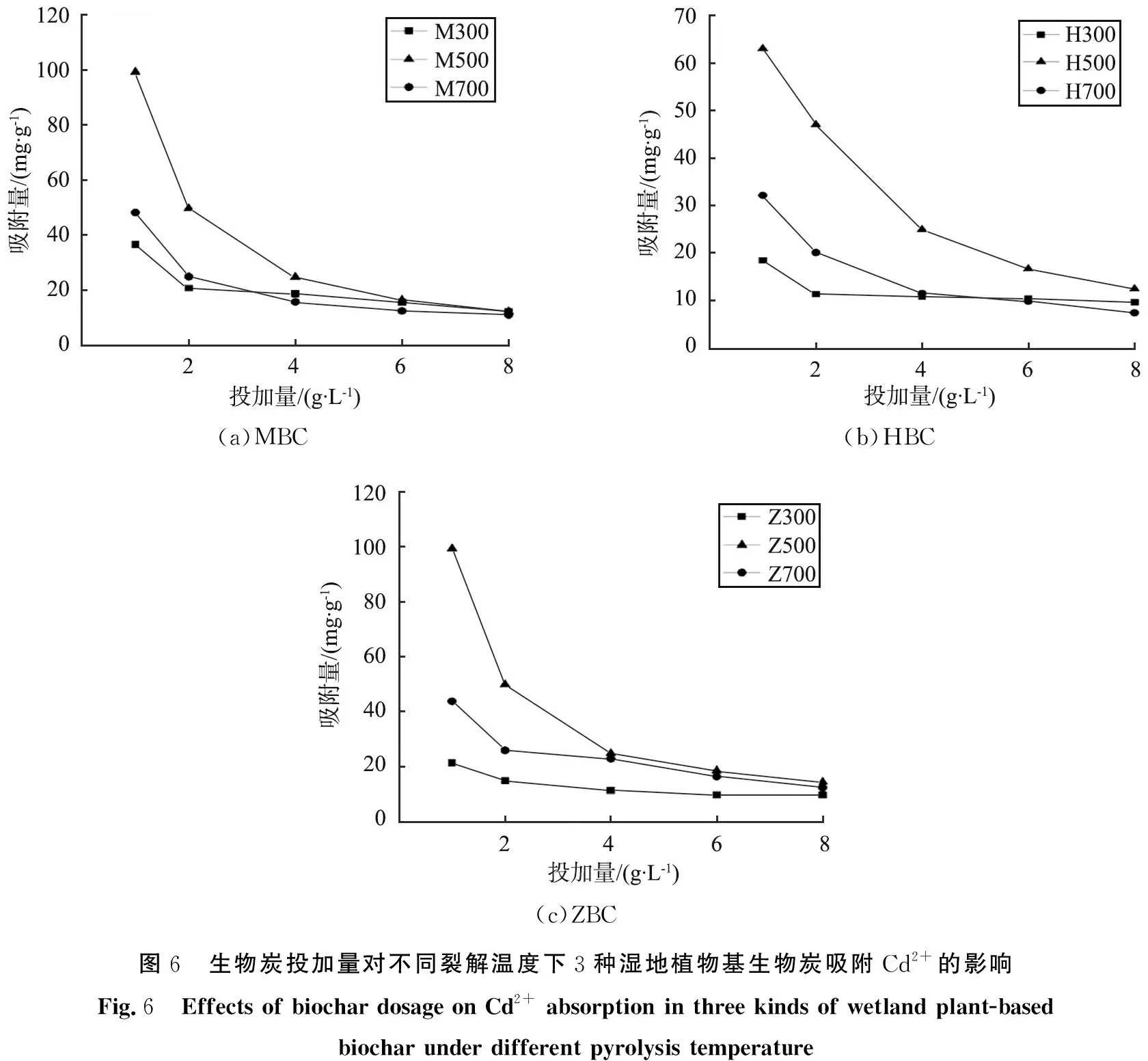
(a)MBC(b)HBC(c)ZBC图6 生物炭投加量对不同裂解温度下3种湿地植物基生物炭吸附Cd2+的影响Fig.6 Effects of biochar dosage on Cd2+ absorption in three kinds of wetland plant-based biochar under different pyrolysis temperature
2.2.5 离子初始质量浓度的影响
图7所示为不同裂解温度下制备的湿地植物生物炭在不同离子初始质量浓度下对Cd2+的去除情况。 由图可知, 随着离子初始质量浓度的增加, 湿地植物基生物炭对Cd的吸附量均呈增大趋势。 对于MBC和ZBC而言, 离子初始质量浓度一定时, 生物炭吸附Cd2+性能受裂解温度的影响较小, 但是当离子初始质量浓度超过100 mg·L-1时, 裂解温度对HBC生物炭吸附Cd2+产生一定影响, 裂解温度为500 ℃时, 吸附效果最好, 其次是700 ℃。 当吸附位点一定时, 若离子初始质量浓度较高, 过剩的重金属离子可能会在生物炭表面发生堆叠, 吸附位点被覆盖进而不利于其与金属离子相结合, 导致吸附能力下降, 但是在本研究中, 即使当离子质量浓度较高(500 mg·L-1)时, 吸附量仍在不断增大, 这或许可以用传质推动力的增加促进吸附进行来解释。
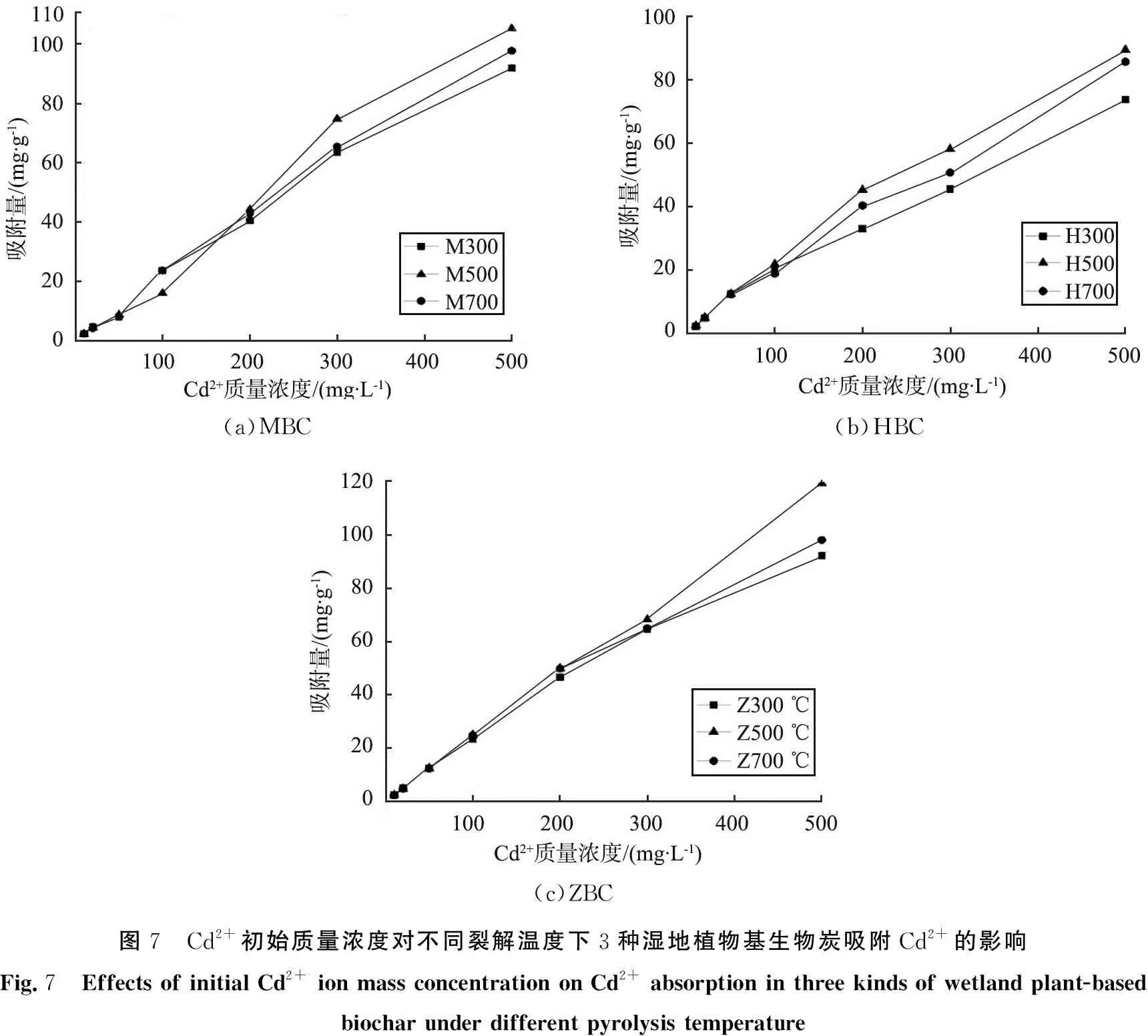
(a)MBC(b)HBC(c)ZBC图7 Cd2+初始质量浓度对不同裂解温度下3种湿地植物基生物炭吸附Cd2+的影响Fig.7 Effects of initial Cd2+ ion mass concentration on Cd2+ absorption in three kinds of wetland plant-based biochar under different pyrolysis temperature
2.3 湿地植物基生物炭对Cd的吸附机制
2.3.1 等温吸附属性
运用Langmuir和Freundlich等温吸附模型对500 ℃下制备的湿地植物基生物炭(M500、 H500、 Z500)在不同温度下(15、 35、 55 ℃,对应的热力学温度分别为288、 308、 328 K)对Cd2+的吸附量随其离子质量浓度的变化进行拟合。通过分析拟合所得的等温吸附参数见表3所示。
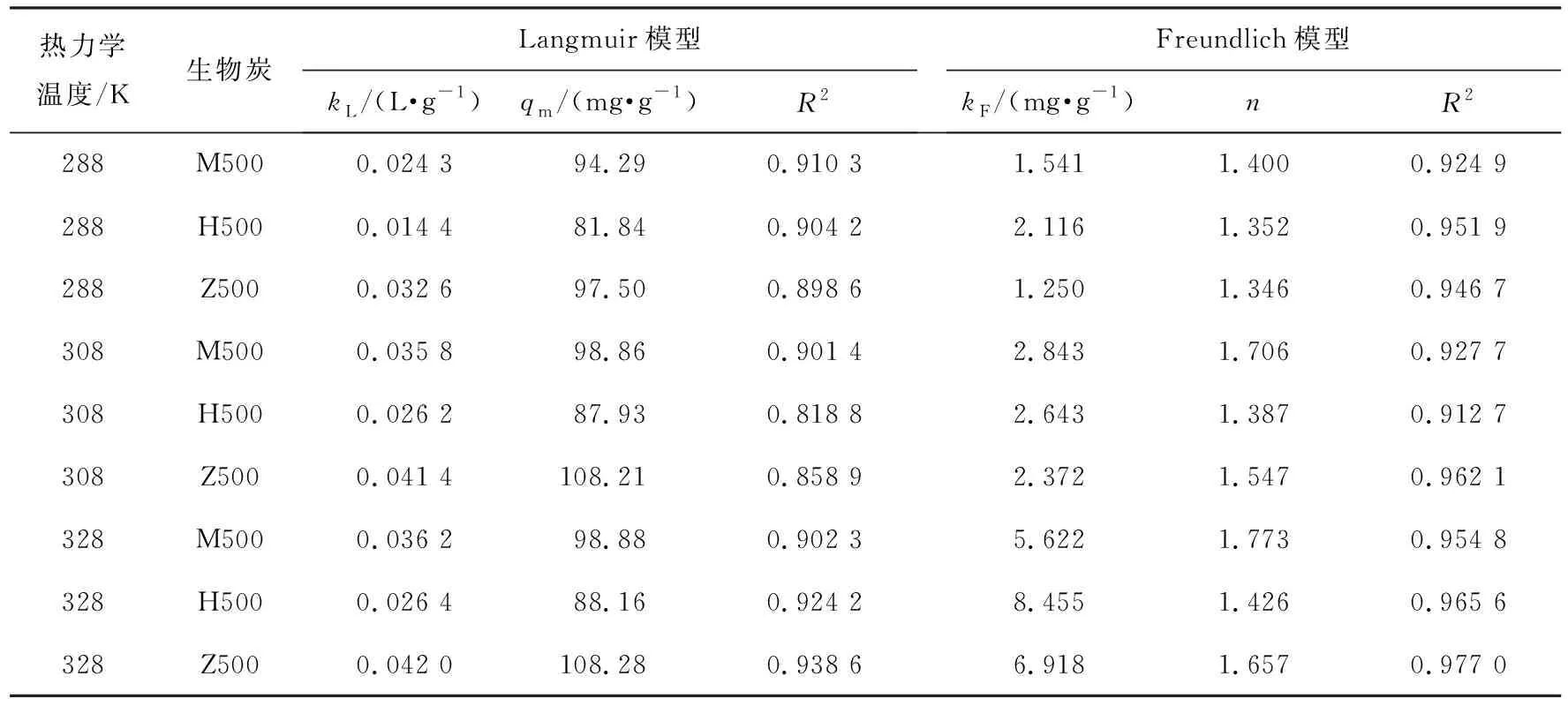
表3 湿地植物基生物炭对Cd2+的等温吸附参数
由表可知, 不同离子初始质量浓度下, 湿地植物基生物炭对Cd2+的吸附过程可以用Freundlich等温吸附模型更好地拟合, 且为多分子层吸附。 在热力学温度为308 K时, 根据Langmuir等温吸附方程拟合计算得到的M500、 H500、 Z500对Cd2+的最大吸附量从大到小排序为Z500、 M700、 H300, 说明在质量浓度较高的Cd2+溶液中, Z500对Cd2+的吸附能力高于M500和H500。 通常可以根据Langmuir模型常数kL来判定生物炭对金属离子的吸附作用力强弱。 9种湿地植物基生物炭中Z500拥有最大的kL值, 由此可见Z500对Cd的吸附作用更强、 吸附过程更稳定。 9种湿地植物基生物炭的Freundlich模型常数n>1, 表明制备所得的湿地植物基生物炭对Cd的吸附过程较为容易进行, 属于优惠吸附。 湿地植物基生物炭对Cd2+的吸附量均随着温度升高而增加, 说明升温能够提高湿地植物基生物炭对Cd2+的去除率。
2.3.2 吸附动力学属性
将实验数据代入拟一级动力学方程和拟二级动力学方程中进行拟合,所得参数结果列于表4。由表可知,拟一级动力学方程拟合R2值范围为0.727 7~0.983 8,而拟二级动力学方程拟合R2值范围为0.999 1~0.999 9,说明拟二级动力学模型能更好地描述湿地植物基生物炭对Cd的吸附过程,吸附是以化学吸附为主,物理吸附为辅。吸附过程中存在多步骤反应,其中反应速率最慢的步骤称之为速率控制步骤,一般可以分为3个过程:首先溶液中的Cd2+自由扩散至湿地植物基生物炭表面,然后继续穿过表面进入到湿地植物基生物炭的孔隙中,最后在湿地植物基生物炭孔隙内表面发生吸附反应。
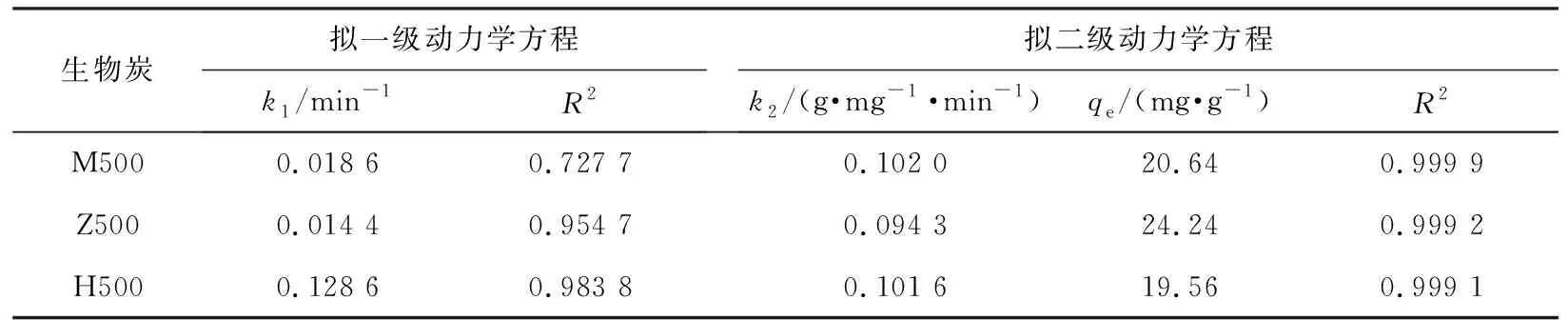
表4 湿地植物基生物炭吸附Cd2+的吸附动力学
3 结论
1)生物炭理化性质与裂解温度有关。 随着制备时裂解温度的升高, 产率、 挥发分、 C和N、 C和H、 (O+H)和C的相对原子质量比值均呈现下降趋势, 而灰分含量、生物炭的BET表面积、孔容积和孔径有所增加。
2)生物炭吸附性能与吸附条件有关。随着吸附时间的延长,生物炭对Cd2+的吸附量呈先增大后趋于平缓趋势;随着溶液pH、离子初始质量浓度和反应温度的增大,生物炭对Cd2+的吸附量呈增大趋势;随着投加量的增加,生物炭对Cd2+的吸附量呈减小趋势。
3)不同温度制备的湿地植物基生物炭对Cd的吸附能力有明显差异,中温(500 ℃)、 高温(700 ℃)裂解形成的生物炭对Cd的吸附效果优于低温(300 ℃)裂解生物炭。总体而言,500 ℃下制备的生物炭的吸附能力更强,从大到小排序为ZBC、 MBC、 HBC,因而选择500 ℃裂解制备的生物炭作为后续土壤培育试验中的湿地植物基生物炭材料。
4)选取500 ℃下制备的湿地植物基生物炭对Cd2+吸附数据进行等温吸附和动力学模型拟合,结果表明,M500、 Z500和H500对Cd2+的吸附过程更加符合Freundlich等温吸附模型和拟二级动力学模型,且属于优惠吸附。
