高效液相色谱法测定聚丙交酯乙交酯支架涂层的体外降解产物的含量
2022-09-22杜福映张花美吴长岩刘莉莉赵长帅施燕平
杜福映,张花美,吴长岩,陈 方,刘莉莉,赵长帅,彭 健,沈 永,施燕平
(1.山东省医疗器械和药品包装检验研究院,济南 250101;2.国家药品监督管理局生物材料器械安全性评价重点实验室,济南 250101;3.山东省医疗器械生物学评价重点实验室,济南 250101)
药物洗脱支架在心血管领域已广泛应用,将可降解材料应用于药物涂层,在缓释药物的同时,改善了支架的生物相容性,降低了晚期支架内血栓的风险[1-3],成为目前的研究热点之一。
在药物洗脱支架的研究中,药物释放已受到广泛关注[4-10]。药物释放机理研究表明,可降解涂层中药物的释放主要是通过扩散机理及聚合物降解溶蚀实现[8,11]。另有研究表明,可降解材料涂层可提高合金的耐腐蚀性[12-13]。此外,支架球囊扩张过程中,涂层如有剥落,则会进入血液,造成血管堵塞,危害极大[14]。聚合物的降解不仅影响药物释放行为,还对支架平台的腐蚀及使用安全产生一定作用。因此,对涂层多聚物的降解情况进行考察具有重要意义。
目前国内外研究多以质量损失、相对分子质量及其分布、力学性能及热力学性能为研究指标来评价材料降解[15-17]。然而作为涂层覆于支架表面的聚合物量较低[本工作所用支架涂层聚丙交酯乙交酯(PLGA)量仅为0.16 mg/支架],且支架涂层降解引起质量、相对分子质量及热力学性能的变化,其准确数值难以获取。因此,建立灵敏度高、重复性好、操作简便的测定方法已迫在眉睫。本工作旨在对一种新型可吸收锌合金药物洗脱冠脉支架系统(以下皆简称支架)中聚合物涂层的体外降解性能进行考察,采用高效液相色谱法(HPLC)测定降解液中乙醇酸、L-乳酸的含量,并对降解过程中支架的表观形貌进行观察,进而评估药物涂层的降解情况,为支架设计、使用提供技术参考。
1 试验部分
1.1 仪器与试剂
Agilent1260型高效液相色谱仪;Mettler Toledo XPR2型微量电子天平;SHA-C型往返水浴振荡器;Millipore-Q 型超纯水系统;ZEISSSIGMA 300型热场发射扫描电子显微镜(SEM);BRUKER XFlas 6/60型能谱仪;Bright KAS-2000F型铂金靶型离子溅射仪。
乙醇酸和L-乳酸标准储备溶液:1 g·L-1,分别称取乙醇酸和L-乳酸对照品约10 mg,用水溶解并定容至10 mL,于4 ℃保存。
混合标准溶液系列:取适量的乙醇酸和L-乳酸标准储备溶液,用水逐级稀释,配制成乙醇酸质量浓度分别为1.99,9.93,19.86,39.72,59.58 mg·L-1,L-乳酸质量浓度分别为2.92,14.60,29.20,58.39,87.59 mg·L-1的混合标准溶液系列,分别用磷酸调节pH 至2.8±0.2。
乙醇酸对照品的纯度不小于99.0%;L-乳酸对照品的纯度为90.5%;磷酸为优级纯;试验用水为去离子水。
支架来自某公司,PLGA 的标示值为0.16 mg/支架。
1.2 仪器工作条件
XBridge Shield RP18 色谱柱(250 mm ×4.6 mm,3.5μm);柱温40 ℃;检测波长214 nm;进样量20 μL;流 量0.2 mL·min-1;流动相 为20 mmol·L-1磷酸二氢钾溶液(磷酸调节pH 至2.8);等度洗脱。
1.3 试验方法
取支架5个,将每个支架用尼龙绳穿过并悬吊于50 mL离心管中,用已预热至37 ℃的10 mL 磷酸盐缓冲液(PBS,pH 7.4)将所有支架浸没。将离心管置于37℃往返恒温水浴振荡器中振荡,转速为60 r·min-1。分别在0,7,14,21,28 d时将支架取出,超纯水冲洗后,吸干表面水分后置于放有10 mL PBS(pH 7.4)的离心管中,重新放回37 ℃水浴振荡器中,直至试验结束。取每个时间点降解液,用磷酸调节pH 至2.8±0.2,经0.20μm 滤膜过滤后进行HPLC测定。
取各降解阶段的支架样品,用导电胶黏贴固定至SEM 样品台上,经离子溅射仪喷金(铂金)后进行形貌观察。
2 结果与讨论
2.1 支架涂层的表征
体外降解试验开始前,对支架涂层进行表征。按照临床使用方法,将球囊扩张后,取支架进行测定、分析。结果显示:支架涂层的可降解材料为乙醇酸、L-乳酸的开环共聚物,乙醇酸和L-乳酸的质量比为30∶70;重均分子量为1.5×105,数均分子量为0.9×105,分布系数为1.7(以聚苯乙烯标准品为对照);PLGA 的玻璃化转变温度为48.2 ℃。SEM图像显示支架涂层完整,未有脱落现象的发生。
2.2 色谱行为
按仪器工作条件对乙醇酸、L-乳酸混合标准溶液进行测定,其色谱图见图1。
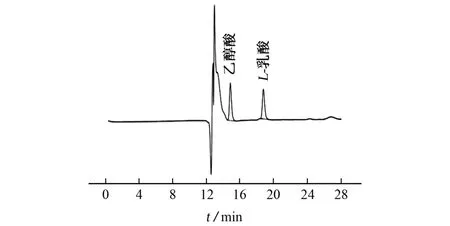
图1 混合标准溶液的色谱图Fig.1 Chromatogram of the mixed standard solution
结果表明:乙醇酸和L-乳酸的保留时间分别为14.8,18.8 min,各色谱峰无拖尾、峰形对称完整,达到较好分离,专属性较好;乙醇酸、L-乳酸的测定也不受其他水溶性降解产物干扰。在体外降解过程中,PLGA 逐渐水解为相对分子质量更小的多聚物和寡聚物,乙醇酸、L-乳酸为其终产物,而相对分子质量较大的产物不能溶解于降解液中,进样前被滤去。
2.3 标准曲线、检出限和测定下限
按照仪器工作条件对混合标准溶液系列进行测定,以乙醇酸和L-乳酸的质量浓度为横坐标,对应的峰面积为纵坐标绘制标准曲线。结果表明:乙醇酸和L-乳酸的质量浓度在一定范围内与对应的峰面积呈线性关系,线性回归方程和相关系数见表1。
根据3倍信噪比(S/N)计算方法的检出限(3S/N),根据10 倍信噪比计算方法的测定下限(10S/N),结果见表1。
由表1 可知:乙醇酸的检出限为0.50 mg·L-1,测定下限为2.00 mg·L-1;L-乳酸的检出限为0.70 mg·L-1,测定下限为3.00 mg·L-1。

表1 线性参数、检出限和测定下限Tab.1 Linearity parameters,detection limits and lower limits of determination
2.4 精密度试验
取空白降解样品溶液(样品基质为PBS)若干份,分别加入低、中、高等3 个浓度水平的乙醇酸、L-乳酸混合标准溶液,按照试验方法进行处理,平行测定6 次,记录峰面积,计算其相对标准偏差(RSD),结果见表2。
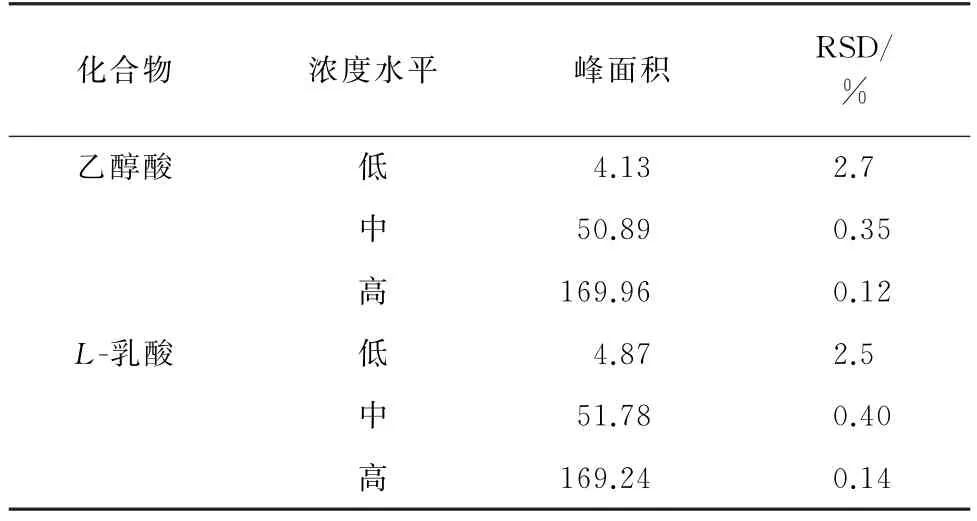
表2 精密度试验结果(n=6)Tab.2 Results of test for precision(n=6)
由表2可知,乙醇酸的RSD 为0.12%~2.7%,L-乳酸的RSD 为0.14%~2.5%,说明方法具有较高的精密度,满足分析要求。
2.5 回收试验
取空白降解样品溶液(样品基质为PBS)若干份,分别加入低、中、高等3 个浓度水平的乙醇酸、L-乳酸混合标准溶液,按照试验方法进行处理、测定,计算加标回收率,结果见表3。
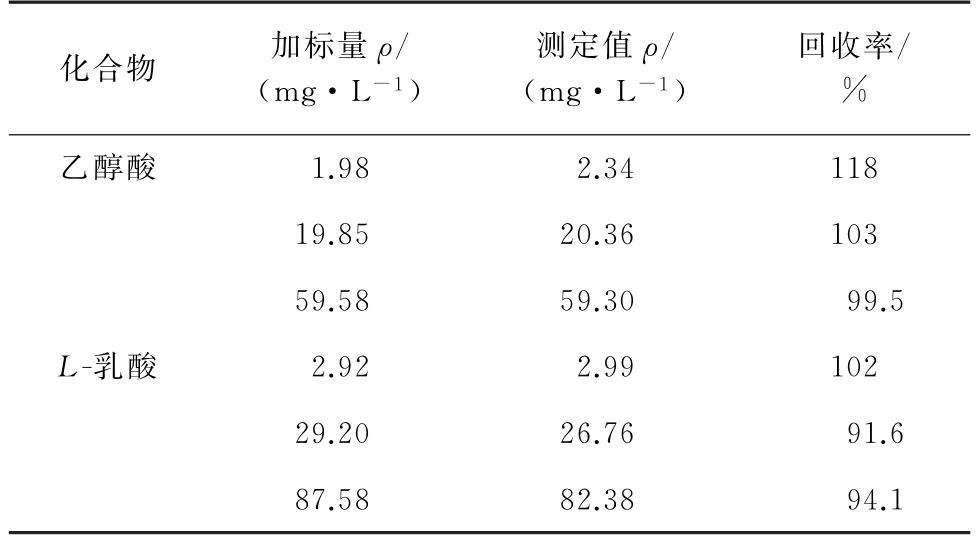
表3 回收试验结果Tab.3 Results of test for recovery
由表3可知:乙醇酸的加标回收率为99.5%~118%,L-乳酸的加标回收率为91.6%~102%,说明方法具有较高的准确度,满足分析要求。
2.6 样品分析
2.6.1 降解液中乙醇酸、L-乳酸的测定
按仪器工作条件对降解液中乙醇酸、L-乳酸进行测定,并计算各时间点的累积量,结果见表4。

表4 降解产物的累积量Tab.4 Cumulative amounts of the degradation products mg
由表4可知:在降解的前7 d,降解液中乙醇酸、L-乳酸的含量低于方法的检出限;随后在降解液中检出乙醇酸、L-乳酸,且累积释放量逐渐增加,28 d内的总量为0.902 5 mg,降解回收率约为113%,说明支架中的聚合物涂层基本完全降解。
2.6.2 支架表观形貌的变化
采用SEM 对降解后经干燥的支架进行观察,如图2所示,分别为支架降解0,7,14,21,28 d的SEM 图。如图2(a)所示,本工作所用支架涂层表面完整,光滑且无明显缺陷。随着降解进行,聚合物水解为小分子并释放到降解液中,光滑的涂层表面逐渐出现微小孔隙[图2(b)],孔隙随后变大[图2(c)]并连成较大的洞[图2(d)],直至完全溶蚀至降解液中[图2(e)]。将28 d样品放大约1万倍,如图2(f)所示,聚合物涂层降解后,金属表面形成一层薄膜,能谱分析结果显示,除含有锌元素(质量分数63.6%)外,还含有碳、氧、钠等元素,可能是锌和钠的碳氧化物薄膜,该膜能够继续保护锌支架,防止支架过快腐蚀。

图2 降解中的支架SEM 图Fig.2 SEM images of the degrading stents
本工作采用HPLC 测定新型药物洗脱支架涂层聚合物的降解产物乙醇酸、L-乳酸的含量,该测定方法操作简单、灵敏度高、精密度与回收率均满足测定要求;同时通过SEM 直观、形象地观察到支架降解过程中的形貌变化,达到测定、分析新型药物洗脱支架涂层聚合物的降解产物乙醇酸、L-乳酸的目的,为支架设计、使用提供了技术参考。
