新型叔胺类光敏剂的合成及性能研究
2022-07-14唐永强李米绮陈万彦
唐永强 李米绮 许 杏 杨 森 陈万彦
(合肥师范学院,安徽合肥,230601)
光聚合也就是光固化,其固化时间比传统热固化要短,早在上世纪80年代,该项技术就已经被认可为一项绿色环保技术,其具有高效节能、经济环保以及固化产物性能较优异等优点[1]。光固化配方[2]包括光引发剂、齐聚物[3]、单体及助剂等多个组分。光引发剂,可从基态跃迁至激发态,发生化学改变并引发聚合反应的反应中间产物,它在体系中有着非常重要的作用,光固化速率就取决于它。目前研究的光引发剂主要有四类,其中自由基型和阳离子型较为常见[4]。依据不同类型,自由基光引发剂可分为裂解型和夺氢型[5]。二苯甲酮和蒽醌是常见的用于光固化体系中的引发剂,其衍生物的制备[6-8]也在光聚合中有着广泛的应用。从节能减排的角度考虑,合成新型的、更安全的环境下引发聚合的光引发体系很有必要[9,10]。本研究尝试将叔胺结构引入二苯甲酮及蒽醌类衍生物的结构中,研究其在复合树脂中的光引发性能。
1 试验部分
1.1 主要原料
2-氨基蒽醌(分析纯,上海阿拉丁生化科技有限公司);4-氨基二苯甲酮(分析纯,上海阿拉丁生化科技有限公司);丙烯酸丁酯(分析纯,上海麦克林生化科技有限公司);乙酸(分析纯,江苏强盛功能化学股份有限公司);乙酸锌(分析纯,天津博迪化工股份有限公司);双酚A(分析纯,上海阿拉丁生化科技有限公司)。
1.2 仪器测试
FTIR采用美国Nicolet 380型傅立叶红外光谱仪测定;1H NMR采用氘代氯仿为溶剂,采用Bruker AV-400型核磁共振仪器进行测定;紫外光谱采用UV-2550型号的UV-可见分光光度计进行测试;光固化实验采用圆柱形塑料模具(2mm×φ5mm);UV-LED紫外灯(型号UVSP81,光源波长为:260~280nm,360~380nm)。
1.3 叔胺类光敏剂的合成
1.3.1 2-N,N-(二丙烯酰氧基丁基)氨基蒽醌(BPDAQ)的合成
称取5.90g 2-氨基蒽醌与10.8mL丙烯酸丁酯,加入100mL的三口烧瓶中,加入0.17g双酚A阻聚剂和0.82g醋酸锌作催化剂,并加入5.8mL醋酸作为溶剂,控制反应温度为100℃,且不高于醋酸的回流温度,磁力搅拌子匀速搅拌,反应5h。反应完成,将反应液置于分液漏斗中,用1mol/L的NaOH溶液对滤液进行碱洗,除去醋酸,分出有机相。粗产品用三氯甲烷∶石油醚=3∶1作为展开剂过层析柱,得到产物BPDAQ。BPDAQ的合成路线见图1。
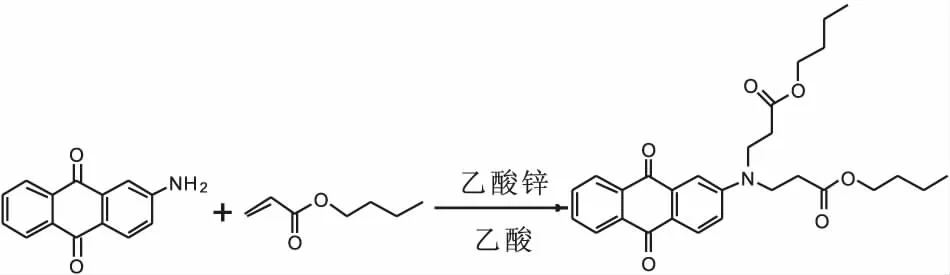
图1 BPDAQ的合成路线
1.3.2 4-N,N-(二丙烯酰氧基丁基)氨基二苯甲酮(BPDBP)的合成
称取1.97g 4-氨基二苯甲酮与4.3mL丙烯酸丁酯,加入100mL的三口烧瓶中,加入0.05g双酚A阻聚剂和0.33g醋酸锌作催化剂,并加入2.5mL醋酸作为溶剂,控制反应温度为100℃,且不高于醋酸的回流温度,磁力搅拌子匀速搅拌,反应5h。反应完成,将反应液置于分液漏斗中,用1mol/L的NaOH溶液对滤液进行碱洗,除去醋酸,分出有机相。粗产品用三氯甲烷∶石油醚=2∶1作为展开剂过层析柱,得到产物BPDBP。BPDBP的合成路线见图2。
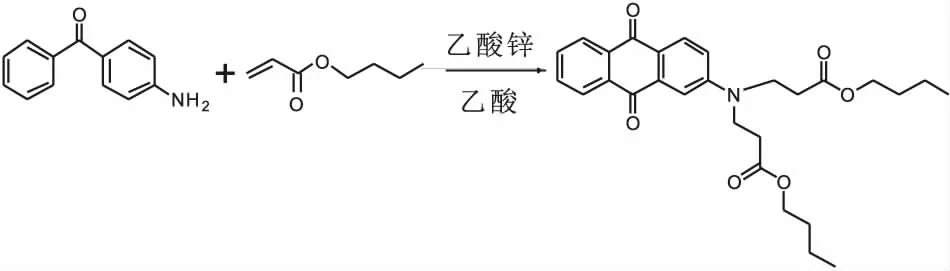
图2 BPDBP的合成路线
2 结果与讨论
2.1 光敏剂的结构表征
图3给出的是BPDAQ的核磁氢谱图。其中δ(ppm):7.26为溶剂CDCl3中H的化学位移。δ(ppm):8.26、8.12、7.73、7.36和7.09为蒽醌环上H的化学位移;δ(ppm):3.62为与氮原子相连-CH2中H的化学位移;δ(ppm):2.68为碳链上C=O相连的-CH2中H的化学位移;δ(ppm):4.12为碳链中与中-O-C所相连的-CH2中H的化学位移;δ(ppm):0.98处为两个末端的甲基的质子的化学位移值。图4表示的是BPDBP的1HNMR谱图。δ(ppm):7.71和δ(ppm):7.44、δ(ppm):6.60处为苯环上未被取代的H原子的化学位移,溶剂中CDCL3中的质子的特征峰在δ(ppm):7.30处,与氮原子相连的-CH2的质子化学位移在δ(ppm):3.49处,δ(ppm):2.62为叔胺的对称结构中的-CH2的H原子的化学位移,δ(ppm):4.17和δ(ppm): 1.65处为-CH2的氢原子的化学位移,δ(ppm):0.95处为两个末端的甲基的质子的化学位移值。
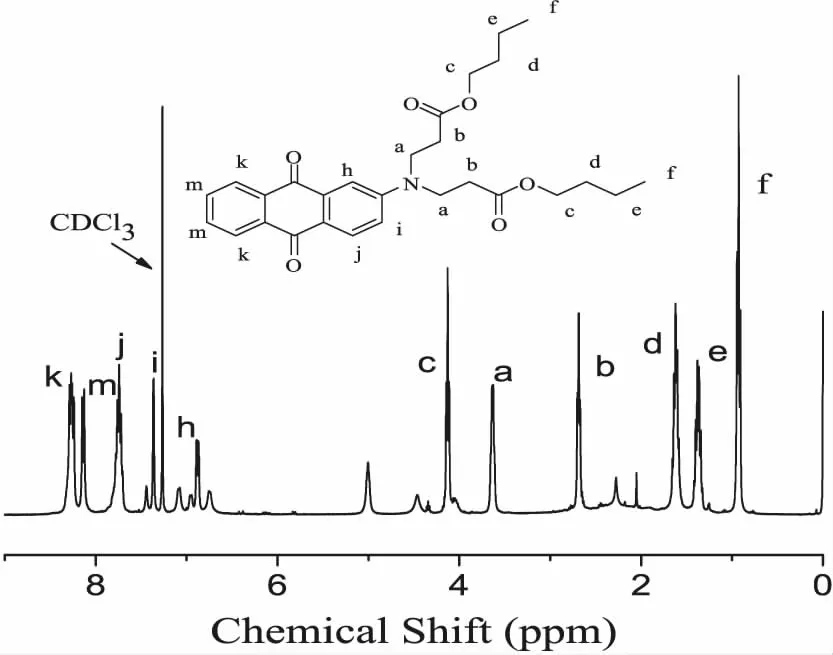
图3 BPDAQ的核磁氢谱
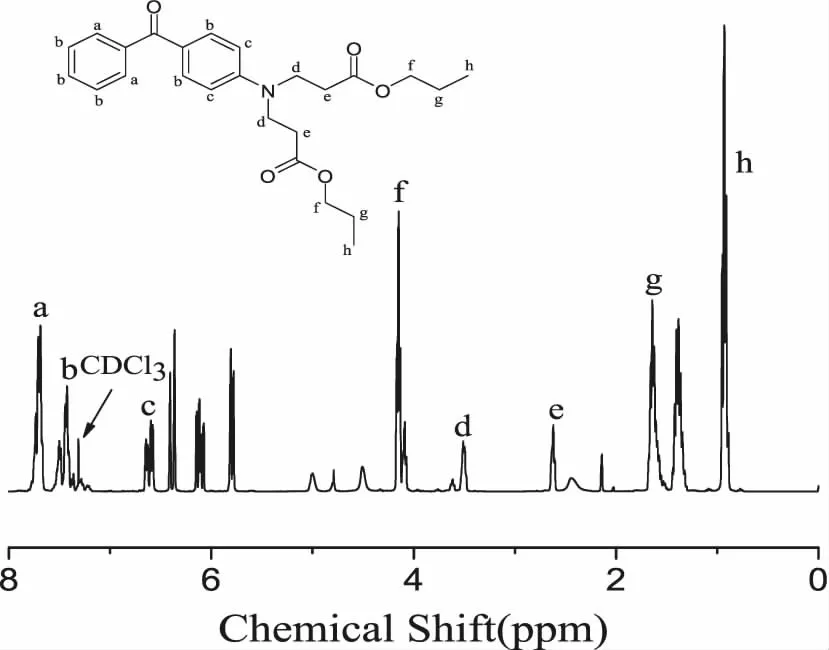
图4 BPDBP的核磁氢谱
图5给出的是2-氨基蒽醌与BPDAQ的红外谱图。对比原料及产物的红外谱图,原本在3349cm-1处的伯胺基团中的N-H伸缩振动峰消失,在3434cm-1出现了叔胺的特征吸收峰,证明有叔胺的存在。在1193 cm-1出现的新强峰是C-O-C的不对称伸缩振动。1727cm-1处出现的新强峰,是酯羰基C=O的伸缩振动。图6表示的是4-氨基二苯甲酮和BPDBP的红外光谱图。通过对比原料及产物的红外谱图,原本结构中的3500cm-1处伯胺基团中的N-H单键伸缩振动峰消失,同时在3300cm-1处发现了新的叔胺特征吸收峰,即叔胺基团中氨基对称伸缩振动特征吸收峰。同时比较BPDBP的红外谱图,可以看到在1750cm-1处出现新的特征峰,这是酯羰基C=O的伸缩振动。
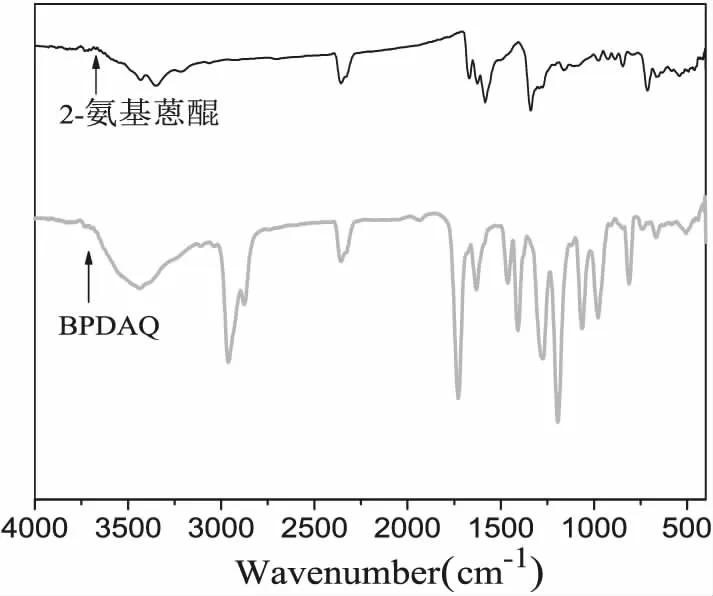
图5 BPDAQ的红外光谱
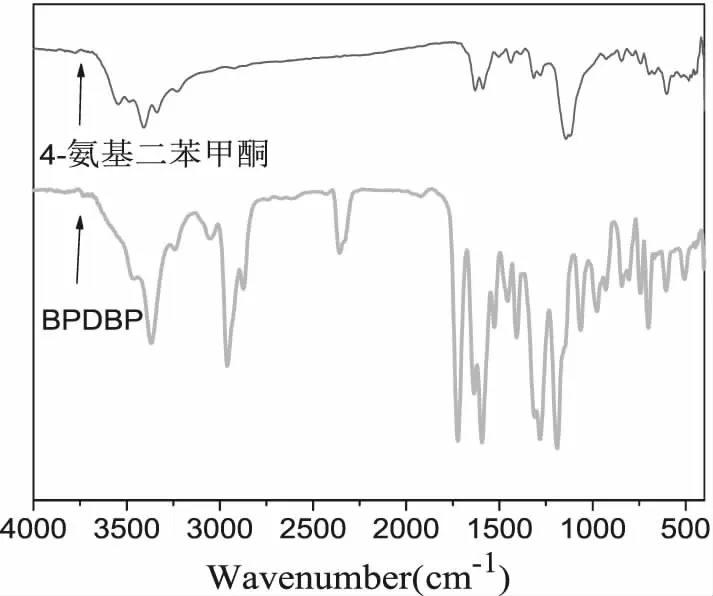
图6 BPDBP的红外光谱
2.2 光敏剂的光引发性能研究
图7给出的是2-氨基蒽醌与BPDAQ的紫外吸收光谱。在200nm—400nm范围内,BPDAQ的最大吸收波长为317nm,2-氨基蒽醌的最大吸收波长297nm。属于紫外光区的波长范围,这说明BPDAQ在紫外区有良好的吸收作用。反应前后的原料和产物的最大吸收波长出现轻微的红移。图8给出的是4-氨基二苯甲酮与BPDBP的紫外吸收光谱。在200nm—400nm范围内,BPDBP的最大吸收波长为341nm,2-氨基蒽醌的最大吸收波长335nm。属于紫外光区的波长范围,最大吸收波长同样出现红移的现象。主要因为氨基是常见的助色团,发生反应后与生色团相连,饱和杂原子上的n电子对邻近的生色团的π轨道的能级和状态产生了影响,导致吸收带朝着长波的方向移动。
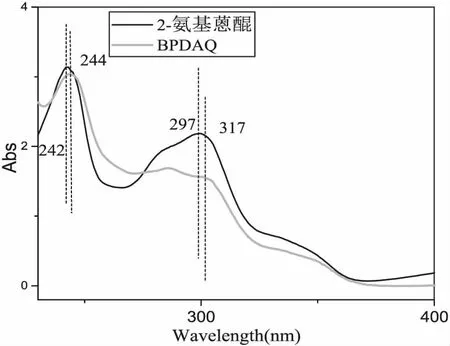
图7 BPDAQ的UV吸收光谱
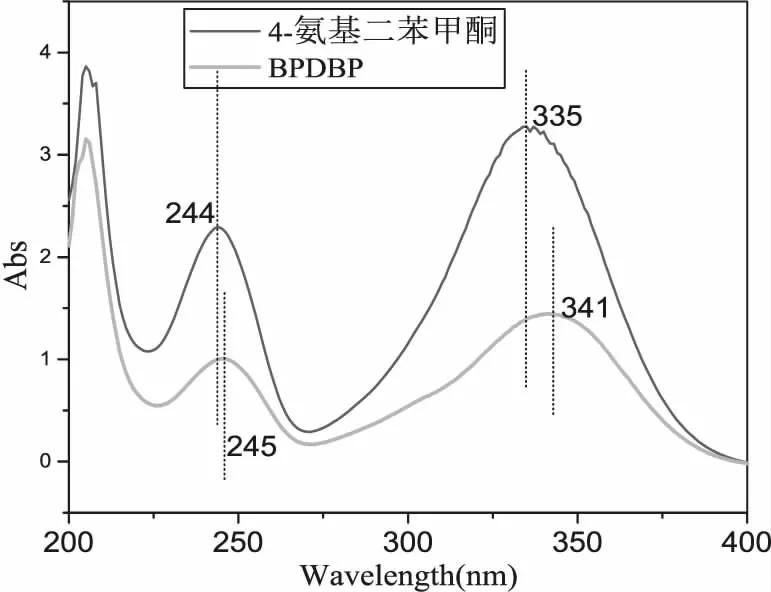
图8 BPDBP的UV吸收光谱
图9是两类叔胺光敏剂加入树脂单体后的表面固化时间随含量变化的关系图。将圆柱形模具(2mm×φ5mm)放在载玻片上,分别将含有1%、1.5%、2%、2.5%、3%、3.5%质量分数的BPDAQ与BPDBP光敏剂与预制的TEGDMA单体充分混匀注满模具,并稍高出模具,排除气泡,在模具顶端放置另一个盖玻片并压平,清理多余样品。用UV-LED紫外灯对准样品照射,并用探针轻压样品表面,直到样品表面不再出现明显压痕后停止,记录表面固化时间。树脂的表面固化时间一开始下降趋势较快,随后下降趋势变缓,随着光敏剂含量的增加,复合树脂固化速率变快,表面固化所需时间减少,当光敏剂含量大于3%后,表面固化时间基本不再发生变化。分别加入质量分数3%的BPDAQ和BPDBP的树脂样品表面固化时间为85秒和75秒,体现出了较好的光固化性能。
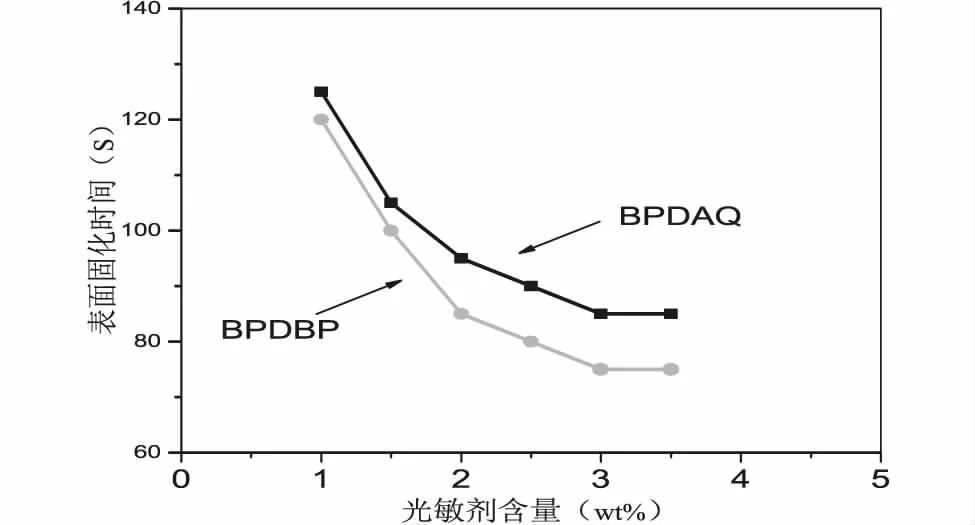
图9 加入不同含量光敏剂的复合树脂表面固化时间
3 结论
本文通过含有氨基官能团的二苯甲酮及蒽醌衍生物制备得到了含有叔胺结构的新型紫外光固化引发剂,产物通过紫外光谱的表征,BPDAQ及BPDBP的紫外最大吸收波长分别为317nm和341nm。不同含量的光敏剂加入树脂单体后能够有效引发紫外光聚合,含量达到3%wt时表现出良好的紫外光引发效率。加入BPDAQ和BPDBP两类叔胺光敏剂的树脂表面固化时间分别达到85s和75s。
