个体化医学营养疗法对妊娠期糖尿病患者血糖管理及产后糖脂代谢的影响
2022-06-21邓建军宋春容
唐 秦,魏 敏,邓建军,赵 林,宋春容,陈 鸿
(四川绵阳四〇四医院 1.产科;2.检验科;3.内分泌科;四川 绵阳 621000)
妊娠期糖尿病(gestational diabetes mellitus,GDM)是常见的妊娠并发症,其特征为妊娠期间胰岛素抵抗和胰腺β细胞功能障碍引起的短暂性糖耐量异常[1]。GDM患者的糖脂代谢相关指标大多于产后1~3个月可恢复至正常水平范围,但有三分之一的GDM女性会于产后存在持续的糖代谢紊乱状态,甚至可进展为2型糖尿病[2]。此外,GDM中糖代谢紊乱可进一步引起脂代谢紊乱,并增加不良妊娠结局的发生风险[3]。因此,采用积极有效的干预方式进行血糖管理和控制热量摄入是当前GDM患者转归的重要途径。医学营养疗法是临床GDM患者治疗和管理的重要疗法,其通过在医疗干预过程中积极地针对膳食指南提出或推荐的某些食物进行合理适当的替换,以完善科学计划,针对性地实施个性化饮食疗法,从而间接地改善GDM患者的血糖水平,以达到妊娠期血糖管理和改善产后糖脂代谢的预期目标[4]。本研究拟探讨个体化医学营养疗法对GDM患者血糖管理及产后糖脂代谢的影响,以期为GDM的临床干预提供科学依据。
1 资料与方法
1.1 一般资料
选择2019年1月1日至2021年1月1日在四川绵阳四〇四医院常规产检且收治入院分娩的500例GDM患者为研究对象。纳入标准:①年龄>18岁;②分娩结局为单胎活产;③于孕24~28周行75g口服葡萄糖耐量试验并诊断为GDM[5];④定期产检,定期随访;⑤知情同意参与本研究。排除标准:①诊断为糖尿病合并妊娠;②口服影响糖脂代谢药物;③合并其他的内外科疾病;④既往患有多囊卵巢综合征、妊娠期高血压综合征等疾病;⑤既往有习惯性流产、多次稽留流产、死胎等不良孕产史;⑥研究期间出现内外科疾病、依从性差、失联、转诊、中途退出研究者。
采用随机数字法将患者分为观察组和对照组,每组250 例。观察组平均年龄为(31.72±4.93)岁,平均确诊孕周为(25.73±2.57)周,初产妇123例,经产妇127例,平均体质量指数(body mass index,BMI)为(25.28±3.15)kg/m2;对照组平均年龄为(32.11±5.02)岁,平均确诊孕周为(25.68±2.91)周,初产妇126例,经产妇124例,平均BMI为(25.19±3.42)kg/m2。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究已经本院伦理委员会批准。
1.2 研究方法
对照组采用常规干预,帮助患者了解GDM的相关知识,指导其合理进行餐次安排、饮食搭配和自主控糖,并开展积极的运动干预。对于血糖控制始终不满意的患者及时予以药物治疗。
观察组采用个体化医学营养疗法:①制定个体化的食谱帮助患者进行科学合理的膳食摄入及三大营养配比,控制每日的热量摄入,尤其在孕中、后期,蛋白质不超过30%、脂肪30%左右、碳水不超过50%。早、中和晚餐热量配比则分别为15%、30%和30%,每日的额外加餐不超过30%。②通过每日自身血糖自测表、膳食及运动记录单了解患者情况,不断调整和优化个体化医学营养疗法的方案。③通过多形式的知识宣讲、健康教育和模具演示,帮助患者了解GDM发生的原因、风险、阶段性治疗、食物替换方法等,提高患者对GDM的综合认识。④组织GDM信息交流微信群,定期推送GDM及产后膳食营养的相关知识,每周为患者进行答疑,追踪了解患者的饮食控制情况。⑤开展运动干预,对于分娩后无明显并发症者,鼓励其产后尽早下床,每餐餐后缓慢步行10~15分钟,并且根据机体恢复情况和身体综合状况开展有氧运动;产后42天内积极进行床上的肢体运动、室内散步,每次不超过10分钟;根据个体的综合耐受情况指导患者开展有氧操或瑜伽等,每日一次,每次不超过20分钟,并且监测心率情况。
1.3 观察指标
观察两组患者干预前后血糖水平[空腹血糖(fasting plasma glucose,FPG)和餐后2 h血糖(2h postprandial blood glucose,2hPG)],产前、产后12周和产后1年的糖脂代谢指标水平[FPG、2hPG、稳态模型胰岛β细胞功能(homeostasis model assessment of β-cell function,HOMA-B)、甘油三酯(triglycerides,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)]和糖脂代谢异常[空腹血糖调节受损(6.0mmol/L≤FPG<7.0mmol/L)、葡萄糖耐量受损(FPG<6.0mmol/L、或7.8mmol/L≤2hPG<11.1mmol/L)、糖尿病(FPG≥7.0 mmol/L、和(或)2hPG≥11.1mmol/L)、高TG 血症(TG≥1.7 mmol/L)、高TC血症(TC≥5.2 mmol/L)、低HDL-C血症(HDL-C≤1.0 mmol/L)和高LDL-C血症(LDL-C≥3.2 mmol/L)]情况,以及新生儿并发症(低体重儿、巨大儿、新生儿低血糖、新生儿呼吸窘迫综合征和新生儿窒息)的发生率。
1.4 统计学方法
2 结果
2.1 干预前后两组血糖指标的比较
干预前两组FPG及2hPG水平差异均无统计学意义(t值分别为-0.22、-0.41,P>0.05)。干预后两组FPG及2hPG水平显著低于干预前(t值为6.05~35.31,P<0.05),且干预后观察组FPG及2hPG水平显著低于对照组(t值分别为-4.87、-6.78,P<0.05),见表1。
表1 干预前后两组血糖指标的比较Table 1 Comparison of blood glucose indicators between the two groups before and after
2.2 不同时间两组糖脂代谢指标的比较
产前,观察组和对照组FPG、2hPG、HOMA-B、TG、TC、HDL-C和LDL-C水平差异均无统计学意义(t值为-0.91~0.77,P>0.05)。产后12周,观察组FPG、2hPG、TG、TC和LDL-C水平显著低于对照组(t值为-20.82~-5.91,P<0.05),HOMA-B和HDL-C水平显著高于对照组(t值分别为9.15、11.91,P<0.05)。产后1年,观察组FPG、2hPG、TG、TC和LDL-C水平显著低于对照组(t值为-25.02~-6.93,P<0.05),HOMA-B和HDL-C水平显著高于对照组(t值分别为14.54、11.89,P<0.05),见表2。
2.3 不同时间两组糖脂代谢异常情况的比较
产后12周,观察组葡萄糖耐量受损、高TG血症、高TC血症、低HDL-C血症和高LDL-C血症的发生率显著低于对照组(χ2值为7.35~44.80,P<0.05),但观察组和对照组空腹血糖调节受损和糖尿病的发生率差异无统计学意义(χ2值分别为0.17、0.01,P>0.05)。产后1年,观察组空腹血糖调节受损、葡萄糖耐量受损、糖尿病、高TG血症、高TC血症、低HDL-C血症和高LDL-C血症的发生率显著低于对照组(χ2值为5.46~15.02,P<0.05),见表3。
表2 不同时间两组糖脂代谢指标的比较Table 2 Comparison of glycolipid metabolism indicators between the two groups at different time
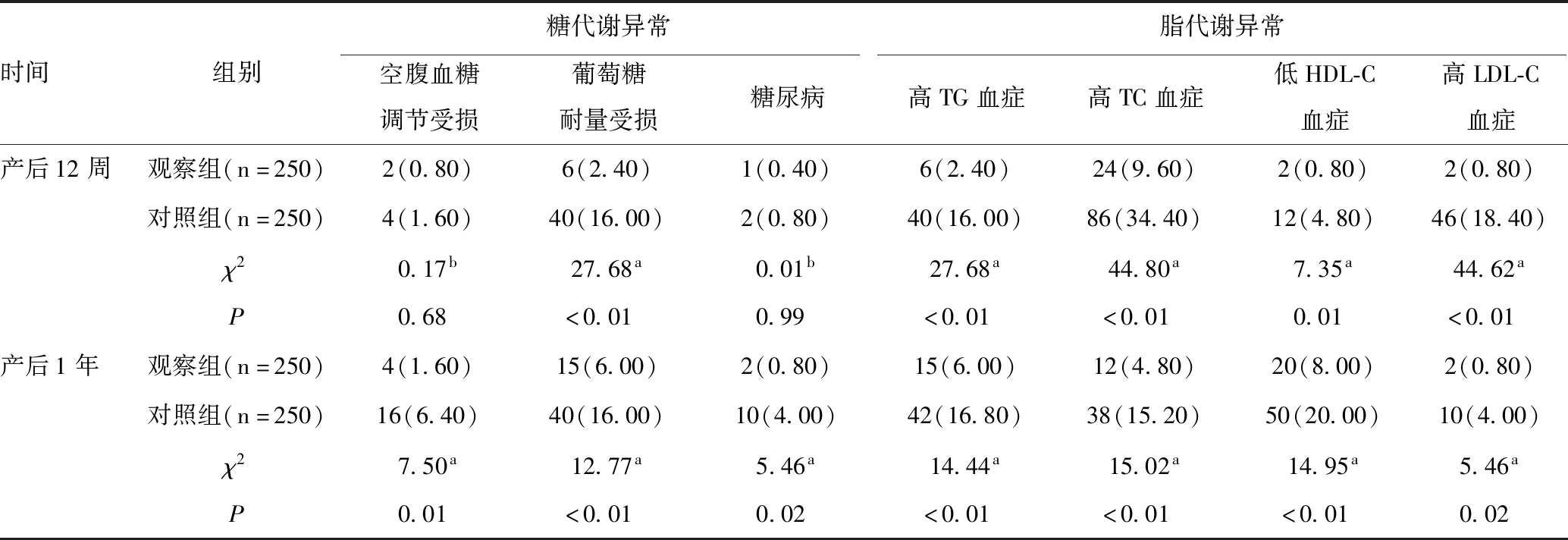
表3 不同时间两组糖脂代谢异常情况的比较[n(%)]Table 3 Comparison of abnormal glycolipid metabolism status between the two groups at different time points[n(%)]
2.4 两组新生儿并发症发生率的比较
观察组新生儿并发症总发生率为3.20%,显著低于对照组的15.20%(χ2=21.55,P<0.05)。观察组巨大儿和新生儿低血糖发生率显著低于对照组(χ2值分别为5.46、4.56,P<0.05),但两组低体重儿、新生儿呼吸窘迫综合征和新生儿窒息发生率差异均无统计学意义(χ2值为2.27~3.07,P>0.05),见表4。
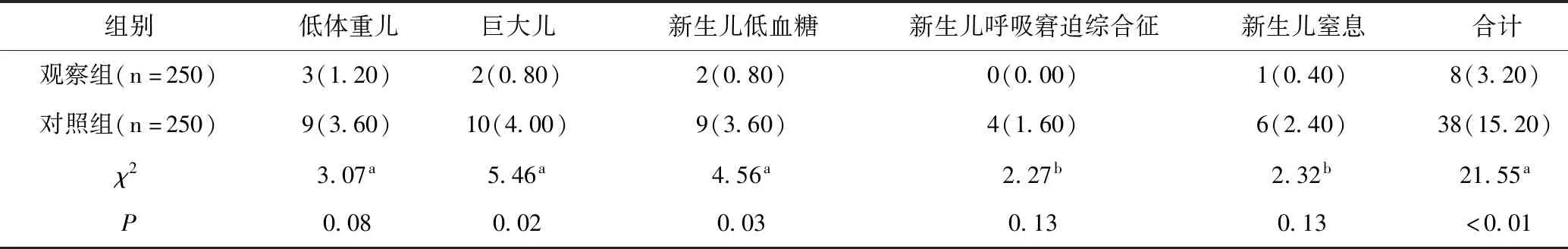
表4 两组新生儿并发症发生率的比较[n(%)]Table 4 Comparison of incidences of neonatal complications between the two groups[n(%)]
3 讨论
3.1 个体化医学营养疗法对血糖管理的影响
GDM受胎盘、体内激素、胎儿、糖尿病史等多种因素的影响。妊娠期间胰岛素敏感性下降,肾上腺皮质激素对胰岛素具有一定的拮抗作用,胎盘所分泌的相关激素均存在类似作用[6]。在GDM的发病过程中,激素水平、胎盘功能等客观因素存在较大的管理难度,难以达到临床预期的控制效果,而膳食摄入管理是主观上最容易实现的控制途径。既往研究证实,合理的膳食摄入干预可以一定程度上有效改善GDM患者的临床血糖情况,并且有利于孕期血糖管理[7]。本研究对观察组开展积极的个体化营养疗法干预,通过综合评估并制定适合GDM患者的营养改善方案,并积极地指导膳食摄入均衡配比,干预后的餐后血糖较对照组有显著改善。这是因为常规干预仅仅是健康宣讲,并不能从主观上提高GDM患者的血糖管理认知,且仅依靠患者自身主动的膳食管理,难以纠正其以往的生活和膳食习惯。血糖控制不规范时,还可能出现酮症,这不仅不利于临床血糖管理,甚至还会影响到妊娠结局[8]。个体化医学营养疗法脱离传统的营养干预,结合患者的孕周健康情况,在保障母婴营养均衡的前提下,系统、全面、规范地制定科学合理的营养方案,帮助患者稳定血糖。
3.2 个体化医学营养疗法对产后糖脂代谢的影响
GDM孕妇产后糖脂代谢情况是临床随访观察的重要部分。虽然GDM患者产后OGTT可恢复至正常水平,但其自身胰岛β细胞相关的生理功能较正常孕妇弱,会出现不同程度的糖脂代谢异常,甚至最终进展为2型糖尿病。本研究观察组的糖脂代谢异常率低于对照组,但两组在产后1年内的糖脂代谢异常率均高于产后12周,提示GDM患者产后存在远期糖脂代谢异常风险。这可能是因为妊娠期间的血糖控制可以在一定程度上改善GDM患者产后短期糖脂代谢,但是产后主观上较难控制自身活动量,加之病理、生理等因素的综合影响,产后远期糖脂代谢可能出现异常[9]。因此,虽然个体化医学营养疗法能够在一定程度上改善GDM患者的产后糖脂代谢水平,但仍需加强产后随访和血糖管理。
3.3 个体化医学营养疗法对新生儿并发症的影响
Mistry等[10]开展的系统评价发现GDM与胎儿不良结局之间存在正相关关系。GDM患者体内的血糖会直接通过胎盘进入胎儿体内,从而引起胎儿体内胰岛细胞增生,甚至导致脂肪蛋白大量合成,从而出现巨大儿[11-12]。而胎儿的高血糖水平则会进一步导致母体内的羊水含糖量过高,引发羊水过多,最终出现妊娠期高血压疾病[13]。此外,胎儿高血糖会进一步导致体内的肺泡表面物质减少,使得在发育过程中,其肺功能发育不完善。在进入产程分娩期间则会有应激反应,进一步释放大量的β-内啡肽,使得胎儿在分娩过程中出现一定程度的呼吸抑制或肺部换气不足,从而出现窒息,甚至是低氧、低血糖情况[14]。本研究中观察组新生儿并发症总发生率为3.20%,显著低于对照组的15.20%,表明积极的个体化医学营养疗法有利于降低新生儿并发症的发生率,改善临床结局。Zhang等[15]的研究也证实使用个体化医学营养疗法干预的实验组中新生儿窒息和巨大儿的发生率均低于使用常规方法干预的对照组,与本研究结果一致。
综上所述,个体化医学营养疗法能够帮助妊娠期糖尿病患者控制血糖水平,并且有利于改善产后糖脂代谢,降低新生儿并发症风险,值得临床应用并推广。
