肝动脉灌注化疗联合免疫及靶向治疗不可切除肝癌的临床研究
2022-05-27李有赞侯一夫唐几超吴春霖杨洪吉
李有赞,陈 凯,赵 冀,侯一夫,唐几超,吴春霖,杨洪吉,
(1.西南医科大学临床医学院,四川 泸州 646000;2.四川省医学科学院.四川省人民医院器官移植中心,四川 成都 610072;3.成都市第三人民医院肝胆外科,四川 成都 610043)
根据世界卫生组织(WHO)统计数据,原发性肝癌(肝癌)仍是最常见的恶性肿瘤之一[1],在全球恶性肿瘤排名第6位,死亡率排名第4位[2],肿瘤恶性程度极高。根据中国国家癌症中心发布的肿瘤数据显示,中国男性肝癌数量位居男性所有恶性肿瘤的第3位,女性肝癌数量位居女性所有恶性肿瘤的第7位[3],且预后极差,5年生存率仅约12%[4],每年因肝癌疾病死亡人数高达约39000例[5,6]。
对于失去手术治疗机会的肝癌患者,根据SHARP、Oriental试验结果,单药索拉非尼与安慰剂相比,中位总生存期(mOS)仅延长约3个月[7,8];在2017年美国临床肿瘤学会(ASCO)公布的REFLECT研究结果显示,仑伐替尼的mOS可达到了13.6个月[9];当前美国食品药品监督管理局(FDA)批准的纳武利尤单抗(nivolumab)、帕博利珠单抗(pbrolizumab)等PD-1/PD-L1抗体用于肝癌的二线治疗[10],但研究显示,无论何种PD-1/PD-L1抗体,单药治疗的客观缓解率(ORR)为15%~20%,疾病控制率(DCR)为56.6%~60%,总生存期(OS)为10.4~15个月[11~13]。显而易见,单药治疗不可切除肝癌,其效果是有限的,且根据既往众多联合治疗的临床研究,均体现出了联合治疗的优势[14~16]。为了寻找更适合的不可切除肝癌患者的治疗方案,本中心以奥沙利铂和氟尿嘧啶为基础的化疗方案进行肝动脉灌注化疗(HAIC),同时联合免疫及分子靶向治疗,即mFOLFOX-HAIC联合免疫及靶向治疗,探索该方案对不可切除肝癌治疗的效果,以及治疗的安全性,为临床工作提供参考。
1 资料与方法
1.1 一般资料2018年9月至2021年11 月于四川省人民医院就诊的肝癌患者63例,纳入标准:①行病理学或腹部增强CT/MRI检查,并符合中国2019版原发性肝癌诊疗规范定义的肝癌患者;②符合RECIST标准的可测量病灶;③不可切除定义为有4个或4个以上的双叶病灶,肿瘤占肝脏体积50%以上或伴明显肝硬化背景,或肿瘤对主要血管结构的侵袭,且经评估不能一期手术切除;④既往未经治疗的患者;⑤肝功能Child-pugh分级A/B级,且美国东部肿瘤协作组体力状态活动(ECOG PS)评分<2分;⑥白细胞计数≥3.0×109/L,且无肾、心、脑等重要脏器功能不全疾病;⑦对各种治疗方案均知情了解且门诊随访依从性好,有完整的随访数据。排除标准:①合并心、肾等重要器官器质性病变或伴随其他恶性肿瘤的患者;②既往曾行肝癌治疗的患者;③肝功能失代偿(肝功能Child-pugh C级);④临床资料缺失不全的患者;⑤用药依从性差的患者、妊娠或哺乳期妇女。63例患者中男48例(76.2%),女15例(23.8%),年龄(55.3±12.2)岁,合并慢性乙型肝炎52例(82.5%),肝硬化57例(90.5%),大血管侵犯33例(52.4%),伴有腹水8例(12.7%),CNLC分期Ⅲa期及其以上35例(55.6%),总胆红素≥34 μmol/L 28例(44.4%),靶病灶最大直径≥5 cm 43例(68.3%),甲胎蛋白AFP≥400 ng/ml 29例(46.0%)。本研究已取得患者的知情同意,获得医院伦理委员会批准。
1.2 方法所有患者HAIC均在我院完成,使用局部浸润麻醉,选择经股动脉入路,术中选用5F RH导管挂钩腹腔干,以流速5 ml/s的碘海醇进行造影,确认肿瘤供血动脉后,使用2.7 FP rogreat微导管进入左/右肝动脉,或留置肝固有动脉;必要时于肿瘤异常供血动脉行小剂量栓塞剂栓塞。微导管放置完成后,注入肝素水防止导管凝血,导管外露部分用无菌医用纱布覆盖,用3M透明敷贴固定在腹股沟和右下腹的皮肤上。手术结束,将患者转移致病房,卧床休息,双下肢可间断行踝泵运动,防止下肢深静脉血栓形成。按照mFOLFOX 化疗方案序贯化疗药物,化疗过程辅以水化、止吐、止痛、保肝、护胃等治疗,灌注结束后予以拔除鞘组、导管、微导管,重力按压穿刺点约30 min[17]。同时,所有入组患者均予以口服甲磺酸仑伐替尼胶囊行分子靶向治疗(<60 kg:8 mg/d;≥60 kg:12 mg/d),联合PD-1抗体(替雷利珠或信迪利单抗,200 mg 静脉滴注,21天/周期)免疫治疗。观察治疗过程的不良反应,6~8周复查评估一次。
1.3 治疗评价①临床疗效[18]:用mRECIST 1.1标准对肿瘤靶病灶进行疗效评价,主要分析肿瘤ORR及疾病无进展时间(Progression Free Survival, PFS),次要分析DCR、肿瘤手术转化率。② 药物安全性评估[19]:采用通用不良反应术语标准版5.0评价不良反应分级(CTCAE 5.0)。
1.4 统计学方法所有数据应用SPSS 26.0统计学软件处理分析。生存指标分析采用生存曲线描述,符合正态分布的计量资料以均数±标准差描述,比较采用t检验;不符合正态分布的计量资料比较采用Mann-WhitneyU检验。患者预后采用Cox比例风险回归模型多因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 肿瘤临床疗效评价及转化治疗经治疗后肿瘤反应:完全缓解(CR)2例,部分缓解(PR)23例,疾病稳定(SD)28例,疾病进展(PD)10例;ORR 39.7%,DCR 84.1%;肿瘤转化手术治疗12例(19.0%)(肝移植4例,微波消融5例,手术切除3例)。
2.2 患者生存情况患者中位随访时间为8.2个月(1.5~19.7个月),6个月OS为90%,12个月OS为62.8%,mOS未达到;6个月PFS为71.2%, mPFS为9.50个月(95%CI:7.27~11.73),见图1、图2。

图1 患者OS
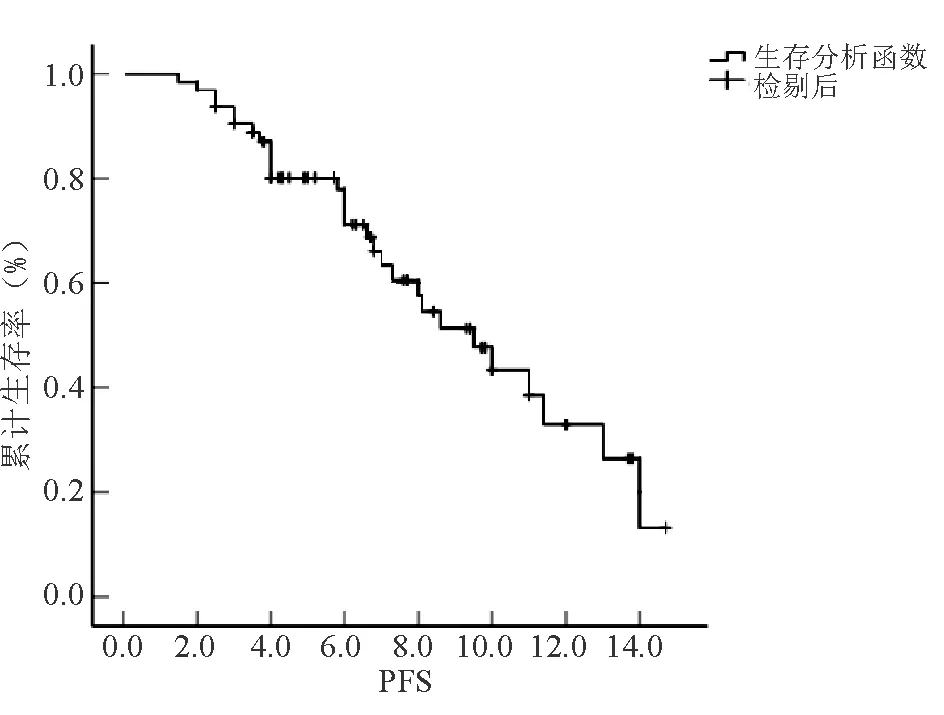
图2 患者mPFS
2.3 患者预后分析门静脉无癌栓的患者较门静脉合并癌栓的患者PFS延长,差异有统计学意义(P=0.018);不同肿瘤靶病灶直径及不同AFP、AST、总胆红素含量的患者mPFS比较,差异无统计学意义(P>0.05)。见表2。
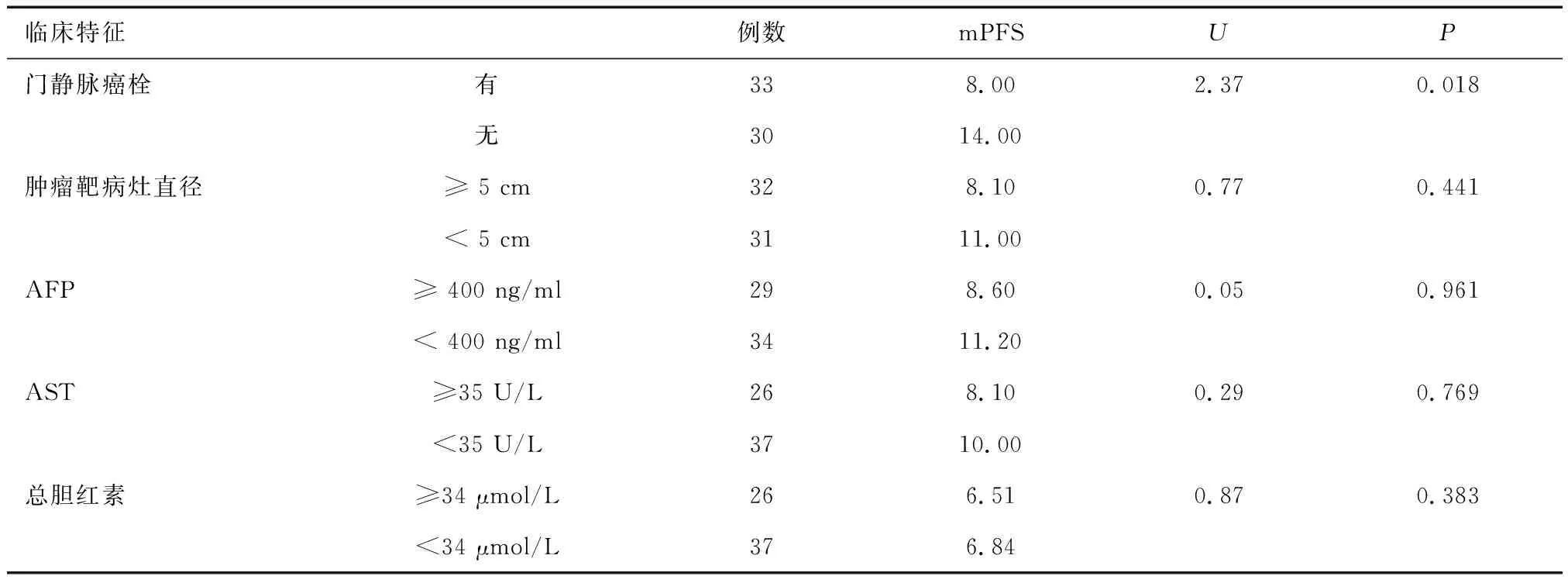
表2 不同临床特征患者mPFS比较 (月)
Cox比例风险回归模型对门静脉癌栓、靶肿瘤最大直径、AFP、AST、总胆红素进行多变量分析,结果显示,门静脉癌栓是中晚期肝癌的独立预后因素(P=0.014),见表3。

表3 中晚期肝癌患者独立预后的COX 多因素分析
2.4 治疗安全性治疗过程中,无患者出现导管留置相关并发症,无患者出现5级药物不良反应。16例患者发生3~4级药物不良反应,分别是消化道出血1例,白细胞减少3例,血小板减少3例,严重呕吐1例,高血压8例,均延长住院治疗后好转;1~2级药物不良反应主要表现为厌食(61.9%)、呕吐(32.1%)、腹痛(44.4%)、白细胞减少(31.7%)、血小板减少(31.7%)等症状,上述不良反应均未进行药物减量,予以对症处理后缓解。
3 讨论
肝癌是临床常见的消化系统恶性肿瘤之一,据2020年全球最新癌症负担数据显示,在全球范围内,每年新增肝癌患者高达91万例,因肝癌死亡人数每年高达83万例[20]。早期进行根治性手术切除,是获得长期生存最为重要的治疗手段[21],但由于肝癌发病隐匿、恶性程度高、病情进展迅速,因此,大多数肝癌患者确诊时就已经进入肿瘤中晚期,错失了手术时机。在广义上来讲,肝癌不可切除的原因包括了肝功能储备不足以及肿瘤因素,如何提高目前肝癌的手术切除率,不仅需要依靠外科技术的提高,或者是辅助设备的进步,肿瘤降期转化治疗也是至关重要的。在Sun 等[22]发布的一项转化治疗中,纳入了60例不可切除肝癌病人,经仑伐替尼联合PD-1抗体治疗后,9例患者获得手术转化治疗,转化率是15%;在本次临床研究中,不可切除肝癌经mFOLFOX-HAIC联合免疫及靶向治疗后,改变了肝癌不可切除的肿瘤因素,实现了12例患者成功进行转化治疗,转化率高达21.6%,肿瘤治疗反应明显。
HAIC并非是一门新兴技术,早在上世纪70年代日本学者就开始了该项技术的探索[23]。但HAIC的化疗方案组合各异,随着第三代铂类,奥沙利铂的出现,具备更快、更强的细胞毒活性,与多种药物具有协同增效作用[24],围绕在奥沙利铂为基础的序贯FOLFOX方案,在HAIC治疗中也不断得到优化,并取得了较好的治疗效果。根据He等[25]研究,较单用索拉菲尼治疗,HAIC联合索拉菲尼获得更长的生存时间(13.37 vs 7.13个月,P<0.05)。在本次临床研究中,所有纳入组的不可切除肝癌患者均经过了至少两个周期的mFOLFOX-HAIC化疗,并联合免疫、靶向治疗,结果显示mPFS为9.50个月,6个月PFS为71.2%、ORR为39.7% 以及 DCR为84.1%,肿瘤治疗效果明显,此外,产生的不良治疗反应也是可控和安全的;同期与目前在肝癌治疗领域取得较为优异成果的IMbrave150[26]研究相比,阿替利珠单抗和贝伐珠单抗联合应用(T+A组合)也同样显示了非常明确的抗肿瘤活性和安全性,但尽管如此,T+A组合方案疗效结果显示mPFS 6.8个月,6个月PFS为54.5%,ORR为33.2%,与本次临床研究相比,无论是PFS,亦或是ORR,均优于T+A组合治疗方案。也有研究[27]报告特瑞普利单抗联合HAIC及仑伐替尼治疗晚期肝癌,较单用仑伐替尼组PFS明显改善(9.3 vs 4.8个月),且OS延长(17.13 vs 10.1个月)、肿瘤反应DCR和ORR更有优势(86.8% vs 69.2%,47.2% vs 9.2%),与单用仑伐替尼治疗组相比,有着显著性差异(P<0.01)。这就说明了在肝内局部化疗的基础上,辅以免疫、靶向治疗,是可以使肝癌患者获益的,可能原因:①奥沙利铂本身就具备强大的的细胞毒活性,可以通过上调细胞凋亡相关基因Bax表达,抑制Bcl-2表达,诱导肝癌细胞株HepG2凋亡,通过肝内高浓度局部灌注,更加强了对肝癌细胞的杀伤作用[28];②奥沙利铂与多种药物具有协同增效作用[24],mFOLFOX方案也是经过漫长的临床研究总结出来的,具备更强大的抗肿瘤作用,并且副作用也较小;③经介入化疗后,在肿瘤微环境发生改变,肝癌细胞的凋亡、坏死,肿瘤被破坏,瘤体内会出现缺氧的状态[29],可引起血管内皮生长因子(VEGF)表达活性增强,这也将阻断抗原递呈细胞对T淋巴细胞的激活作用,此外,肿瘤细胞的坏死使肿瘤新抗原释放,促进树突状细胞在微环境中的招募和激活,使得肿瘤微环境由免疫抑制性转变为免疫支持性,促进免疫治疗发挥其效应;另一方面,化疗可以诱导肿瘤细胞的免疫原性死亡,减少肿瘤微环境中的“非靶点”免疫抑制,从而提高肿瘤的抗原性。因此,在化疗作为基础治疗上,配合阻断PD-1/PD-L1通道以及抗VEGF靶向治疗,可以提高抗肿瘤的效果[30];④局部灌注化疗对肝癌微小子灶、隐匿病灶以及大血管侵犯的癌栓也有很好的治疗效果。
虽然本次临床研究中,患者的治疗效果是明确的,但对于免疫及靶向治疗,是否该先于HAIC治疗前启动,提前多久最为恰当;经4-6次HAIC治疗后,若肿瘤处于稳定状态,是否该继续追加HAIC治疗;针对手术转化的患者,何时为转化的最佳时期,术后是否需要行预防性化疗。诸多问题需要更多的研究进行探讨并达成共识,才能更好地为患者提供合理、个性化且获益最大的治疗方案。
