吸附溶出伏安法检测吸毒人员尿液中吗啡
2022-05-25殷勤红张建强李越凡李龙发赵文嵩杨红梅杨发震倪春明
陈 瑾,殷勤红,刘 燕,张建强,李越凡,李龙发,陈 航,赵文嵩,杨红梅,杨发震,倪春明**
(1.云南警官学院 刑事侦查学院,云南 昆明 650221;2.毒品分析及禁毒技术公安部重点实验室,云南 昆明 650223;3.云南省公安厅 刑侦总队技术处理室,云南 昆明 650228;4.云南省玉溪市公安局 刑事科学技术研究所,云南 玉溪 653100)
阿片类毒品是目前世界上使用历史最长、流行范围最广、危害最严重的毒品[1].据2020 年中国毒情形势报告,在180.1 万名现有吸毒人员中,滥用阿片类毒品人数为73.4 万名,占现有吸毒人员总数40.8%.吗啡是海洛因、吗啡和可待因的最终代谢物.吗啡除了因其成瘾性、危害性、滥用性而具有毒品的角色外,它的镇痛麻醉作用还使其成为一种良好的镇痛剂用于临床.尿液中治疗吗啡的量通常为8~80 ng/mL[2].传统的毒品现场快速检测[3]方法主要有试纸法(免疫胶体金技术)、化学法以及便携式光谱检测法,这些方法检测快速,操作方便,但也具有特异性不强、灵敏度不高等缺点.因此还需要送入实验室采用GC-MS[4]、HPLC-MS 等精密仪器进行分析确认.电化学传感器[5](ECS) 基于待测物本身的电化学性质,能够将待测物化学量转变成电学量进行检测,并在这两个变量之间建立起一定的联系,通过检测电化学信号达到检测待测物化学量的目的.电化学仪器操作简单,价格低廉,不需要复杂的仪器维护,同时电化学传感器还具有较高的灵敏度、较快的分析速度、越来越微型化与集成化等优点,因而被广泛应用在基础研究、生物、临床化学、化学分析等领域[6],是目前最热门的研究领域之一.吸附溶出伏安法 (ASDPV)[7]是将目标分析物从溶液相向电极表面吸附传递,并不断富集在电极上,因为电极面积很小,这样电极表面被测物浓度远远大于本体溶液中的浓度,从而增加待测物的检测灵敏度.利用吗啡在电极上的氧化电流对其进行电化学检测的研究已有一些文献报道,其中使用的工作电极多为化学修饰电化学,修饰材料包括六氰基高铁酸钴[8]、羧基化碳纳米管[9]、普鲁士蓝[10]、聚乙撑二氧噻吩[11]、铁卟啉[12]以及分子印迹材料[10]等,检测技术有循环伏安法 (CV)、计时电流法(i−t)以及差分脉冲伏安法(DPV).但这些检测方法的灵敏度较本文中的ASDPV 法低,且修饰材料制备较为复杂.此外,据查阅文献,目前还未见用电化学传感器检测实际吸毒人员尿液中吗啡的报道.
本文将多壁碳纳米管经简单羧基化处理后作为检测吗啡的电极修饰材料,通过滴涂法制备了羧基化多壁碳纳米管 (MWNTs-COOH) 修饰玻碳电极 (MWNTs-COOH/GCE),并将其作为工作电极,采用吸附溶出伏安法对尿液中的吗啡进行检测.在检测过程中发现,尿酸的氧化电位与吗啡的氧化电位接近,对吗啡的检测有很大干扰.因此,提出了用尿酸酶去除尿液中尿酸的方法,提高了检测结果的准确性,实现了对尿液中吗啡的快速、简单、高选择性检测.
1 实验部分
1.1 实验原理吗啡含有两个羟基[2],其中3 位上的酚羟基可被氧化,吗啡氧化过程分为两步:第一步3 位上的酚羟基 (M―O−) 失去电子生成M―O*,M―O*很不稳定会生成伪吗啡 (PM―OH);第二步PM―OH 含有的酚羟基 (PM―O−) 会氧化生成PM―O*.这个过程氧化中会引起电流的变化,根据被测吗啡溶液引起的电流改变位置、变化大小及电流改变与浓度的联系对吗啡进行定性或定量分析.

总反应式为:2M—OH ⇌PM—O∗+3e−+3H+,其中M—OH 和PM—OH 分别代表吗啡和伪吗啡.
1.2 试剂与原材料吗啡碱(云南省公安厅,w=98.4%±1.1%);多壁碳纳米管(泰坦科技有限公司,管径3~15 μm,管长15~50 μm);K3[Fe(CN)6](风船化学试剂科技有限公司,分析纯);KCl、K2HPO4、NaH2PO4(泰坦科技有限公司,分析纯);尿酸酶(泰坦科技有限公司,500U);4 份吸毒人员实际尿样(云南省司法鉴定中心提供).
1.3 主要仪器所有的电化学数据由CHI 760E电化学工作站(上海辰华仪器有限公司)测得,测量时采用三电极系统,使用的参比电极(Ag/AgCl),Pt 丝电极,玻碳电极(GCE)均购自上海辰华.KQ-300DE 数控超声清洗仪(昆山市超声仪器有限公司);PHS-3G 恒温加热磁力搅拌pH 计(上海仪电科学仪器股份有限公司);DHG-9055A 鼓风干燥箱(上海一恒科学仪器有限公司);PR224ZHI 天平(奥豪斯仪器常州有限公司);明澈TM-D 24UV 纯水/超纯水系统.
1.4 实验方法
1.4.1 MWNTs-COOH 的制备 将MWNTs 置于250 mL 圆底烧瓶中,加入100 mL 浓硝酸,于油浴锅中90 ℃下搅拌反应4 h.反应结束后用去离子水洗涤至中性,烘箱内干燥,备用.
1.4.2 MWNTs-COOH/GCE 的制备
玻碳电极的处理:首先用0.3 μm 的Al2O3加适量去离子水在麂皮上进行打磨抛光,之后使用0.05 μm 的Al2O3颗粒按上述同样方法进行打磨抛光,然后在去离子水中超声清洗干净,直到CV 扫描得到的K3[Fe(CN)6]的氧化还原峰电位差小于100 mV,否则重复上述打磨抛光过程,直至CV 扫描结果满意.将处理好的玻碳电极室温下干燥.
MWNTs-COOH/GCE 的制备:用移液枪取适量经水超声分散均匀的MWNTs-COOH 分多次滴涂于处理好的GCE 表面,然后放置于红外灯下烘烤5 min 左右,待水分挥干后羧基化碳纳米管就吸附在玻碳电极表面,即制得羧基化多壁碳纳米管修饰的玻碳电极(MWNTs-COOH/GCE) .
1.4.3 电化学检测方法 采用三电极系统,将MWNTs-COOH/GCE 放入含有一定浓度吗啡的磷酸盐缓冲溶液(PBS)中,用计时电流法在一定电位下富集一定时间后,使用DPV 从0.2~0.7 V 进行扫描,记录其氧化峰电流.
每次检测结束后,把工作电极置于去离子水中放置60 s,以去除测量时吸附在电极表面的物质.
2 结果与讨论
2.1 羧基化碳纳米管的修饰效果实验对比了裸GCE 与MWNTs-COOH/GCE 在同一浓度(3.0×10−5mol/L)吗啡溶液中的电化学响应情况.结果表明,裸GCE 和MWNTs-COOH/GCE 上的响应峰电流分别为4.334×10−7A 和1.342×10−5A.可见,3.0×10−5mol/L 的吗啡在MWNTs-COOH/GCE 的响应电流约为其在裸GCE 的31 倍.说明羧基化多壁碳纳米管可作为吗啡电化学传感器的修饰材料,提升其检测灵敏度.
2.2 MWNTs-COOH 修饰量的选择MWNTs-COOH 用量过少,不能完全覆盖GCE 电极表面;用量过多,则修饰膜过厚,容易脱落并导致背景电流过强,使吗啡的氧化峰受到影响.适量的修饰层厚度不仅能有效提升传感器性能,节约试剂,还可以保证修饰电极的稳定性.为了得到较理想的滴涂量,实验分别滴涂了2、3、4 μL 和5 μL 1 mg/mL 的MWNTs-COOH 于玻碳电极表面,制备修饰电极.结果表明,当滴涂量为2 μL 时,GCE 电极表面不能被完全覆盖;滴涂了3、4、5 μL MWNTs-COOH 制备的修饰电极对3.0×10−5mol/L 吗啡的响应电流分别为5.58、9.324 μA 和8.71 μA,说明当MWNTs-COOH 的修饰量为4 μL 时,电极对吗啡的DPV 响应效果最好.故实验选择MWNTs-COOH 的滴涂量为4 μL.
2.3 富集时间与富集电位的优化采用差分脉冲吸附溶出伏安法检测吗啡,富集电位与富集时间都对其响应峰电流有较大影响.如图1 所示,富集电位从−1.0 V 升至−0.6 V 时,峰电流有较大的提高;从−0.6 V 升至−0.2 V 时,峰电流没有明显差异;当富集电位从−0.2 V 继续升高时,DPV 响应开始大幅下降,特别是使用正电位富集时,DPV 响应快速降低.这可能是因为负电位下玻碳电极表面羧基化碳纳米管上有较多—COO−基团暴露于电极表面,便于吗啡的吸附.为避免过低电位下一些金属离子析出,实验选择−0.2V 作为富集电位.

图1 不同富集电位下3.0×10−5 mol/L 吗啡在MWNTs-COOH/GCE 上的峰电流响应(富集时间300 s,pH7.0)Fig.1 Peak current of 3.0×10−5 mol/L of MOP at different preconcentration potential on the MWNTs-COOH/GCE
当固定富集电压为−0.2 V 时,在富集时间从60 s 增加到480 s 的过程中(图2),3.0×10−5mol/L吗啡的氧化峰电流不断上升,但在富集时间超过300 s 后增幅减小.考虑到检测时间,实验选择富集时间为300 s.
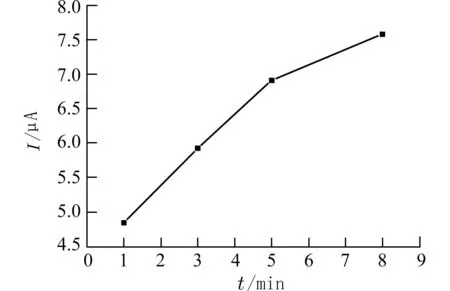
图2 不同富集时间下3.0×10−5 mol/L 吗啡在MWNTs-COOH/GCE 上的峰电流响应(富集电位−0.2 V,pH 7.0)Fig.2 Peak current of 3.0×10−5 mol/L of MOP at different preconcentration time on the MWNTs-COOH/GCE
2.4 缓冲溶液pH 的优化吗啡的氧化过程伴随着H+的产生,所以缓冲溶液的pH 值对其氧化峰电流有影响.分别在pH 为5.8、6.5、7.0、7.5、8.0 的Na2HPO4-KH2PO4缓冲溶液中对3.0×10−5mol/L 吗啡进行ASDPV 检测.DPV 响应峰电流随Na2HPO4-KH2PO4缓冲溶液pH 值的变化如图3 所示.可见当缓冲溶液pH 值在6.5~7.5 范围内时,响应峰电流较高,且在pH7.0 时有最大值.当缓冲溶液酸性较强 (pH<6.5) 或偏碱性 (pH>7.5) 时,吗啡的峰电流急剧下降.因此,实验选择pH7.0 的Na2HPO4-KH2PO4缓冲溶液为电解质溶液.

图3 缓冲溶液pH 对3.0×10−5 mol/L 吗啡在MWNTs-COOH/GCE 上的峰电流响应的影响(富集时间300 s,富集电位−0.2 V)Fig.3 Effect of pH on the MWNTs-COOH/GCE response of 3.0×10−5 mol/L MOP
2.5 标准工作曲线的绘制在最优检测条件下,用差分脉冲吸附溶出伏安法测定了不同浓度吗啡的响应峰电流,并绘制了标准工作曲线.如图4 所示,吗啡在MWNTs-COOH/GCE 上的峰电流随吗啡浓度的增加而增大.在吗啡浓度为1.0×10−7~1.0×10−4mol/L 范围内,吗啡浓度的对数值 (lgc) 与DPV 峰电流的对数值 (lgI) 呈线性关系,线性回归方程为lg(I/μA)=0.687lg[c/(μmol·L−1)]−0.068 (r2=0.992 0).
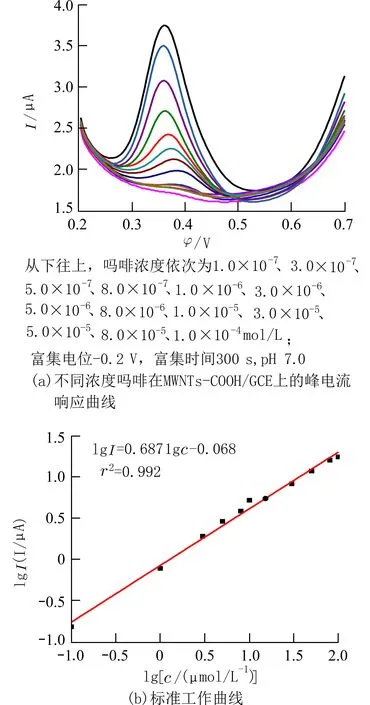
图4 响应峰电流及标准工作曲线Fig.4 The pulse voltammetry and the calibration curve
2.6 MWNTs-COOH/GCE 的重现性及稳定性实验进一步研究了该传感器的重现性及稳定性.使用相同方法制备了5 支传感器并用其在同一检测条件下对3.0×10−5mol/L 的吗啡进行检测,峰电流的相对标准偏差为4.1%;用同一支电极对同一份吗啡溶液平行测定5 次,峰电流的相对标准偏差为3.8%;将此传感器连续使用30 次或室温下储存于纯水中2 个月后,仍能维持最初响应的90%以上.可见,本实验方法制备的传感器具有较好的重现性以及稳定性.
2.7 实际样品吗啡的检测直接使用MWNTs-COOH/GCE 检测尿液中吗啡的含量时,发现尿液中的尿酸有很大干扰.因此,实验在尝试了多种消除尿酸的方法后,选择了用尿酸酶除去尿液中的尿酸.结果显示,在1 mL 的尿液中加入1 mg 的尿酸酶(500 U),然后在37 ℃水浴中酶解2 h 后,用MWNTs-COOH/GCE 检测不到尿酸峰的存在,说明尿酸的干扰已经消除.
将用尿酸酶消除尿酸后的实际尿样(4 份阳性样品)采用MWNTs-COOH/GCE 进行检测,结果见表1 所示.可见用MWNTs-COOH/GCE 得到的检测结果(4 次平均值)与HPLC 检测结果的相对误差的绝对值在4.24%以内.并通过t 检验法发现在置信度为95%时,两种方法并无显著性差异,说明MWNTs-COOH/GCE 可以用于实际尿样中吗啡的检测.
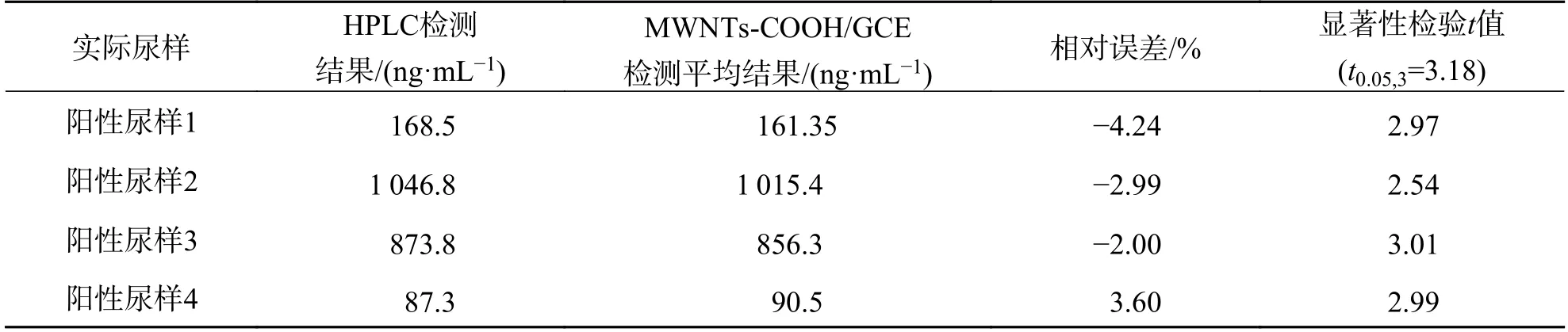
表1 MWNTs-COOH/GCE 对实际尿样的检测结果Tab.1 The determination results of MOP in the drug addicts’ urine samples
3 结语
本文通过直接滴涂法制备了一个简单的检测传统毒品吗啡的电化学传感器,其修饰材料为自制的羧基化碳纳米管,基底电极为玻碳电极,检测方法为差分脉冲吸附溶出伏安法.在优化了相关检测条件后,该传感器在吗啡浓度为1.0×10−7~1.0×10−4mol/L 的范围内,其DPV 峰电流的对数值(lgI)与吗啡的浓度对数值 (lgc) 呈线性关系,线性回归方程为lg(I/μA)=0.687lg[c/(μmol·L−1)]−0.068(r2=0.992 0).在使用尿酸酶除去尿液中的尿酸后,用该传感器可以准确测定实际尿样中吗啡的含量,具有在公安基层中快速检测尿液中吗啡含量的应用前景.
