食品及其原料中的黑色素研究进展
2022-05-14沈玥祺吴文标
沈玥祺,吴文标
(西南大学食品科学学院,重庆 400715)
黑色素是含芳香基团的高分子聚合物,它吸收可见光(一般可采用分光光度计在405 nm等处测定吸光度以检测黑色素的含量),具有黑色特征[1]。一定量的黑色素赋予食品黑色,各类消费者对于“黑色的天然/加工食品”的接受程度变得越来越高,近年来甚至有将“黑色的天然/加工食品”作为健康食品标志的趋势。黑色素在食品中分布广泛,普通人群对黑色素的摄入量达到约10 g/d[2−3]。奥利奥黑色饼干的每年世界消费次数达到75亿以上,其年销售额达到20亿美元以上,是目前世界消费量最大的饼干品种[4−5]。联合国粮农组织预测到2023年具黑色的红茶年增长率将达到2.9%,总产量达到417万吨,产值达到10亿美金以上[6]。黑色的咖啡在全球市场的销售额达到1730亿美金[7];黑色的巧克力在全球市场的销售额预计至2026年将达到1899.9亿美金[8];黑色的可口可乐在2020年的全球销售额达到715亿元[9],此外,还有许多具有黑颜色的畅销食品或饮料。
目前,越来越多的研究表明许多存在于食品及其原料中的黑色素(定义为食品黑色素)对人体健康有利。对于“黑色食品”的基础应用以及开发研究正日益增长。例如,利用墨鱼汁[10−11]、红茶[12]、食用菌[8,13]和其它各种食品或食品原料[14]所含的黑色素开发功能食品和食用色素。常见的食品黑色素主要有三种:天然食品黑色素、美拉德反应生成黑色素和焦糖型黑色素。本文就上述三类黑色素的食品来源、组成及结构、功能特性和食用安全性等方面进行综述。
1 生物体内合成的天然食品黑色素
黑色素广泛地存在于天然黑色食品中,例如,各种类别的黑米、黑豆、黑麦、各类黑色水果(如黑莓、桑葚)、黑玉米、黑色真菌(如黑木耳)、黑藻类(如紫菜)、黑肉(如乌鸡肉)、黑色鱼皮、黑色发酵食品(如黑豆豉)和黑色蚂蚁等昆虫,其分布的广泛性使得天然黑色素的种类、结构和性质具有一定差异,从而表现出特异性。因此,以下根据天然食品黑色素不同来源分为形成黑色素的前体物质、动物黑色素、植物黑色素、食用菌黑色素、细菌黑色素和昆虫黑色素几个方面分别论述。
1.1 天然食品黑色素的前体物质
图1中展示的是天然食品黑色素在生物体内合成的主要或最常见的前体物质。以L-酪氨酸和L-多巴为前体物质可形成真黑素(eumelanin),L-多巴可由L-酪氨酸衍生而来。一般而言,以5-硫-半胱氨-多巴为前体物质可形成假黑(褐)色素(pheomelanin),这类色素中,有的可能会增加癌症风险,具有危害食品安全方面的风险,需要严格控制其在食品中的含量[15−17];以多巴胺和5-硫-半胱氨-多巴胺为前体物质可形成神经黑色素,这类色素在非人灵长动物大脑中有少量存在,在许多低等动物组织中及其它食品或原料中没有发现[18]。以N-乙酰-多巴胺为前体物质可形成昆虫类黑色素,其在食物中作为色素的适用性可能取决于可食昆虫作为食品资源的发展潜力[19]。以儿茶酚为前体物质可以生成植物类儿茶酚-黑色素,此类色素的颜色为黑褐色至完全黑色,在红茶中的黑色素可能主要属于这类色素。由于其分布广泛,特别是加工或储藏过程中的酶促或非酶促褐变产生的黑色或褐色物质都属于此类色素,所以其随日常饮食被摄入的概率较高。以1,8-二羟基萘(DHN)为前体物质可生成真菌类DHN类-黑色素,有的可能会成为毒性因子,进而存在危害食品安全方面的风险,需要监测其含量[20−22]。以4-谷氨酰胺基羟基苯(GHB)为前体物质可形成蘑菇类GHB类-黑色素(此类色素既可能在食用菌中形成,也可能在致病菌中形成,实际应用时应该小心区分;虽然基本只在蘑菇中发现此类色素,但其不一定是蘑菇中存在的唯一黑色素)。以2,5-二羟苯乙酸(HGA)为前体物质可形成脓黑素(pyomelanin)多为细菌黑色素,通常因为致病菌的生长而产生,有的可能会成为毒性因子,从而产生危害食品安全方面的风险,因此,对其含量进行监测很重要[23−24]。
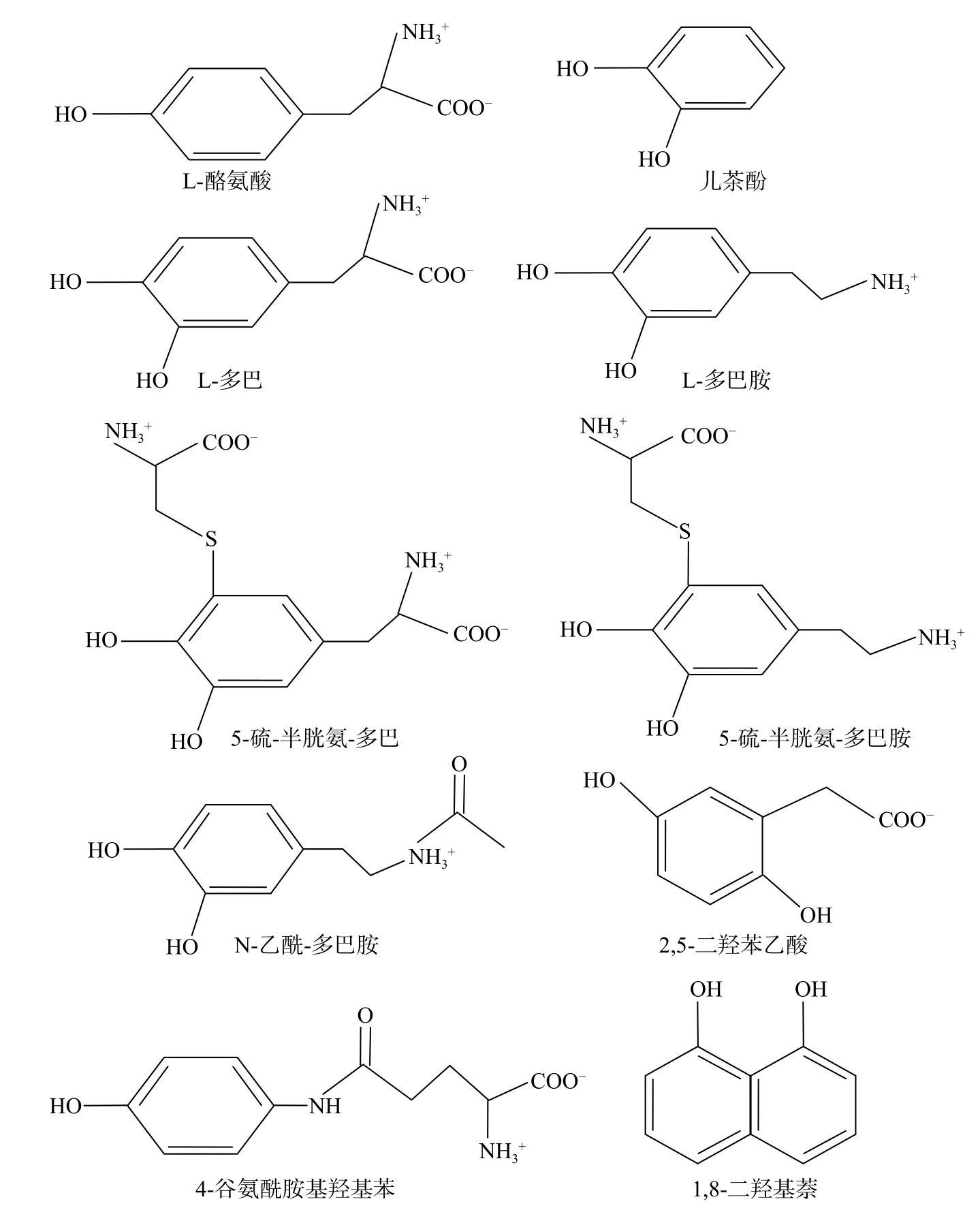
图1 天然黑色素在生物体内合成的主要前体物质Fig.1 Main precursors of forming melanin in bio-tissues
1.2 动物黑色素
在一些动物体内,以酪氨酸为前体物质形成黑色素是主要途径。这种途径主要产生褐色至黑色的真黑色素。真黑色素是一种高分子聚合物,由于其溶解性较差且不易分解,难以得到结晶态的纯品,所以研究其结构较为困难。这也是至今为止,对此类黑色素的结构不能完全确定的原因。尽管有研究运用核磁共振技术对此类黑色素的结构进行了研究,但是这类研究所获得的结果对于准确地判定这类黑色素的分子结构而言仍具有局限性[25−27]。
1.2.1 组成及结构 日本学者Ito及其团队研究表明,通过用碱性介质中的高锰酸钾或双氧水加热化学降解真黑色素可得到不同比例的5,6-二羟基-2-吲哚甲酸(5,6-dihydroxyindole-2-carboxylic acid,DHICA)和5,6-二羟基-2-吲哚(5,6-dihydroxyindole,DHI)。这些吲哚碎片能在碱性过氧化氢的氧化作用下转化为吡咯-2,3,5-三羧酸(pyrrole-2,3,5-tricarboxylic acid,PTCA)、吡咯-2,3-二羧酸(pyrrole-2,3-dicarboxylic acid,PDCA)、吡咯-2,3,4,5-四羧酸(pyrrole-2,3,4,5-tetracarboxylic acid,PTeCA)、吡咯-2,3,4-三羧酸(pyrrole-2,3,4-tricarboxylic acid,isoPTCA)以及少量其它吡咯羧酸和氨基羟苯丙氨酸(AHP)[28−32]。科学界一般普遍接受5,6-二羟基-2-吲哚是构建黑色素的基本单元,其2,3,4和7位通常是参与聚合的活性位置,在位点2可能会羧化[29,32−36],但至今没有新的聚合理论或模式提出,传统认定的动物黑色素的经典推导模式如图2所示,可用傅里叶变换红外光谱仪对芳香烃骨架、脂肪族烃基和酚型或醌型碎片进行鉴定[37]。
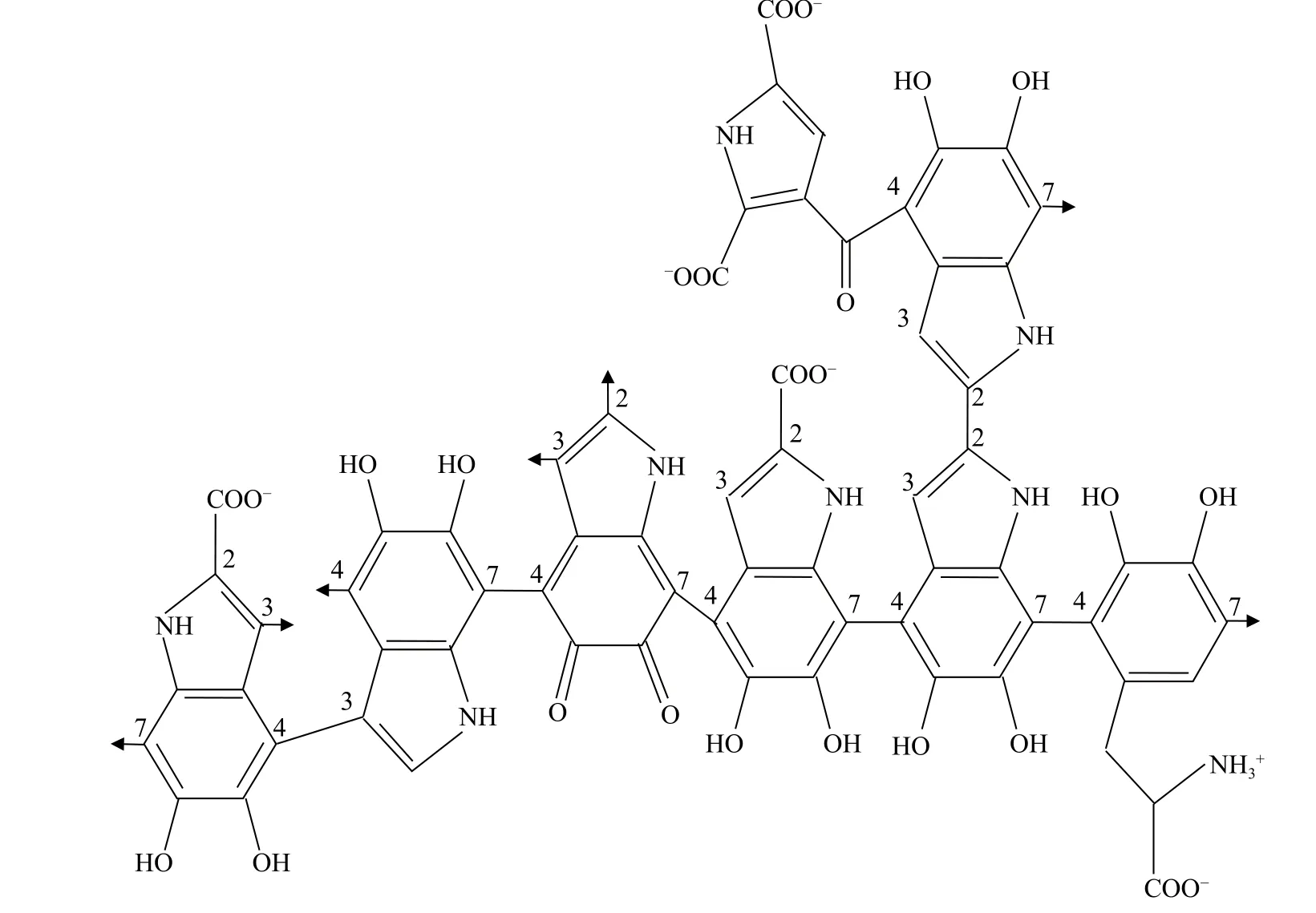
图2 推导的天然动物黑色素的经典分子结构模式[38]Fig.2 Structural model of eumelanin commonly accepted[38]
1.2.2 在可食动物组织或器官中的含量 表1中展示了一些可食动物组织中黑色素的含量。除了表中展示的数据以外,乌骨类动物的其它可食组织中也含有相当高的黑色素;例如,黑色骨骼肌中的尺侧腕屈肌的黑色素可占其在乌骨鸡中总量的3.19%[42]。

表1 一些动物组织或器官中黑色素的含量Table 1 Melanin content of some animal tissues or organs
一般而言,绝大多数天然动物黑色素不溶于水,但是也有少量能存在于水基介质中的黑色素。例如在山羊血清中发现有黑色素[41],墨鱼的墨汁中存在有大量的黑色素[41]。这些可溶性黑色素为膳食发展提供了一定的贡献。
1.2.3 功能特性及食用安全性 由于水溶性差和不容易降解,所以多数天然动物黑色素很难被人体消化吸收,但是随饮食摄入后,其在人体的肠胃系统中会停留一定的时间,因而对人体会产生一定的作用。有研究结果表明这类黑色素具有很强的抗氧化活性[43−44],可能具有强的抗氧化损伤或衰老的作用;海洋动物黑色素被发现具有抗炎症作用[45];动物黑色素具有螯合重金属离子的作用,因而具有抗化学损伤的功能;其还可能抑制肠胃系统溃疡病的发生[46]。动物黑色素是否具有其它方面的功能特性有待于进一步研究。
因为多数此类黑色素的水溶性和降解性较低,理论上而言,其对人体致毒的可能性比较低,文献中难以找到有关这类色素的毒性方面的实验科学评价信息,未来值得在这方面开展研究。
1.3 植物黑色素
相对于动物黑色素而言,植物体内天然形成的黑色素更为复杂。除了可能具有以酪氨酸为前体物质形成的黑色素以外[4],还可能含有以酚类化合物为前体物质在多酚氧化酶的作用下氧化而形成的黑色素。此外,还有花青素类黑色物质。关于食品或食品原料中具有黑色的此类物质的信息资料非常有限;有大量关于食品中由原花色素产生的具有各种不同颜色的花青素的研究报道[47−48],天然食品原料或加工食品的颜色可能有各种花青素或原花色素贡献的复合色,这类色素经深度氧化后也可能产生黑色素;原花色素是由含有儿茶酚(邻苯二酚)单元的儿茶素或表儿茶素为基础单元组成的高分子酚类化合物等。
关于一些黑色植物食品例如黑豆、黑米、黑麦中本身具有黑色的物质的组成及结构研究资料很有限。一般而言这些黑色食品中的花青素含量相对较高,其深度氧化后也可能变成黑色素,这对组成和结构研究应该会有一定的启示作用,也难以找到关于在这些食品中黑色素的含量及其功能评价等方面的实验研究报道,未来值得加强上述方面的研究工作。
1.3.1 酚类氧化形成的黑色素 不以酪氨酸为前体物质的植物黑色素形成途径较为多样化,其主要涉及以酚类化合物为前体物质的氧化过程。根据形成机制不同,分为酶促和非酶促作用形成的黑色素。
关于酶促作用下形成的黑色素,学者普遍接受在植物酚类(多酚)氧化酶的作用下形成黑色素的机制。常见的有以儿茶素为前体物质形成的儿茶素类黑色素或异黑色素(allomelanin),关于儿茶素在多酚氧化酶作用下形成黑色素的过程展示于图3。儿茶酚(邻苯二酚)还可以由苯酚氧化而得。除了图3所示的途径以外,酚类氧化成醌类后可与含硫化合物(R’-SH;例如半胱氨酸、谷胱甘肽)反应在铜蓝氧化酶(laccase)作用下或进一步与O-醌反应形成黑色的或褐色的高聚物,与水反应并进一步与O2或O-醌反应在多酚氧化酶作用下形成深色的高聚物。
关于非酶促作用形成的黑色素,酚类氧化成醌类后可与氨基酸、低聚肽或蛋白质反应并进一步与O2或O-醌反应形成深色的高聚物。根据反应程度不同或氨基酸等反应物的不同,可能产生黑色的高聚物,也可能产生其它类深色化合物。
1.3.2 组成及结构 酚类氧化而形成的黑色素不含氮、硫等,其具体的组成非常复杂,目前现有的研究结果尚难以完全揭示其组成与结构。除了如图3以儿茶酚为前体形成的黑色素外,还有以其它酚类例如咖啡酸为前体物质形成的黑色素。

图3 推导的儿茶酚黑色素的形成机制Fig.3 Predicted mechanism of forming catechol melanin
在这方面已进行大量的初探性研究。对此类黑色素进行组成和结构研究时,一般采用碱提酸沉的方法予以初步纯化,得到能溶于碱不溶于水、有机溶剂和酸的、有光泽的黑色粉,然后通过强氧化剂例如溴水、高锰酸钾或双氧水分解,得到失去原来颜色的物质[49]。这种物质不溶于稀氯化铁溶液中,但能溶于高浓度氯化铁溶液,鉴定发现其含有醌型和酚型化合物[13]。有研究利用紫外-可见光分光光度计辅助确证不同来源黑色素的结构特征,其在190~300 nm有最高吸收峰[50]。此类黑色素中的脂肪族烃基、芳香烃骨架和酚型或醌型碎片可用傅里叶变换红外光谱仪鉴定;芳香环上的碳、氢、连接氮或氧的甲基或亚甲基、连接吲哚基的氨基、烷基碎片可用核磁共振予以鉴定;半醌自由基可用电子顺磁共振波谱法鉴定[51];此外,可用分光光度法对以下的一些植物组织中的黑色素组成/结构进行过初步分析:西瓜籽、葵花籽、荞麦、葡萄籽、番茄籽、桂花籽、夜茉莉籽、芝麻籽、甘薯(紫色)、黑芥籽和油菜籽、板栗、大蒜、燕麦和大麦[13,52−59]。飞行时间质谱(MALDI-TOF MS)显示,燕麦黑色素是由p-香豆素组成的单一高聚物;含有3~9个单元[13]。
此类黑色素的结构也较为复杂,至目前为止完全揭示其具体结构的研究报道仍然很有限。或许未来在这方面值得进行较为深入的研究。
1.3.3 在可食性植物组织中的含量 几乎难以查找到关于此类黑色素在各种植物性食品中的含量的直接测定值。因其由酚类化合物氧化而产生的,所以在酚类化合物含量高的食品中此类黑色素的含量可能会高。这跟酚类化合物暴露在空气中的程度有关,因此,不同的加工方法可能得到黑色素含量不同的食品。例如,马铃薯、苹果等被切开或打碎后很快就会变成黑色或黑褐色。
虽然关于一些植物组织中黑色素的含量报道较少,但是有一些有关其提取率方面的结果发表。例如,自红茶中能提出约2 g/100 g黑色素,自黑豆中能提出约0.17 g/100 g黑色素[60];焙烤过的咖啡中能提出约25 g/100 g[61],其中有一部分是此类黑色素。
1.3.4 功能特性及食用安全性 涉及以酚类化合物为前体物质形成的黑色素的功能特性方面研究文献资料较少,特别是对应于精确结构的功能研究结果信息更为有限。例如,用碱提、酸解和重复沉淀制得的红茶黑色素类似物被发现具有促进免疫功能的活性[62],来源于茶叶[63]和咖啡[64]等的黑色素具有强抗氧化活性和保护大脑功能,杏子类黑色素能通过阻止线粒体氧化和膜去极化而防止氧化型内皮细胞死亡[65],来源于黑种草(Nigella sativa)籽的黑色素具有预防肠胃溃疡的作用[46],来源于茶叶[66]、葡萄[67]和黑种草[68]等的黑色素具有保护肝脏的作用,来自于黑豆和黑芝麻中不含蛋白质的黑色素被发现具有抗肿瘤的作用[69],来源于黑种草[70]和葡萄[67]的黑色素具有抗炎症作用。
在过去已发表的文献中可以找到大量关于抑制此类黑色素生成的研究报道[71],主要集中于对酶促褐变抑制方法的研究,即开发多酚氧化酶抑制剂。例如,用生姜萃取物和桂皮油抑制多酚氧化酶以阻止蔬菜和水果褐变[72];用辣椒、洋葱和菠萝萃取物抑制生姜多酚氧化酶的活性[73],还有通过抑制多酚氧化酶制止蔬菜和水果褐变的综述性文章[74]。这可能主要是基于对感官性质影响的考虑。黑变或褐变后对人体健康是有利还是有害,可能取决于所形成黑色素的组成与结构。需要注意的是:黑变或褐变可能是有害微生物生长的标志,这种变化可能会伴随有其它有害变化(例如压榨油或腊肉变黑可能伴随有苯并芘(Benzopyrene),即一级致癌物的产生)等。总之,在这方面的研究还不是很充分,或许未来应该加强这方面的实验研究工作,关于抑制和加强此类褐变谁更有利的争议仍将继续。
1.4 食用菌类黑色素
从食用菌中也能分离出以多巴或酪氨酸为前体物合成的黑色素,其合成途径和分子结构组成与前述的基本类似(见“1.1”和“1.2”)。此外,还能分离出含硫的黑色素。在黑木耳中,还发现有以1,8-二羟基萘(DHN)为基本单元形成的黑色素,1,8-二羟基萘由1,3,6,8-四羟基萘转化而来。还有一类只在蘑菇或其它担子菌中发现的黑色素,其以4-氨基苯酚(PAP)或谷氨酰胺-4-羟基苯(GHB)为前体物合成的。
1.4.1 GHB-黑色素 这类色素又称为PAP-黑色素。芳香环最初来源于分支酸,其转化成4-氨基苯酚后,与谷氨酸结合形成谷氨酰胺-4-羟基苯,在酪氨酸酶的作用下逐步转化成醌类化合物后聚合成黑色素。图4展示了其形成机制。此类黑色素主要由2-羟基对亚基苯醌(2-HpIBQ)为基本单元聚合而成,但是有少量的中间体,即4-谷氨酰胺基二羟基苯(GDHB)和4-谷氨酰胺基苯醌(GBQ)参与到最终形成的黑色素分子中。
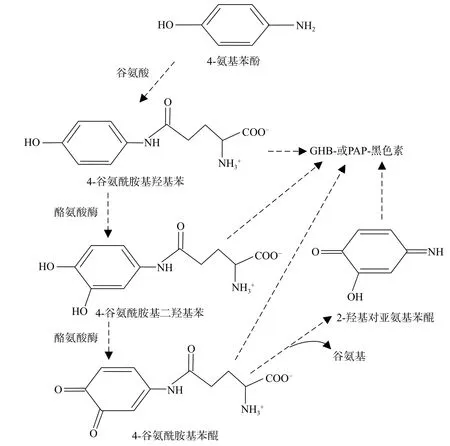
图4 GHB-黑色素的形成机制Fig.4 Mechanism of forming GHB-melanin
1.4.2 组成及结构 关于菌类黑色素的具体组成和结构非常复杂,缺乏对其进行完全揭示的科学数据。但是,文献中能找到给出部分相关信息的研究报道。例如,黑木耳黑色素中含41%碳、5%氢和1.6%氮(含S少);可能是DHICA/DHI-和 DHN-类黑色素的混合物;关于DHN-类黑色素和含硫黑色素的结构式也有建议[72]。对于鸡枞菌(Termitomyces albuminosus)中的黑色素的结构用扫描电镜(scanning electron microscopy)、元素分析、紫外-可见分光光度计、傅里叶变换红外光谱(Fourier transformed infrared spectroscopy)、电子顺磁共振(electron paramagnetic resonance)和13C(CP/MAS)核磁共振进行过表征研究,这种纯黑色素中含有碳、氮、氧和硫[75]。
1.4.3 在食用菌组织中的含量 在一些黑色的食用菌或某些食用菌组织中,黑色素的含量相对很高。例如,黑色素在黑木耳中的含量可以高达10%。黑色素在双孢蘑菇(Agaricus bisporous)和四孢蘑菇(Agaricus campestris)的孢子壁中的含量分别高达26%~28%和24%~26%[75]。
1.4.4 功能特性及食用安全性 关于食用菌中特有的一些黑色素的功能性质评价研究结果相对不多。但是,其肯定具有较强的抗氧化性。有研究认定食用菌具有降血压、调节免疫力、降血脂、抗癌、抗炎症或抗菌作用[76],这些功能是否全部或部分由其特有的黑色素贡献的尚待进一步实验研究。
关于来源于食用菌的黑色素的食用安全性的评价研究资料或结果仍然有待于加强。但是,考虑到原料被长期食用而没有出现中毒现象,此类黑色素能被安全食用的可能性很大。实际应用中需要注意的是:有研究认为DHN-黑色素可以具有毒性[77],应当加强其监测工作,未来值得加强获取其食用安全性方面数据的实验研究。
1.5 细菌黑色素
一般而言,在动物、植物食品和食用真菌中能发现的黑色素也可能存在于细菌中。此外,细菌中还有可能形成2,5-二羟苯乙酸(HGA)-型黑色素,其生成途径如下:酪氨酸在转氨酶的作用下变成p-羟基-苯酚基丙酮酸,然后在对羟基苯丙酮酸双加氧酶作用下转化成2,5-二羟苯乙酸(HGA);在缺乏高龙胆酸双加氧酶活性的情况下受铜蓝氧化酶或其它酚氧化酶的作用将2,5-二羟苯乙酸转化成p-醌;p-醌可进一步转化成2,5-二羟苯乙酸二聚合体;2,5-二羟苯乙酸、p-醌或2,5-二羟苯乙酸二聚合体可转化成2,5-二羟苯乙酸(HGA)-型黑色素.
1.5.1 组成及结构 与前面所述其它类黑色素一样,至今为止,细菌类黑色素的组成与结构也没有完全被理解或揭示清楚。这主要受其不溶于水的限制,不破坏其原始结构很难将其萃取出来。不过,学术界对揭示细菌类结构也作了一些初步探索。例如,采用扫描电镜、紫外-可见分光光度计、傅里叶变换红外光谱和核磁共振对淡青链霉菌(Streptomyces glaucescensNEAE-H)黑色素的结构进行了表征[61]。
1.5.2 功能特性及食用安全性 至今为止,对于细菌类黑色素的功能性质的研究非常有限。这类黑色素中有一部分是无毒的,即可以被安全食用。此外,有少量关于此类黑色素的生物活性方面的研究,例如,自淡青链霉菌中分离纯化出来的黑色素具有抗氧化性和抗癌性[78]。
2,5-二羟苯乙酸(HGA)-型黑色素可能是致毒的,因此在利用细菌生产应用于食品中的黑色素时,应该充分考虑其存在的可能性,如果存在就需有合适的方法予以除去或脱毒。过去对于此类毒素的研究动力主要是源于了解其毒性的欲望。未来在细菌黑色素的功能性质或生物活性、毒性评价和脱毒方面加强研究具有很好的前景。
1.6 昆虫黑色素
对于昆虫黑色素方面的研究相对于动植物或甚至微生物黑色素而言较为有限。一般认为昆虫黑色素是以酪氨酸或多巴为前体物质而形成的,但是相比较而言,具有不同的途径。一种典型的昆虫黑色素形成途径如下:酪氨酸→多巴→多巴胺→N-乙酰-多巴胺→N-乙酰-多巴胺醌→黑色素[79]或见图5。
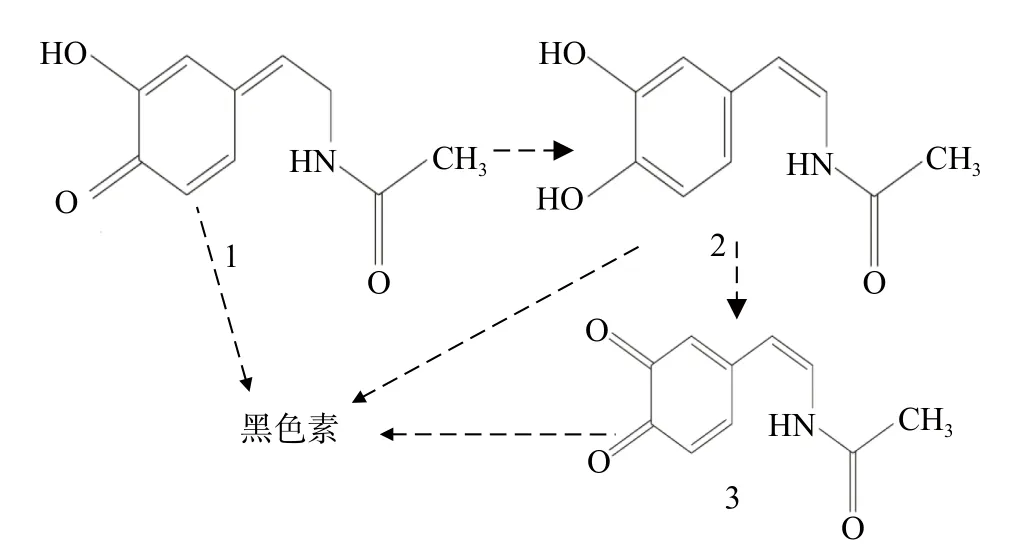
图5 N-乙酰-多巴胺醌异构成亚甲基醌中间体以后形成黑色素机制Fig.5 Mechanism of forming melanin after N-Ac-Dopamine tautomerized to a quinone methide
关于此类黑色素在可食昆虫(如蚂蚁)中含量的数据、组成与结构、功能性质或生物活性、食用安全性方面的数据都很有限。未来值得在这些方面加强实验研究。但是,近年来对存在于可食用昆虫-黑兵蝇幼虫(Black Soldier Fly,Hermetia illucens)[80]中的黑色素有较为广泛的研究,内容涉及抗氧化性等功能性质[81]、抗菌活性[82]和物理化学性质/抗氧化性[83]等。
2 美拉德反应生成的黑色素
食品中含有的还原糖性基团例如葡萄糖的醛基、果糖的酮基、及其它类有机化合物的羰基可以与自由氨基例如氨基酸、多肽或蛋白质中的氨基发生羰胺反应,并进一步发生系列聚合反应而最终形成黑色素。这种反应主要发生在对食品进行蒸煮、烘烤等热加工处理过程中。虽然有大量关于此类反应的研究报道[84],对其反应机理也有大量的探索[85−86],但是至今对于其终端产物-黑色素的结构仍然没有完全了解。
2.1 在食品中的含量
美拉德反应生成的黑色素在未经加工的食品原料中含量很少,但是它在经过热加工处理的食品,尤其是富含还原糖和氨基酸或肽或蛋白质的食品中含量却较高。例如,咖啡、可可粉或可可饮料、面包、松饼或蛋糕、其它烘焙食品、早餐谷物或麦片、烹饪过的肉、制麦芽、蜂蜜、加工牛乳(尤其是高温灭菌乳)、黑啤、深色酒或甜葡萄酒、香醋、加工番茄、烤土豆、酱油都含有一定量的此类黑色素。此类黑色素在咖啡饮料干物质中的含量约为7.2%~35%[87−89]、在面包皮中的含量为14%~30%[90]。此类黑色素在部分其它加工食品中的含量如下:含55%可可粉的巧克力约15%、100%可可粉约22%、饼干10%~20%、早餐谷物约25.5%、全面包1.6%~6.0%、占传统香醋干物质的74%~93%、大麦咖啡约1.44%、每100 mL啤酒0.06~10.4 g、每100 mL甜葡萄酒11~17 g[91]。
2.2 功能特性及食用安全性
关于此类黑色素(一种不溶于水的黑色素蛋白复合体)通过化学保护机制抑制肠胃癌发生的研究始于2002年[92],当时以面包皮为原料进行了实验,结果证明有效。2003年,用饼干中的水溶性黑色素蛋白复合体做实验,也证明其具有抗癌潜力[93]。2005年,以面包皮和制麦芽为原料做实验证明其所含的黑色素蛋白复合体有抗癌性[94]。2011年,咖啡黑色素被实验证明具有抗癌潜力[95]。2014年,对不同来源黑色素的抗癌潜力进行了比较研究,结果证明咖啡黑色素最具潜力[96]。
除上一段中所述的以外,此类黑色素还具有其它多种功能特性。比如较强的抗氧化性。存在于膳食例如面包皮、咖啡和黑啤中的此类黑色素能提高低密度脂蛋白的氧化稳定性;过去研究得最多的是咖啡(一种典型的黑色素饮料)中的黑色素,其具有防止DNA氧化损伤的能力[97];由于此类黑色素不能被消化吸收,所以它可能具有膳食纤维功能,其结构特征在一定程度上类似于含有阿魏酸的阿拉伯木聚糖,其在肠道内可能被发酵[91,98];自咖啡、啤酒和甜葡萄酒中分离出来的纯黑色素具有血管紧张素转化酶(ACE)抑制活性[99]。此外,从葡萄糖-氨基酸反应产物中纯化出来的黑色素也具有ACE抑制活性[100]。因此,此类黑色素具有降低血压的潜力,螯合金属离子的作用。因此此类黑色素对于食品中可能有的重金属污染具有消除毒性的作用[101−102]、抗菌和抗炎症的作用。当然,这种作用与黑色素的具体组成和结构、浓度、形成条件、培养基pH和温度、以及分子量(一般高于1000 Da的抑菌活性高于低分子量的)有关[95,103];最新研究表明咖啡和面包中存在的黑色素具有降低能量摄入量的作用[104]。尽管自日本黑醋中分离出一种黑色素是否美拉德反应生成的尚待进一步研究,但是它具有抑制脂肪细胞或组织形成的作用[105]。咖啡黑色素具有保护细胞的作用[106]。
关于此类黑色素的食用安全性方面的资料较为有限。既然此类黑色素具有螯合金属离子的作用,那么就应该在应用的过程中注意避免引起微量矿质元素缺乏的问题。另外,美拉德反应过程中可能产生具有致基因突变的物质,但是关于其终端产物-黑色素在这方面的作用尚需可靠的科学证据。在制作和应用此类黑色素时应该严格控制各方面条件,尤其需要严格控制杂质含量,以避免风险,或许分离和纯化此类黑色素后再评价其食用安全性是一种好的方法。
3 焦糖色素
焦糖色素属于人造黑色素,其颜色为黑褐色至黑色,形态为液体或固体,气味有烧焦的糖味,食味令人愉悦但略带苦味。目前此类色素被大量地应用于某些加工食品或饮料(例如可口可乐、啤酒)中。
一般将糖与碱或酸混合一起加热通过醛和酮缩合反应聚合而成。氨型焦糖色素通过美拉德型反应制得,即羰基与氨基或氨反应形成的黑色素。硫酸盐型焦糖色素也是美拉德型高分子聚合物。 目前生产的有四类焦糖色素:焦糖色素I(不能用氨或硫酸盐制作,又称为酒焦糖)、焦糖色素II(用硫酸盐但不用氨制作)、焦糖色素III(用氨但不用硫酸盐制作,又称为啤酒焦糖、面包或糕点焦糖)、焦糖色素IV(使用硫酸铵制作,软饮料焦糖或耐酸焦糖)。
关于焦糖色素的功能性质或生物活性方面,有研究证明其具有抗氧化活性[107−110]。至今为止,难以找到其它功能性质方面的科学研究证据,值得进一步加强相关研究。
在焦糖色素的食用安全性方面,目前对于焦糖色素I还没有可接受摄入量设定值,其它焦糖色素的可接受摄入值(mg/kg体重)如下:焦糖色素II 0~16、焦糖色素III 0~200、焦糖色素IV 0~200[110−111]。
4 结论
黑色素品种繁多,形成机制也是多种多样,这主要与酪氨酸酶和多酚氧化酶的催化活动有关。酶促生成的天然黑色素存在于许多动物、植物、微生物(尤其是真菌)、昆虫食品或原料中;美拉德反应形成的黑色素广泛地存在于许多加工食品中。目前虽已对于各类食品原料或食品中以及一些热加工食品存在的黑色素的形成机制、黑色素结构进行了大量的探索,也提出了普遍接受的模式,但是由于其非常复杂,尚需更多的和可靠的科学数据以将其完全揭示出来。
在黑色素的功能性质或生物活性方面,已开展了大量研究。现有研究结果证明其具有以下几方面的功能特性:抗氧化性、抗癌性、抗菌和抗炎性、降血压或血脂性、保护肠胃系统、螯合金属离子。酚类氧化形成的色素还被证明有护肝和调节免疫功能的作用。除了抗氧化性以外,对于常用于加工食品或饮料的人造焦糖色素是否具有其它方面功能性质尚需可靠的评价结论,在这方面仍有广阔研究前景。
在食用安全性方面,根据长期饮食实践应该可以推定食品中存在的绝大多数黑色素是安全的。虽然在形成或生产黑色素的过程中可能伴随有致毒因子产生,并且有部分天然形成的黑色素具有毒性,但是对于各种食品或食品原料中的黑色素或人造焦糖色素本身是否具有毒性尚无相关方面的研究证据,未来值得在各种黑色素的纯化和毒性评价方面进一步开展实验研究。
