PEComa临床病理分析与影像诊断
2022-05-10张泳欣肖学红唐秉航黎卫黄红星袁润强卢扬柏
张泳欣 肖学红 唐秉航 黎卫 黄红星 袁润强 卢扬柏
1中山市人民医院影像中心,中山 528403;2中山市人民医院泌尿外科,中山 528403
血管周上皮样细胞肿瘤(perivascular epithelioid cell tumor,PEComa)属于较为罕见的间叶源性肿瘤,由具有特殊的组织学和免疫组织化学特征的血管周围上皮样细胞组成。2002年,世界卫生组织(WHO)将PEComa定义为“由组织学和免疫组织化学上独特的血管周上皮样细胞组成的间叶性肿瘤[1]。PEComa可分为良性、恶性、恶性潜能3类,以良性居多,好发于女性[2]。PEComa可发生于肾、肝、肺、子宫、卵巢、胃肠道、胰腺、前列腺和软组织等部位。据文献查阅,涉及肾脏恶性肿瘤的PEComa研究仍然很少[3-5]。笔者收集2010—2021年中山市人民医院确诊的1例肾脏恶性PEComa,结合2000—2021年期间中国知网(CNKI)、万方数据库报道的文献探讨其临床表现、病理及免疫表型特点、诊断与鉴别诊断、治疗及预后,旨在提高对本病的认识。
资料与方法
1、临床资料
回顾性分析2021年12月30日中山市人民医院收治的1例肾脏恶性PEComa患者的临床病理特点,经病理科最终确诊,符合WHO对PEComa的诊断分类。在CNKI、万方数据库搜索2000—2021年期间,关键词:“肾脏”“上皮样血管周细胞肿瘤”“血管周上皮样细胞肿瘤”“PEComa”文献,总共得到18篇文献,239例患者,明确指出恶性的有20例,所有病例均进行不定期随访。
2、方法
2.1、扫描方法 采用Siemens Somatom 256排螺旋CT扫描仪(德国),嘱患者仰卧,扫描范围自膈顶至双侧髂前上棘水平。行平扫及增强扫描,扫描参数如下:管电压120 kV,管电流200~300 mA,层厚5 mm,层间距5 mm,重建层厚1 mm,重建矩阵256×256。增强扫描:经肘正中静脉注射对比剂1.5 ml/kg体质量,流率3.0~3.5 ml/s。6例在注射对比剂30 s、60 s、300 s时行皮髓质期、实质期及排泄期增强扫描。将原始数据传输至CT机配套后处理工作站进行处理。
2.2、病理检查方法 采用4%中性甲醛液固定,常规脱水,经石蜡包埋后切割成4~5μm切片,经苏木精-伊红染色(HE染色)后用光镜观察。免疫组织化学染色采用En Vision两步法,具体步骤参照说明书进行。所用抗体黑色素瘤相关抗原(HMB45)、T细胞识别的黑色素瘤抗原(Melan-A)、酸性钙结合蛋白(S100)、锌依赖性细胞膜金属蛋白酶(CD10)、Ki67等及En Vision试剂盒均购自福州迈新生物技术开发有限公司。
3、图像分析
由2位经验丰富的影像诊断医师(1名主治医师和1名副主任医师)进行阅片、分析及记录,并与相关专科医生讨论达成一致。影像学评价包括肿瘤的位置、大小、形态、密度、强化特点、有无钙化及液化坏死、肿瘤边缘、是否有子灶、是否转移及其与周围组织关系。
结 果
1、临床资料特点
本例患者为女性,58岁,在2021年11月无明显诱因出现腹胀而检查发现病变。回顾文献资料,一共239例患者,男54例(22.6%)、女185例(77.4%),其中20例明确指出恶性;临床表现无特异性,常见的临床表现为腰痛、腰胀;其次是体检偶尔发现;再者较少见的就诊原因为肿瘤破裂出血急诊就诊、血尿、腹部包块、其他地方病变检查无意中发现等。本例患者位于左肾,经腹腔镜病灶根治术切除,术后病灶经病理证实为恶性PEComa,本研究病例在随访期内,未见转移或复发。
2、影像学表现
肾脏恶性PEComa的影像学表现具体见图1。
3、病理特点分析
镜检:肿瘤细胞呈泡巢状、乳头状增生,肿瘤中见由小的薄壁血管构成网状结构,肿瘤中央可见大片坏死。瘤细胞多角形,胞浆嗜酸,部分透明。细胞核圆形或卵圆形,染色质增多,核仁明显,周围纤维组织增生,纤维化、玻璃样变及钙化。免疫组化:Ki67 10%+、细胞角蛋白(CK)-、高分子量细胞角蛋白CK(HMW)-、P63-、CD10散在+、碱性细胞角蛋白(CK7)-、Ⅲ型受体酪氨酸激酶(CD117)-、a-甲基酰基辅 酶A(AMACR)-、转录因子E3(TFE3)-、波 形 蛋白(Vimentin)+、HMB45+,Melan-A+,S100-,细胞周期蛋白依赖激酶4(CDK4)-,鼠双微体基因2(MDM2)-,突触素(SYN)-,嗜铬素A(CgA)-。具体见图1G。
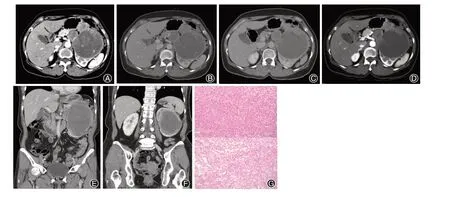
图1 肾脏恶性血管周上皮样细胞肿瘤患者的影像学表现及病理特点分析。A~F为左侧腹膜后见分叶状巨大肿块,密度混杂,内侧成分房状改变,可见实性成分及斑点状钙化灶,实性成分轻度强化,病灶最大截面约98 mm×96 mm,与左肾及胰尾分界欠清,其余周围结构受压改变,腹膜后未见明显肿大淋巴结未见腹水征象;G为病理切片(HE染色 ×100)
讨 论
1、发病机制
PEComa是罕见的间叶性肿瘤,1996年Zamboni等[6]首次将其报道并命名。许多人努力研究这些肿瘤在多潜能原始细胞中的起源,特别是那些位于血管周围区域的细胞。最近,人们提出了几个假设[7]。一种理论认为,能够表达黑素细胞和平滑肌表型的神经嵴未分化细胞代表PEComa细胞的起源。其次,有人提出PEComa可能来源于周胞质元素。此外,有研究认为PEComa起源于成肌细胞和平滑肌,并具有获得性黑素细胞标志物表达[8]。
2、病理特点
组成PEComa的上皮样细胞呈放射状排列分布于血管周围,胞浆透明至嗜酸性,常表达黑素细胞和肌源性标记物[9]。由于PEComa的罕见性,直到2010年才制定出区分良性和恶性肿瘤的诊断标准[10]。Folpe等[11]提出了目前被接受的良性、恶性潜能或恶性PEComa的诊断标准:良性(直径<5 cm、低核级别、细胞密度低、有丝分裂率<1/50高倍视野、未见浸润/坏死/血管侵犯);以下标准出现其中一个考虑恶性潜能:核异型性、多核巨细胞以及大小≥5 cm;显示以下2种或多种情况的肿瘤被认为是恶性的:直径>5 cm、浸润性生长、细胞密度大、核大和着色过深、有丝分裂活性高、有丝分裂像不典型、合并凝固性坏死/血管侵犯等。
PEComa表达一种肌黑素细胞表型,其对黑素细胞和平滑肌标志物具有免疫反应性。已经证实HMB45和某些其他黑素细胞标记物是PEComa的免疫组织化特点[11-15];与其最相关的是小眼症转录因子(MTF)、Melan-A/Mart-1和HMSA-1[16]。大约70%的病例出现了平滑肌肌动蛋白(SMA)+、波形蛋白和/或结缔组织蛋白+、组织蛋白酶K+等[17-20]。Fadare等[21]在近期的文献综述中发现,在子宫出现的PEComa中表达的免疫组化指标及阳性百分比是HMB45 100%+,SMA 73%+,波形蛋白56%+,CD10 25%+,Melan-A 24%+,CD117 9%+,高度糖基化Ⅰ型跨膜蛋白(CD34)5%+,S100 3%+,角蛋白3%+等。其中,HMB45+为特征性表现。本研究病例及搜索到的文献HMB45均为阳性。
3、临床特征
PEComa好发于女性[21]。2004年WHO将其归为具有恶性的潜能[22]。有研究认为PEComa有1/3的病例会出现局部复发和/或远处转移[22]。恶性者的常见起源部位包括肾脏和腹膜后软组织,以及女性生殖道的子宫和宫颈[23]。恶性PEComa伴随着复发和/或转移,转移部位最常见的是肝脏[24-25]。
4、影像学表现
影像学表现缺乏特异性,CT、磁共振成像(MRI)、超声检查(US)和正电子发射型计算机断层显像(PET-CT)等影像学研究可以帮助检测肿瘤的位置、大小以及与周围组织的关系。术前影像学检查大多表现为混杂密度,边界相对清楚的病灶,增强后表现为明显强化,因此容易误诊为恶性肿瘤,在无邻近器官侵犯或局部转移的情况下,较难与良性者相鉴别,恶性者最常见的CT表现是内脏或腹膜后肿块边界清楚,与同层面肌肉相比,平扫为低/等密度,明显强化,需要注意的是,强化模式以不均匀强化更常见[24]。点状钙化相对少见。在MRI上,相对于同层面骨骼肌,大多数肿瘤T1WI表现为等/稍低信号。有研究提示,若病灶具有T2WI低信号,弥散加权成像(DWI)受限扩散,明显强化(快进快出)等特点,需考虑PEComa[26-27]。本例患者为位于左侧腹膜后的巨大分叶状肿块,密度混杂,内部见分房,可见实性成分(轻度强化)及斑点状钙化灶。林乐等[28]报道的10例肾血管周上皮样细胞肿瘤,大部分病例表现为B超高回声,CT下密度混杂[29-30]。
5、诊断
在病理学和影像学检查中,此类肿瘤很容易被误诊为肾细胞癌[31-32]。在图像上未发现脂肪的PEComa将难以与乏脂肪的血管平滑肌脂肪瘤的其他亚型以及肾细胞癌相鉴别[33]。肾细胞癌中的脂肪成分通常不明显,若合并钙化,则通常较大且粗糙。含有脂肪但无钙化的肾细胞癌极为罕见[34-35]。
影像学的某些表现对提示患者预后有一定价值,包括肿瘤大小、是否存在其他血管平滑肌脂肪瘤、是否有转移、淋巴结肿大、肾外侵犯、肾盂受累和肾静脉受累等[36]。Cui等[37]报告1例巨大肾PEComa伴巨大腹膜后转移性淋巴结病。在Froemming等[38]报道的9个病例中,术前CT和MRI显示肿大的淋巴结,其中1个被病理证明是转移性PEComa;另外5个病例中出现了向肾窦的延伸,这与肾细胞癌吞噬肾窦脂肪相似。
6、治疗
手术是PEComa的主要和最有效的治疗方法。恶性者除手术切除外,化疗和放疗效果仍不明确,预后差[39]。本病采用腹腔镜肾癌根治术(左侧)+胰腺部分切除+脾脏切除术+降结肠部分切除术+横结肠端侧吻合+腹膜后淋巴结清扫术+肠粘连松解术,在术后的随访期间内,暂无出现复发/转移,但无病生存期的长短仍需继续随访。
综上所述,原发性肾脏恶性PEComa是罕见的间叶源性肿瘤,组织学和免疫组化有一定特征,影像学检查具有一定的特点。鉴于恶性PEComa的发病机制和生物学行为目前尚不清楚,因此手术仍然是最佳治疗的主要方法。
利益冲突 所有作者均声明不存在利益冲突
