颈动脉内膜剥脱术后严重并发症2例报告及文献复习
2022-05-02张永建冉忠营赢1贵州医科大学研究生院贵州贵阳550004贵州省人民医院神经外科贵州贵阳550001
张永建, 尹 浩, 马 俊, 冉忠营, 谭 赢1.贵州医科大学研究生院,贵州 贵阳 550004;.贵州省人民医院 神经外科,贵州 贵阳 550001
颈动脉硬化狭窄是导致缺血性脑卒中的较常见原因之一,显著颈动脉狭窄的患病率是4.4%~7.0%[1]。颈动脉内膜剥脱术(carotid endarterectomy,CEA)是目前治疗重度颈动脉狭窄的常用手术方式,但术后一些严重并发症如何避免及处理,是手术医师必须重视的问题。本研究结合国内外文献对2例CEA术后严重并发症患者诊疗过程进行分析。现报道如下。
1 病例资料
例1,患者男性,59岁,因“体检发现右侧颈内动脉斑块10余天”入院。既往高血压病史10余年,长期规律服用非洛地平缓释片、厄贝沙坦片,血压控制可;糖尿病病史10余年,规律甘精胰岛素20 U皮下注射,控制血糖水平餐前7 mmol/L、餐后12 mmol/L。2019年4月28日患者头颈部CT血管成像(CT angiography,CTA)示右侧颈内动脉起始部混合性斑块,管腔重度狭窄(图1a)。2019年5月6日行“经右股动脉插管全脑血管造影术”, 术中发现右侧颈内动脉起始部重度狭窄(狭窄度73%),左侧颈内动脉起始部轻度狭窄(37%),左侧颈内动脉床突上段中度狭窄(45%)(图1b)。2019年5月10日8:00行“神经电生理监测下颈动脉内膜剥脱术”,显微镜下发现颈内动脉增生内膜导致其狭窄率>70%,肝素盐水冲洗并剔除剩余的增生内膜。颈总动脉后壁有一中膜破损可见外膜,予7-0 Proline线铆钉两针后好转,继续予7-0 Proline线连续缝合颈动脉切口。阻断时间约40 min,电生理监护全程未见明显相关参数变化。吲哚菁绿荧光造影提示颈总颈内颈外动脉通畅,术野无明显斑块。术毕于2019年5月10日10:33。术后麻醉预期苏醒不满意,呼之能睁眼,左侧肢体活动不利,肌力3级。复查头颈部血管CTA示右侧颈总动脉仅起始部部分显影、右侧颈内动脉全程未见显影(图1c)。CT脑灌注成像示右侧大脑半球脑梗死、局部存在缺血半暗带(图1d),考虑右侧颈内动脉切口处血栓形成。2019年5月11日00:10急诊行“经右股动脉插管全脑血管造影术、原切口右颈动脉取栓术、右颈动脉血栓介入抽吸机械碎栓术”,术中移动数字减影血管造影(digital subtraction angiography,DSA)示右侧颈内动脉颈外动脉起始部开始完全闭塞(图1e)。遂原切口显露右侧颈内动脉起始部,清除颈动脉血栓凝血块约8 ml,向上一直探查清除凝血块。使用Guiding导管经软导丝进入颅内海绵窦段,发现从该部位开始一直到眼动脉段显影不清,疑是多发血栓,予导管抽吸导丝机械碎栓,最后右侧大脑前、大脑中动脉可以显影,观察10 min血流稳定但仍纤细。术毕患者双瞳圆形等大,光反射迟钝。术后患者呈昏睡状,长期卧床。术后第8天(2019年5月19日)复查头部CT示右侧大脑半球脑组织肿胀并大片状低密度影,考虑脑梗死(图1f)。术后1月余,患者家属放弃治疗,经电话随访家属告知患者出院后于家中死亡。
例2,患者男性,71岁,因“头昏3年,加重3周”入院,既往高血压病史6年余,血压控制欠佳(具体降压药物及量不详)。2021年4月18日头颈部CTA示双侧颈总动脉分叉处、双侧颈内动脉起始部见多发钙化及非钙化性斑块,右侧颈内动脉起始处管腔重度狭窄-近似闭塞,左侧颈内动脉起始部管腔重度狭窄(图2a)。2021年4月22日磁共振灌注加权成像(perfusion-weighted imaging,PWI)见右侧大脑半球脑血流量(cerebral blood flow,CBF)、脑血容量(cerebral blood volume,CBV)减低不明显,平均通过时间(mean transit time,MTT)、达峰时间(time to peak,TTP)明显延长,提示右侧大脑半球慢性脑缺血改变(图2b~e)。2021年4年28日16:03行“脑氧监测下右侧CEA、颈动脉补片扩大成形术”,术中见颈动脉分叉部有一明显斑块,予剥离颈动脉增生内膜,颈外动脉增生硬膜,最后切断颈总动脉增生内膜。发现颈动脉增生内膜加之颈内动脉纤细导致其狭窄率>90%。肝素盐水冲洗并剔除剩余增生内膜。予7-0 Proline线缝合切口,并取一块人工血管补片修补扩大成形颈内动脉。血压维持约120 mmHg(1 mmHg=0.133 kPa),脑氧监护全程未见明显相关参数变化。2021年4月30日术后第2天复查头颈部CTA示原右侧颈内动脉起始处混合斑块未见显示,右侧颈内动脉管腔未见明显狭窄(图2f);头颅CT示右侧额叶出血并溃入双侧侧脑室(图2g);CT脑灌注成像见右侧额叶异常灌注,其MTT、TTP明显延长,CBF、CBV增高(图2h~2k)。考虑右额脑出血,向患者家属交代相关情况后家属拒绝手术治疗,遂予加强脱水、对症等支持治疗。术后23天(2021年5月21日)复查头颅CT示右侧额叶出血较前吸收(图2l),好转出院,术后随访患者无不适症状。
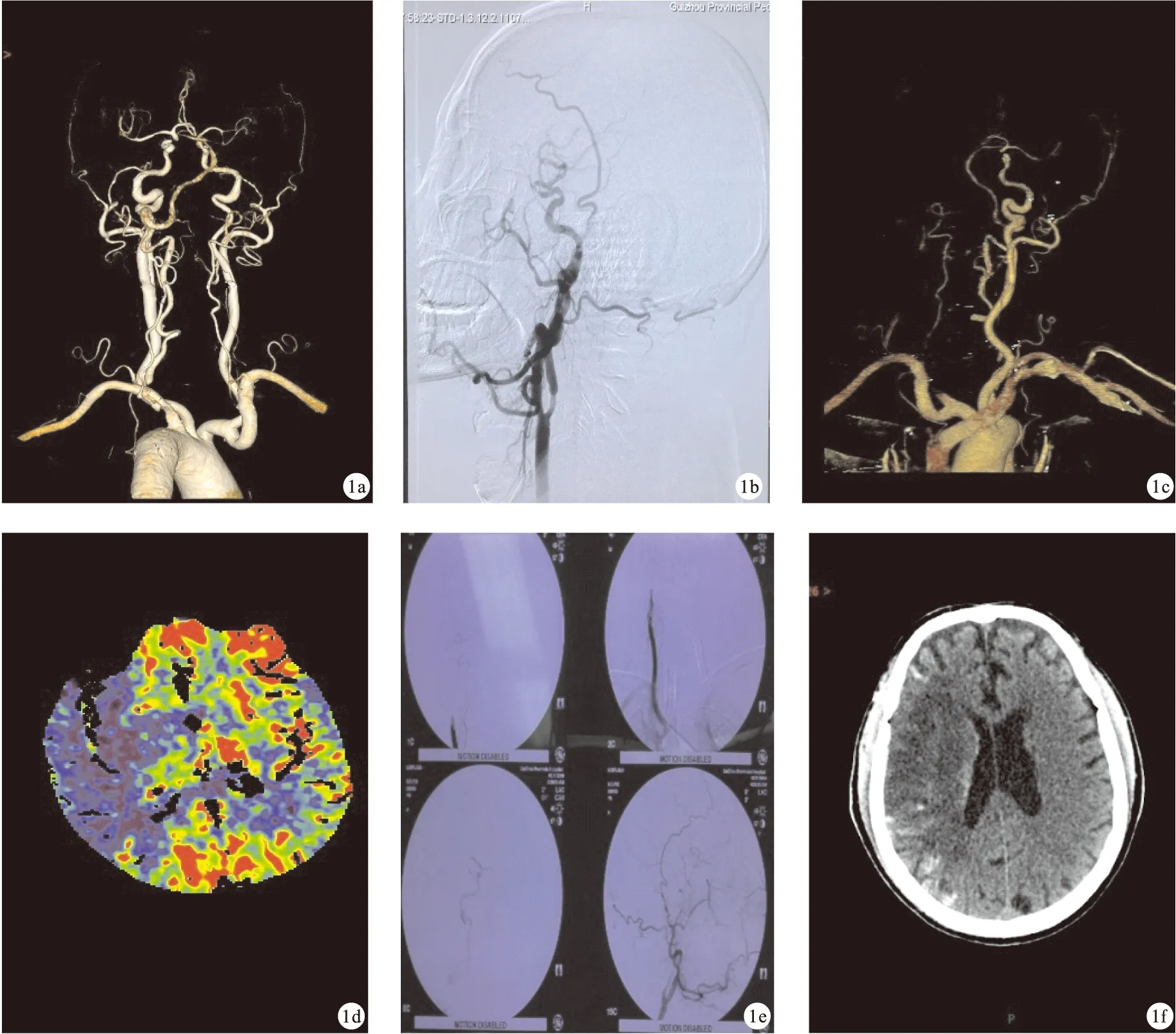
图1 例1患者术前、术中、术后部分影像学图像[a.头颈部CTA示右侧颈内动脉管腔重度狭窄;b.全脑血管造影术见右侧颈内动脉起始部重度狭窄(狭窄度73%);c.术后当日复查头颈部CTA示右侧颈内动脉全程未见显影;d.术后当日复查CT脑灌注成像示右侧大脑半球脑梗死;e.术中移动DSA示右侧颈内动脉颈外动脉起始部开始完全闭塞;f.术后第8天复查头颅CT示脑梗死]
2 讨论
CEA术后急性血栓形成是一种罕见的并发症。其原因,如术中内膜损伤、血管剥离、颈动脉内膜瓣或继发于颈动脉的闭合狭窄[2]。例1患者术中发现颈总动脉后壁有一中膜破损,并予7-0 Proline线铆钉两针,可能因异物反应导致血管腔内血栓形成。其次抗血小板治疗不足也可致使术后急性血栓形成,术前3日,依照2015版CEA指南[3]予停氯吡格雷改为阿司匹林单抗治疗,且术后经询问患者因术前禁食禁饮,在手术当日未服用阿司匹林,致使抗血小板治疗不足。有研究表明,早期实施双重抗血小板治疗不仅可减少有症状患者CEA前脑事件的复发,亦可降低术后早期颈动脉血栓形成引起卒中的发生风险[4]。血流动力学也是CEA术后急性血栓发生的一大因素,该患者糖尿病病史10余年,长期甘精胰岛素20 U降糖治疗,血糖仍控制不佳,血液处于高凝状态。早期识别和立即手术决定了CEA术后急性血栓形成患者的预后[5]。CEA术后急性血栓形成临床失代偿通常发生于术后2~72 h,表现为严重神经功能缺损的急性发作,较具特征性的是手术侧对侧的重度偏瘫[6]。虽然有研究显示,即使在缺血性卒中发生后6 h以上,血管内血栓清除术仍是有效的[5]。但大多数意见更偏向于对于术后伴有神经功能缺损的卒中患者立即行手术探查,而非颈动脉造影。本例患者在CEA术后出现神经功能缺损的急性发作时,行CTA及CTP检查已经提示右侧颈内动脉切口处血栓形成,但由于缺乏相关诊疗经验先进行了经右股动脉插管全脑血管造影术,这是一个耗时的诊断程序。从本例患者处置流程上看,对于一旦确诊的患者应立即行再手术探查并取出血栓以快速重建脑血流,最大限度地挽救神经功能,待清除血栓后再行脑血管造影。目前,经颅多普勒(transcranial doppler,TCD)等监测技术已被证明在颈动脉手术干预中是有效的[7]。TCD的早期干预可降低与颈动脉血栓这一并发症相关的发病率和病死率,因此在今后的临床工作中,应加强围术期TCD的监测工作。

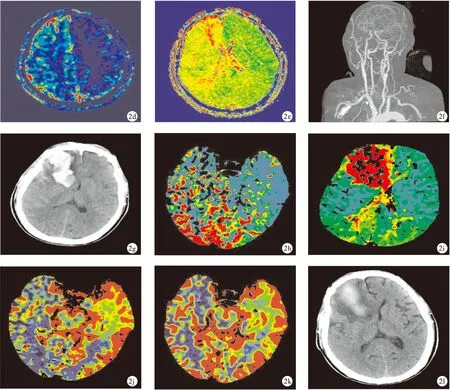
图2 例2患者术前、术后部分影像学图像(a.术前头颈部CTA示右侧颈内动脉起始处管腔重度狭窄,几近闭塞,左侧颈内动脉起始部管腔重度狭窄;b.术前磁共振脑灌注成像CBF图像;c.术前磁共振脑灌注成像CBV图像;d.术前磁共振脑灌注成像MTT图像;e.术前磁共振脑灌注成像TTP图像;f.术后第2天复查头颈部CTA;g.术后第2天复查头颅CT;h.术后第2天复查CT脑灌注MTT图像;i.术后第2天复查CT脑灌注TTP图像;j.术后第2天复查CT脑灌注CBF图像;k.术后第2天复查CT脑灌注CBV图像;l.术后第23天复查头颅CT图像)
术后脑高灌注是CEA后脑出血的重要原因,而长期脑缺血和抗凝治疗亦是其发生的危险因素[8]。脑高灌注综合征(cerebral hyperperfusion syndrome,CHS)是一种常发生于CEA术后5 d内严重的并发症,继发于脑血流动力学改变,自动调节障碍和压力感受器功能障碍是脑高灌注的主要机制。而长期的颈动脉阻塞疾病和低灌注引起的脑缺血也是术后脑出血的一大原因,因为其会导致脑组织产生大量活性氧和自由基,使同侧大脑动脉内皮细胞广泛损伤,血管扩张和脑血管通透性增加,自凝功能丧失,从而增加术后早期颅内出血的风险[9]。例2患者头颈部CTA见双侧颈内动脉起始部均为重度狭窄,加上长期高血压病史,平时血压控制不佳,已导致内皮功能障碍和微血管病变,脑自身调节功能受损,血脑屏障也受到了一定破坏。PWI提示右侧大脑半球慢性脑缺血改变,而CEA使先前长期缺血的脑区灌注过度,这一点通过术后脑灌注成像得以证实,可能为术后并发脑出血的首要原因。CEA术后脑出血与CHS相关病死率达36%~63%[10]。但CHS起初的水肿是可逆的,如果发展为脑出血,则预后很差。因此,早期识别CHS对防治脑出血有重要意义。术后动态复查脑灌注成像,一旦发现脑高灌注,及时予脱水降压治疗,能有效降低脑出血的发生率。围术期抗血小板治疗及术中肝素的叠加使用是否会增加脑出血的发生率仍有争议。例2患者高龄且双侧颈内动脉重度狭窄,因为有了例1的经验,因此围术期未停止双重抗血小板治疗,且术中使用肝素,可能也是并发脑出血的一个重要原因。虽然有研究表明,使用鱼精蛋白逆转肝素可减少CEA术后严重出血需再手术的风险,而双重抗血小板治疗与出血并发症的显著增加无关[4]。但综合本例患者脑出血的发生及抗凝治疗情况,仍需警惕围术期抗凝治疗诱发脑出血的风险。
综上所述,对于重度颈动脉狭窄患者CEA是必要的并且手术安全性较高,但一旦发生术后并发症则后果通常十分严重。从单中心临床经验来看,术后急性血栓形成罕见而危急,术中谨慎操作、围术期控制血糖、坚持双重抗血小板治疗、加强围术期TCD监测都是必要的;时间即是关键,一旦发现并发血栓形成,应尽早重建脑血流,改善预后。而对于并发颅内出血,脑高灌注是一个重要原因,加强监测是其防治的重要方法,而控制血压是有效的干预手段。通过加强围术期TCD监测、血压控制、脱水等措施,可降低CEA术后脑出血的发生率。
