4-芳基-3-羟基异噻唑衍生物的合成与生物活性研究
2022-04-27周聪伟林义峰郭林朝巨修练刘根炎
周聪伟,林义峰,郭林朝,肖 胜,巨修练,刘根炎
(武汉工程大学化工与制药学院 绿色化工过程教育部重点实验室 新型反应器与绿色化学工艺湖北省重点实验室,湖北 武汉 430205)
γ-氨基丁酸(γ-aminobutyric acid,GABA)是动物神经系统中一种重要的抑制性神经递质,通过作用于GABA受体(离子型和代谢型)而发挥生理功能[1-3]。离子型GABA受体(以下GABA受体均指离子型)属于一种配体门控氯离子通道,被GABA激活后通道打开,氯离子流入细胞内,从而产生抑制效应[4-5]。GABA受体是杀虫剂重要的作用靶标之一,也是目前绿色农药领域的研究热点之一[6-7]。
GABA受体可被多种类型的小分子配体拮抗,根据作用机制不同,一般可分为非竞争性拮抗剂(noncompetitive antagonists,NCAs)和竞争性拮抗剂(competitive antagonists,CAs)[7-8]。NCAs可直接影响氯离子通道的开放,阻滞氯离子内流,使神经兴奋不能得到有效抑制,最终导致昆虫死亡[9-11]。目前靶向GABA受体的商用杀虫剂均为NCAs。传统的GABA受体NCAs类杀虫剂如林丹和氟虫腈等,在20世纪末期被广泛使用,但由于对环境存在安全隐患,多数已被禁用或限制使用[12-14]。近年来,新型的NCAs类杀虫剂,如氟雷拉纳和溴虫氟苯双酰胺等被相继报道,其作用位点可能位于受体跨膜段的一个独特区域,有别于传统的NCAs类杀虫剂[15-16]。研究表明,氟雷拉纳和溴虫氟苯双酰胺对抗性昆虫活性高,且对非靶标生物的安全性好[17-18],作为绿色高效的农用杀虫剂具有广阔的开发前景。
作者所在课题组前期研究发现,昆虫GABA受体CAs可与激动剂竞争同一结合位点从而调节GABA受体的功能,表现出一定的杀虫活性[19-20],有潜力开发为作用机制新颖的新型杀虫剂,克服昆虫对现有NCAs类杀虫剂的抗性问题[21]。3-羟基异噻唑作为一种独特的杂环小分子,具有丰富的生物活性[22],在异噻唑环上引入不同取代基或构造双环,会大幅改变其药理活性。课题组前期研究证明,3-羟基异噻唑是设计昆虫GABA受体CAs的有效骨架结构之一,通过结构修饰所得部分衍生物对昆虫GABA受体的拮抗作用较为显著[23-24]。在此基础上,作者通过两步法[25]合成原料3-羟基异噻唑,对异噻唑环3位羟基进行保护后,通过N-碘代丁二酰亚胺(NIS)在4位引入碘,随后采用Suzuki-Miyaura偶联反应引入芳基,最后在强酸性条件下脱保护合成一系列4-芳基-3-羟基异噻唑衍生物,通过1HNMR、13CNMR和HRMS对目标化合物进行结构表征,并测试目标化合物的昆虫GABA受体抑制活性及杀虫活性,以期发现活性较高的昆虫GABA受体CAs,为探寻新型杀虫剂的先导化合物提供更多理论依据。合成路线如图1所示。
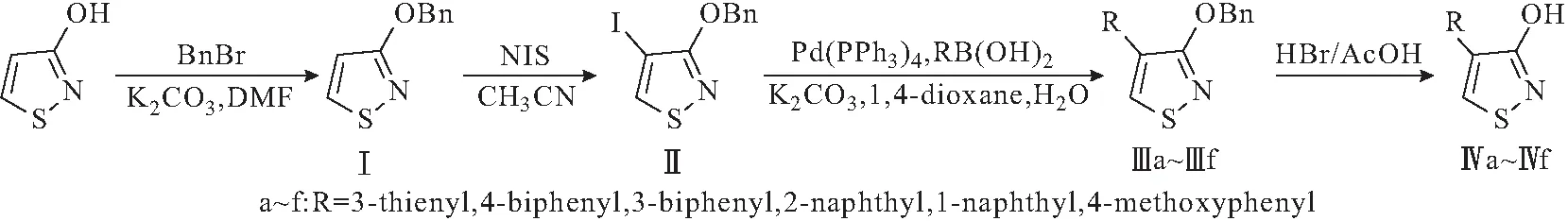
图1 4-芳基-3-羟基异噻唑衍生物的合成路线
1 实验
1.1 试剂与仪器
溴苄、无水碳酸钾、N-碘代丁二酰亚胺(NIS)、五水合硫代硫酸钠、无水硫酸钠、四(三苯基膦)钯、3-噻吩硼酸、3-联苯硼酸、4-联苯硼酸、1-萘硼酸、2-萘硼酸、4-甲氧基苯硼酸、溴化氢醋酸溶液、N,N-二甲基甲酰胺(DMF)、乙腈、1,4-二氧六环、氨水、乙酸乙酯(EA)、石油醚(PE,60~90 ℃)、二甲基亚砜(DMSO)等试剂均为分析纯,购自国药集团、Sigma-Aldrich公司等;层析柱纯化用200~300目硅胶;实验用水为去离子水。
400/54 Premium Shielded型核磁共振波谱仪,安捷伦科技股份有限公司;Thermo LTQ XL型液相色谱-质谱联用仪,美国Thermo Fisher公司。
1.2 材料
昆虫GABA受体抑制活性测试:供试品为6个目标化合物,溶剂为DMSO,待测对象为斜纹夜蛾(Spodopteralitura)和家蝇(Muscadomestica),雌性非洲爪蟾(Xenopuslaevis)卵母细胞,无Ca2+卵母细胞培养液[100 mmol·L-1NaCl,2 mmol·L-1KCl,1 mmol·L-1MgCl2,5 mmol·L-14-羟乙基哌嗪乙磺酸(HEPES),pH值7.6],无菌标准卵母细胞培养液(100 mmol·L-1NaCl,2 mmol·L-1KCl,1.8 mmol·L-1CaCl2,1 mmol·L-1MgCl2,5 mmol·L-1HEPES,0.1%间氨基苯甲酸乙酯甲磺酸盐,2 mg·mL-1胶原酶,50 μg·mL-1庆大霉素,100 U·mL-1青霉素,100 μg·mL-1链霉素,2.5 mmol·L-1丙酮酸钠,pH值7.6),纳升微量注射系统。
杀虫活性测试:供试品为6个目标化合物,溶剂为DMSO,待测对象为3龄斜纹夜蛾幼虫,所用人工饲料在实验室配制,其配方为:黄豆粉450 g,麦胚粉250 g,酵母80 g,干酪素40 g,对羟基甲酸酯15 g,胆固醇0.6 g,肌醇0.7 g,山梨酸6.0 g,氯化胆碱3.0 g,抗坏血酸14 g,甲醛3 mL,灭菌蒸馏水2 800 mL。
1.3 目标化合物的合成
1.3.1 中间体3-苄氧基异噻唑(Ⅰ)的合成
在冰浴条件下依次将3-羟基异噻唑(2.02 g,20.0 mmol)、无水碳酸钾(4.15 g,30.0 mmol)和DMF(30 mL)加入100 mL单口瓶中,搅拌均匀后,缓慢滴加溴苄(3.76 g,22.0 mmol),滴完6 h后撤除冰浴,室温继续反应12 h;加入去离子水100 mL淬灭,用EA萃取(80 mL×2),合并有机相,用饱和食盐水洗涤(60 mL×2),用适量无水硫酸钠干燥后抽滤,减压浓缩。粗产品经层析柱纯化(洗脱剂为PE-EA,体积比40∶1),得无色油状液体中间体Ⅰ3.28 g,产率85.7%。
1.3.2 中间体4-碘-3-苄氧基异噻唑(Ⅱ)的合成
依次将中间体Ⅰ(1.91 g,10.0 mmol)、NIS(4.50 g,20 mmol)和乙腈(20 mL)加入50 mL单口瓶中,65 ℃下搅拌36 h;加入饱和硫代硫酸钠溶液40 mL淬灭,用EA萃取(40 mL×2),合并有机相,用饱和食盐水洗涤(30 mL×2),用适量无水硫酸钠干燥后抽滤,减压浓缩。粗产品经层析柱纯化(洗脱剂为PE-EA,体积比30∶1),得无色油状液体中间体Ⅱ2.54 g,产率80.0%。
1.3.3 中间体4-芳基-3-苄氧基异噻唑(Ⅲa~Ⅲf)的合成
依次将中间体Ⅱ(1.27 g,4.0 mmol)、芳基硼酸(4.0 mmol)、四(三苯基膦)钯(0.12 g,0.1 mmol)、无水碳酸钾(0.83 g,6.0 mmol)、1,4-二氧六环(15 mL)和去离子水(5 mL)加入100 mL双口瓶中,将装置通氩气5 min以排净空气,随后升温至95 ℃,搅拌8 h;加入去离子水40 mL,用EA萃取(40 mL×2),合并有机相,用饱和食盐水洗涤(30 mL×2),用适量无水硫酸钠干燥后抽滤,减压浓缩。粗产品经层析柱纯化(洗脱剂为PE-EA,体积比1∶2),得中间体Ⅲa~Ⅲf,产率73.7%~83.7%。
4.事件发生的必然性。“冰冻三尺,非一日之寒”,群体性公共事件的突发并非是偶然的,其大多属于“能量积累型”,当事件累积到其所能承受的临界点时就会突然引爆。一般在群体性公共事件发生之前,社会周遭轻微躁动已初见端倪,当问题累积的愈多或问题久拖不决,这种躁动迹象则会愈明显。如果忽视周围环境产生的这些预兆,或阻断民众搜集消息的来源,最终会导致事件一触即发,大规模、突发性群体性公共事件的发生也就不可避免。
1.3.4 目标化合物4-芳基-3-羟基异噻唑(Ⅳa~Ⅳf)的合成
依次将中间体Ⅲa~Ⅲf(3.0 mmol)和质量浓度为33%的溴化氢醋酸溶液(18 mL)加入50 mL单口瓶中,常温搅拌12 h;缓慢滴加20 mL去离子水,再滴加质量浓度为25%的氨水,直到无气泡产生;所得溶液用EA萃取(60 mL×2),合并有机相,用饱和食盐水洗涤(40 mL×2),用适量无水硫酸钠干燥后抽滤,减压浓缩。粗产品经层析柱纯化(洗脱剂为PE-EA-MeOH,体积比10∶10∶1),真空干燥,得目标化合物Ⅳa~Ⅳf。
1.4 昆虫GABA受体抑制活性测试
采用电生理法测试目标化合物在100 μmol·L-1浓度下对斜纹夜蛾和家蝇GABA受体的抑制率。以斜纹夜蛾和家蝇GABA受体RDLbd亚基的cDNA为模板,通过聚合酶试剂盒(mMESSAGE mMACHINETMT7 Ultra Kit;Ambion,Austin,TX,USA)合成并纯化得到受体亚基的cRNA。利用纳升微量注射系统,将cRNA注入非洲爪蟾卵母细胞中,每个细胞5 ng,培养48 h。确认受体成功表达后,通过双电极电压钳技术测定目标化合物对斜纹夜蛾和家蝇GABA受体的抑制活性。
1.5 杀虫活性测试
配制目标化合物浓度分别为100 mg·kg-1和500 mg·kg-1的有毒饲料,分别加入2个6孔板中,每孔0.5 g。将大小一致且生长健康的3龄斜纹夜蛾幼虫接入孔中,每孔10只,每隔24 h更换一次有毒饲料;48 h后,触碰所有虫体,将无任何反应的受试虫计入死亡数。做3个平行实验,按下式对死亡率进行校正,排除溶剂等因素的干扰。

式中:P为实验组死亡率;P0为对照组死亡率。
2 结果与讨论
2.1 目标化合物的结构表征
4-(3-噻吩基)-3-羟基异噻唑(Ⅳa):紫色固体,产率78.0%。1HNMR(400 MHz,DMSO-d6),δ:12.03(s,1H,OH),8.99(s,1H,CH),7.89(s,1H,ArH),7.65~7.50(m,2H,ArH);13CNMR(100 MHz,DMSO-d6),δ:166.87,144.12,133.18,127.43,126.62,121.85,120.59;HRMS,m/z:calcd for C7H6NOS2[M+H]+183.989 1,found 183.988 5。
4-(3-联苯基)-3-羟基异噻唑(Ⅳc):淡黄色固体,产率70.9%。1HNMR(400 MHz,DMSO-d6),δ:12.03(s,1H,OH),9.14(s,1H,CH),8.20~7.20(m,9H,ArH);13CNMR(100 MHz,DMSO-d6),δ:166.95,146.27,140.88,140.61,133.49,133.18,129.53,129.40,128.00,127.43,127.26,126.63,126.53,126.09,125.91,124.58;HRMS,m/z:calcd for C15H12NOS [M+H]+254.064 0, found 254.063 4。
4-(2-萘基)-3-羟基异噻唑(Ⅳd):淡黄色固体,产率72.1%。1HNMR(400 MHz,DMSO-d6),δ:11.97(s,1H,OH),9.06(s,1H,CH),7.90~7.30(m,7H,ArH);HRMS,m/z:calcd for C13H9NOSNa [M+Na]+250.030 3,found 250.029 7。
4-(1-萘基)-3-羟基异噻唑(Ⅳe):淡黄色固体,产率77.1%。1HNMR(400 MHz,DMSO-d6),δ:11.77(s,1H,OH),8.86(s,1H,CH),8.10~7.40(m,7H,ArH);13CNMR(100 MHz,DMSO-d6),δ:167.40,148.66,133.69,131.81,131.13,128.66,128.52,128.26,126.67,126.36,125.90,125.81,124.45;HRMS,m/z:calcd for C13H9NOSNa [M+Na]+250.030 3,found 250.029 7。
4-(4-甲氧基苯基)-3-羟基异噻唑(Ⅳf):白色固体,产率72.7%。1HNMR(400 MHz,DMSO-d6),δ:11.88(s,1H,OH),8.87(s,1H,CH),7.68(d,2H,ArH),6.94(d,2H,ArH),3.75(s,3H,CH3);13CNMR(100 MHz,DMSO-d6),δ:166.79,167.18,143.36,128.76,124.89,123.86,116.09,115.63,114.29,55.54;HRMS,m/z:calcd for C10H9NO2SNa [M+Na]+230.025 2,found 230.024 6。
2.2 目标化合物对昆虫GABA受体的抑制活性(表1)

表1 目标化合物(100 μmol·L-1)对斜纹夜蛾和家蝇GABA受体的抑制活性
由表1可知,6个目标化合物在100 μmol·L-1浓度下对斜纹夜蛾和家蝇GABA受体均表现出一定的抑制活性,其中3-联苯衍生物Ⅳc对家蝇GABA受体的抑制活性最高,抑制率为36.9%,远高于4-联苯衍生物Ⅳb(6.5%),说明联苯环上取代位置可能对抑制活性有显著影响;3-联苯衍生物Ⅳc对斜纹夜蛾和家蝇GABA受体的抑制活性差别较大,说明其对2种昆虫受体可能具有一定的选择性;萘环上取代位置也对目标化合物的抑制活性影响较大,2-萘衍生物Ⅳd对2种昆虫GABA受体的抑制率较高,其中对斜纹夜蛾GABA受体的抑制率达到了28.6%,而1-萘衍生物Ⅳe对2种昆虫GABA受体的抑制活性均很低;3-噻吩衍生物Ⅳa对2种昆虫GABA受体均表现出相对较高的抑制活性,说明后续可设计和合成更多杂环取代的衍生物。
2.3 目标化合物的杀虫活性
采用混药接虫法测试了6个目标化合物分别在100 mg·kg-1和500 mg·kg-1浓度下对斜纹夜蛾幼虫的杀虫活性,结果见表2。
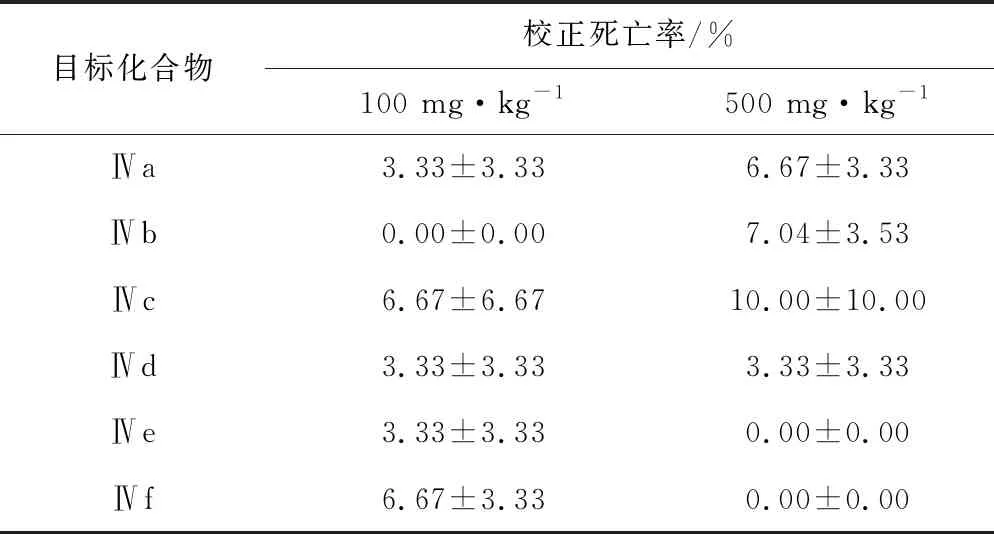
表2 目标化合物在100 mg·kg-1和500 mg·kg-1浓度下对斜纹夜蛾的杀虫活性
由表2可知,目标化合物Ⅳa、Ⅳc和Ⅳd在100 mg·kg-1和500 mg·kg-1浓度下对斜纹夜蛾幼虫均有一定的杀虫活性,且对斜纹夜蛾GABA受体的抑制率相对较高(表1),表明较好的拮抗活性可能是产生杀虫活性的因素之一;在100 mg·kg-1浓度下,除目标化合物Ⅳb外,其它目标化合物均对斜纹夜蛾幼虫表现出不同程度的杀虫活性,且杀虫活性并不随着浓度的升高而显著升高。
3 结论
以3-羟基异噻唑为原料,设计并合成了一系列4-芳基-3-羟基异噻唑衍生物,其中,4位单取代的3-羟基异噻唑衍生物对斜纹夜蛾和家蝇GABA受体的抑制活性偏低,仅有少数衍生物的抑制活性接近中等,这也可能是目标化合物对斜纹夜蛾幼虫表现出较低杀虫活性的原因之一。基于此,认为对3-羟基异噻唑环在4位进行单取代或芳环修饰不能显著提高该类化合物的活性,可能还需引入含氮杂环或同时在5位引入其它基团。该研究为昆虫GABA受体新型CAs的设计提供了重要信息和理论依据。
