中药灵芝降羊毛甾烷三萜类成分研究
2022-02-19梁旭博司盈盈赵琪璐赵晨光冯卫生赵珍珠
梁旭博,王 妍,司盈盈,赵琪璐,赵晨光,杜 锟,冯卫生*,赵珍珠*
1河南中医药大学药学院;2河南省中药开发工程技术研究中心,郑州 450046
目前被报道的真菌约有100 000种,但是据估计仍有更多的真菌还未被具体鉴定种类[1]。许多大型真菌(俗称蘑菇)是许多结构新颖和(或)活性显著的天然产物的来源,多孔菌科的灵芝便是其中一种[2-5]。
灵芝为担子菌门多孔菌科灵芝属多种灵芝的干燥子实体,是我国常见的药食两用的真菌,作为药物使用最早见于《神农本草经》,迄今已有上千年的用药历史[9-11]。自20世纪50年代以来,灵芝子实体已实现了人工栽培,随着灵芝菌丝体深层发酵培养技术的发展,灵芝的研究和开发日益广泛[11]。灵芝中的化学成分十分丰富,包含多糖、蛋白质、有机酸、小分子生物碱、倍半萜、三萜、甾体,这些化合物均表现出多种药理活性,如抗炎、抗肿瘤、抗氧化等[6-8]。其中三萜是灵芝子实体中的主要活性次生代谢产物,具有广泛药理活性,逐步引起人们的重视[11,12]。目前从灵芝中分离得到的三萜多为6/6/6/5骈合的四环羊毛甾烷类,数量已超过200个[5,11-13]。前期,我们从不同种类的灵芝中发现了大量新颖三萜、少量生物碱和倍半萜[14-16]。为了进一步了解中药灵芝的药效物质基础,提高其资源综合利用效率,本文对灵芝子实体的95%乙醇部位的化学成分进行了分离纯化和结构鉴定,并测试了分离化合物的体外抗肿瘤活性,以期发现具有进一步研究价值的活性分子。
1 材料与方法
1.1 仪器与材料
白血病(HL-60)、肺癌(A549)、肝癌(SMMC-7721)、乳腺癌(MCF-7)、结肠癌(SW480)细胞均由中国科学院昆明植物研究所天然药物活性筛选中心提供。
柱色谱为正相硅胶(青岛海洋化工有限公司)和Sephadex LH-20凝胶(40~70 μm,Amersham Pharmacia Biotech AB,Uppsala,瑞士);预制硅胶薄层G板(10~40 μm青岛海洋化工厂);ODS(40~60 μm,YMC);中压制备色谱系统Sepacore X10(德国Büchi公司);1260高压制备液相色谱仪(美国安捷伦公司);AVANCE 600核磁共振仪(TMS为内标)(德国布鲁克公司);Maxis HD型飞行时间质谱仪(德国布鲁克公司);Agilent Zorbax SB-C18液相色谱柱(粒径5 μm,规格9.4 mm × 150 mm);SCIEX Qtrap 5500质谱仪(美国应用生物系统公司),所用分析纯和色谱纯试剂为天津恒兴和天津四友精细化学有限公司生产。显色剂:10%浓硫酸乙醇,同时结合紫外灯(254 nm)观察。
灵芝2015年买自云南省昆明市螺蛳湾中药材市场,经北京林业大学戴玉成教授鉴定为G.lingzhi,标本(NO.HFC 20150518)收藏于河南中医药大学天然产物研究室。
1.2 实验方法
1.2.1 提取分离
灵芝子实体G.lingzhi自然晾干并称重(10.0 kg),粉碎后,95%的工业乙醇提取三次(每次浸泡3天,每次50 L)。将三次收集的乙醇液合并得含有灵芝成分的提取液,随后减压浓缩至10 L的水浓缩液。浓缩液用等体积乙酸乙酯萃取四次得到总乙酸乙酯层,减压浓缩得粗浸膏400 g。粗浸膏拌样后过正相硅胶柱,石油醚和丙酮梯度洗脱(体积比10∶1洗脱10 L;5∶1洗脱10 L;2∶1洗脱10 L;1∶1洗脱10 L),每500 mL接一瓶,减压浓缩至溶剂挥干;根据硅胶薄层层析结果合并成5个组分(A~E)。
组分C(27 g)和D(34 g)经中压色谱制备系统分别制备得到22个组分(C1~C22)和10个组分(D1~D10),洗脱剂为甲醇/水(V/V,20∶80、40∶60、60∶40、80∶20、100∶0,每个梯度各冲5 000 mL,流速为35 mL/min)。
组分C17(44 mg)过甲醇凝胶柱,结合硅胶薄层层析结果合并后减压浓缩得到6个组分C17a~C17f。组分C17a经丙酮凝胶(型号LH-20)分成5个部位(C17a1~C17a5),最后化合物1(8.5 mg,tR= 15.0 min)经高压制备液相色谱分离纯化得到(条件为梯度洗脱,MeCN/H2O(V/V):45∶55→65∶35,25 min,7 mL/min)。组分D9经甲醇凝胶色谱分为6部分(D9a~D9f),接着各组分分别经丙酮凝胶处理。经高压制备液相色谱纯化,化合物2(1.3 mg,tR= 20.2 min)从D9d8组分获得(条件为梯度洗脱,MeCN/H2O(V/V):60∶40→80∶20,25 min,7 mL/min)。组分D8经甲醇凝胶得D8a~D8i组分,接着D8d经丙酮凝胶分离得6个组分(D8d1~D8d6),然后D8d2过正相色谱(洗脱剂为石油醚/丙酮,体积比为2∶1,等度洗脱)得到8个组分,而化合物3(4.4 mg,tR= 8.8 min)从组分D8d28制备(条件为梯度洗脱,MeCN/H2O(V/V):28∶72→53∶47,25 min,7 mL/min)获得。组分D4经甲醇凝胶色谱分为10个组分(D4a~D4J),组分D4b经高压制备液相色谱(条件为梯度洗脱,MeCN/H2O(V/V),25∶75→50∶50,25 min,7 mL/min)纯化获得化合物4(12.3 mg,tR= 11.0 min)和化合物5(14.6 mg,tR= 19.0 min)。
1.2.2 细胞毒活性筛选
MTS法检测细胞活性原理:MTS为一种全新的MTT类似物,全称为3-(4,5-dimethylthiazol-2-yl)-5(3-carboxymethoxyphenyl)-2-(4-sulfopheny)-2H-tetrazolium,是一种黄颜色的染料。活细胞线粒体中琥珀酸脱氢酶能够代谢还原MTS,生成可溶性的甲臜(formazan)化合物,甲臜的含量可以用酶标仪在490 nm处进行测定。在通常情况下,甲臜生成量与活细胞数成正比,因此可根据光密度OD值推测出活细胞的数目。具体实验方法为:
接种细胞:用含10%胎牛血清的培养液(DMEM或者RMPI1640)配成单个细胞悬液(白血病(HL-60)、肺癌(A549)、肝癌(SMMC-7721)、乳腺癌(MCF-7)、结肠癌(SW480)),以每孔3 000~15 000个细胞接种到96孔板,每孔体积100 μL,细胞提前12~24 h接种培养。加入待测化合物溶液:化合物用DMSO溶解,化合物以40 μM浓度初筛,每孔终体积200 μL,每种处理均设3个复孔。显色:37 ℃培养48 h后,贴壁细胞弃孔内培养液,每孔加MTS溶液20 μL和培养液100 μL;悬浮细胞弃100 μL培养上清液,每孔加20 μL的MTS溶液;设3个空白复孔(MTS溶液20 μL和培养液100 μL的混合液),继续孵育2~4 h,使反应充分进行后测定光吸收值。比色:选择492 nm波长,多功能酶标仪(MULTISKAN FC)读取各孔光吸收值,记录结果,数据处理后以化合物编号为横坐标,细胞抑制率为纵坐标绘制5株细胞的抑制率图。
抑制率的计算公式为:
抑制率=(1-OD加药/OD对照)× 100%
2 结果
2.1 结构鉴定
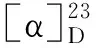

表1 化合物1和2的1H和13C NMR数据(600和150 MHz)

续表1 (Continued Tab.1)
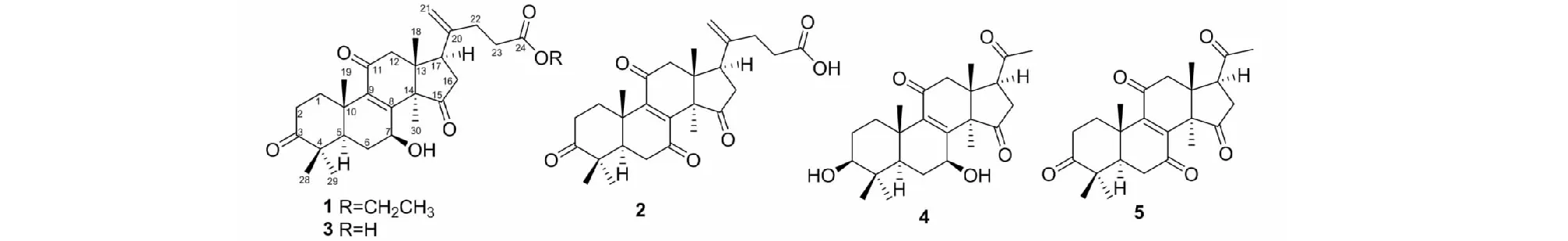
图1 化合物1~5的化学结构Fig.1 The chemical structures of compounds 1-5

图2 化合物1的结构及关键2D NMR相关信号Fig.2 The structure and key 2D NMR correlations of compound 1
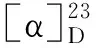
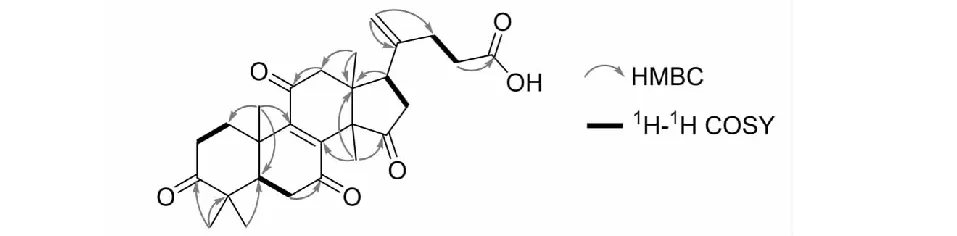
图3 化合物2的结构及关键2D NMR相关信号Fig.3 The structure and key 2D NMR correlations of compound 2
化合物3白色粉末;ESI-MS:m/z456.5,结合13C NMR和DEPT谱推导其分子式为C27H36O6。1H NMR(600 MHz,CD3OD)δ:2.87(1H,m,H-1),1.59(1H,m,H-1),2.54(1H,m,H-2),2.49(1H,m,H-2),1.75(1H,dd,J= 13.6,1.1 Hz,H-5),2.12(1H,dd,J= 12.3,8.4 Hz,H-6),1.61(1H,m,H-6),4.93(1H,d,J= 5.8 Hz,H-7),3.02(1H,d,J= 17.0 Hz,H-12),2.57(1H,m,H-12),2.69(1H,m,H-16),2.59(1H,m,H-16),3.15(1H,m,H-17),0.90(3H,s,H-18),1.23(3H,s,H-19),5.08(1H,s,H-21),4.94(1H,s,H-21),2.43(1H,m,H-22),2.31(1H,m,H-22),2.50(1H,m,H-23),1.13(3H,s,H-28),1.09(3H,s,H-29),1.43(3H,s,H-30);13C NMR(150 MHz,CD3OD)δ:36.7(C-1),35.1(C-2),219.7(C-3),47.8(C-4),49.5(C-5),29.0(C-6),67.1(C-7),160.0(C-8),142.2(C-9),39.3(C-10),200.0(C-11),50.2(C-12),46.4(C-13),59.7(C-14),218.1(C-15),39.8(C-16),47.1(C-17),19.5(C-18),18.6(C-19),146.9(C-20),112.2(C-21),33.4(C-22),34.7(C-23),178.1(C-24),27.5(C-28),21.1(C-29),25.3(C-30)。由EI-MS、1H NMR、13C NMR、DEPT及2D NMR数据确定化合物3的结构,并且数据与文献报道的20(21)-dehydrolucidenic acid A[17]一致。
化合物4针状结晶(甲醇);mp.280~281 ℃,ESI-MS:m/z402.2,结合13C NMR和DEPT谱推导其分子式为C24H34O5。13C NMR(150 MHz,C5D6N)δ:37.1(C-1),29.0(C-2),77.9(C-3),39.7(C-4),50.0(C-5),28.6(C-6),66.9(C-7),158.8(C-8),143.2(C-9),39.7(C-10),197.8(C-11),50.0(C-12),45.7(C-13),58.9(C-14),215.2(C-15),35.8(C-16),54.6(C-17),19.0(C-18),20.0(C-19),206.5(C-20),31.4(C-21),29.1(C-28),16.8(C-29),25.6(C-30)。经与文献[18,19]对照,鉴定化合物4为赤芝酮A。
化合物5无色油状;ESI-MS:m/z398.2,结合13C NMR和DEPT谱推导其分子式为C24H30O5。1H NMR(600 MHz,CDCl3)δ:2.90(1H,m,H-1),1.75(1H,m,H-1),2.63(1H,m,H-2),2.48(1H,m,H-2),2.32(1H,dd,J= 15.0,2.2 Hz,H-5),2.70(1H,dd,J= 15.0,13.9 Hz,H-6),2.49(1H,dd,J= 13.9,2.2 Hz,H-6),3.06(1H,d,J= 15.8 Hz,H-12),2.84(1H,d,J= 15.8 Hz,H-12),2.85(1H,overlapped,H-16),2.62(1H,overlapped,H-16),3.37(1H,dd,J= 8.7,8.7 Hz,H-17),0.77(3H,s,H-18),1.27(3H,s,H-19),2.20(3H,s,H-21),1.14(3H,s,H-28),1.11(3H,s,H-29),1.69(3H,s,H-30)。经与文献[20]对照,鉴定化合物5为4,4,14α-trimethyl-3,7,11,15,20-pentaoxo-5α-pregn-8-en(即lucidadone H)。同时结合lucidone D[21]和lucidone H[22]的碳谱数据,首次归属了化合物5的碳谱数据。13C NMR(150 MHz,CDCl3)δ:34.5(C-1),33.9(C-2),215.3(C-3),43.8(C-4),51.0(C-5),37.4(C-6),199.1(C-7),146.3(C-8),150.1(C-9),39.6(C-10),198.3(C-11),47.7(C-12),47.1(C-13),56.8(C-14),205.5(C-15),34.7(C-16),52.5(C-17),18.8(C-18),20.4(C-19),205.2(C-20),31.5(C-21),27.8(C-28),17.9(C-29),21.2(C-30)。
2.2 体外细胞毒活性筛选
对分离得到化合物1~5在五株常规肿瘤细胞株进行活性筛选。结果显示在40 μM时,化合物1~5均未表现出明显的细胞毒活性。
3 结论
灵芝三萜类化合物相对分子质量一般为400~600,母核上常见含氧官能团,如羟基、羧基、酮基、甲氧基、乙酰氧基等。根据骨架上碳原子数灵芝三萜可分为C30、C27和C24;依据所连接官能团和侧链结构不同,又可分为灵芝酸类、醇类、醛类、内酯类等几大类[11,12]。通过对灵芝(G.lingzhi)子实体进行提取分离,共得到5个高氧化度的降羊毛甾烷三萜,其中化合物1和2为新的24-降羊毛甾烷三萜类化合物,和化合物3同属于C27类;化合物4和5属于C24类羊毛甾烷三萜。灵芝中的三萜结构复杂多样,表现出生物活性也十分丰富,尤其是抗肿瘤活性[11,12]。因此,对化合物1~5进行了体外抗肿瘤活性筛选(HL-60、A549、SMMC-7721、MCF-7、SW480),但均未表现出明显细胞毒活性。G.lingzhi是2012年首次被戴玉成教授提出的灵芝新种[23],后来被认为和G.sichuanense是同一个品种[24],对其化学成分的报道较少[16,25]。本文的研究为更好地开发利用灵芝属的灵芝、丰富该菌化学成分的种类和探究其有效活性成分奠定了一定的理论基础。
