阿帕替尼联合GP方案治疗巨块型局部晚期乳腺癌一例
2022-02-16黄世芬燕冰雪何方夏云霞赵达令晓玲
黄世芬 燕冰雪 何方 夏云霞 赵达 令晓玲
患者,女,55岁,因“左乳肿块进行性增大,破溃渗血伴胸部疼痛1个半月”于2017年6月13日就诊于兰州大学第一医院。患者于2016年6月29日因发现左乳肿块于外院就诊,乳腺超声检查结果示左侧乳腺实性占位[乳腺超声影像报告和数据系统(BI-RADS)4级,55 mm×60 mm],伴左侧腋窝淋巴结肿大。遂行左乳肿物穿刺术,术后病理结果提示:(左乳)浸润性癌,非特殊类型,Ⅲ级,伴大片凝固坏死。免疫组化结果示:ER(++,30%),PR(-),Her-2(++),Ki-67(70%)。2016年7月~10月行FEC方案(氟尿嘧啶+表柔比星+环磷酰胺)化疗3个周期,按照RESIST 1.1[1]评价为部分缓解(PR)。建议手术治疗,患者拒绝,且未返院继续治疗。2016年11月患者肿物较前明显增大,遂就诊于外院,2016年11月~2017年3月行DN方案(多西他赛、长春瑞滨)化疗3个周期,疗效评价为PR。建议手术治疗,患者再次拒绝,遂行托瑞米芬60 mg每日1次口服内分泌治疗。2017年4月底,患者左乳肿块进行性增大,破溃渗血伴胸部疼痛,遂来我院就诊。入院体格检查:生命体征平稳,心、肺、腹检查未见明显异常。专科体格检查:左侧胸壁可见巨大肿物,呈“菜花状”膨胀性生长,大小约30 cm×25 cm,累及整个左侧乳房,未见乳头乳晕结构,肿块固定,表面破溃有渗血、渗液,伴有恶臭。完善血常规、肝肾功能、心电图、心脏超声等检查未见明显异常。浅表淋巴结超声检查结果:左侧锁骨上窝淋巴结肿大,左侧腋窝多发淋巴结肿大。胸部CT检查结果:左侧乳腺区巨大菜花样软组织肿块,局部皮肤增厚,纵隔及左侧腋窝多发增大淋巴结,考虑乳腺癌(图1)。头腹部CT、骨扫描检查结果未见明显转移病灶。会诊既往外院病理结果提示:(左乳)浸润性癌,非特殊类型,Ⅲ级(图2)。免疫组化结果:ER(++),PR(-),Her-2(+),Ki-67(60%)。患者明确诊断:局部晚期乳腺癌(LABC),左侧Luminal B型浸润性癌,临床分期:cT4N3M0 ⅢC期。经院内多学科会诊后于2017年6月16日行GP方案(吉西他滨1.4 g静脉滴注d1、8;顺铂60 mg静脉滴注d1、30 mg静脉滴注d2;每3周1次)再次化疗,同时联合阿帕替尼500 mg每日1次连续口服治疗。在第1周期化疗的第4天,患者左乳肿物局部渗出减少(图3A),在第1周期化疗的第8天,左乳肿物局部缺血坏死(图3B),之后肿块逐渐缩小。联合治疗2个周期后,菜花状肿物坏死脱落,左乳11点方向可见一大小约10 cm×10 cm破溃区,其内可见肉芽组织(图3C)。阿帕替尼用药期间患者出现3级高血压,使用血管紧张素转化酶抑制剂(ACEI)降压治疗后血压恢复正常,阿帕替尼减量为250 mg每日1次,余治疗过程中仅见轻微不良反应,患者均可耐受。联合治疗2个周期后疗效评价为PR,但是肿块贴近胸壁尚无法手术切除,继续行上述方案治疗,4个周期GP方案化疗后给予单药阿帕替尼的维持疗法(250 mg每日1次)。单药阿帕替尼治疗1个月后,局部破溃创面消失,可见再生上皮及瘢痕(图3D)。之后患者拒绝来院进一步治疗。定期电话随访,患者均未规律服用阿帕替尼,且于2018年12月起停药。2019年5月,患者因左乳肿块再次增大并左上肢肿胀疼痛再次就诊,体格检查:胸壁破溃,伴有恶臭,左上肢肿胀活动受限,颈部多发肿块。浅表淋巴结超声检查:左侧颈根、左侧腋窝、双侧锁骨上肿大淋巴结。建议住院治疗,患者及家属均拒绝,要求仅给予对症止痛治疗。后患者于2019年10月死亡。回顾治疗过程,该患者三线阿帕替尼联合GP方案治疗的无进展生存(PFS)期为18个月。

图1 2017年6月13日患者胸部CT检查结果 图2 2017年6月15日患者左乳肿物病理检查结果[苏木素-伊红(HE)染色,×200]
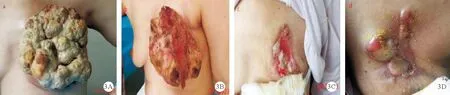
图3 患者联合方案治疗后左乳肿块脱落[A:阿帕替尼联合GP方案第1周期化疗的第4天(2017年6月19日);B:阿帕替尼联合GP方案第1周期化疗的第8天(2017年6月23日);C:阿帕替尼联合GP方案2个周期治疗后(2017年8月8日);D:单药阿帕替尼维持治疗1个月后(2017年11月18日)
讨 论
LABC是指肿瘤直径>5 cm、肿瘤累及皮肤或胸壁、伴有腋窝淋巴结融合固定或同侧锁骨上淋巴结转移,但在临床上未发现远处转移的一类乳腺癌[2]。LABC常无法直接进行根治性手术切除,进行术前治疗使其原发病灶迅速缩小,局部控制后,争取手术根治是LABC的标准治疗方案。LABC术前化疗的一线药物常选蒽环联合或序贯紫杉类,蒽环紫杉类治疗失败或耐药的患者可选择吉西他滨、长春瑞滨、卡培他滨和铂类药物等。
本例患者为经治的巨块型LABC,分子分型为Luminal B型,选择GP方案的分析如下:(1)托瑞米芬内分泌治疗仅1个月,病情很快进展,考虑对内分泌药物原发耐药。(2)肿瘤短期内生长迅速,需要尽快控制疾病进展,改善生活质量,此时内分泌治疗起效缓慢,多选择化疗;(3)患者既往已经使用过蒽环、紫杉类及长春瑞滨等治疗,且肿瘤呈外生性生长,瘤体巨大伴破溃渗出,肿瘤负荷大,单药化疗很难控制病情,需要联合化疗,而顺铂属于细胞周期的非特异性药物,癌细胞对其细胞毒性作用敏感。因此三线治疗时给予GP方案。
肿瘤的生长离不开丰富的血供,同时肿瘤的增大会促进新生血管生成,因此在巨大肿块型肿瘤患者中抗血管生成的意义重大[3]。抗血管生成药物是靶向治疗中的一大类药物,具有抑制肿瘤血管生成、促使肿瘤血管正常化及重新编辑肿瘤免疫微环境的作用[4]。阿帕替尼是一种高选择竞争性结合血管内皮生成因子受体-2(VEGFR-2)胞内ATP结合位点药物,与其他小分子酪氨酸激酶抑制剂(TKI)相比具有更高的抑制血管生成活性[5-6]。Hu等[7]的研究表明,阿帕替尼单药对非三阴性乳腺癌患者显示出良好的疗效,中位PFS期达4.0个月。本例患者为巨块型LABC,因此在化疗基础上联用阿帕替尼强化治疗。
从本例患者的治疗情况来看,阿帕替尼联合GP方案治疗乳腺癌局部肿块疗效显著。阿帕替尼联合GP方案治疗2个周期左乳巨型肿块完全脱落,考虑主要与阿帕替尼抗血管生成药物的作用相关。阿帕替尼引起肿块脱落的主要机制为选择性抑制VEGFR-2的酪氨酸激酶活性,从而抑制PI3K-AKT-mTOR和Ras-Raf-MEK-ERK信号通路,减少肿瘤血管生成,阻断肿瘤血供,导致瘤体缺血坏死[8-13]。另一方面,表明阿帕替尼与常规化疗存在协同或叠加作用,从而增加抗肿瘤效果。本例患者后续拒绝进一步治疗,仅使用阿帕替尼单药维持治疗,PFS期达18个月,表明阿帕替尼单药治疗具有很好的抗肿瘤作用。
此例患者为反复治疗的巨块型LABC,阿帕替尼联合GP方案三线治疗取得如此显著的疗效,临床上比较少见。但本例患者的治疗仍存在一些遗憾:患者对疾病认知差,两次拒绝行手术治疗,且未按时化疗,肿块很快再次增大,导致疾病恶化为无法直接手术治疗的巨块型LABC。阿帕替尼联合GP方案治疗后肿块迅速脱落,疗效显著。若患者按时化疗,后续给予局部放疗很可能达到治愈。但患者拒绝进一步治疗,导致疾病再次进展。虽然患者仅口服阿帕替尼单药维持治疗PFS期达到18个月,但患者的生活质量严重降低,最终死亡。
综上,本病例提示,阿帕替尼对于未行手术的乳腺局部呈外生性生长的巨块型肿瘤,可迅速使肿块脱落,近期效果显著,远期也可延长PFS期,值得临床进一步研究。
