接受免疫检查点抑制剂治疗患者发生急性肾损伤的相关危险因素分析
2022-02-16嵇铭苏乌日力格王文娟冯哲王涌张利孙雪峰陈香美蔡广研
嵇铭苏 乌日力格 王文娟 冯哲 王涌 张利 孙雪峰 陈香美 蔡广研
免疫检查点抑制剂(ICIs)的发展推动了恶性肿瘤治疗的革命性变化[1],显著改善了许多恶性肿瘤患者的疗效和预后[2]。ICIs的机制主要是抑制下调的免疫途径,包括细胞毒性T淋巴细胞抗原4(CTLA-4)、程序性死亡受体1(PD-1)及程序性死亡配体1(PD-L1),目的是增强抗肿瘤免疫反应[3]。抑制这些负调控通路会增加患者免疫系统的抗肿瘤反应,但一系列非特异性免疫激活会引发不良事件,称为免疫相关不良事件(irAE)。ICIs诱导的irAE几乎可以影响所有系统器官[4],如皮肤、胃肠道、内分泌系统[5]及肾脏。急性肾损伤(AKI)是一种以肾功能下降为特征的临床综合征,与多种病因和病理生理机制有关[6],AKI急性期不仅可引起内环境紊乱,增加死亡风险,且对心、肺、脑等多系统器官产生长期重要影响,由此增加了医疗卫生费用负担。有文献报道ICIs相关AKI(ICIs-AKI)的发病率为1.4%~4.9%[7-8],国内仅有个例报道,缺乏对ICIs治疗患者AKI危险因素的系统总结,本研究旨在对ICIs-AKI的临床资料进行回顾性分析,研究其发病率及危险因素。
对象与方法
1.对象:回顾性分析2014年1月~2019年12月于中国人民解放军总医院第一医学中心肾脏病医学部接受至少一剂ICIs的恶性肿瘤患者1 615例,其中男1 115例,女500例,平均年龄(57.41±11.59)岁。排除标准:(1)年龄<18岁;(2)终末期肾病患者;(3)既往有肾脏切除、肾移植病史患者;(4)住院期间临床资料不完整患者。根据是否发生ICIs-AKI将1 615例患者分为AKI组(114例)与非AKI组(1 501例),AKI组男76例,女38例,平均年龄(56.52±11.46)岁;非AKI组男1 039例,女462例,平均年龄(56.52±11.46)岁。两组患者性别年龄比较差异均无统计学意义(P>0.05)。本研究通过我院伦理委员会审核批准。
2.方法:收集患者的性别、年龄、BMI、基线血清肌酐(SCr)、基线估算的肾小球滤过率(eGFR)、基线血清白蛋白(Alb)水平、肿瘤类型、基础疾病(脑血管疾病、冠心病、糖尿病、高血压、肝病、贫血、慢性肾脏病、自身免疫性疾病)、ICIs药物种类(伊匹木单抗、纳武利尤单抗、帕博利珠单抗、度伐利尤单抗、特瑞普利单抗、信迪利单抗、卡瑞利珠单抗、阿替利珠单抗)及分组情况(PD-1、PD-L1、CTLA-4)、合并使用其他肾毒性药物[血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)化疗药物、抗生素、利尿剂、质子泵抑制剂、非甾体抗炎药]情况、AKI发病情况及分期。化疗药物包括顺铂、卡铂、丝裂霉素、异环磷酰胺、培美曲塞、西妥昔单抗、甲氨蝶呤、秋水仙碱;抗生素药物包括氨基糖苷类抗生素、万古霉素、两性霉素B、利福平、环丙沙星、磺胺类抗生素,合并用药情况为ICIs治疗期间的用药情况。基线数据为首次使用ICIs前最接近用药日期测得的基线值。AKI的诊断标准及分期标准采用改善全球肾脏病组织(KDIGO)-AKI标准[9],即48小时内SCr水平升高超过26.5 μmol/L,或7天内升高超过基础值的1.5倍及以上;eGFR计算采用eGFR-EPI公式[10];终末期肾病定义为eGFR<15 ml·min-1·(1.73 m2)-1或需要依赖透析;慢性肾脏病定义为eGFR<60 ml·min-1·(1.73 m2)-1。

结 果
1.所有患者的一般情况:ICIs治疗的前3名药物分别为纳武利尤单抗(37.0%)、帕博利珠单抗(30.8%)和接信迪利单抗(21.6%)。1 615例患者中最常见的基础疾病是高血压(27.2%),其次是是糖尿病(16.8%)。最常见的合并用药是质子泵抑制剂(65.5%)。AKI的发病率为7.1%(114例),其中76.3%(87例)为AKI1期,16.7%(19例)为AKI 2期,7.0%(8例)为AKI 3期。
2.两组患者一般资料和临床资料比较:AKI组患者基线SCr水平、使用特瑞普利单抗及信迪利单抗、服用ACEI/ARB类药物患者比例均低于非AKI组,基线eGFR、基线血清Alb<30 g/L、贫血、使用纳武利尤单抗、服用质子泵抑制剂、利尿剂、非甾体抗炎药、抗生素患者比例均高于非AKI组(P<0.05)。两组患者年龄、性别、BMI、ICIs药物分组、服用化疗药物比较差异均无统计学意义(P>0.05)。见表1。
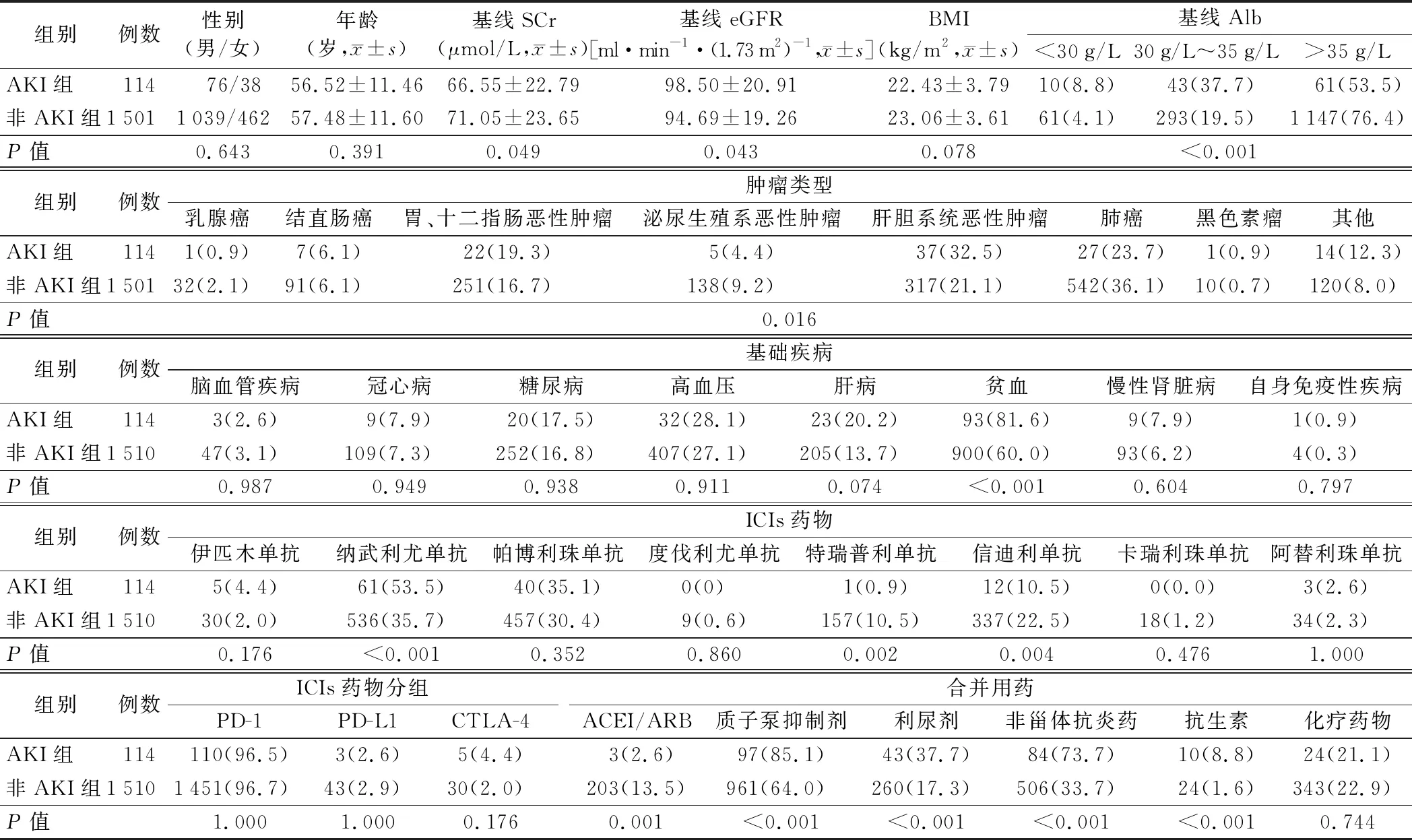
表1 两组患者一般资料和临床资料比较[例,(%)]
3.ICIs-AKI的危险因素分析:单因素logistic分析结果显示,基线eGFR、贫血、基线Alb水平、抗生素、服用ACEI/ARB类药物、利尿剂、非甾体抗炎药、质子泵抑制剂及使用纳武利尤单抗、特瑞普利单抗、信迪利单抗与ICIs-AKI发生相关(P<0.05)。将单因素分析中具有统计学意义的变量纳入多因素logistic回归分析结果显示,贫血、基线Alb<30 g/L、使用抗生素、利尿剂、非甾体抗炎药、质子泵抑制剂为ICIs-AKI发生的独立危险因素(P<0.05)。见表2。

表2 ICIs-AKI的危险因素分析
讨 论
肿瘤治疗引起的肾毒性是临床常见且日益严重的问题,“肿瘤肾病学”的分支应运而生。ICIs是肿瘤治疗的新型药物,能够改善许多恶性肿瘤的自然病程[11]。然而,同传统化疗药物和靶向药物类似,ICIs也带来了不利影响,即irAE,其中包括AKI。
本研究探讨了恶性肿瘤患者ICIs-AKI的相关危险因素,结果显示,ICIs-AKI发病率为7.1%。既往相关文献报道ICIs-AKI发病率为1.4%~4.9%[7-8]。但近两年来,随着ICIs的应用日益增多,新近的关于ICIs-AKI的研究结果显示,ICIs-AKI的发病率约为14%~18%[3,12-15]。本研究及一些新近的研究结果均显示ICIs-AKI发病率在既往研究中被低估,可能是由于近年来更完善的随访及监测系统在客观上提高了该病的诊断率。有研究结果显示,ICIs-AKI患者若肾功能不恢复,则与较高的死亡率独立相关[16]。因此,ICIs-AKI应引起临床医生的警惕。
本研究中,AKI组与非AKI组性别、年龄、BMI、ICIs药物分组、服用化疗药物比较差异均无统计学意义。AKI组患者基线SCr水平较低,基线eGFR较高,进一步分析发现,对于基线肾功能较好的患者,医生给予了更大比例的有潜在肾毒性合并药物,因此与非AKI组比较,AKI组患者使用质子泵抑制剂、利尿剂、非甾体抗炎药以及抗生素的比例较高。
既往研究报道的ICIs-AKI最常见的病理类型为急性肾小管间质性肾炎(ATIN)[17]。目前,ICIs如何触发ATIN的确切机制尚不清楚,其中一种理论是“免疫刹车”机制。“免疫刹车”机制是指ICIs抑制CTLA-4/PD-1/PD-L1的同时[18],释放了机体的“免疫刹车”,由于ICIs在激活T细胞对肿瘤细胞免疫能力的同时,也触发了对肾脏自身抗原的自身免疫反应。
单因素及多因素logistic回归分析结果发现,使用非甾体抗炎药、利尿剂、抗生素及质子泵抑制剂为ICIs-AKI发生的独立危险因素。质子泵抑制剂、非甾体抗炎药及抗生素均可引起急性间质性肾炎(AIN)。上述3种药物引起AIN的机制可能与其导致的超敏反应药物特异性T细胞激活有关[19-20]。ICIs-AKI患者中大部分接受了已知的导致AIN的药物,包括非甾体抗炎药、抗生素和质子泵抑制剂[8,16],这与本研究结果一致,其可能机制为ICIs降低了机体对潜在肾毒性药物(抗生素、非甾体抗炎药、质子泵抑制剂)的耐受阈值[21],即“多重攻击”。
本研究结果还显示,患者基础疾病及营养状态对AKI也有影响,贫血及Alb水平<30 g/L为AKI的危险因素。贫血是AKI的常见病因,由于肾脏特别容易受到缺氧损伤,急性失血、血容量减少、血液稀释或肾动脉在外科手术过程中阻断所致的氧气供应减少均可能导致AKI。由于本研究中所有入组患者皆为恶性肿瘤患者,多种因素均可影响Alb水平,包括炎症、感染及营养不良和蛋白丢失性疾病(恶性肿瘤恶病质、肝功能障碍等),因此,Alb水平可能在一定程度上作为疾病的严重程度和营养不良的标志物。
本研究尚存在以下不足:(1)本研究为单中心回顾性研究,样本量偏小,结果可能存在一些偏倚;(2)本研究中AKI组患者无肾穿刺活检报告,ICIs-AKI的病理类型缺乏组织病理学活检证据,也未纳入尿量、尿常规等肾内科实验室检查指标;(3)由于患者恶性肿瘤类型较多,本研究未收集肿瘤分级相关数据;(4)本研究未设置不使用ICIs治疗的患者作为对照组。
综上所述,ICIs-AKI应该引起临床医生警惕。ICIs-AKI受多种危险因素影响,对于高危患者需要肾内科医师治疗。本研究发现的结论还需要在大样本量、多中心研究中进行验证。
