核心素养下高中化学教学设计
2021-12-30邓亚鹏
邓亚鹏
【摘要】《化学能与电能》是高中化学必修阶段的重要学习内容,本节核心知识“原电池原理”对氧化还原反应、化学能与热能、化学电源、电解原理等基本概念和基本理论的学习起着承上启下的作用。本文以此为例,重点通过对铜锌原电池原理的“宏观辨识与微观探析”及“证据推理”,建立一般的“单池”原电池的“模型认知”,实践探索基于学科核心素养培养的高中化学课堂教学设计。
【关键词】高中化学;教学设计;《化学能与电能》;原电池原理
【中图分类号】G633.8【文献标志码】A【文章编号】1004—0463(2021)11—0120—02
教育部制定的《普通高中化学课程标准(2017版)》指出,化学学科核心素养包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”等五个方面[1]。化学学科核心素养要做到真正的落实,离不开全体化学教师的具体教学实践,特别是在进行课堂教学设计时要根据具体的知识内容、采取适宜的教学方法、设计高效的学习活动,确保学生在学习过程中实实在在地逐步形成必备品格、关键能力和正确的价值观念。本文以人教版《化学2(必修)》第二章第二节“原电池原理”为例[2],实践探索基于学科核心素养培养的高中化学课堂教学设计。
一、“原电池原理”教学设计
【情景引入】教师利用真实的情景引入,展示新能源汽车与飞机起飞的竞速视频以及其动力电池的结构图片,激发学生的学习兴趣;引导学生回顾生活中的干电池、纽扣电池、手机电池等;展示实物——音乐贺卡、南孚5号干电池。提出疑问:化学电池是如何产生电流的?
核心活动一:通过宏观辨识与微观探析,初步建立原电池的概念。
教师打开音乐贺卡,音乐响起,取下纽扣电池,音乐停止;重新装上纽扣电池,音乐再次响起,让学生对化学电池能提供电能,产生电流形成了初步的感性认识。
【实验1】用干电池、灵敏电流计、小灯泡(带灯座)以及导线组装成一个串联电路,并画出电路图。观察现象:电流表指针偏转(提示学生注意电流表指针偏转方向与电池正负极之间的关系)、小灯泡发光,说明有电流产生。
【实验2】将实验1装置中的干电池取下,用导线连接锌片和铜片,平行(不要接触)插入盛有稀硫酸的烧杯中,观察现象。
【学生讨论】学生讨论观察到的现象,并分析得出结论。铜片上有气泡,锌片上也有少量气泡并不断溶解,溶液为无色;灯泡发光,电流表指针偏转,说明有电流产生。该装置将化学能转化为电能,形成原电池;从电流表指针的偏转方向判断,铜片是原电池的正极,则锌片是负极。
【板书】定义——将化学能转化为电能的装置称为原电池。
核心活动二:通過宏观辨识与微观探析,证据推理与模型认知,以锌铜原电池为模型,学生自主探究原电池的工作原理。
【提出问题】原电池是如何产生电流的?
【提出假说】学生大胆推测,提出假设。锌和稀硫酸发生氧化还原反应,有电子转移;铜片上产生的氢气不可能是铜和稀硫酸反应生成,唯一的可能是锌失去的电子沿导线转移到铜片上,整个装置构成完整的闭合电路。
【实验探究】学生提出问题,设计实验,观察现象,分析讨论,得出结论。
问题:①Zn和Cu分别能与稀硫酸反应生成氢气吗?
②如何实现将化学能转化为电能?
实验及现象:
①分别将Zn片、Cu片插入稀硫酸中。现象:Zn片表面有气泡产生;Cu片上没有明显现象,溶液不变蓝色。
②Zn片、Cu片平行(不要接触)插入稀硫酸中;现象与实验①相同。
③将Zn片、Cu片用连有电流计和小灯泡的导线连接,并插入稀硫酸中;现象:铜片表面有气泡,锌片不断溶解,溶液为无色,灯泡发光,电流表指针偏转。
④将实验③装置的Cu片换成碳棒,重新实验。现象:碳棒表面有气泡,锌片不断溶解,溶液为无色;灯泡发光,电流表指针偏转。
⑤将实验③装置的Zn片换成镁条,重新实验。现象:铜片表面有气泡,镁条不断溶解;灯泡发光,电流表指针偏转。
【学生讨论】教师引导学生讨论以下问题:实验①Zn与稀硫酸反应的电子转移情况?可否用双线桥画出电子转移的方向和数目(为电极反应式的书写做知识储备)?实验③为什么有电流产生,如何判断电子的流向?实验①和③发生的氧化反应和还原反应在区域上有什么不同?
【学生分析】实验①证明,Cu不与稀硫酸反应;实验②证明Zn能与稀硫酸发生氧化还原反应。实验③的现象说明形成原电池,且Zn为负极,Cu为正极,溶液不变蓝,说明Cu没有反应,只起导电作用;铜片上有氢气生成,说明H+在铜片上得到电子生成氢气。那么,H+的电子从何而来呢?从微观分析,电子的来源只有一个合理的可能性——Zn失电子生成Zn2+进入溶液,电子沿着导线定向移动到铜片上。电子沿导线定向移动必然产生电流,而且电流的方向和电子移动的方向相反,即外电路导线中,电流从Cu片流出,从锌片流入,所以Cu片是正极,锌片是负极。在原电池装置内部,电解质溶液中的阴、阳离子定向移动形成电流,电流从负极流向正极,所以阳离子向正极定向移动,阴离子向负极定向移动,构成完整的闭合回路。实验③④⑤形成闭合回路的原理相似,都需要有活泼性不同的电极、电解质溶液、自发的氧化还原反应、形成闭合回路。
【模型认知】以铜锌原电池为模型,归纳原电池的工作原理,展示小组的学习成果。
负极(锌):失去电子,元素化合价升高,发生氧化反应,(外电路)电子流出、电流流入,(内电路)阴离子移向负极。
正极(铜):得到电子,元素化合价降低,发生还原反应,(外电路)电子流入、电流流出,(内电路)阳离子移向正极。
【教师板书】规范符号标准——电极反应式的定义及书写规则。用特定的化学用语表征原电池负极和正极两个不同的区域发生氧化反应和还原反应的式子称为电极反应式。
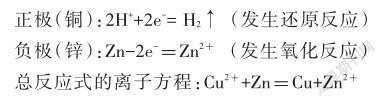
核心活动三:通过小组实验,自主探究构成原电池的一般条件。
【实验用品】镁条、铜片、铝片、锌片、碳棒各两个,稀硫酸、NaOH溶液、酒精、橙汁、西红柿、苹果,100ml烧杯几只,灵敏电流计、小灯泡(带灯座)以及导线若干。
以下是学生实验探究活动过程中组装的数十个实验装置的一部分,在较短的实验时间内,没有考虑氧气作用的金属缓慢腐蚀过程。
构成原电池:Zn-碳棒∣稀硫酸;Al-Cu∣NaOH溶液;MgFe∣橙汁;Fe-Cu∣苹果;Mg-Zn∣一个西红柿;现象均为电流表指针偏转,灯泡发光。
不能构成原电池:Zn-Zn∣稀硫酸;Fe-Cu∣NaOH溶液;Cu-碳棒∣橙汁;Mg-Zn∣两个西红柿;Mg-Fe∣酒精。
【师生归纳】分析以上实验结果,得出构成原电池的一般条件:两个活泼性不同的电极;电解质溶液;形成闭合回路;自发进行氧化还原反应。
【思考交流】如何根据氧化还原反应原理来设计原电池呢?请将反应:Zn + Cu2+= Cu + Zn2+设计成电池,并画出装置示意图。
二、教学反思
本文尝试基于“宏观辨识与微观探析”“证据推理与模型认知”等化学学科核心素养培养的课堂教学设计。依托铜锌原电池工作原理的自主实验探究,通过宏观辨识物质的形态及变化现象,从微观层面理解产生电流与物质组成、结构和性质的联系;通过设计有针对性的问题,组织学生自主学习,逐步树立证据意识,能基于證据对原电池产生电流的原因提出可能的假设,并通过分析推理加以证实;培养学生的分析、归纳、推理能力、实验能力;依据铜锌原电池工作原理构建模型、通过模型认知并解决原电池的有关问题[3]。
参考文献
[1]中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018(01):18-21.
[2]王秀红,李志航,张冬华.发展学生化学学科核心素养的“化学能与电能”教学[J].化学教育(中英文),2020(03):27-32.
[3]戴雨濛,吴新建,张贤金.基于“证据推理与模型认知”的对话教学评析[J].案例研究,2019(07):51-54.
(本文系2018年度甘肃省“十三五”教育科学规划一般自筹课题《基于学科核心素养的高中化学教学研究》的研究成果,课题立项号:GS[2018]GHB0294)
编辑:张昀
