基于新型CdS量子点的光电化学传感器用于检测铜离子
2021-12-25温广明杜晓宇董文霞张宝柱柴杰
温广明 ,杜晓宇 ,董文霞 ,张宝柱 ,柴杰
(1.晋中学院 化学化工学院,山西 榆次 030019;2.山西大学 化学化工学院,山西 太原 030006)
0 引言
铜是人体中第三种丰富的微量金属元素,当人体缺铜时,会产生缺铁样血红素减少进而形成低色素性小细胞性贫血,这与人类健康密切相关。但是,过量Cu2+会损害人体中的肾脏和肝脏。从环境角度来看,Cu2+还可能降低天然水的自净能力[1]。基于有机荧光团或发色传感器[2-6]、新型金属纳米团簇[7-9]、量子点或纳米棒[10-11]等技术已经建立了许多检测铜离子的策略。如荧光[12],比色法[13],电化学传感器[14]和光电化学(PEC)传感器[15-16]。但是,这些方法需要昂贵的仪器和复杂的操作,限制了铜离子的便携式检测和现场应用。
近年来,作为一种新兴技术的光电化学分析在诸如太阳能电池,环境监测和生物分析等许多研究领域中引起了广泛的关注。由于激发源和检测信号的分离,光电化学策略与电化学发光相比具有不同的优势,例如背景低,电势低,并且具有良好的分析性能。光电化学传感器是基于物质的光电转换特性确定待测物质浓度的一类检测装置。光电化学过程即光作用下的电化学过程,在光照射条件下,物质中电子从基态跃迁到激发态,进而产生电荷传递。与电化学反应类似,在光电化学反应体系中也会产生电流的流动。因此,利用光电化学反应可以把光能转变成化学能或电能,通过其逆过程则可以把化学能或电能转换为光能。因此,设计了用于检测农药[17],谷胱甘肽[18],DNA[19],Cu2+离子[20],葡萄糖[21]和 H2O2[22]的光电化学平台。上述光电化学策略通常通过空穴氧化,染料敏化和能量转移增强光电流,并通过量子点分解抑制光电流,消耗核心反应物并阻止电子转移[23]。另一方面,当光电化学材料被光激发并形成电子-空穴对时,可能发生电荷复合,这极大地限制了光电转换效率[24-25]。影响与分析物相关的光电流的另一种方法是通过固定在电极上的纳米颗粒与分析物之间的相互作用[26],形成中间体以破坏纳米颗粒向电极电子转移的导带。该方法对于通过阳极光电化学检测铜离子是有效的。
在这项工作中,基于一种新型的与激发有关的光电化学材料二巯基琥珀酸-CdS量子点(DMSACdS)构建了光电化学传感器,并成功用于检测铜(II)离子(图1)。在光的照射下,量子点的表面上产生的激子和电子被释放到空导带中,从而形成光电流。在铜(II)存在下,Cu2+与DMSA-CdS QD反应生成激子捕获位点。激子陷阱的产生抑制了光电子的逸出,从而构筑了对铜离子“信号降低”的PEC检测方法。这种光电化学策略在较宽的四阶动态范围内表现出良好的性能。该传感器具有操作简单,成本低,灵敏度高的优点,可应用于各种类型的领域,例如免疫分析和即时诊断。
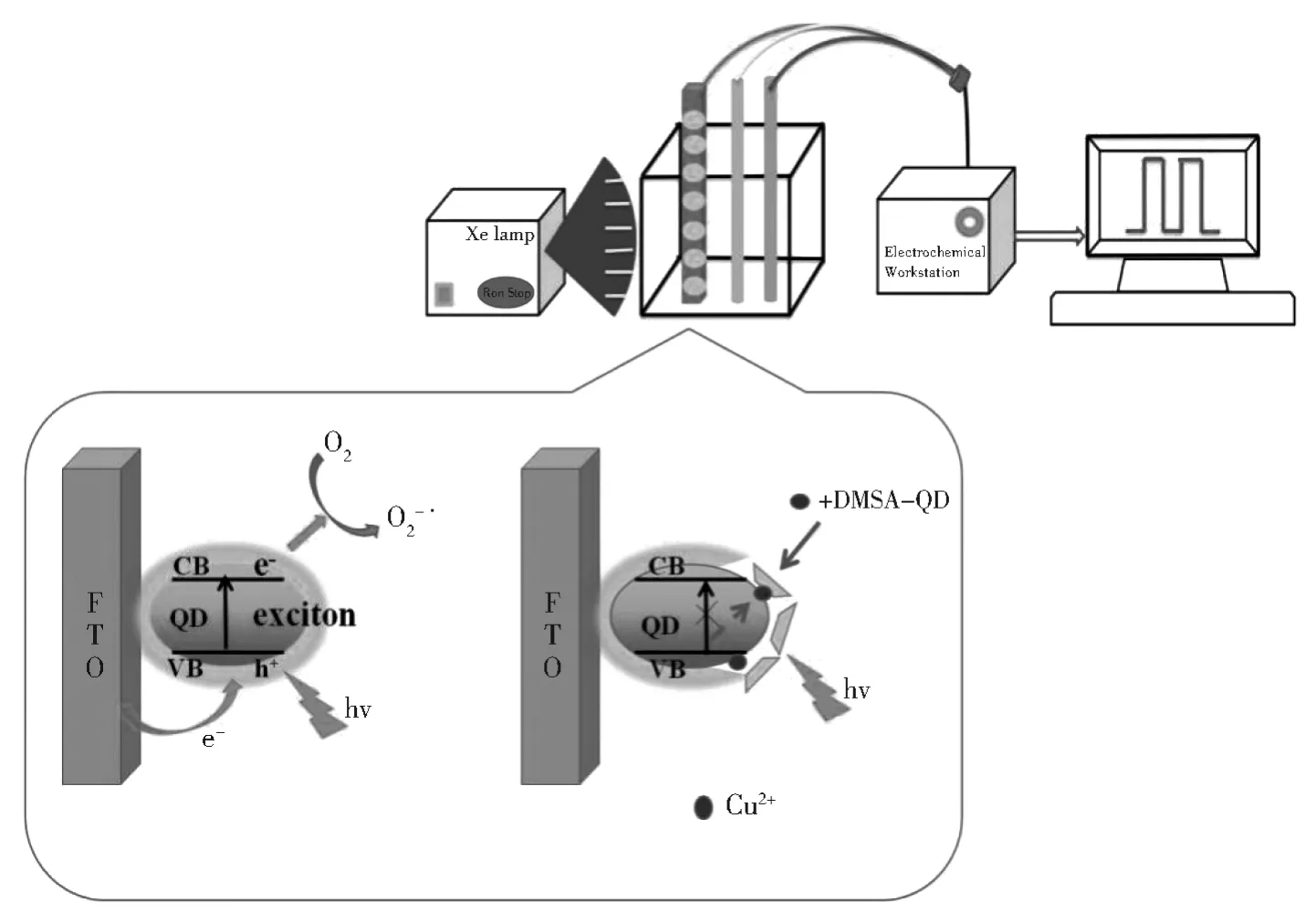
图1 激子俘获机理和光电化学法检测铜离子的示意图Fig.1 Schematic illustration of exciton trapping mechanism and photoelectrochemistry for sensing of Cu2+
1 实验
1.1 试剂
Meso-2,3-二巯基琥珀酸(DMSA),CdCl2·2.5H2O和Na2S·9H2O购自上海金山亭新化工厂。硝酸铜[Cu(NO3)2·3H2O]购自上海阿拉丁公司。聚二烯丙基二甲基氯化铵溶液(PDDA)(20%,分子式(C8H16CIN)n)从Sigma-Aldrich获得。所有其他化学品均为分析纯。用Millipore水净化系统(≥18 MΩ·cm,Milli-Q,Millipore)的超纯水制备水溶液。使用0.01 mol/L,pH 6.0,H3BO3-Na2B4O7缓冲液作为电解液。高纯度氮气用于合成QD。用质量分数70%硝酸和质量分数60%高氯酸(3∶1V/V)的混合物硝化人的头发样品。硝化后,将得到的样品溶液稀释并用0.5 mol/L NaOH溶液中和至pH 6.0,用于进行试剂样品的检测。
1.2 仪器
人发样品中金属元素的电感耦合等离子体(ICP)光谱检测是在J-A1100电感耦合等离子体光谱仪(Jarrell-Ash Co.USA)上进行的。用PHI5000 VersaProbe X射线光电子能谱仪(日本ULVAC-PHI公司)获得X射线光电子能谱(XPS)数据。用JEOL-2100透射电子显微镜(日本)获得透射电子显微镜(TEM)图像。氟氧化锡(FTO)膜盖玻璃购自江苏康迪光学电子有限公司(中国)。在使用前,将FTO玻璃切成4.5 cm×0.8 cm的切片。
1.3 DMSA-CdS量子点的合成
DMSA稳定的CdS QDs通过使用稍微修改的程序合成[27]。将 250 μL DMSA添加到 50 mL的 0.01 mol/L CdCl2水溶液中,然后将N2鼓泡通到整个溶液30 min以除去O2。在此期间,添加1.0 mol/L NaOH将上述溶液的pH值调节至11。然后,将5.0 mL的0.1 mol/L Na2S水溶液倒入溶液中,以获得DMSA封端的水溶性CdS QDs和反应混合物,并将其在N2气氛下回流4 h。最后,获得所需的DMSA稳定的CdS QDs,然后用相同体积的水稀释,并保存在4℃的冰箱中以备将来使用。
1.4 电极的制造和光电化学检测
根据先前建立的方法[28],FTO截面上CdS QDs的修饰是基于PDDA和DMSA封端的CdS QDs之间的静电相互作用。将FTO电极浸入2 mol/L沸腾的KOH溶液和2-丙醇中溶解20 min,用水彻底洗涤,然后在120℃下干燥2 h。将清洁后的FTO切片分别浸入含有0.5 mol/L NaCl的2%PDDA溶液和已获得的CdS QDs溶液中浸泡10 min。在每个浸泡步骤之后,用蒸馏水仔细冲洗电极。将CdS QDs修饰电极指定为FTO/PDDA/CdS。通过将10 μL一定浓度的Cu2+滴到FTO/PDDA/CdS电极上,在室温下干燥,然后用PBS缓冲液洗涤,得到工作电极备用。

图2 CdS量子点的TEM图平均直径约为4 nm~6 nmFig.2 TEM image of the CdS QDs.The average diameter is around 4 nm~6 nm.
PEC测量是在组装好的系统上使用500 W氙灯(CHF-XM-500 W,购自中国北京Trusttech有限公司),单色仪(Omni-λ150,购自 Zolix Instruments Co.,Ltd,中国)和CHI660D电化学工作站(上海晨华仪器有限公司)作为外部电压供应商和光电流检测器。将改进的FTO电极用作工作电极,将铂丝电极用作辅助电极,并将饱和甘汞电极用作参比电极,以将其插入石英PEC电池中以形成三电极系统。将10 mL的0.01 mol/L H3BO3-Na2B4O7缓冲液作为电解质添加到反应池中。通过将单色仪和电化学工作站设置为所需的照明波长和所需的外部电压,在光照下记录光电流信号。
2 结果与讨论
2.1 CdS量子点的电镜图
CdS QDs的透射电镜图表明,其粒径尺寸大约为4 nm~6 nm,且均匀地分布在电极表面,这有利于提高光电转换效率。
2.2 光电化学机理
辐射源是用于激发FTO电极的500 W Xe灯。在0.01 mol/L H3BO3-Na2B4O7缓冲液(pH=6.0)中辐照FTO/PDDA/CdS电极产生较大的光电流(约16 μA,图3,红线),FTO/PDDA电极的光电流很小(黑色线)。CdS QDs的光电流形成机理如图1所示。在材料吸收与其带隙相匹配能量的光子之后,电子从价带(VB)激发到导带(CB),从而形成电子-空穴对。一旦发生该过程,电子将重新复合或被转移。然后,导带中的电子被O2吸收生成O2-,并且价带中的轨道孔可以从FTO电极获得电子,从而产生光电流。
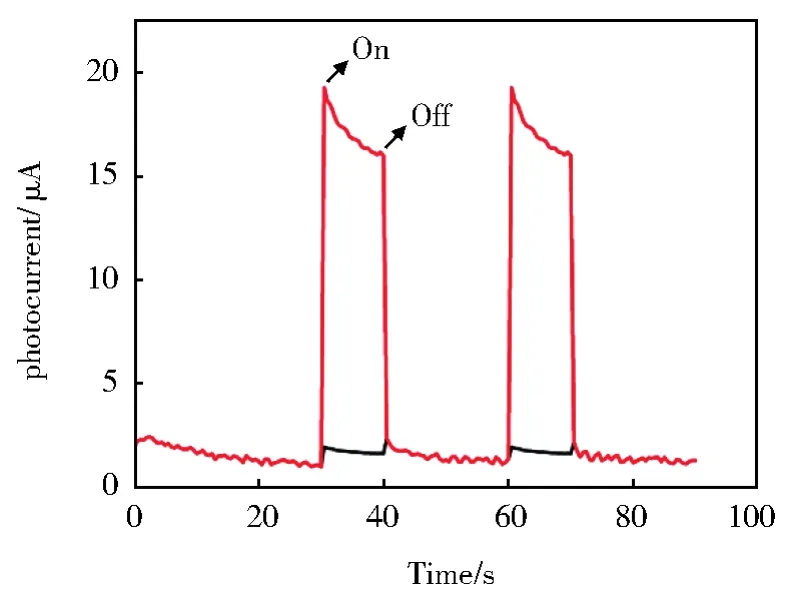
图3 FTO/PDDA/CdS电极(红线)和FTO/PDDA电极(黑线)在0.01 mol/L空气饱和H3BO3-Na2B4O7缓冲液(pH 6.0)中的光电流Fig.3 Photocurrent of the FTO/PDDA/CdS electrode(red line)and FTO/PDDA electrode(black line)in 0.01 mol/Lair saturated H3BO3-Na2B4O7buffer(pH 6.0)
添加铜离子后,量子点修饰的FTO电极的光电流显著下降。这可能归因于DMSA分子中QDs的S原子与QDs的Cu2+和Cd2+之间的竞争,因为CuS的沉积平衡常数(8×10-36)比CdS的沉积平衡常数(7×10-27)小得多[29],表明铜和硫原子之间的金属-S键比镉和硫原子之间的键强。这种相互作用破坏了DMSA和CdS之间的原始Cd-S键[30],导致了量子点的部分分解。另外,Cu2+和S原子之间的相互作用导致Cu2+的部分还原,这为形成激子俘获奠定了基础。量子点表面形成的激子将电子释放到空的导带中,然后被O2吸收产生O2-,价带中的轨道孔可以从FTO电极获得电子,从而产生光电流。
可以通过X射线光电子能谱(XPS)测量来验证QDs表面上Cu2+的产生和激子捕获。Cu2+与量子点相互作用后,Cu 2p3/2的结合能分为两部分,分别具有931.4 eV和932.7 eV的峰(图4A)。932.7 eV处的峰表示Cu(II)的存在,931.4 eV处的峰源自Cu(I)。Cu(I)的氧化还原能级发生在量子点的价带和导带之间,导致产生帽形位点[31]。陷阱位点的形成阻止了激子的产生,从而阻止了光电子和轨道空穴的产生,从而减小了光电流。结合能为404.72 eV和411.47 eV的Cd 3d光谱(图4B)与Cd 3d5/2和Cd 3d3/2匹配良好,证明了Cd2+的存在。S 2p在163.6 eV,164.73 eV和161.2 eV处的峰归结于S 2p1/2和S 2p3/2(图4C),证明了硫元素的存在。
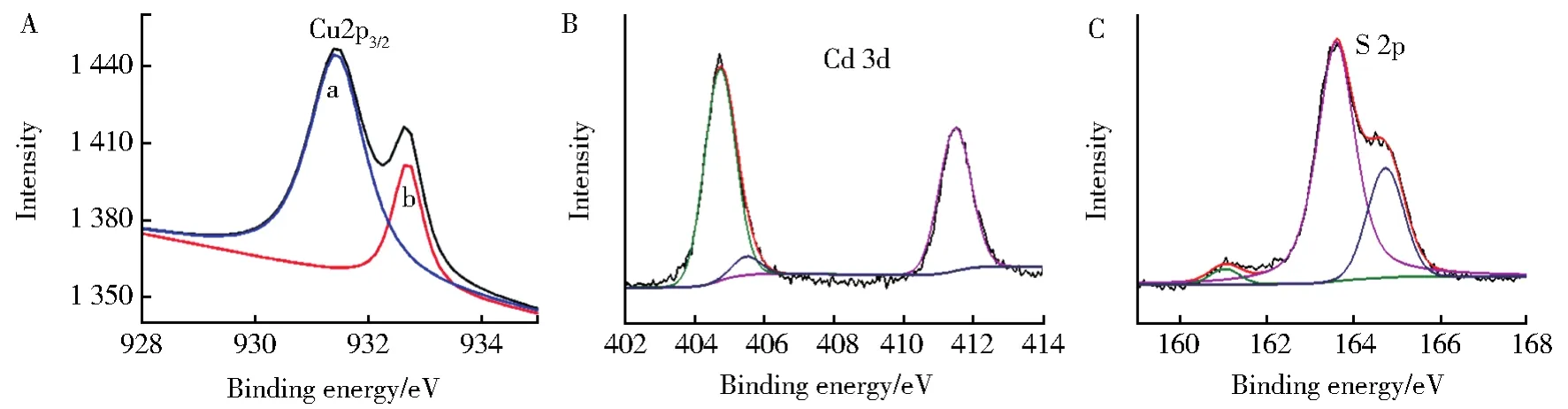
图4 Cu 2p(A),Cd 3d(B),S 2p(C)的XPS光谱Fig.4 XPS spectra of Cu 2p(A),Cd 3d(B),S 2p(C)
2.3 pH的影响
电解质的pH是与光电流响应有关的另一个重要因素。为了研究pH的影响,在4.0~8.0范围内的不同pH下测量了光电流(图5)。在低pH下,QDs容易分解,导致光电流响应变小。在高pH下,暴露于表面缺陷部位的Cu2+将吸附OH-,这将阻止电子从QDs转移到O2,从而降低光电流。光电流响应的最大值出现在pH值为6的情况下。因此,在以下整个实验中均使用0.01 mol/L pH 6.0的H3BO3-Na2B4O7缓冲液。
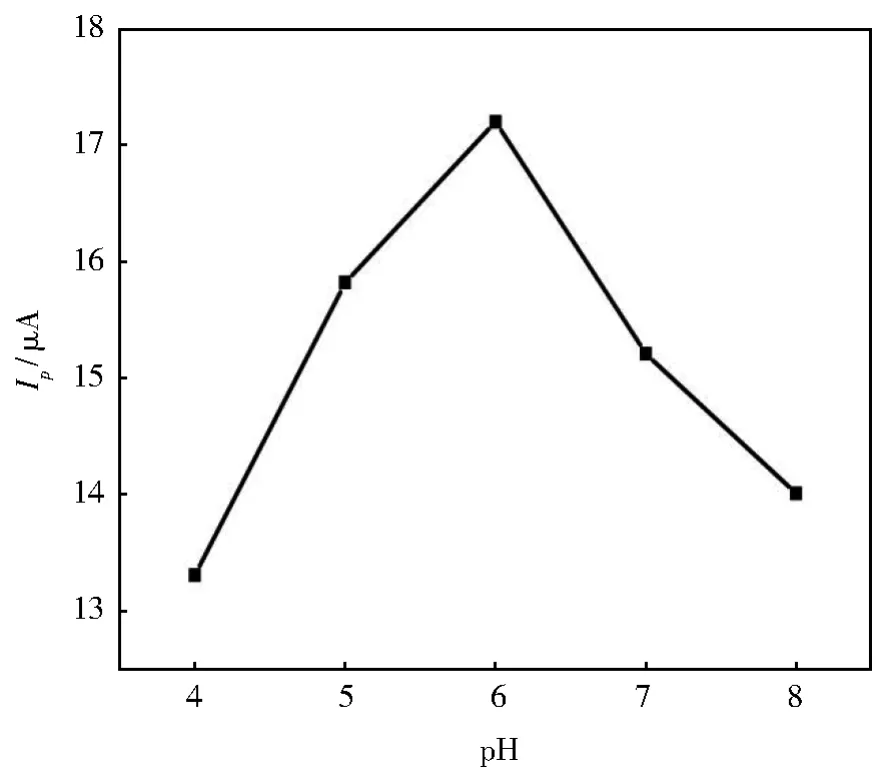
图5 pH的影响Fig.5 The effect of pH
2.4 分析性能
QDs修饰的FTO电极的光电流-时间曲线清楚地显示了在-0.2 V的施加电势下对Cu2+的快速响应。在空气饱和H3BO3-Na2B4O7缓冲溶液的最优条件下,光电流值与Cu2+浓度的对数值呈良好的线性关系(图6)。线性范围为0.01 μmol/L至0.1 mmol/L,信噪比为3时的检出限为0.3×10-8mol/L。如表1所示,线性响应范围比基于荧光猝灭的范围(12.3 nmol/L~2 μmol/L)[32],聚集诱导发射(0 μmol/L~10.0 μmol/L)[33],比色法(0.0015 μmol/L~31.2 μmol/L)[34],荧光共振能量转移(0 nmol/L ~10 nmol/L)[35],原子吸收(0.0157 μmol/L ~0.157 μmol/L)[36]和伏安法(0.05 μmol/L ~6.0 μmol/L)[37]检测范围宽。LOD也低于通过阳极光电化学方法(0.01 mmol/L),原子吸收(0.2 mmol/L)和伏安法(0.031 mmol/L)的检测[38-40]。宽线性范围和低LOD扩展了该方法的实际应用。
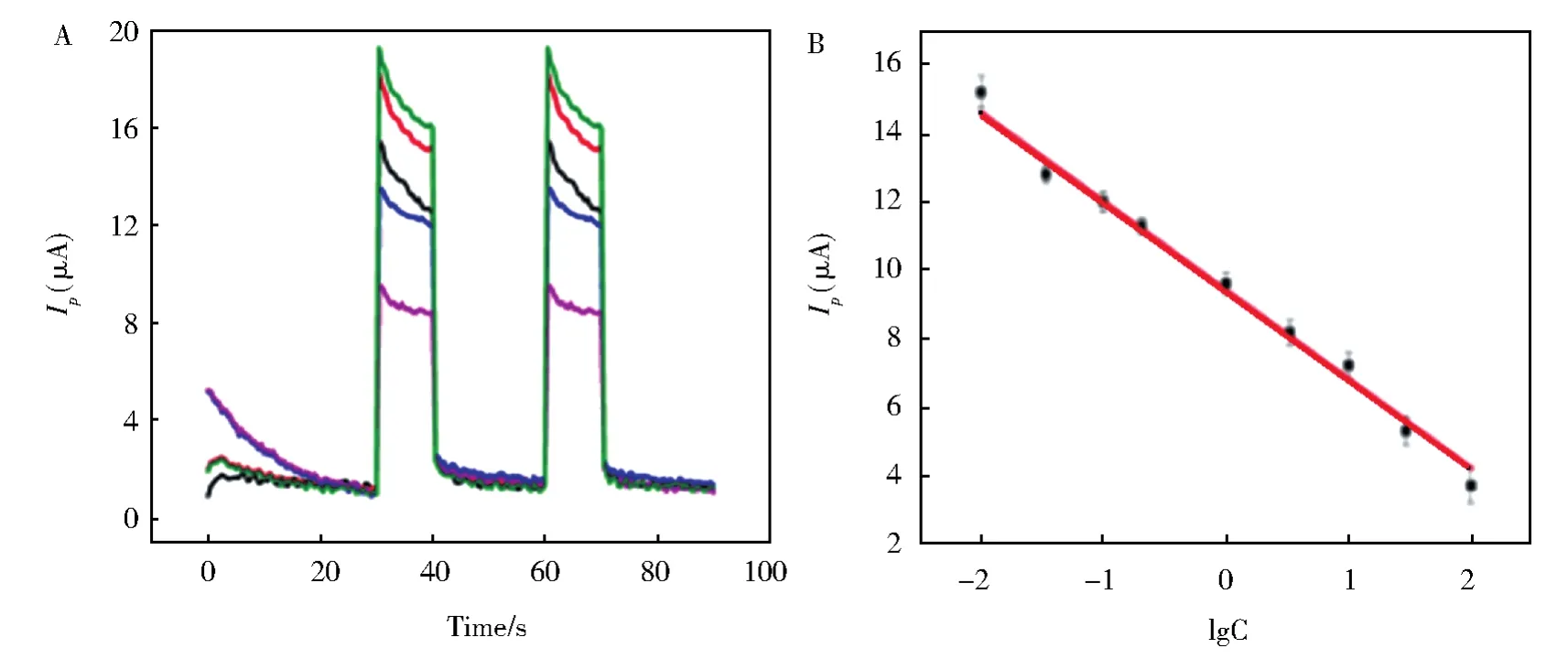
图6 (A)FTO/PDDA/CdS电极在0、0.01、0.05、0.1和1 μmol/L Cu2+存在下的光电流响应(从曲线到底部,0.01 mol/L空气饱和H3BO3-Na2B4O7缓冲液pH 6.0;光照时间=20 s;E=-0.2 V vs SCE);(B)光电流强度与Cu2+浓度的对数的校准曲线Fig.6 (A)Photocurrent responses of the FTO/PDDA/CdS electrode in the presence of 0,0.01,0.05,0.1 and 1 μmol/L Cu2+(from curve up to bottom,0.01 mol/L air saturated H3BO3-Na2B4O7buffer pH 6.0;tlight=20 s;E=-0.2 V vs SCE).(B)The calibration curve of photocurrent intensity upon the concentration of Cu2+

表1 不同材料对Cu2+检测线性范围比较Table 1 Comparison of linear ranges for detection of Cu2+by different materials
2.5 PEC传感器的重现性和稳定性
通过分析独立准备的六个生物传感器,评估了所制备的PEC传感器的可重复性。电流响应相对于1×10-6mol/L Cu2+具有3.4%的相对标准偏差(RSD),这证实了上述方案具有可接受的重复性和准确性。探索了所制备传感器的光电流响应的稳定性(图7)。在光照和避光时各检测10次且光电流值基本保持不变(RSD=2.0%),这证明了制备的传感器具有良好的稳定性。
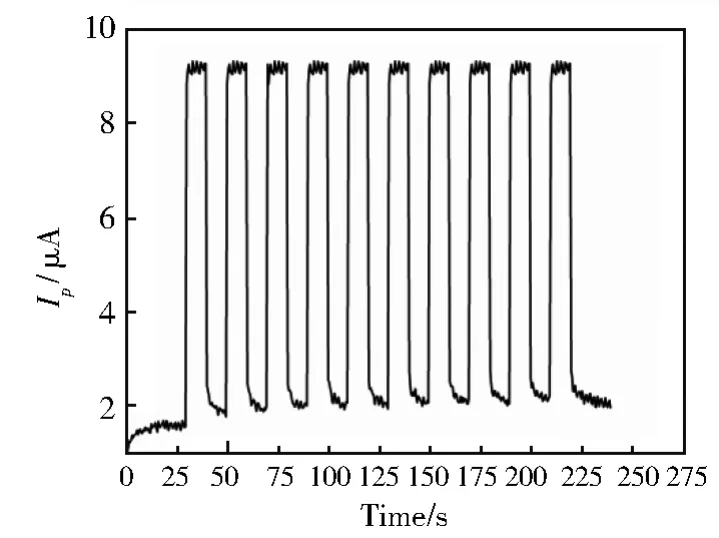
图7 PEC生物传感器在0.01 H3BO3-Na2B4O7缓冲液(pH 6.0)中的光电流响应,该缓冲液包含1×10-6mol/L Cu2+,且在光照和避光时各检测10次Fig.7 Photocurrent response of the PEC biosensor in 0.01 H3BO3-Na2B4O7buffer(pH 6.0)contain1×10-6mol/L Cu2+at 10 intervals of excitations with light on and off
2.6 干扰物
为了方便,准确地监测人发样品中铜元素的含量,需要研究 1×10-6mol/L Cd2+,Fe2+,Mg2+,Ca2+,Ba2+,Fe3+,Ni2+,Zn2+,Mn2+和Pb2+作为潜在干扰物时的光电流响应(图8)。结果证实上述每种可能的干扰剂对检测几乎没有影响。因此,该方法具有良好的抗干扰能力。而且,可以在低还原电位下进行检测,还原剂不干扰检测。
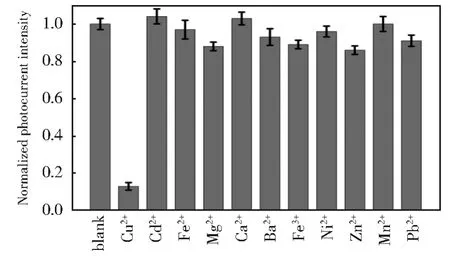
图8 在相同条件下,在存在1×10-6mol/L单个离子的情况下,FTO/PDDA/CdS电极的归一化光电流强度Fig.8 Normalized photocurrent intensities of FTO/PDDA/CdS electrode in the presence of 1×10-6mol/L individual ions under the same conditions
2.7 样品分析
为了评估该方法的分析可靠性和应用潜力,将其用于检测人头发中铜的含量。将测量结果与从电感耦合等离子体(ICP)光谱法获得的参考值进行比较,以评估PEC传感器的分析可靠性和可能的应用。结果显示在表2中。PEC传感器和ICP之间的相对偏差范围是-4.9%至2.6%,这证实了该方法对于真实样品检测具有良好的准确性。
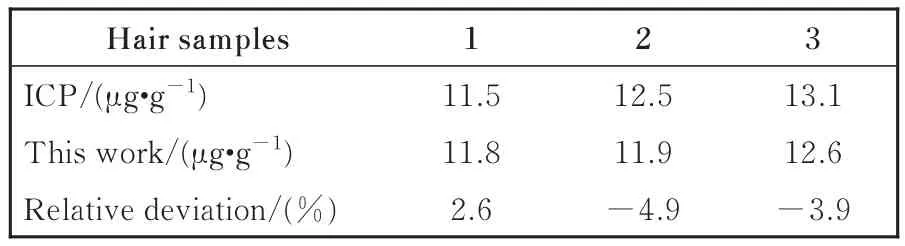
表2 两种方法分析人发样品的比较Table 2 Comparison of two methods in analyzing human hair samples
3 结论
开发了一种基于激子俘获的新型光电化学传感策略,用于铜离子的选择性检测。在光的作用下,一些分析物与量子点相互作用,在量子点的表面上形成激子俘获位点,从而降低了光电转换效率和光电流响应,从而提供了一种新的光电化学方法。所获得的光电化学传感器具有性能好,线性范围宽,电势低,灵敏度高,精度准确的优点。它可以成功地应用于铜离子的检测。这项工作为光电化学传感提供了一种新颖而有希望的方法。
