基于网络药理学探讨三棱-莪术治疗慢性萎缩性胃炎的分子机制
2021-12-24涂文玲林泽豪连雄瀚甘慧娟
涂文玲,林泽豪,连雄瀚,甘慧娟*
(1.福建中医药大学 中医证研究基地,福建 福州 350122;2.福建省中医健康状态辨识重点实验室,福建 福州 350122)
慢性萎缩性胃炎(Chronic atrophic gastritis,CAG)是胃癌发展过程中的关键环节,被视为胃癌前疾病,近年来发病率呈明显上升趋势,癌变率为1.2%~7.1%,并向低龄化发展。西医治疗CAG主要采取根除Hp、胃黏膜保护等方法[1],临床取得了一定疗效,但多以对症治疗为主,易反复发作,因而迫切需要寻求新方法用以防治CAG。中医药在整体观念指导下进行辨证论治,能够有效改善CAG临床症状和逆转胃黏膜萎缩,具有很好的防治作用[2-3]。中医认为CAG患者久病体虚,久病必瘀,血瘀始终是CAG的病理因素,贯穿始终[4-6]。三棱性平,莪术性温,均归肝、脾经,均具有破血行气、消积止痛之功效,两者常常用来治疗CAG,郭云协等[7]在治疗CAG伴肠化过程中加入三棱、莪术破血消积,起到逆转肠化生的作用。虽然三棱、莪术在临床得到肯定,但是其作用机理并不明确,因此本研究运用网络药理学对三棱、莪术治疗CAG作用机理进行研究,并利用分子对接技术进行验证,以期为后续研究提供参考。
1 材料与方法
1.1 三棱-莪术中药成分和靶点筛选
利用TCMSP数据库(https://tcmspw.com/tcmsp.php)检索“三棱”“莪术”两味中药,以口服生物利用度(OB≥30%)和类药性(DL≥0.18)进行筛选,收集三棱-莪术的活性成分,同时检索活性成分的蛋白靶标,将蛋白靶标一一输入Uniprot(https://www.uniprot.org/)数据库进行基因名转化。以“chronic atrophic gastritis”为检索词在Gene Cards数据库(https://www.genecards.org/)、OMIM数据库(https://omim.org/)、PharmGKB数据库(https://www.pharmgkb.org/)、DrugBank数据库(https://go.drugbank.com/)进行检索,综合各个数据库检索得到的靶点,并去除重复项,得到CAG疾病相关靶点。
1.2 韦恩图、蛋白网络互作(PPI)网络及药物-活性成分-靶点网络构建
利用Venny(https://bioinfogp.cnb.csic.es/tools/venny/)在线工具绘制韦恩图,获取三棱-莪术和CAG的共同靶点,将共同靶点输入String数据库(https://string-db.org/),设置置信度为0.4,制作PPI网络图,用Cytoscape3.8.0 软件进行可视化,最后将活性成分-共同靶点信息导入Cytoscape3.8.0软件,绘制出活性成分-共同靶点网络图。
1.3 共同靶点的GO、KEGG富集分析和分子对接
利用R软件进行GO和KEGG富集分析,以P<0.05为差异有统计学意义,在PDB、PubChem数据库获取三棱-莪术的主要活性成分和核心靶点的晶体结构,再借助AutoDockTool Vina软件将主要活性成分与核心靶点进行分子对接,搜集结合值,佐证三棱-莪术治疗CAG的合理性。
2 结果
2.1 三棱-莪术中药活性成分及靶点筛选结果
通过TCMSP数据库收集、筛选(OB≥30%、DL≥0.18)出三棱-莪术活性成分8个,其中三棱5个、莪术3个。对该活性成分进行靶点查找,剔除未找到靶点的活性成分,获取5个有效活性成分,见表1。对通过TCMSP数据库找到的药物靶点进行基因名转化,去除重复项,共得到66个靶点;从GeneCards、OMIM、PharmGKB、DrugBank数据库获得疾病靶点377个;将三棱-莪术的作用靶点和疾病靶点分别输入Venny在线工具绘制韦恩图取交集,匹配得到三棱-莪术治疗CAG的共同靶点9个,见图1。

注:A:韦恩图;B:三棱-莪术与CAG的共同靶点。图1 疾病共同作用靶点

表1 三棱-莪术的活性化合物
2.3 网络构建及蛋白互作结果
利用Cytoscape3.8.0软件构建出活性成分-共同靶点模型,见图2A,其中绿色节点代表该活性成分来自三棱(4个),绿色和蓝色各半节点代表该活性成分来自三棱和莪术(1个),黄色节点代表药物与疾病的共同靶点(9个)。最后利用String数据库和Cytoscape 3.8.0软件进行制作共同靶点PPI网络图,见图2B。依据所构建的结果,发现CASP3、PPARG、PTGS2、JUN、NOS2是三棱-莪术治疗CAG的核心靶点(Degree>4.89(平均值)),见表2;且β-谷甾醇、芒柄花黄素是三棱-莪术治疗CAG的主要活性成分(Degree>3.6(平均值)),见表3。

注:A:活性成分-靶标网络图;B:核心靶点的相互作用网络图。图2 药物与CAG 之间网络

表2 PPI网络中靶点的相关参数

表3 活性成分-共同靶点网络图中活性成分的相关参数
2.4 GO和KEGG富集分析
通过R软件对9个共同靶点进行GO功能富集分析,根据P<0.05,得到生物过程(Biological process,BP)条目878个,细胞组成(Cell composition,CC)条目21个,分子功能(Molecular function,MF)77个,其中生物过程主要富集于对细菌源分子的反应、细胞对外界刺激的反应等,细胞组成主要富集于RNA聚合酶Ⅱ转录因子复合物、线粒体外膜等,分子功能主要富集于半胱氨酸型内肽酶活性参与细胞凋亡过程、死亡受体结合等,见图3,红色越深代表P值越小,节点越大代表富集靶点数量越多。
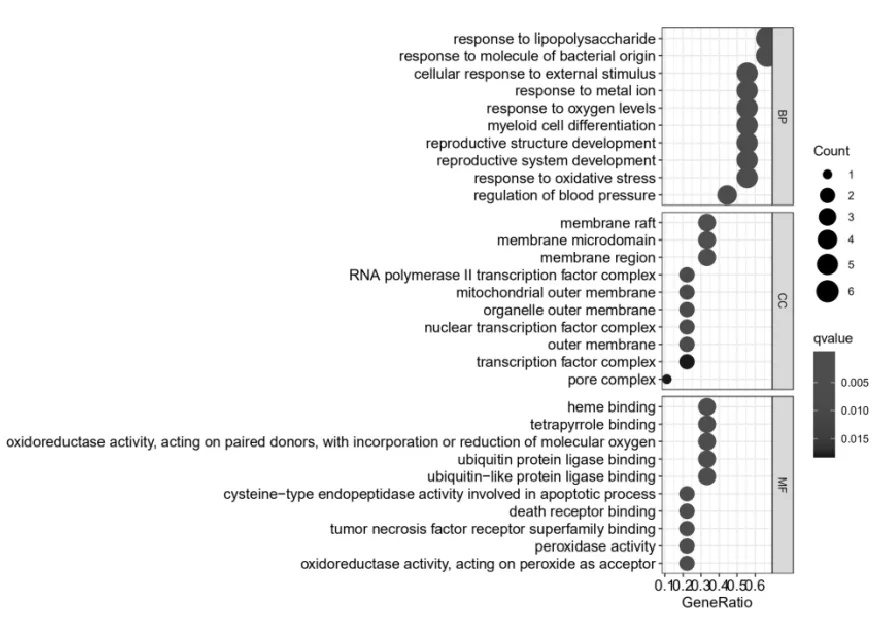
图3 GO富集结果信息(top10)
通过R软件对9个共同靶点进行KEGG通路富集分析,根据P<0.05筛选到74条信号通路,主要涉及IL-17信号通路、TNF信号通路、P53信号通路、HIF-1信号通路等,见图4,红色越深代表P值越小,节点越大代表富集靶点数量越多。

图4 KEGG富集结果信息(top30)
2.5 分子对接结果
核心靶点CASP3、PPARG、PTGS2、JUN、NOS2在PDB数据库进行搜索,获得晶体结构ID依次为2C1E、2Q59、5F19、1JNM、2NSI,再与核心活性成分进行分子对接,得出其对接的结合能(kcal/mol)数值,见表4。结合能为负值表明配体和受体可以自发结合[8],并且结合能越低,该结合构象越稳定,发生作用的可能性越大[9]。

表4 分子对接结合能信息
3 讨论
当前CAG被认为是胃癌的癌前病变,其经历的过程为:正常胃黏膜-慢性浅表性胃炎-萎缩性胃炎-肠上皮化生-异型增生-胃癌,随着病情加重,胃黏膜萎缩可发展为肠上皮化生,这其实与叶天士“久病入络”“久痛入络”学说有异曲同工之处[10]。现代医学认为胃黏膜血流量减少、微循环灌注差,进而导致CAG,这与中医瘀血具有很大相似性。研究发现胃黏膜萎缩伴重度肠上皮化生多以胃络瘀血证为主[11]。三棱、莪术作为活血化瘀的代表中药,现代药理学研究表明,两药均有改善血液流变学、扩张血管、调节血管通透性和抗癌作用[12];临床研究发现三棱-莪术药对可通过显著抑制内皮细胞增殖、 抑制肿瘤细胞生成、直接杀死肿瘤细胞、抑制血管生成、阻断信号传导通路等机制起到治疗胃癌的作用[13-15]。近年来,愈来愈多研究者对活血化瘀治疗CAG进行临床研究,在治疗一些肠上皮化生CAG患者过程中,可以适当选加具有一定防癌、治癌作用的清热活血之品,通过改善胃黏膜微循环状态,增加胃黏膜血流,可逆转黏膜腺体萎缩和肠上皮化生等病变[16]。
通过分析PPI网络分析和“药物-活性成分-靶点”网络的相关参数,可知三棱-莪术治疗CAG的核心活性成分是 β-谷甾醇和芒柄花黄素,β-谷甾醇是一种安全的天然药物,具有抗炎、抑制肿瘤等广泛的药理活性,研究表明β-谷甾醇可通过提升血清 NO 含量而提高受损胃黏膜的修复能力[17]。芒柄花黄素为一种生物活性异黄酮,具有完善的生物功能和抗肿瘤作用[18],研究发现芒柄花黄素可防止血管生成和癌转移,可抑制人胃癌 MKN-45 细胞株的增殖[19]。三棱-莪术主要作用靶点是CASP3、PPARG、PTGS2、JUN、NOS2。CASP3 是在整个凋亡通路中起到枢纽作用的重要凋亡信号分子[20],研究发现CASP3的表达在人的胃癌组织比正常组织要明显降低[21]。PPARG是由配体激活的转录因子,研究发现PPARG在胃癌组织的低表达可能是胃癌转移的早期事件[22]。PTGS2是一种促炎症因子,其高表达与肿瘤细胞快速生长、凋亡受抑制以及浸润转移有关[23]。JUN原癌基因的激活在肿瘤的发生发展中起到重要作用,能调控细胞的生长、分化、凋亡[24]。NOS2在多种生物过程中充当生物介质,包含抗肿瘤活性,研究发现,NOS2与肿瘤血管形成有关,可能通过抑制NOS2的表达来抑制肿瘤血管的发生,这可能是治疗肿瘤的一种方法[25]。因此,三棱-莪术的β-谷甾醇、芒柄花黄素这两种核心成分可能是通过抗炎、调控细胞凋亡、抑制肿瘤血管的形成对CAG起到治疗作用。
GO功能富集发现,三棱-莪术活性成分的生物学过程涉及脂多糖、细菌源分子的反应等,分子功能主要富集于半胱氨酸型内肽酶活性参与细胞凋亡过程等,KEGG通路富集分析可知其主要涉及IL-17信号通路、TNF信号通路、P53信号通路、HIF-1信号通路等。IL-17 由辅助性 T 细胞(Th17)及先天性免疫细胞等分泌的促炎症因子,在多种炎性反应发挥关键作用,研究发现 IL-17可通过NF-κB 信号通路刺激下游效应因子发生转录,参与胃癌的免疫调控以及促进胃癌的发生发展[26]。TNF具有多种生物学功能,可诱导细胞增殖分化,抑制细胞凋亡,促进炎症和肿瘤发展,加重CAG[27]。P53是一种抑癌基因,能抑制细胞增殖、生长和转化,在CAG过程中,病情越严重,p53的表达率越高[28]。HIF-1由HIF-α和HIF-β组成[29],其中HIF-1α在缺氧环境下可促进肿瘤血管生成,因此抑制HIF-1α的表达可减少肿瘤血管生成[30]。因此,三棱-莪术可能是通过抗炎、调控细胞凋亡、抑制肿瘤血管形成来达到治疗CAG的效果。分子对接显示三棱-莪术的核心活性成分与核心靶点有着很好的结合性,发挥作用的可能性极大。
综上,本研究从三棱-莪术中筛选出两个核心活性成分(β-谷甾醇和芒柄花黄素)和5个核心靶点(CASP3、PPARG、PTGS2、JUN、NOS2)进行结合的潜能,并且得出三棱-莪术治疗CAG的可能机制是通过抗炎、调控细胞凋亡、抑制肿瘤血管形成,这为治疗CAG的中药天然药物和单体药物的研发提供了新思路。但计算机生物方法本身具有局限性,我们在接下来将结合动物实验来进行验证。
