早产儿支气管肺发育不良的影响因素
2021-11-03李瑞改
李瑞改
(邓州市人民医院 新生儿监护室,河南 南阳 474150)
支气管肺发育不良(bronchopulmonary dysplasia,BPD)是新生儿重症监护病房(Neonatal Intensive Care Unit,NICU)中早产儿较为常见的并发症之一,患儿长期依赖氧生存,生长发育过程中易因反复肺炎而多次住院,且BPD与神经系统并发症密切相关,可引起患儿体能、智力发育障碍等,导致早产儿预后不良[1]。尽管国内外对BPD已经进行了较为深入的研究,普遍认为BPD是在遗传易感性的基础上,由氧中毒、低出生体质量等多种因素所致,但其确切病因仍不明确,防治效果并不理想[2-3]。因而,探讨更多引起BPD发生、发展的危险因素具有必要性。鉴于此,本研究旨在分析NICU中早产儿发生BPD的可能影响因素。
1 资料与方法
1.1 一般资料回顾性收集2019年5月至2021年5月邓州市人民医院NICU收治的50例发生BPD的早产儿的临床资料,设为发生组。按1∶1纳入同期收治的50例未发生BPD的早产儿的临床资料,设为未发生组。100例NICU早产儿:男55例,女45例;出生方式为剖宫产84例,阴道分娩16例;出生时胎龄26~32周,平均(29.29±0.48)周;出生时体质量992~1 503 g,平均(1 329.96±26.85)g;出生时身长28~49 cm,平均(38.68±2.76)cm;多胎9例;存在宫内窘迫31例;出生1分钟Apgar评分≤7分31例;存在败血症19例;存在宫内感染51例。
1.2 入选标准(1)纳入标准:①于本院出生,出生时胎龄≤32周;②出生后24 h内转入本院NICU;③住院时间>28 d;④临床资料完整。(2)排除标准:①存在呼吸系统畸形;②染色体异常、遗传代谢类疾病;③先天性心脏病、气胸、胸腔积液及膈疝等疾病;④合并肝肾疾病;⑤先天性肺部发育不全;⑥存在外科疾病或转至外科手术;⑦住院期间转院或发生院内病死。
1.3 BPD评估方法根据美国国立儿童保健与人类发展研究院(National Institute of Child Health and Human Development,NICHD)制定的相关标准[4]评估BPD发生情况:(1)任何氧依赖(吸入氧浓度>21.00%)>28 d;(2)有慢性或进行性呼吸功能不全,表现为低氧血症或高碳酸血症;(3)存在肺部影像学表现(胸部X线或CT下可见两肺纹理增强、通透性降低、磨玻璃样等表现)。符合以上指征则可评估为BPD。
1.4 临床资料收集方法查阅早产儿出生后相关资料,包括性别(男、女)、出生方式(剖宫产、阴道分娩)、出生时胎龄、出生时体质量、出生时身长、多胎(是、否)、存在宫内窘迫(是、否)、出生1分钟Apgar评分≤7分(是、否)( Apgar评分标准[5]:总分为0~10分,正常新生儿8~10分,轻度窒息5~7分,重度窒息≤4分)、存在败血症(是、否)、存在宫内感染(是、否)、机械通气(mechanical ventilation,MV)治疗时间及血清25-羟维生素D[25-hydroxy-vitamin D,25-(OH)D]水平等。25-(OH)D检测方法:采集早产儿出生时足底静脉血2 mL,于常温下静置10~20 min,于4 ℃环境中保存,以3 000 r·min-1速率离心处理15 min,离心半径为13.5 cm,取血清,采用迈瑞CL-1000i化学发光免疫分析仪检测血清25-(OH)D水平。试剂盒选自广州万孚生物技术股份有限公司,相关操作需严格遵照试剂盒说明书进行。

2 结果
2.1 临床资料与未发生组比较,发生组存在宫内感染占比较高,MV治疗时间较长,出生时血清25-(OH)D水平较低(P<0.05);两组性别、出生方式、出生时胎龄、出生时体质量、出生时身长、多胎、存在宫内窘迫、出生1分钟Apgar评分≤7分占比、存在败血症比较,差异无统计学意义(P>0.05)。见表1。

表1 两组NICU早产儿临床资料比较
2.2 NICU早产儿发生BPD的影响因素将NICU早产儿BPD发生情况作为因变量(发生=1,未发生=0,将2.1中比较结果P放宽至<0.15,纳入符合条件的变量(自变量赋值见表2),建立logistic回归分析模型,结果显示,存在宫内感染、MV治疗时间较长、出生时血清25-(OH)D低表达均为NICU早产儿发生BPD的影响因素(P<0.05)。见表3。

表2 赋值说明
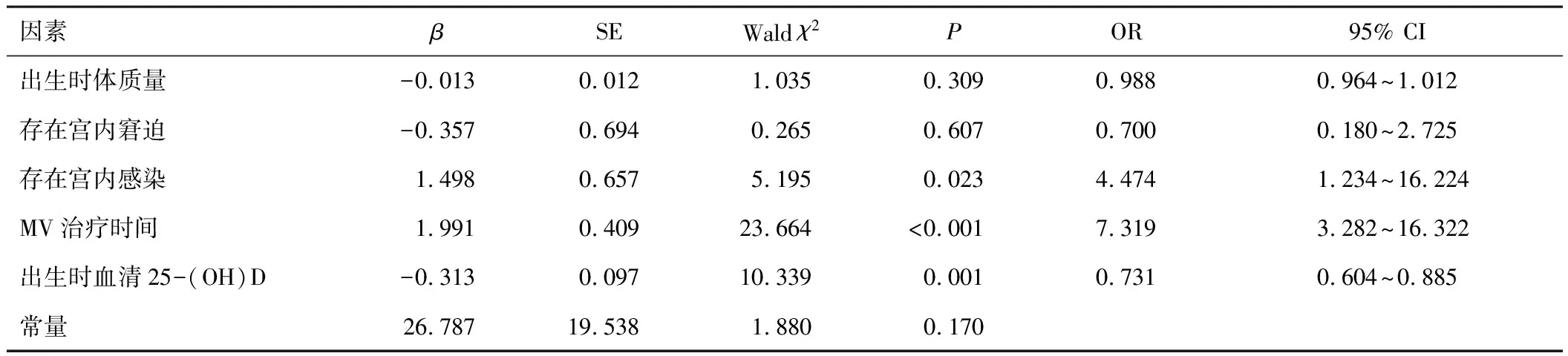
表3 NICU早产儿发生BPD的影响因素
3 讨论
BPD是一种早产儿慢性肺部疾病,是目前早产儿致残、致死的主要原因之一。目前BPD发病机制尚不明确,但为多种因素综合作用的结果。因此,寻找可能影响NICU早产儿发生BPD的影响因素,对临床干预措施的制定具有重要的参考价值。
本研究经logistic回归分析结果显示,存在宫内感染、MV治疗时间较长、出生时血清25-(OH)D低表达均可能是NICU早产儿发生BPD的影响因素。产前母体患有细菌性阴道炎、巨细胞病毒感染等可使各种炎症因子水平升高,导致胎肺发育受阻并触发早产[6]。各种炎症因子可损伤呼吸道上皮与肺毛细血管内皮细胞,增加血管通透性,导致肺间质、肺泡和气道水肿;炎症因子可抑制肺泡成纤维细胞和弹性蛋白纤维束生成,促使正常肺泡、肺血管的发育停滞,进而增加BPD风险[7]。早产儿体液免疫和细胞免疫均不成熟,感染可造成早产儿脱机困难、延长MV治疗时间等,加重肺组织充血、水肿及炎症等反应,促使BPD发生发展。对此建议,积极防治母体感染,避免胎儿出现感染,以降低BPD发生率。MV治疗时间较长引起的呼吸机相关性肺炎(ventilator associated pneumonia,VAP)的风险越高,而VAP可致肺部继发感染,影响早产儿肺部发育;VAP病原菌多具有多重耐药性,可加重早产儿病情,进一步延长MV治疗时间,加重肺损伤,增加BPD发生的风险[8]。MV时高气道压或高潮气量可引起肺泡过度扩张,导致毛细血管内皮、肺泡上皮细胞等出现机械性损伤,液体渗漏至肺泡腔,大量促炎因子、炎症因子被释放,引起肺水肿、纤维蛋白沉积、肺表面活性物质降低,导致肺部损伤,进而诱发BPD[9]。对NICU早产儿进行MV治疗时需根据早产儿的病情、血气结果来调整呼吸机参数,给予适宜的氧浓度,尽快撤机,以降低BPD风险。多项研究显示,维生素D与肺部疾病的发生、发展密切相关[10-11]。维生素D的生物学功能复杂多样,可能通过参与多个环节对BPD的发生和发展过程产生影响。维生素D在肺发育的腺体期和囊泡期分别在近端气道和远端气道形成时上调维生素D通路基因,促进肺发育;维生素D可刺激肺泡表面活性物质,促进Ⅱ型肺泡上皮细胞的分化和增殖,同时可抑制肺泡纤维细胞的凋亡[12]。因而,维生素D水平的改变可影响胎儿的肺部发育。血清25-(OH)D低表达抑制基质金属蛋白酶和肿瘤坏死因子-α合成能力减弱,导致纤维母细胞增殖和胶原合成增加,破坏肺间质,影响胎儿早期肺发育和晚期肺重建,加重气道重塑,诱发BPD。对此建议,母亲孕期需适当补充维生素D,促进胎儿肺发育,以此降低出生后BPD发生率。
综上所述,临床应针对上述因素,实施相应干预措施,如尽快撤机、补充维生素D等来降低BPD发生的风险。
