右美托咪定在晚期癌痛中的镇痛作用及安全性评价
2021-10-30赵星黄芳蒲军成
赵星,黄芳,蒲军成
(南充市嘉陵区人民医院麻醉科,四川 南充 637000)
0 引言
疼痛是癌症患者最常见的临床症状之一,据报道,晚期癌症患者中有60%-80%存在慢性疼痛[1],其中64%为中重度疼痛,严重影响患者的生活质量。因此,对于癌症患者来说,控制疼痛是终末期关怀的最基本要求。根据“癌痛的三阶梯疗法”,晚期癌痛患者主要以阿片类镇痛药为主[2]。但是,阿片类镇痛药伴随的剂量依赖性呼吸抑制、便秘、瘙痒、恶心呕吐等副作用极大地影响其临床应用。右美托咪定是高选择性α2受体激动剂,不仅具有镇静、镇痛作用,还有抑制交感、抗炎和脏器保护等作用[3-4]。起初,FDA批准将其应用于成人重症监护病房短时间的镇静与镇痛,但是随着研究的不断深入,右美托咪定早已属于“规定之外”的药物。研究表明,右美托咪定通过抑制疼痛相关炎症因子、受体、酶的表达而发挥疼痛效应[5]。此外,右美托咪定还可缓解长期服用阿片类止痛药后的痛觉过敏[6]。基于上述,右美托咪定作为需长期使用阿片类药物的晚期癌痛患者的辅助镇痛药物可能具有极高的临床应用价值。
1 资料与方法
1.1 一般资料
收集2020年1月至2021年1月南充市嘉陵区人民医院就诊的晚期癌痛患者40例,根据入院顺序编号,按照随机数字表法分为右美治疗组和常规治疗组,每组20例。所有纳入研究的患者及其家属均签署知情同意书,且研究经医院伦理委员会的同意。两组患者的一般情况比较差异无统计学意义,P>0.05(见表1)。病例纳入标准:符合癌症诊断标准,且丧失放、化疗及手术治疗机会者;VAS评分≥4分且年龄≥18岁;签署知情同意书,自愿作为受试对象,接受本实验方法治疗。排除标准:合并有严重心脑血管、肝、肾疾病者;对右美托咪定以及阿片类镇痛药有严重过敏反应者;因病情需要改用其他治疗方法者;拒绝抽血,不配合本实验方法治疗者。
1.2 材料及试剂
LDZ4-0.8型低速自动平衡离心机(北京医用离心机厂),GNP-9080隔水式电热恒温培养箱(上海精宏实验设备有限公司),TG-16W台式高速离心机(湖南湘仪实验室仪器有限公司)-80℃超低温冰箱MDF-C8V(N)(日本三洋公司),爱普微电脑电动注药泵(南通爱普科学仪器有限公司),爱普微电脑电动注药泵配用液袋(南通爱普科学仪器有限公司),盐酸右美托咪注定射液(江苏恩华),舒芬太尼注射液(宜昌人福),盐酸托烷司琼注射液(河北信康),人P物质及皮质醇ELISA试剂盒(上海碧云天)。
1.3 方法
常规治疗组患者给予单纯舒芬太尼治疗:舒芬太尼150μg+托烷司琼20mg用0.9%氯化钠注射液稀释到300mL至爱普输注泵,维持剂量为5-8mL/h根据疼痛程度调整;右美治疗组患者使用右美托咪定辅助治疗:右美托咪定400μg+舒芬太尼150μg+托烷司琼20mg用0.9%氯化钠注射液稀释到300mL至爱普输注泵,维持剂量为5-8mL/h根据疼痛程度调整。两组患者的观察周期均为7天,常规心电监护,使用过程中注意观察注药泵是否运行正常,动态监测心率、血压及氧饱和度,如有不良反应出现,及时处理,必要时停用输注泵。分组及药物的配制均由同一护士完成,且该护士不参与到研究中,保证研究人员与患者双盲。
1.4 观察指标
观察患者治疗前1天(T0)、治疗后3天(T1)、治疗后7天(T2)的VAS、SAS评分,VAS评分采用长度为10 cm的标尺,标有10个刻度,两端分别标为“0”和“10”,其中0代表不痛,10代表最剧烈的疼痛,嘱患者在标尺上标出能代表自己疼痛程度所对应的位置,根据标出的位置给出评分;Zung焦虑自评量表进行SAS评分,评分结果: 50~59分为轻度焦虑、60~69分为中度焦虑、70分以上为重度焦虑。
在上述时间点清晨8点空腹状态下,用促凝试管抽取患者的肘正中静脉血2mL。4℃静置30min待血液凝固后,放入高速离心机(4000转/min,4-5min),提取上清液-80保存,按照ELISA试剂盒说明书检测皮质醇(Cortisol, Cor)、P物质浓度。
1.5 统计学方法
使用 SPSS 19.0 统计软件对数据进行统计分析,计量资料以均数 ± 标准差(±s)表示,两组比较采用独立样本的t检验,组内比较采用单因素方差分析,计数资料比较采用c2检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 两组晚期癌痛患者一般资料比较
两组晚期癌痛患者性别、年龄、病种均差异无统计学意义,(P>0.05),具有可比性,见表1。
2.2 两组晚期癌痛患者不同时间点VAS评分比较
两组患者治疗前T0时的VAS 评分差异无统计学意义(P>0.05);经治疗后VAS 评分随治疗进展而降低,于治疗后T1、T2时间点,VAS评分均明显低于T0,差异有统计学意义(P<0.05); T1、T2时,右美治疗组VAS评分均低于常规治疗组,差异有统计学意义(P<0.05),见表2。
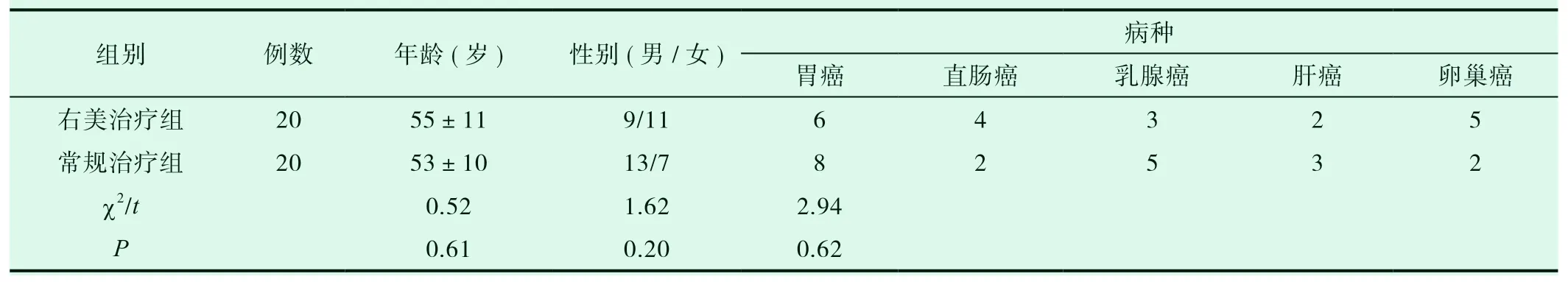
表1 两组晚期癌痛患者一般情况比较
表2 两组晚期癌痛患者治疗前后VAS评分比较(±s,分)
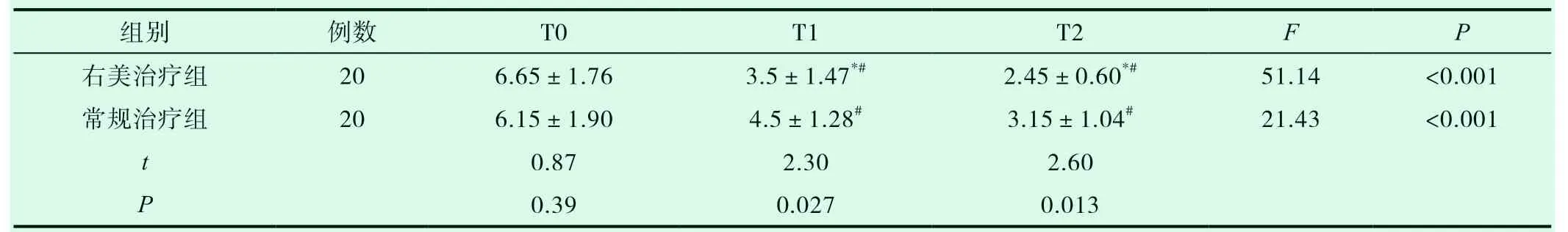
表2 两组晚期癌痛患者治疗前后VAS评分比较(±s,分)
注:与常规治疗组比较, *P<0.05;与同组T0比较, # P<0.05。
?
2.3 两组晚期癌痛患者治疗前后焦虑程度比较
两组患者治疗前T0时的SAS评分差异无统计学意义(P>0.05);经治疗后SAS 评分随治疗进展而降低,于治疗后T1、T2时间点,SAS评分均明显低于T0,差异有统计学意义(P<0.05);T1、T2时,右美治疗组SAS评分均低于常规治疗组,差异有统计学意义(P<0.05),见表3。
表3 两组晚期癌痛患者治疗前后SAS评分比较(±s,分)
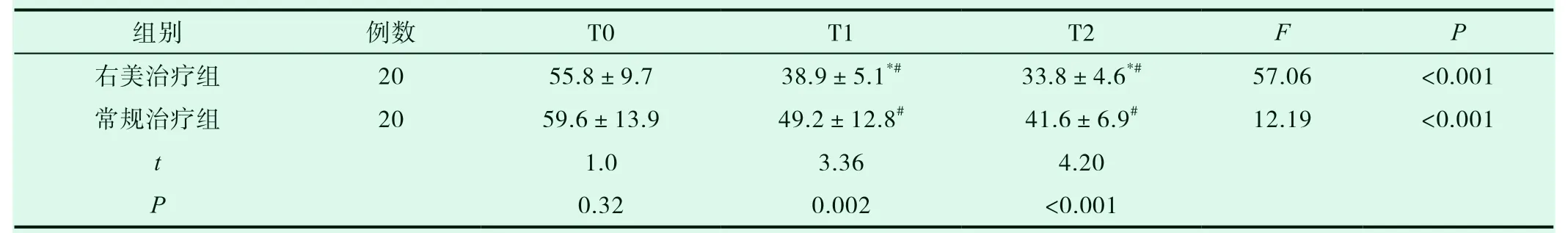
表3 两组晚期癌痛患者治疗前后SAS评分比较(±s,分)
注:与常规治疗组比较, *P<0.05;与同组T0比较,#P<0.05。
?
2.4 两组晚期癌痛患者治疗后药物相关不良反应
在整个治疗过程中,常规治疗组8例出现恶心呕吐,5例出现便秘,1例呼吸抑制(需要吸氧),1例心率低于50次;右美治疗组恶心呕吐3例,便秘2例,3例心率低于50次(阿托品可纠正);两组患者动态检测血压,平均动脉压均大于60mmHg。见表4。
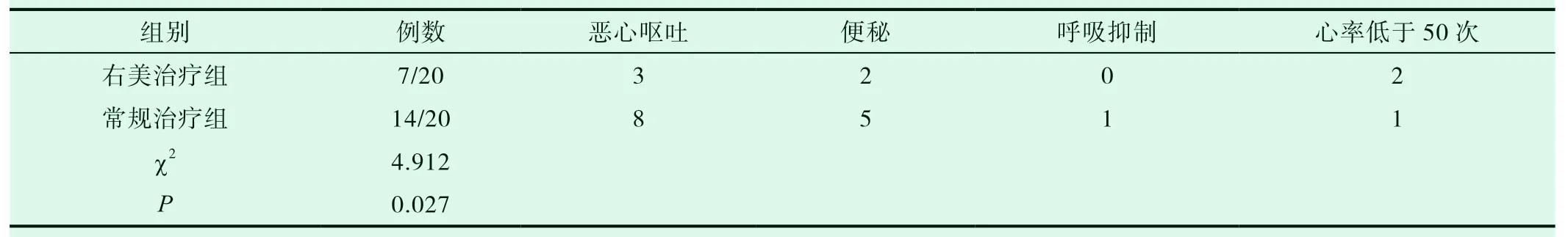
表4 两组晚期癌痛患者治疗后药物不良反应(例)
2.5 两组晚期癌痛患者治疗前后外周血皮质醇的比较
两组患者治疗前T0时的外周血皮质醇差异无统计学意义(P>0.05);经治疗后皮质醇浓度降低,于治疗后T1、T2时间点,外周血皮质醇均明显低于T0,差异有统计学意义(P<0.05); T1、T2时,右美治疗组外周血皮质醇均低于常规治疗组,差异有统计学意义(P<0.05),见图1。
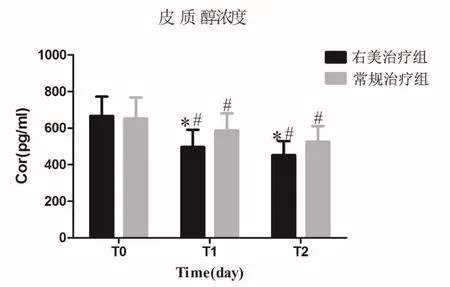
图1 两组皮质醇浓度变化
2.6 两组晚期癌痛患者治疗前后外周血P物质的比较
两组患者治疗前T0时的外周血P物质差异无统计学意义(P>0.05);经治疗后P物质浓度降低,于治疗后T1、T2时间点,外周血P物质均明显低于T0,差异有统计学意义(P<0.05); T1、T2时,右美治疗组外周血P物质均低于常规治疗组,差异有统计学意义(P<0.05),见图2。
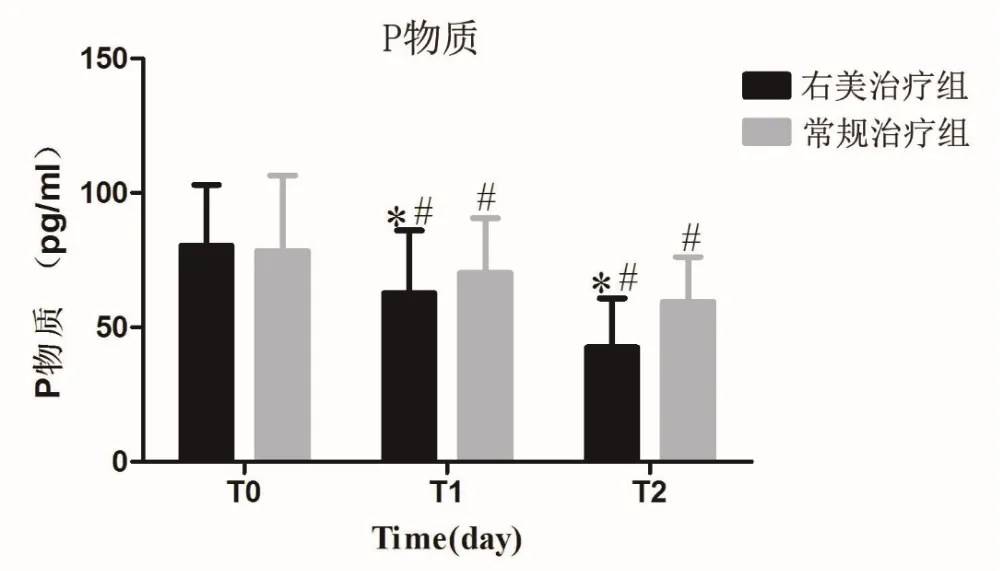
图2 两组P物质浓度变化
3 讨论
晚期癌症患者在入院治疗前大多受到中重度疼痛的折磨,同时患者还要承受巨大的经济压力和心理压力,因此患者多合并有失眠焦虑甚至抑郁等不良心境。然而,不良心理的存在反过来又加重了患者对于疼痛的感知及体验。因此,疼痛和不良心境形成恶性循环,严重影响晚期癌痛患者的生存质量[7]。目前,根据癌痛的治疗原则,晚期癌痛主要以阿片类药物治疗为主。但是阿片类在使用过程中不可避免会出现恶心呕吐、便秘瘙痒等副作用,如果剂量过大还会出现呼吸抑制,甚至危及生命[8]。此外,长期服用阿片类药物进行治疗,患者不仅对药物的耐受性增加,而且还会产生阿片所致的痛觉过敏,一旦停药,疼痛更加剧烈[9]。因此,在治疗前对晚期癌症患者分别作VAS、SAS评分以评价其疼痛和焦虑程度,与预期相符,患者大多数属于重度疼痛和重度焦虑的水平,生存质量极差。
作为高选择性的受体激动剂,右美托咪定作用于蓝斑处受体,可产生良好的镇静作用[10]。此外,右美托咪定的镇静效果好且安全,它诱导的睡眠模式接近于正常的生理睡眠模式,促进3期非快动眼睡眠时程,不会造成药物相关认知功能障碍[11]。本试验中,有关睡眠质量的评价,包含在SAS评分当中,右美治疗组患者自诉睡眠质量得到明显改善,并且显著优于常规治疗组。对于右美托咪定抗焦虑的机制目前仍在研究当中,但可以肯定的是,右美托咪定能够抑制交感神经系统的活性,而交感神经紧张性增加与焦虑、抑郁密切联系[12]。两组患者在实施镇痛治疗后,SAS评分明显降低,焦虑的心理问题得到明显改善,提示晚期癌痛患者的焦虑与疼痛具有显著关联性。此外,右美治疗组的焦虑改善程度更优。其潜在机制可能从以下三方面进行解释:①右美托咪定本身具有镇痛作用、或者与其他止痛药产生协同作用,增强镇痛效应;②右美托咪定辅助治疗可以减少阿片类药的需求量,从而降低相关副作用,患者舒适度增加;③右美托咪定本身的抗焦虑作用[13-14]。
为了增加研究的可靠性,我们抽取外周血检测血清中P物质和皮质醇的浓度变化,作为评价治疗效果的客观指标。众所周知,P物质是最常见的疼痛递质,主要由传递痛觉的神经末梢释放,作为兴奋性神经递质,使下一级神经元兴奋性增强,从而导致疼痛信号在传递过程中被放大[15]。因此,体内P物质的水平可客观反映疼痛的严重程度。研究表明,皮质醇不仅是调节机体糖代谢的重要激素,也是反映机体应激的一个较敏感指标[16]。在疼痛和焦虑时,机体处于强烈的应激状态,因此两组患者在治疗前皮质醇均处于高水平状态。经过治疗后,右美治疗组P物质及皮质醇显著低于常规治疗组,客观提示右美托咪定辅助治疗癌痛效果更优。
综上所述,右美托咪定作为辅助药物用于晚期癌痛患者的治疗,可以显著改善其疼痛及焦虑程度,同时降低外周血P物质和皮质醇水平,同时减少不良反应的发生,给晚期癌痛患者带来更加满意的生存质量。但由于该研究样本量较小并且缺乏长期随访,因此需要更深入的研究进行验证。
