抗乳腺癌基质金属蛋白酶9类抑制剂的分子设计研究*
2021-10-20张茹玉李月潞陈秀奎
张茹玉,叶 潘,李月潞,周 迎,陈秀奎,刘 桦
1.成都医学院 临床医学院(成都 610050);2.成都医学院 生物医学实验教学中心(成都 610050)
乳腺癌是女性常见的恶性肿瘤,它起源于乳腺导管内上皮或乳腺腺泡上皮细胞恶变,远处转移是其致死的主要原因之一[1-2]。上皮间质转化(epithelial-mesenchymaltransition,EMT)是乳腺癌细胞获得转移能力的关键起始步骤[3]。EMT途径可帮助乳腺癌细胞获得间充质表型[4],使癌细胞远离原发病灶并转移到远处淋巴结或其他器官[5]。该途径是乳腺癌细胞获得侵袭能力及发生远处转移的重要生物学过程[6],是乳腺癌细胞启动转移最重要的机制[7]。在乳腺癌EMT过程中,基质金属蛋白酶(matrixmetallo-proteinases,MMPs)发挥了重要作用[8]。MMPs是一类锌离子依赖性的蛋白水解酶,可降解细胞外基质(extracellularma-matrix,ECM)[9],诱发EMT,为乳腺癌的侵袭转移创造条件[10]。MMP-9蛋白又称明胶酶,是MMPs家族的重要成员之一,可降解ECM中的明胶、Ⅳ型和Ⅴ型胶原等主要成分[11],破坏ECM和基底膜结构,促进癌细胞向周围组织浸润,帮助肿瘤细胞的侵袭和转移[12],协同EMT途径[13]。因此,MMP-9抑制剂为乳腺癌的治疗开辟了一条新途径。传统抗癌药物开发周期长,投入资金量大[14],若能利用现有小分子药物配体进行药物设计,可提高新药物开发效率[15]。三维定量构效关系(three-dimensional quantitative structure-relationship,3D-QSAR)研究可利用药物分子结构和生物学活性[16],通过计算机实现模拟运算和预测,指导新型药物的设计、改造和优化,相比传统药物的研制更有针对性、高效性[17],可为MMP-9抑制剂的研发及治疗乳腺癌提供思路。
目前,关于氧肟酸类MMP-9抑制剂3D-QSAR与分子设计相关研究还鲜见报道。本研究将经典的3D-QSAR技术即比较分子力场分析(comparative molecular field analysis,CoMFA)和第二代3D-QSAR技术即Topomer-CoMFA两种方法联合运用构建3D-QSAR模型,确保新建模型的稳定性与可靠性。依托Topomer search技术的侧链相似性搜索[18],参考3D-QSAR模型提供的模型预测和三维等势图信息,构建新的氧肟酸类MMP-9抑制剂分子,以证明此分子设计的方法,可为新型高效抑制剂的研发、抑制剂结构的优化与设计研究提供参考。
1 材料与方法
1.1 数据来源与分子结构的优化
本文用于分子设计研究的氧肟酸类MMP-9抑制剂均参考文献[19],各化合物结构与活性如下所示。使用SYBYLX 1.1软件中的Sketch模块和Compute模块对小分子抑制剂进行结构与数据表单构建,选择相应的电荷与能量进行优化,将表示分子活性值的半抑制浓度(IC50)转化成pIC50(pIC50=-lgIC50)(图1、表1)[20]。

图1 氧肟酸类MMP-9抑制剂的骨架结构

表1 氧肟酸类MMP-9抑制剂的结构与活性

(续表)
1.2 CoMFA和Topomer-CoMFA的建模
分别采用CoMFA和Topomer-CoMFA技术对氧肟酸类MMP-9抑制剂进行定量构效研究,从构建的分子表单中随机选取24个抑制剂作为训练集,8个抑制剂作为测试集。CoMFA模型选取特征性的公共骨架进行叠合,Topomer-CoMFA模型进行R基团片段切割。
1.3 3D-QSAR模型的验证
用新建CoMFA模型和Topomer-CoMFA模型分别对训练集化合物和测试集化合物活性进行内部测试和外部测试,计算实验值与预测值之间的活性差值。根据两个模型训练集的实验活性值、预测活性值和测试集的预测活性值构建活性拟合图,以验证新建3D-QSAR模型的稳定性、内部和外部预测能力[21]。
1.4 虚拟筛选
基于Topomer-CoMFA的split模块进行分子切割,获得分子侧链基团(R1基团)和分子骨架(R2基团)。以R1基团作为分子活性特征性基团,结合Topomer search技术对ZINC数据库(2012)中的Fragment-like类(34 292个)分子进行分子结构相似性搜索。根据Topomer distance值(默认设为185)来判断并筛选出有特定贡献的R1基团[22],以活性最高的21号分子为模版进行过滤,挑选贡献值明显高于R1基团的侧链基团。将挑选出的侧链基团交替取代模版分子对应的R1基团,以构建新的抑制剂分子。
1.5 统计学方法
采用偏最小二乘法进行交叉验证系数计算q2值,留一法进行拟合验证系数计算r2值,得到最佳组成成分(n)、标准偏差(SEE)和Fisher检验值(F)[23]。
2 结果
2.1 3D-QSAR模型结果
分子叠合和分子切割是建立3D-QSAR模型的关键步骤,CoMFA模型的分子叠合图和Topomer-CoMFA模型的分子切割图(图2~3)。两种技术所建立3D-QSAR模型的各统计学参数汇总分析结果显示,两种模型都具良好的稳定性和较高的可信度(q2>0.5,r2>0.9,F>100,SEE<0.1)(表2)。

图2 CoMFA模型的分子叠合图

图3 Topomer-CoMFA模型的切割方式

表2 CoMFA和Topomer-CoMFA建模结果


图4 模型的线性回归图
2.2 三维等势图结果
选取CoMFA模型中21号分子作为模版进行立体场与静电场的三维等势图分析。在立体场三维等势图中,分子侧链旁的绿色模块表明在此处引入大空间占位基团更有利于增加抑制剂化合物活性;黄色模块表明在此处引入大空间占位基团不利于增加抑制剂化合物活性。在苯基3号位旁有较大的绿色模块,提示此处若有较大空间占位的基团有利于增加化合物活性。
静电场三维等势图中,红色模块表明在此处引入负性基团有利于抑制剂化合物活性的增加;蓝色模块表明在此处引入正性基团有利于抑制剂化合物活性的增加。在苯基4号位旁边有较大的红色模块,提示此处有负性作用强的基团有利于化合物活性的增加(图5)。

图5 三维等势图
2.3 分子设计结果
依托Topomer search技术的虚拟筛选,并结合新建模型的三维等势图和活性预测能力,以活性最高21号分子结构为基础,进行梯度分子设计。根据分子结构的Topomer distance值和贡献度值(>1)来评价化合物与训练集化合物结构的相似度,以筛选出的基团替换模板分子原有的R1基团,初步重构6个新抑制剂化合物。再依据分子结构的三维等势图,分析新建分子R1基团的立体场和静电场对分子活性的影响。用新建CoMFA模型和Topomer-CoMFA模型对新抑制剂进行分子活性预测,保留分子活性>21号分子的化合物结构,最终使用梯度分子设计的方法构建出2个高活性的氧肟酸类MMP-9化合物。新抑制剂的分子结构与预测活性值如下(表3)。
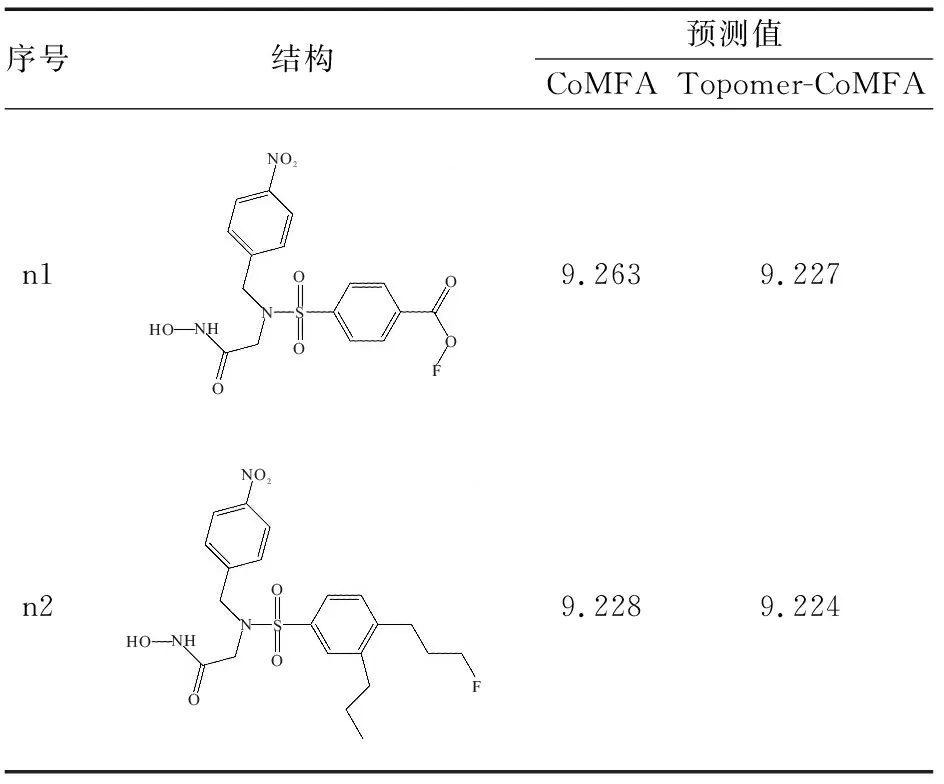
表3 新设计分子的结构及活性预测值
3 讨论
乳腺癌发病率逐年增长,其发病率已占女性恶性肿瘤发病率的第一位[24]。乳腺癌不仅对女性造成身心痛苦,而且给患者家庭、社会带来经济负担。乳腺癌远处转移是乳腺癌恶化的致命因素,而EMT途径与MMP-9的协同作用可加速乳腺癌恶化[25]。因此,寻求安全、经济、有效的抗乳腺癌药物(如MMP-9类抑制剂)治疗方法,已成为医学界以及乳腺癌患者非常关心的问题。
为获得高效、新颖的分子设计方法,本研究运用第一代CoMFA技术和第二代Topomer-CoMFA技术对氧肟酸类MMP-9抑制剂进行3D-QSAR研究[26]。结果显示,新建3D-QSAR模型具有良好的稳定性和可信度。将CoMFA和Topomer-CoMFA模型所测的内部预测活性值、外部预测活性值和化合物实验活性值进行线性回归,实验值与预测值有良好的拟合度,模型外部预测能力比较理想,可用于后续MMP-9抑制剂的分子设计与活性预测。
模型的三位等势图可从分子立体场、静电场等方面对分子设计提供帮助。结合获得的立体场三位等势图分析,15、17、27号分子(pIC50=8.1~8.6)有较高的活性,得益于苯基3号位引入了立体场作用更大的硝基、羧基等基团,在增加立体场同时,也有利于抑制剂化合物活性的增加。从静电场三位等势图研究发现,21号分子有5个氟基团,4号、5号分子也有多个氟基团,这些氟基团提供了强大的负性作用,同时也提高了分子活性。17、26、28、29号分子(pIC50=8.16~8.6)有较高的活性,得益于苯基3号位引入了负性作用强的硝基、甲氧基等基团,增加了负性静电场及抑制剂化合物的活性。
本研究进一步发现,分子结构多样性、活性上的差异主要来自于R1侧链基团的变化。采用Topomer search技术,从小分子数据库进行基于侧链基团的虚拟筛选,参考3D-QSAR模型给出的静电场与立体场三维等势图信息,结合CoMFA模型、Topomer-CoMFA模型的外部预测能力,设计了2个高活性的氧肟酸类MMP-9抑制剂分子。该结果发现,新抑制剂分子n1保留了模板21号分子R1基团的苯环结构,在苯环4号位的氟酸基团不仅增加了n1分子的负性作用,也增加了R1基团的立体场作用,这使得抑制剂活性增加。n2分子的苯环3号、4号位均加入正丙基基团,增加了分子的整体空间结构,提高了分子活性,但是活性稍低于n1分子。三维等势图信息显示,静电场对分子活性影响大于立体场,这与3D-QSAR模型给出的提示一致。结合CoMFA和Topomer-CoMFA模型建模结果可知,静电场的贡献度分别为63.6%、67.3%,立体场贡献度分别为36.4%、32.7%,静电场对活性的贡献度占主导地位。对小分子进行分子设计和结构修饰改造时,研究者应充分考虑静电场与立体场的相互影响,分析基团电荷性、侧链空间结构与能量匹配等因素。
综上所述,本研究基于氧肟酸类MMP-9抑制剂进行的CoMFA和Topomer-CoMFA定量构效关系分析和Topomer search虚拟筛选的方法可用于MMP-9抑制剂的分子设计研究,为小分子药物活性的提高、优质化合物结构的改造与设计提供新的思路,为新型抗乳腺癌药物筛选提供参考。
