不同联合方式的瘤内与瘤周影像组学特征对肺腺癌的诊断价值研究
2021-10-08陈小波郭馨雨于哲轩许茂盛周长玉
陈小波 郭馨雨 于哲轩 许茂盛 周长玉
随着胸部低剂量CT的广泛筛查,肺结节的发现频率也越来越高。如果能尽早地对结节作出诊断和治疗,将极大地提高肺癌患者的生存质量,同时避免不必要的侵入性检查和手术,因此早期区分肺结节良恶性具有潜在的重要临床意义[1]。
影像组学作为一种获取高通量影像图像放射学特征的非侵入性方法,能够反映肿瘤感兴趣区的异质性特征。近年来的研究表明,肿瘤周围实质在细胞迁移、炎症反应和血管形成方面具有重要的生物学特性,对于临床评估病灶侵袭行为具有重要价值[2]。大多数研究主要关注于原发病灶的评估,忽略了瘤周微环境的细微变化。从已有的文献报道来看,最佳瘤周放射学信号位于何处,以及这些特征如何与瘤内特征相互作用仍不清楚[3]。目前联合瘤内和瘤周影像组学特征的研究方法主要有2种:常见的是将瘤内和瘤周区域进行整体分割而得到总区域,提取特征后进行建模分析[4-5];Beig等[6]则对瘤内和瘤周区域进行单独分割,再对各区域特征进行联立并完成建模分析。本研究将通过联合瘤内和瘤周影像组学特征对肺腺癌及肺良性结节进行鉴别,并对2种方法进行对比分析。
方 法
1.一般资料
回顾性分析2017年1月至2019年12月在浙江中医药大学附属第一医院就诊的肺结节患者临床和影像资料。所有患者CT平扫图像都由高年资肺部影像诊断医师进行分析和判断,最后经胸腔镜、肺部穿刺或手术切除标本病理检查明确结节良恶性。纳入标准:①手术治疗前1个月内曾行薄层(0.75 mm或1.0 mm)胸部CT扫描;②病灶最大径≤30 mm;③术前无化疗、放疗、靶向治疗;④无肺部肿瘤病史。排除标准:①图像质量不佳;②CT检查前行肺肿瘤活检、放疗、化疗或手术切除;③同一肺叶多个肺结节。
2.CT检查方法
图像采集采用东芝Aquilion ONE(Toshiba Medical Systems,Japan) 和 西 门 子Somatom sensation 64层CT扫描仪(Siemens Healthcare,Germany)。前者扫描参数:管电压120 kV,管电流200 mA,探测器准直0.5 mm×64 mm,矩阵512×512,重建层厚1.0 mm,旋转时间0.4 s,重建核为FC51。后者扫描参数:管电压120 kV,自动管电流调制,探测器准直0.6 mm×64 mm,矩阵512×512,重构层厚0.75 mm,重建核为B31f。
3.影像组学分析
3.1 图像预处理与图像分割
将DICOM格式的薄层轴位CT平扫图像导入开源软件ITK‑SNAP V3.8.0(https://www.itksnap.org),设置肺窗(窗位:-600 HU;窗宽:1 300 HU),由2名分别具有3年和10年胸部CT影像诊断经验的放射科医师独立完成三维容积感兴趣区(VOI)的勾画。勾画过程中支气管、大血管和胸膜以外的正常组织都被人工尽可能地排除在VOI之外。对于2名放射科医师之间的差异情况,分割模式由1名具有28年肺部影像诊断经验的放射科教授进行评估。
在完成瘤内感兴趣区的分割后,需要进行外扩得到瘤周区域。根据较多文献[3-6]的报道,联合瘤内及瘤周0~5 mm区域时模型的整体预测性能最佳,因此本研究的瘤周区域被定义为3 mm和5 mm。AK软件(Analysis Kit;GE Healthcare,US)可以根据勾画好的VOI来自动分割瘤周区域,瘤内及瘤周总区域,软件内置的边缘识别算法可自动识别胸膜边缘,有效地防止纵隔区域被纳入,保护结节组学特征不被纵隔衰减或改变。最终,依次整理得到瘤内感兴趣区[即肿瘤区(gross target volume,GTV)],瘤周感兴趣区[即肿瘤周围区(peritumoral volume,PTV);分别外扩0~3 mm和3~5 mm,记为PTV3和PTV5],瘤内和瘤周总区域(GPTV;即瘤内至瘤周3 mm和5 mm,记为GPTV3和GPTV5),合计5个区域。
3.2 影像组学特征提取
将分割好的感兴趣区再次导入ITK‑SNAP软件进行核实与修正,无误后利用开源工具Pyradiomics 3.0工具箱[7]对影像体素进行1×1×1重采样,随后完成影像组学特征的计算和提取。包括一阶统计特征、形状特征,灰度区域大小矩阵(GLSZM)、灰度共生矩阵(GLCM)、灰度依赖矩阵(GLDM)等灰度特征等。另外,将小波、平方、对数、指数4种图像滤波器分别应用于原始图像,得到相应衍生图像,并在5种不同类型图像中完成所有类别影像组学特征提取。
3.3 影像组学特征筛选
首先,对所有影像组学特征进行Z⁃score标准化处理,公式为Z=(x-μ)/σ,其中x为某组学特征的数值,μ代表所有患者相应特征的平均值,σ代表相应特征的标准差。对样本按7∶3的比例随机划分为训练集和验证集。为避免特征数量过多而使模型过度拟合,需对特征进行逐步筛选,具体方法如下。①单因素分析:鉴于组学特征均为连续型特征,因此采用独立样本t检验进行逐个分析,初步筛选出具有显著差异的影像组学特征。②Boruta特征选择算法:Boruta算法被用来进一步筛选具有潜在预测性的组学特征,其核心思想是统计比较数据中真实特征与随机加入的原始拷贝特征(也称为影子变量)之间重要性的差异。重要性得分是基于随机森林建模计算的,其中显著重要于最佳影子变量的真实特征被定义为重要特征,重要性低于最差影子变量的特征则被剔除。通过不断迭代最终筛选获得具有潜在预测性的组学特征。
3.4 模型构建与评价
基于最终筛选得到的影像组学特征建立多元logistic逐步回归模型,以P<0.05为显著性阈值,赤池信息准则(Akaike information criterion,AIC)为特征筛选和模型迭代准则,通过不断迭代直至模型AIC值达到最优时完成训练。对筛选得到的GTV、PTV3模型特征进行联立,并再次利用logistic逐步回归建模得到Combined3模型。同理,联立GTV、PTV3、PTV5特征建立Combined5模型。受试者工作特征(receiver operator characteristic,ROC)曲线下面积(AUC)、准确度、灵敏度、特异度、阴性预测值、阳性预测值等指标被用来评价模型效能。
4.统计学分析
采用Python 3.7.4软件的“Pyradiomics”包完成影像组学的特征提取,“scipy.stats”包完成特征的单因素分析,满足方差齐性采用Studentt检验,方差不齐采用校正t检验,P<0.05认为差异有统计学意义。采用R 3.6.1软件完成数据处理与建模,“caTools”包用于分层随机划分数据集,“Boruta”包用于建立Boruta特征选择算法,“glmnet”包用于建立logistic模型,“ROCR”包绘制ROC曲线。DeLong检验被用来评估不同模型之间的效能差异。
结 果
1.一般资料
根据纳入排除标准,295例肺结节中腺癌161例,良性结节134例,其中包括炎性结节60例、肉芽肿38例、结核瘤15例、肺泡细胞瘤6例、错构瘤6例、机化性肺炎5例、非典型腺瘤样增生4例。腺癌平均最大径(11.34±4.47)mm,良性结节平均最大径(11.15±4.05)mm,两者间比较,差异无统计学意义(P>0.05)。
2.影像组学特征分析结果
利用AK软件分别对5个区域(GTV、PTV3、PTV5、GPTV3和GPTV5)进行特征提取,每个区域均得到1 037个影像组学特征。首先对特征进行单因素分析完成特征的初步筛选,5个区域分别得到394、650、614、567和559个显著特征;随后Boruta特征选择算法被用来进一步降维,设置迭代次数为300,以0.01为显著性阈值,分别得到45、69、61、45和36个具有潜在预测性的组学特征。图1示例了GTV中的影像组学特征经Boruta特征选择算法筛选后的结果,即Boruta特征重要性箱线图。

图1 GTV的Boruta特征重要性箱线图
3.肺腺癌及良性结节鉴别模型的效能评估
对筛选得到的影像组学特征建立logistic逐步回归模型,以训练集数据来训练模型参数,以验证集数据进行效能评估,分别得到GTV、PTV3、PTV5、GPTV3和GPTV5模型。对筛选得到的GTV、PTV模型特征进行联立,经过logistic逐步回归得到Combined模型。其中,Combined5模型AIC=143.27,在纳入的9个特征中有4个特征源于GTV,3个特征源于PTV3,2个特征源于PTV5,所有特征间存在统计学差异,具体参数结果如表1所示。Combined3模型AIC=153.93,相比Combined5模型纳入的特征少了2个源于PTV5的特征。图2为组合模型的特征系数条形图,从中可以看出,源于GTV的特征不仅数量居多,而且特征系数的数值也较大,源于最外周PTV5的特征数量最少,且特征系数数值也较小。
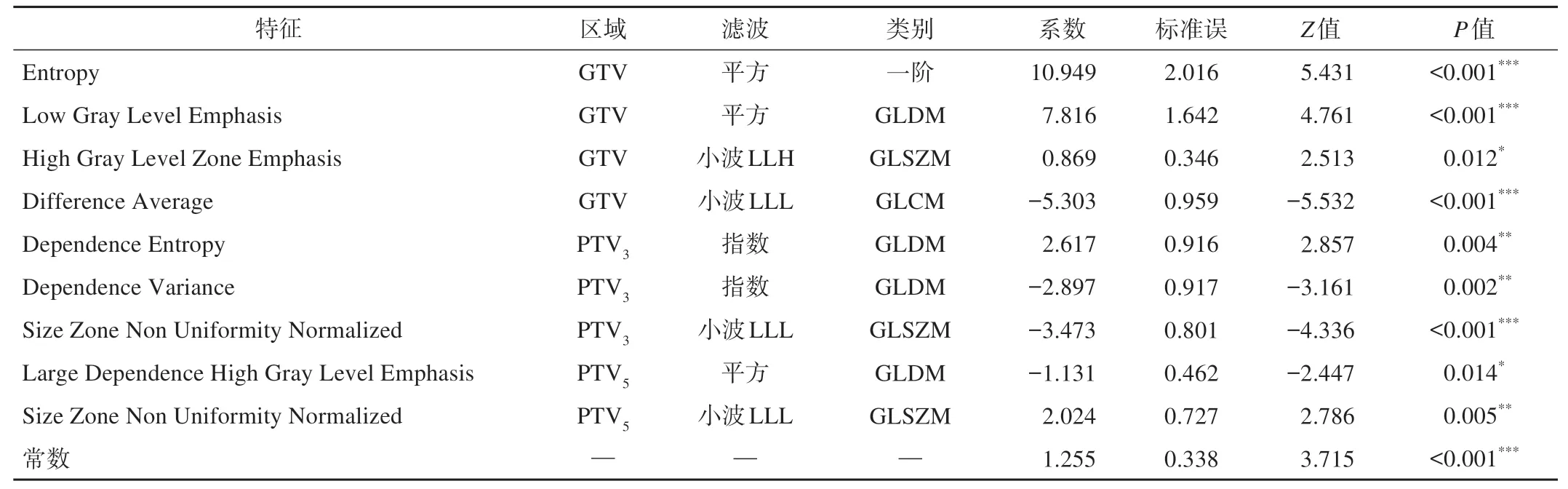
表1 基于瘤内及瘤周特征联合的Combined5模型参数表
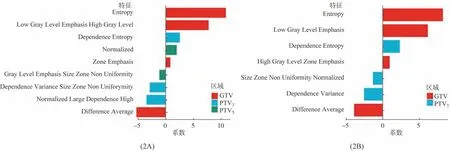
图2 Combined模型特征系数条形图
5种 模 型,即GTV、PTV3、PTV5、GPTV3、GPTV5、Combined3和Combined5对肺结节良恶性的判别效能结果详见表2。各个模型的ROC曲线分析结果(图3)显示,瘤内、瘤周及瘤内与瘤周联合的模型对肺结节均具有良好的预测性,其AUC均大于0.83。其中,PTV模型(AUCPTV3=0.892,AUCPTV5=0.858)和GPTV模型(AUCGPTV3=0.859,AUCGPTV5=0.833)在验证集中的表现效能均低于GTV模型(AUCGTV=0.916)。而Combined模 型 (AUCCombined3=0.953,AUCCombined5=0.953)相比GTV、GPTV3和GPTV5模型,其在肺腺癌和良性结节的鉴别中表现出了更好的效能。
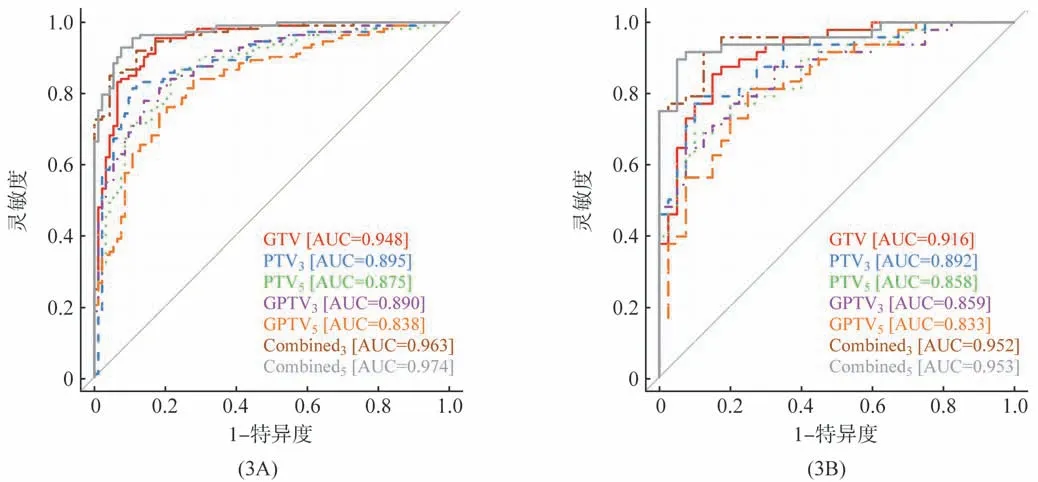
图3 瘤内及瘤周影像组学模型预测肺腺癌及良性结节的ROC曲线
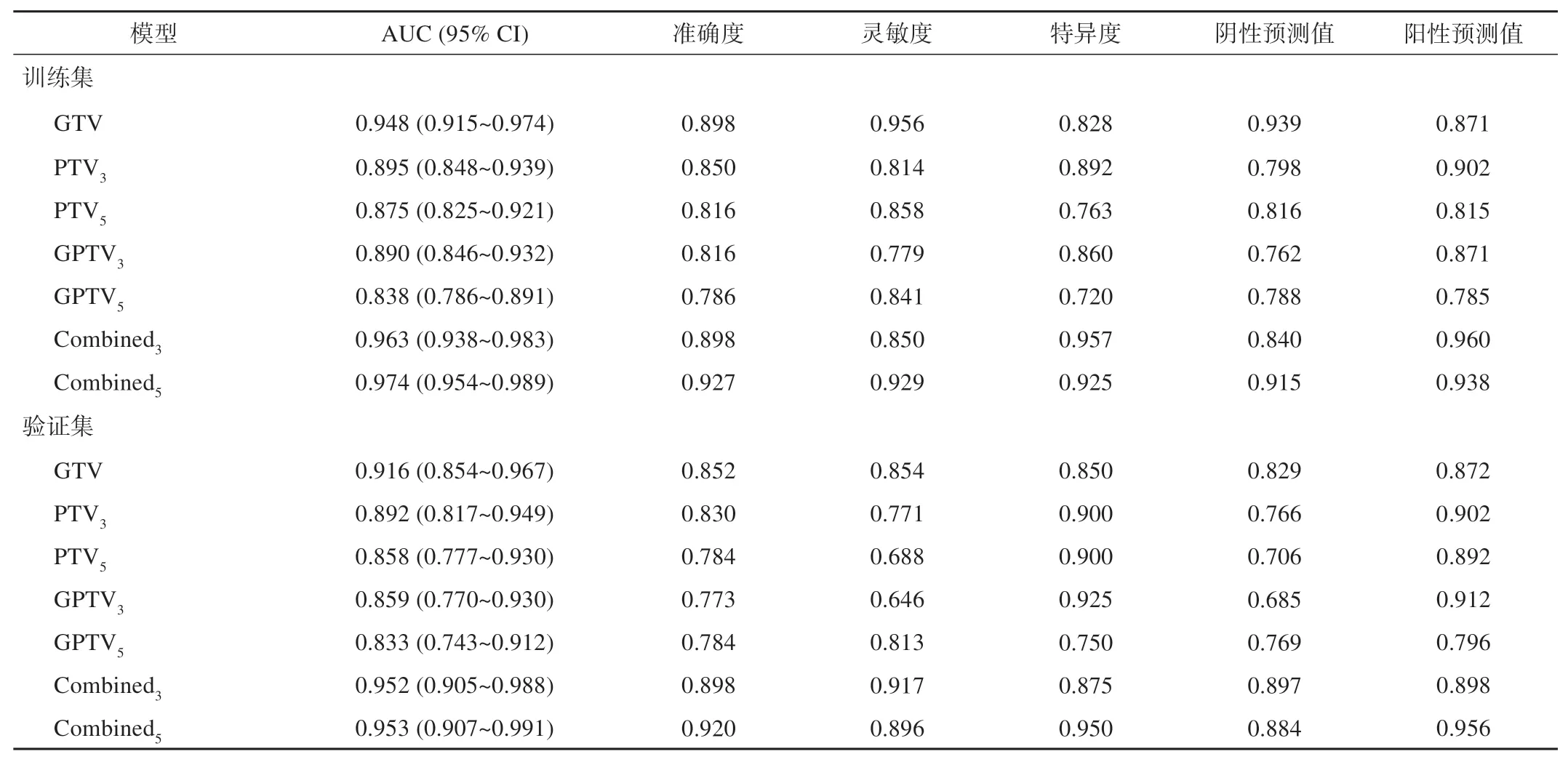
表2 不同联合方式的瘤内及瘤周影像组学模型效能
上述模型的DeLong检验结果见图4,从中可以发现,在验证集中,PTV5与2种Combined模型,GPTV3和GPTV5与2种Combined模型之间的差异均有统计学意义(P<0.05)。2种Combined模型与2种GPTV模型的详细对比信息如表4所示。
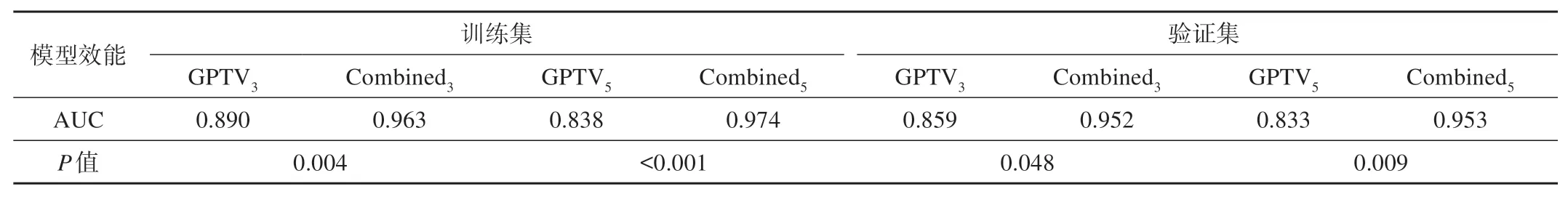
表4 Combined模型与GPTV模型的对比与检验
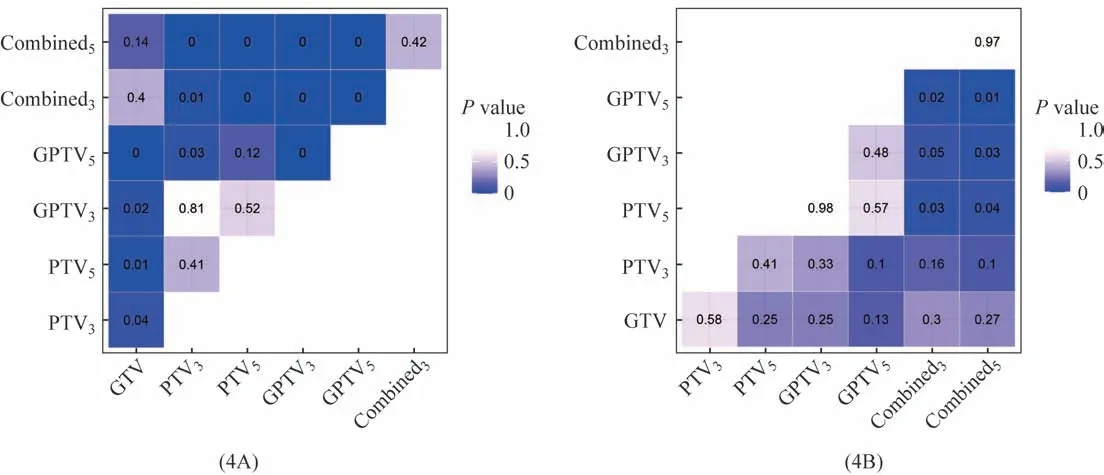
图4 瘤内及瘤周影像组学模型DeLong检验显著性热图
讨 论
在CT图像上,肺良恶性结节在大小、形态上都有部分重叠,在视觉评估的基础上对其进行鉴别具有一定的挑战性。经皮穿刺活检是临床上确定肺结节性质的一种方法,可以提供相对准确的病理信息。然而,经皮穿刺活检是一种侵入性手术,可能会给患者带来一些手术相关的并发症,且有时活检获得的小块组织不能代表整个病变的特征[8]。在这方面,影像组学作为一种定量化的无创手段已经被广泛证明可提供更多的纹理信息来准确地评估病变的异质性,已经有文献报道了影像组学方法在肿瘤分级[9]、肝细胞癌的微血管浸润和预后评估[10]、浸润性肺腺癌和浸润前病变的区分能力[11]等方面的研究。在我们的研究中,GTV模型(AUCGTV=0.916)在肺腺癌与良性结节鉴别中有着良好的表现。
以往的研究主要集中于瘤内的组学特征分析,然而单纯瘤内特征并不足以充分反映病灶的所有特征,例如炎性结节可以表现为典型的磨玻璃样改变,经过治疗,病灶吸收后易被误诊为肺癌,而慢性炎症反应会促进肺免疫抑制微环境形成。目前,人们越来越认识到微环境在肿瘤中包含的丰富生物学信息[12],在肺部结节的诊断方面同样如此。良性肿瘤通常生长缓慢,对周围正常组织主要产生挤压等作用,例如肺细胞瘤可对周围血管产生推移作用甚至造成出血、肺结核周围可有卫星灶、结核球可有毛刺和胸膜牵拉等。恶性肿瘤则通常具有更强的浸润性,会破坏周围实质组织的正常结构,比如造成病灶周围的小叶间隔水肿,病灶外围的小血管、淋巴管、气管周围发生癌性或炎性浸润以及阻塞后扩张等表现。病灶周围的微观环境在影像上难以很好地体现,而这种微环境的异质性变化可以通过瘤周影像组学的方法很好地被挖掘。目前,基于瘤内和瘤周放射学特征的研究方法在非小细胞肺癌的总体生存率和免疫治疗反应[13]、术后复发[14]等方面均有着良好的价值表现。在肺腺癌及良性结节的鉴别研究中,我们发现单纯提取瘤周感兴趣区的PTV模型(AUCPTV3=0.892,AUCPTV5=0.858)、瘤内及瘤周总感兴趣区的GPTV模型(AUCGPTV3=0.859,AUCGPTV5=0.833)在验证集中表现的效能均低于仅提取瘤内感兴趣区的GTV模型(AUCGTV=0.916),同时,随着外扩距离的增加,模型效能会逐渐减弱。同样地,也有研究[4,15]发现,GPTV和GTV在肺腺癌与肉芽肿鉴别、肺腺癌淋巴结转移预测的研究中无统计学差异。其可能的原因是研究所纳入的肺结节体积比较小,恶性结节的瘤周微环境浸润程度不明显,导致瘤周区域的鉴别性能欠佳。同时随着外扩距离的增加,正常的肺纹理组织会被纳入到感兴趣区中,也会导致良恶性结节差异缩小。
除此之外,我们还对比研究了瘤内和瘤周2种不同联合方法构建的模型,第一种是常见的将瘤内和瘤周区域进行整体分割后构建GPTV模型,第二种是对瘤内和瘤周区域单独分割,经特征筛选后再构建Combined模型。2种方法在肺腺癌与良性结节的鉴别研究中,AUCCombined3为0.953,高于AUCGPTV3的0.859(P<0.05),AUCCombined5为0.953,高于AUCGPTV5的0.833(P<0.01)。参考Combined5模型保留的参数结果:纳入的9个特征中有4个源于GTV,3个源于PTV3,2个源于PTV5,推测其可能的原因是各区域单独勾画再联立的组合方法不仅可以保留瘤内的丰富信息,而且瘤周的显著特征也会被保留,同时模型会根据瘤内和瘤周特征的重要性进行加权组合,这也解释了Combined模型(AUCCombined3=0.952, AUCCombined5=0.953)在验证集中效能高于GTV模型(AUCGTV=0.916)的原因。对于瘤内及瘤周的整体分割,良性结节周围的部分重要信息会因为被更大面积的正常组织所“均匀化”而削弱,使良恶性差异变小,因此GPTV模型(AUCGPTV3=0.859,AUCGPTV5=0.833)的验证效能低于GTV模型(AUCGTV=0.916)。相比之下,单独分割瘤内及瘤周感兴趣区,经特征筛选后再合并的方法能够更加全面真实地反映瘤内和瘤周区域蕴含的显著特征。这与实际影像阅片过程中先看瘤内密度或信号强度(GTV),再看边缘形态(PTV),然后结合与周围组织关系(更大的PTV)的“特征联立”综合分析过程相一致。
本研究存在一些局限性:第一,本研究为小样本的回顾性研究。第二,本研究以肺腺癌为恶性结节代表,以炎性结节和肉芽肿为主要良性代表进行了良恶性鉴别研究,这可能存在选择偏倚,因为易产生明显微环境改变的炎性结节、肺细胞瘤等良性肺结节病种,可能会更容易与恶性肺结节进行鉴别,今后仍需扩大样本将研究对象拓展到良恶性亚组以及多中心研究。第三,本研究仅采集了2种CT仪器的肺结节图像,在未来的研究中,瘤内及瘤周影像组学方法对不同型号CT扫描下肺结节鉴别诊断的影响仍需验证。
综上所述,本研究通过影像组学方法和对比分析发现,相比于GPTV整体分割的方法,瘤内GTV及瘤周PTV单独分割后再进行特征联立的方法在肺腺癌及良性结节鉴别中有着更好的效能表现。
