(−)-薄荷酮的制备及比旋光度测定
——介绍一个研究型有机化学实验
2021-09-26韩杰陈文彬李玉新马如江贺峥杰
韩杰,陈文彬,李玉新,马如江,贺峥杰
南开大学化学学院,化学国家级实验教学示范中心,天津 300071
薄荷醇俗名薄荷脑,即5-甲基-2-异丙基环己醇,含有3个手性中心,具有8种异构体。其中(−)-薄荷醇具有清凉的薄荷香气,被大量用于香烟、化妆品、牙膏、口香糖、甜食和药物涂搽剂中[1]。(−)-薄荷酮具有较弱的薄荷气味、较低的刺激性和持久的清凉作用,在医药、食品、化妆品产业中同样得到广泛应用[2,3]。目前,以天然产物(−)-薄荷醇为原料,采用氧化法制备(−)-薄荷酮是最常见的方法。按照氧化剂的类型、反应产率及特点,我们总结分析了氧化法制备(−)-薄荷酮的主要方法。如表1所示,这8种方法具有各自特点,从反应条件、实验操作、收率及氧化剂的获得难易程度等方面考虑,方法1和2更适用于本科生基础有机化学实验。本文以(−)-薄荷醇为原料,分别以重铬酸钠/硫酸溶液(Jone’s试剂)及次氯酸钠为氧化剂制备(−)-薄荷酮,测定了产物的比旋光度,并通过气相色谱分析了差向异构化对产物比旋光度的影响。本实验可采用研究性教学模式用于基础有机化学实验课教学[4],有利于化学及相关专业本科生了解手性化合物的基础理论知识、提高综合实验技能、培养科学研究能力[5,6]。
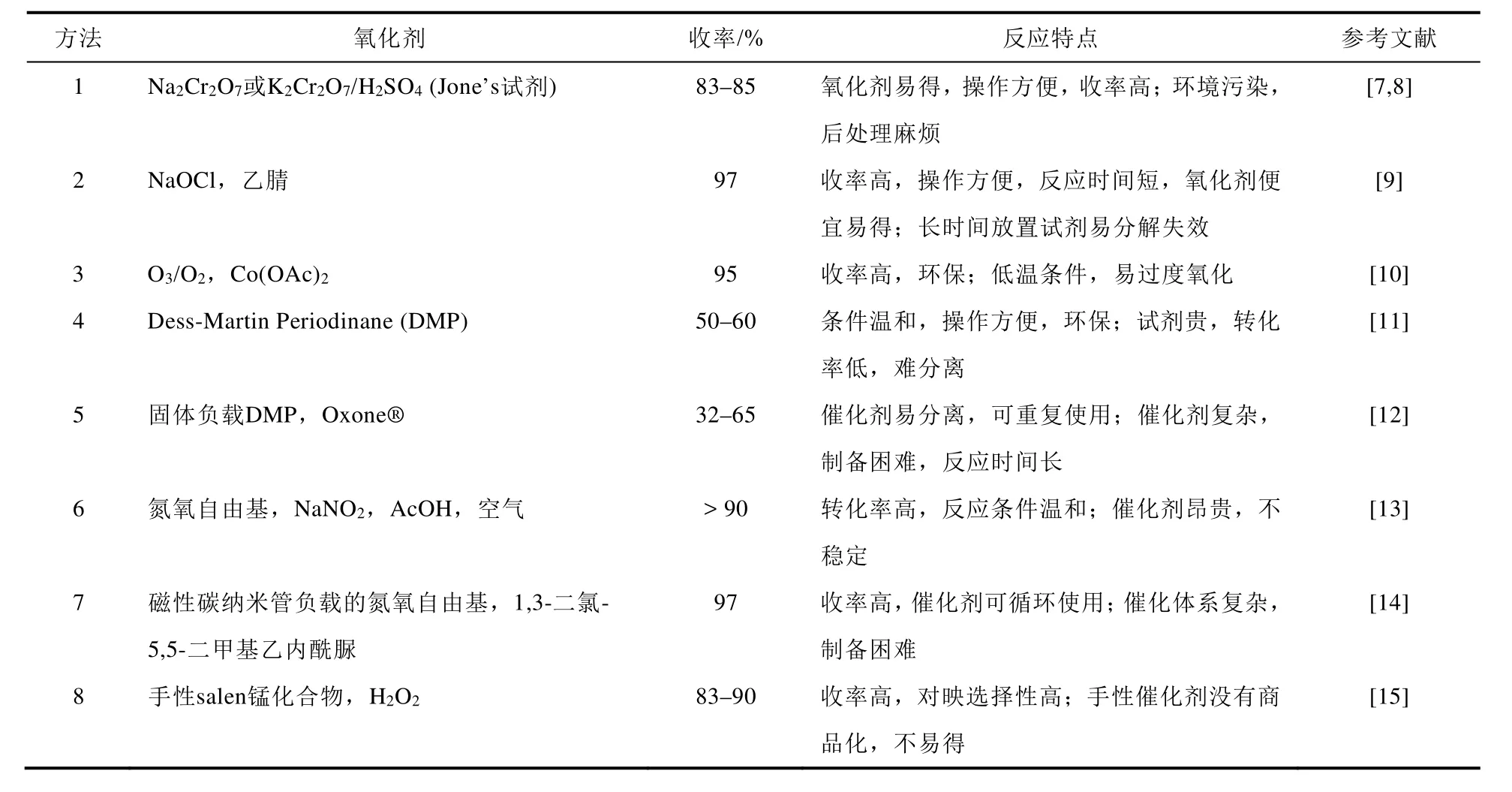
表1 采用氧化(−)-薄荷醇制备(−)-薄荷酮的方法
1 实验目的
(1) 了解手性分子的旋光活性,学习比旋光度的测定方法。
(2) 理解环己烷的构象转化及其反应活性之间的关系。
(3) 理解酮类化合物的互变异构现象及其对比旋光度的影响。
(4) 学习气相色谱原理及其在定性定量分析中的应用。
(5) 巩固蒸馏、液体的洗涤、干燥、过滤等基本操作,正确处理废液,强化绿色化学意识。
2 实验原理
以天然产物(−)-薄荷醇为原料,以重铬酸钠/硫酸溶液(Jone’s试剂)或次氯酸钠为氧化剂制备(−)-薄荷酮的合成路线如图1所示。有关Jone’s试剂氧化二级醇生成酮的反应机理,基础有机化学教材一般均有描述,通常认为该反应过程涉及二级醇与铬酸作用形成铬酸酯,然后铬酸酯发生分子内消除反应产生酮[16,17]。在此过程中,H2CrO4转化为H2CrO3,Cr(IV)不稳定,进一步与Cr(VI)作用转化为Cr(V),Cr(V)与二级醇反应得到Cr(III)和酮。橙黄色的Cr(VI)转化为蓝绿色的Cr(III)的变色现象也是酒驾测试仪的工作原理[18]。次氯酸氧化二级醇生成酮的反应机理,基础有机化学教材一般没有论述,文献中通常认为,次氯酸分解产生的Cl2与二级醇生成烷基次氯酸酯,进而在Cl2作用下发生分子内消除反应生成产物酮[19]。
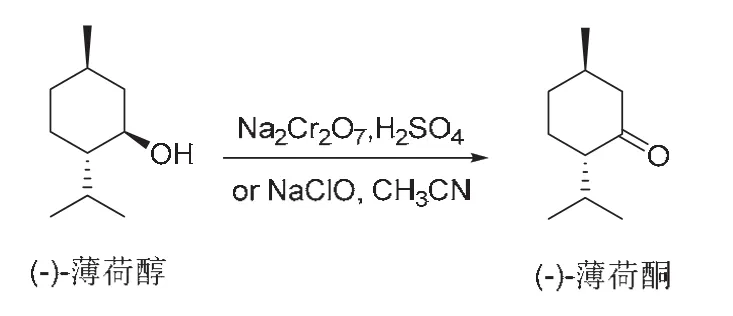
图1 (−)-薄荷酮的合成路线
3 实验部分
3.1 试剂与仪器
98%硫酸(天津市化学试剂六厂),(−)-薄荷醇([α]D= −49.2,20 °C,EtOH)[20],重铬酸钠,乙酸乙酯,5%NaOH溶液,饱和食盐水,无水乙醇,次氯酸钠溶液,乙腈。
Autopol IV-T全自动控温旋光仪(鲁道夫公司,美国)。GC-2014气相色谱仪(岛津公司,日本),HP-5色谱柱,规格为30 m × 0.32 mm,0.25 micron。
3.2 (−)-薄荷酮的合成
方案1:在装有回流冷凝管、温度计和搅拌磁子的100 mL三口瓶中,加入3.9 g (15 mmol)重铬酸钠及20 mL稀硫酸(1.7 mL浓硫酸加入20 mL水中配制而成),搅拌成均相的铬酸溶液。然后将3.1 g(20 mmol)结晶状(−)-薄荷醇分批加入反应瓶中,同时充分搅拌。控制反应温度在50–55 °C。
反应完成后温度下降,继续搅拌下自然冷却至室温,将棕黑色的反应混合物转移至分液漏斗中,采用乙酸乙酯(15 mL × 2)萃取,合并有机相,用水(15 mL × 2)洗两次,充分静置分层。下层水相倒入废液桶中,合并上层有机相,依次用20 mL 5% NaOH溶液及20 mL饱和食盐水水洗。无水硫酸钠干燥15 min、过滤。蒸馏,收集204–208 °C馏分。
方案2:在装有回流冷凝管、温度计和搅拌磁子的100 mL三口瓶中,加入4.7 g (30 mmol)结晶状的(−)-薄荷醇,乙腈(30 mL)、2.4 mL乙酸,搅拌。缓慢滴加NaOCl溶液(12.0 mL,有效氯10%),水浴加热,控制反应温度在30–35 °C,反应1 h。向反应瓶中滴加适量饱和NaHSO3溶液至淀粉KI试纸不变蓝色为止。将反应混合物转移至分液漏斗中,采用乙酸乙酯(15 mL × 2)萃取,合并有机相,用水(15 mL × 2)洗两次。无水硫酸钠干燥15 min,过滤。蒸馏,收集204–208 °C馏分。
方案3:在装有回流冷凝管、温度计和搅拌磁子的100 mL三口瓶中,加入4.7 g (30 mmol)结晶状的(−)-薄荷醇,15 mL乙酸,搅拌。缓慢滴加NaOCl溶液(20.0 mL,有效氯10%),水浴加热,控制反应温度在30–35 °C,反应1 h。反应后处理及纯化方法同实验方案2。
3.3 比旋光度测定及气相色谱表征
比旋光度测定:准确称取约0.10 g产品,配成10.00 mL无水乙醇溶液,采用Autopol IV-T全自动控温旋光仪测定比旋光度。
气相色谱表征:初始柱温80 °C保留4 min,以15 °C·min−1速度升至250 °C保留20 min。
4 结果与讨论
4.1 反应温度对结果的影响
通常,氧化反应是放热反应,尤其采用Jone’s试剂氧化醇放热现象明显,对于简单脂肪醇不需要加热,室温或较低温度下即可顺利进行。而本实验中薄荷醇的氧化反应需要适当加热才能顺利进行,如方案1需要在实验开始时加热到50–55 °C,然后可停止加热,通过反应自身放热即可使反应体系保持在以上温度,即该反应需要一个引发过程。说明(−)-薄荷醇的反应活性低于简单脂肪醇。其原因可从薄荷醇的构象进行合理解释,如图2所示,(−)-薄荷醇稳定的椅式构象中,所有取代基均处于能量较低平伏键,因而需要加热到一定温度,使平伏键的构象转化为能量较高的直立键构象,提高羟基的反应活性[21]。
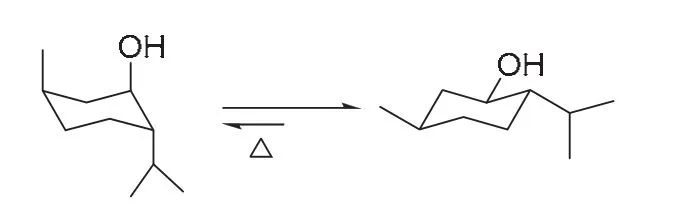
图2 (−)-薄荷醇的构象转化过程
4.2 产物的比旋光度及气相色谱测试结果分析
分别采用实验方案1–3制备了薄荷酮,并测试了产物的比旋光度及气相色谱,结果如表2所示。方案1采用Jone’s试剂为氧化剂,转化率低于文献方法[7],这可能是由于实验操作及产物纯化方法不同造成。而产物的比旋光度值略低于文献值(,乙醇)[20],从气相色谱结果可知,产物中含有少量(+)-薄荷酮及未反应的原料(−)-薄荷酮。如图3所示,保留时间依次为5.189、5.339、5.468 min的三个峰分别归属为(−)-薄荷酮、(+)-异薄荷酮、(−)-薄荷醇。其中(−)-薄荷酮与(+)-异薄荷酮的归属参考文献结果[11],而(−)-薄荷醇的归属则通过标样在相同条件气相色谱中的保留时间进行了确证。(+)-异薄荷酮(,乙醇)[22]的产生使产物的比旋光度值降低,合理解释了比旋光度实验结果。

表2 产物收率、比旋光度及产物组分
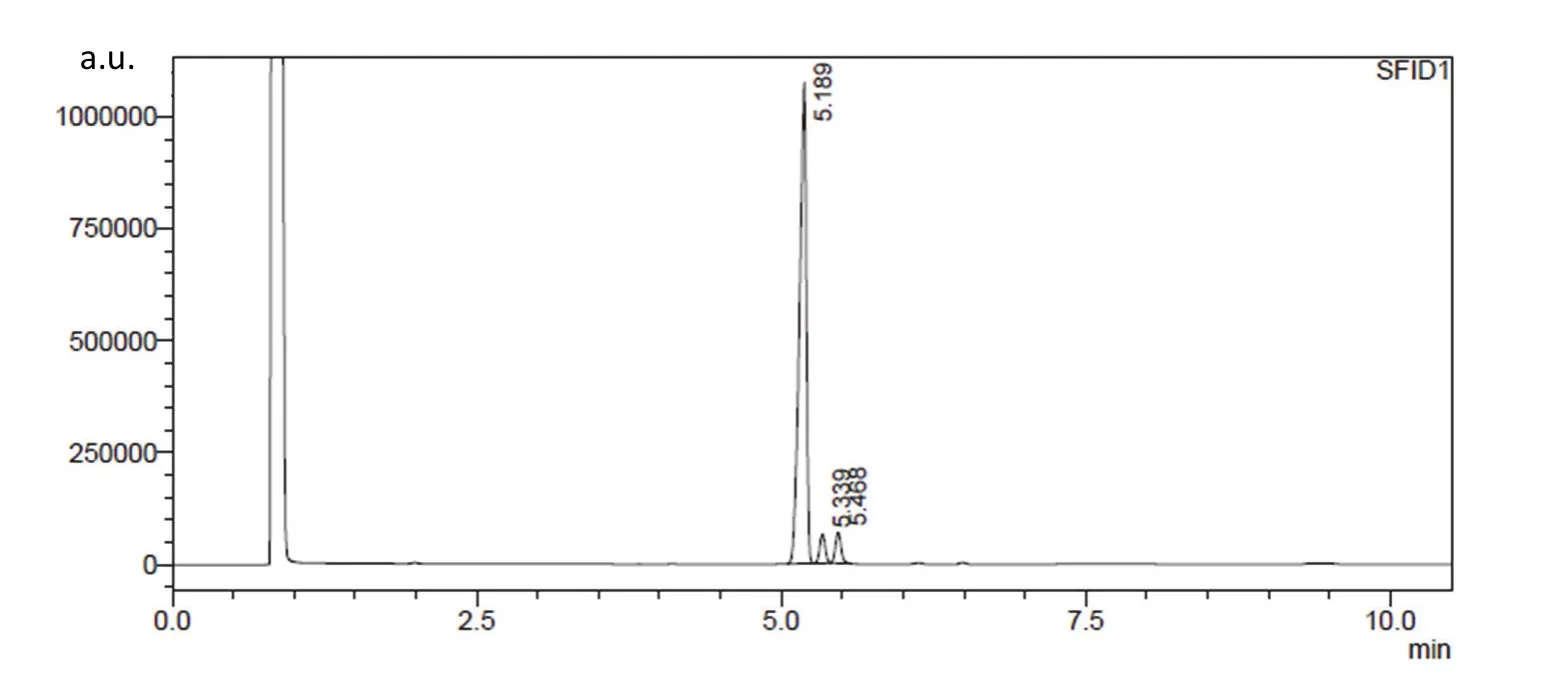
图3 方法1所得产物的气相色谱图
以乙腈为溶剂,采用含有结晶水的次氯酸钠固体氧化(−)-薄荷醇制备(−)-薄荷酮,文献报道的收率高达97%[9],但我们采用次氯酸钠溶液为氧化剂,乙腈为溶剂进行了多次实验并开展了教学实践,反应的收率低于10%,可能是因为该反应条件不利于产生氧化性高的Cl2,文献结果也值得商榷。为此,我们改进了实验条件,设计了实验方案2和3。二者均采用次氯酸钠溶液为氧化剂,前者以乙腈为溶剂,乙酸与次氯酸钠等摩尔量;后者则采用乙酸为溶剂,同时也作为反应试剂。如表2所示,采用方案2,(−)-薄荷醇的转化率提高到16.7%,比旋光值接近文献数据,但气相色谱数据表明,副产物(+)-异薄荷酮比例增大,且大量原料未反应。大量(−)-薄荷醇的存在是产物比旋光度值接近文献值的原因。实验方案3提高了次氯酸钠溶液的用量,同时采用乙酸为溶剂,(−)-薄荷醇的转化率提高到56.3%,但副产物(+)-异薄荷酮比例增大,导致比旋光度远远偏离文献值。通过延长反应时间可进一步提高(−)-薄荷醇转化率,但从转化率及产物纯度而言,以次氯酸钠溶液作为氧化剂的方案不如采用Jone’s试剂的方法。此外,次氯酸钠溶液易分解,使用时须保证有效氯含量,否者会降低(−)-薄荷醇转化率甚至得不到产物。
(+)-薄荷酮与(−)-薄荷酮互为差向异构体,二者可通过烯醇式结构互变(图4),尤其在酸性条件下互变速率显著加快,回流条件下可在1 h内达到平衡,室温放置过夜也可达到平衡[23]。实验方案1在水溶液体系进行,为非均相体系,但反应的后处理涉及NaOH溶液及饱和食盐水洗涤等过程,可能导致(+)-薄荷酮与(−)-薄荷酮异构互变现象。实验方案2以乙腈为溶剂,在均相条件下进行,易于发生互变异构化现象。实验方案3则是在乙酸溶液中进行,酸性及均相条件更有利于互变异构,这也合理解释了气相色谱结果。此外,在实验教学过程中,不同学生实验进度不同,比旋光度测试时间也不一致,即产品放置时间也不同,导致实验结果也有所差异。
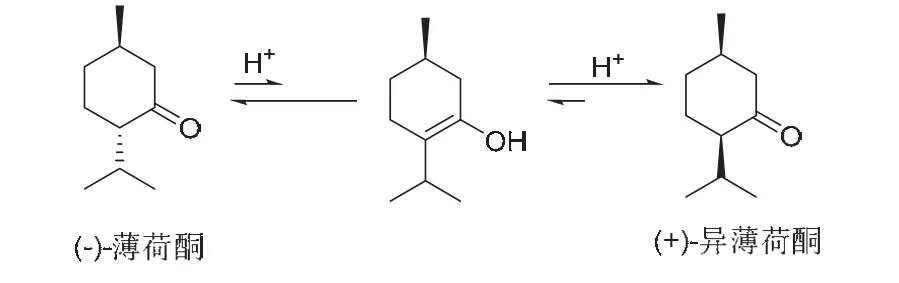
图4 (−)-薄荷酮与(+)-异薄荷酮的互变异构化
5 实验组织运行的建议
(−)-薄荷酮的制备、结构表征及比旋光度测定是一个研究型实验,已在南开大学化学学院2017–2019级伯苓试验班(每班25人)、2018–2019级分子科学与工程试验班(每班30人)、生命科学学院2018级伯苓试验班(30人)及物理学院2019级材料物理专业(15人)有机化学实验开展了教学实践。实验具体组织运行建议如下:
(1) 实验前要求学生查阅薄荷酮制备方法的相关文献,了解薄荷酮的合成方法。
(2) 实验讲授可采用翻转课堂方式,每5个学生一组,各组学生独立完成文献查阅,并准备PPT,重点讲解薄荷酮制备方法及氧化反应机理,每组展讲时间不超过5分钟。教师进行简要点评,强调实验注意事项。
(3) 本实验课时为8学时,其中(−)-薄荷酮的合成与提纯6学时,比旋光度测定及气相色谱表征2学时。
(4) 为比较两种氧化剂的特点,若班级学生为30人,可分为6组,分别采用不同方案完成实验内容。每人独立完成(−)-薄荷酮的合成及反应结束后反应液的洗涤、萃取分液、干燥、过滤等操作,然后将采用相同实验方案的同学每组5人,合并滤液,蒸馏提纯收集产物。计算每组产品收率,测定比旋光度及气相色谱。
(5) 实验完成后,对学生进行问卷调查,了解学生对研究型实验教学模式的看法及建议,反馈实验教学,提高教学质量。
6 结语
本文提供了一例关于手性化合物的合成及其比旋光度测定的研究型有机化学教学实验,通过气相色谱考查了产物的差向异构化现象,对实验结果进行了分析,并成功用于基础有机化学实验教学实践。有机化学实验所涉及的反应原料及产物通常具有气味难闻、有毒、污染环境等特点,大部分试剂还具有易燃甚至易爆等危险性,降低学生对有机化学实验的学习兴趣。本实验采用薄荷醇氧化制备薄荷酮,原料和产物均为天然产物,在化妆品、药品及食品中广泛使用,不仅没有毒性,而且具有令人愉悦的清香,学生表现出很强的学习兴趣。此外,羰基与烯醇式结构的互变异构现象是基础有机化学理论课的重要知识点,可以合理解释产物的比旋光度测试结果,能够培养学生理论联系实际及创新思维能力,同时也培养了学生查找文献及阅读分析文献的能力。
本次实验结束后,我们针对有机化学实验内容是否应该开展探索性新实验进行了问卷调研。调研对象为南开大学2017级化学伯苓试验班学生。调查结果表明,所有学生都希望在有机化学实验教学中开设一些研究型实验内容,认为研究型实验有利于培养创新能力。如同学A提出“有机实验内容应该保留一些经典实验,以练习基本实验操作;另外应该有一些不断更新的实验,使我们的教学内容更加贴近学科的发展。探索性实验能够锻炼我们的思考能力。”同学B认为“新实验内容应跳出课本,如本次实验薄荷醇氧化,具有新颖性和灵活性,能够见识更多的基本操作,达到举一反三的目的。”同学C则认为“探索性实验能够培养学生独立完成全程实验的能力,并对反应中的一些现象解释,真正做到用‘脑子’做实验而不是一味偷懒模仿。”问卷调查结果使我们了解了学生的想法,也为我们开展实验教学改革明确了方向。
致谢:感谢南开大学化学学院2017–2019级伯苓班学生提供参考文献及问卷调查结果。
