肾上腺素受体对慢性阻塞性肺疾病患者内皮祖细胞修复的作用机制
2021-07-13胡萍,徐影,盛净
胡 萍,徐 影,盛 净
(上海交通大学医学院附属第九人民医院,上海 200011)
慢性阻塞性肺疾病(COPD)是中老年人群常见的呼吸系统慢性病,发病率呈逐年上升趋势[1].有研究[2-3]显示:COPD发生、发展的病理过程与心血管疾病的发生密切相关,其中血管内皮细胞结构和功能异常是COPD患者并发心血管疾病的主要因素之一.内皮祖细胞是血管内皮细胞的前体,具备内皮特性,在受损血管内膜修复中发挥重要作用[4].β肾上腺素受体家族包括3个亚型,其中β2肾上腺素受体可通过G蛋白提升细胞内cAMP水平,激活PKA,活化NF-κB等下游靶点,介导细胞多项生理活动[5].有研究[6]发现:大鼠淋巴组织中T细胞、B细胞均存在β2肾上腺素受体表达,参与调控细胞的增殖、分化等过程.亦有研究[7]显示:CD34+干细胞可表达β2肾上腺素受体,其特异性激动剂能够调节细胞迁移.但关于COPD患者外周血内皮祖细胞中β2肾上腺素受体表达情况以及对细胞迁移的影响仍鲜有报道.本研究主要探讨β2肾上腺素受体在COPD患者外周血内皮祖细胞中的表达及作用.
1 对象与方法
1.1 研究对象
收集2019年1月—2019年10月上海交通大学医学院附属第九人民医院收治的COPD患者110例(COPD组),其中,男78例,女32例;年龄58~75岁,平均(67.18±5.30)岁.另收集同期体检的同年龄段健康志愿者62例为对照组,其中,男41例,女21例;年龄60~75岁,平均(66.95±4.16)岁.两组年龄、性别间比较差异均无统计学意义(P>0.05).本研究经医院伦理委员会批准,受试者自愿参与并签署知情同意书.
入选标准:中重度稳定期COPD患者;静息状态下动脉血氧分压>60 mmHg,近1个月未使用激素类药物.
排除标准:原发性高血压、心律失常等原发性心血管疾病;恶性肿瘤、风湿性疾病、肾病等影响外周血干细胞数量的疾病;糖尿病等代谢性疾病.
1.2 主要试剂
胎牛血清、内皮细胞基础培养基(Clonetics公司,美国);β2肾上腺素受体拮抗剂(CI-118551)、β2肾上腺素受体激动剂(去甲肾上腺素,Sigma公司,美国);Trizol总RNA抽提试剂盒、RIPA裂解液(上海捷瑞生物工程有限公司);鼠抗人β2肾上腺素受体单克隆抗体、鼠抗人GAPDH单克隆抗体、山羊抗鼠IgG(上海玉博生物科技有限公司).
1.3 方 法
1.3.1 外周血早期内皮祖细胞制备与鉴定
抽取受试者外周静脉血,分离CD34+细胞;将CD34+细胞种植于内皮细胞基础培养基中,培养48 h,弃去未贴壁的细胞;胰蛋白酶消化贴壁细胞,转入2% BSA封闭液中继续培养30 min,加入CD34 mAb(FITC)、CD133 mAb(PE)、一抗血管内皮细胞生长因子受体2,培养30 min;加入二抗,继续培养30 min后应用流式细胞仪检测.
收集80%表达的外周血早期内皮祖细胞用于实验.取1×106个外周血早期内皮祖细胞接种于含内皮细胞基础培养基的6孔板中培养7 h,加入浓度为3 μg/mL的DiI-acLDL继续培养2 h,弃去培养液;4%多聚甲醛固定10 min,加入浓度为10 mg/L的FITC-UEA-I培养2 h,荧光显微镜下观察到的双染色阳性的细胞为正在分化的早期内皮祖细胞.
1.3.2 RT-PCR检测β2肾上腺素受体mRNA表达
采用Trizol法提取早期内皮祖细胞总RNA,反转录得到cDNA.β2肾上腺素受体及内参GAPDH引物由上海英骏生物技术有限公司设计合成,β2肾上腺素受体引物序列:上游5′-TCCAAGACCTG TACTTAGCG-3′,下游5′-CCTCGTGTTTCGGGAGTT CT-3′;GAPDH引物序列:上游5′-TAGCAGTGGTT GACCCTGCT-3′,下游5′-TCCTTAGGAAGACTGGG TACG-3′.反应条件:94 ℃ 5 min,94 ℃ 30 s,72 ℃ 30 s,共40个循环,延伸72 ℃ 5 min.扩增产物行2%琼脂糖凝胶电泳,并计算相对表达量.
1.3.3 Western blot检测β2肾上腺素受体蛋白表达
应用RIPA裂解液提取早期内皮祖细胞总蛋白,BCA蛋白定量.取50 μg总蛋白行SDS-PAGE凝胶电泳,湿法转至PVDF膜,滴加鼠抗人β2肾上腺素受体单克隆抗体(1∶200稀释),鼠抗人GAPDH单克隆抗体(1∶500稀释),4 ℃过夜,加入HRP标记的山羊抗鼠IgG(1∶1 000稀释),室温下静置2 h,ECL显色,凝胶成像系统拍照.
1.3.4 Transwell小室检测早期内皮祖细胞迁移能力
取早期内皮祖细胞消化、重悬计数后,向上室中加入3×105个早期内皮祖细胞和无血清内皮细胞基础培养基,下室中加入600 μL 10%胎牛血清的内皮细胞基础培养基,孵育24 h后加入40 g/L多聚甲醛固定30 min,洗涤后加入0.1%结晶紫染色,光学显微镜下随机选取10个视野计数.
1.3.5 siRNA转染早期内皮祖细胞下调β2肾上腺素受体表达
使用脂质体2000转染siRNA,操作严格按试剂说明书进行.将siRNA脂质体2000混合液加入含早期内皮祖细胞及含10%胎牛血清的内皮细胞基础培养基中,培养72 h;培养6~8 h后,将培养孔中含siRNA脂质体2000混合液的培养基弃去,更换为新鲜的内皮细胞基础培养基继续培养.
1.4 统计学分析

2 结 果
2.1 早期内皮祖细胞鉴定
光学显微镜下观察早期内皮祖细胞外形与淋巴细胞相似,呈集落样生长,细胞核较大,胞质偏少.荧光显微镜观察显示:早期内皮祖细胞为贴壁细胞,接种24 h后多数呈贴壁生长,继续培养7 d后培养皿中可见早期内皮祖细胞呈梭状致密单层,需传代培养.见图1.
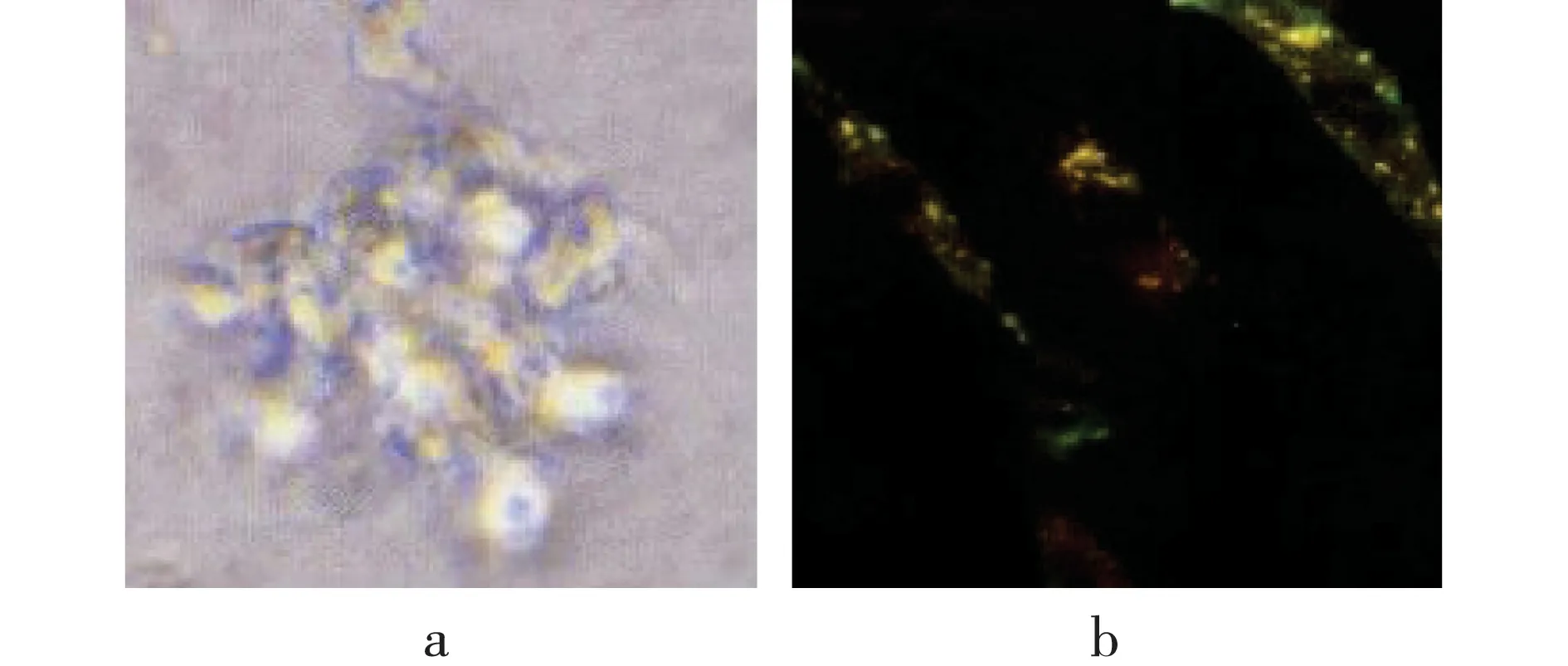
a.光学显微镜观察早期内皮祖细胞(×100);b.荧光显微镜观察早期内皮祖细胞DiI-acLDL 和FITC-UEA-I双染色(×400).图1 光学显微镜及荧光显微镜下观察早期内皮祖细胞Fig.1 Observation of early endothelial progenitor cells under optical microscope and fluorescence microscope
2.2 早期内皮祖细胞中β2肾上腺素受体 mRNA和蛋白表达水平
COPD组内皮祖细胞中β2肾上腺素受体mRNA和蛋白相对表达量均明显高于对照组,差异具有统计学意义(P<0.01).见表1、图2.

表1 两组早期内皮祖细胞中β2肾上腺素受体mRNA和蛋白表达水平Tab.1 β2 adrenoceptor mRNA and protein expression in early endothelial progenitor cells between two groups

A.RT-PCR电泳;B.Western blot电泳.图2 早期内皮祖细胞中β2肾上腺素受体 mRNA和蛋白表达水平Fig.2 Expression level of β2 adrenoceptor mRNA and protein in early endothelial progenitor cells
2.3 不同浓度β2肾上腺素受体拮抗剂对早期内皮祖细胞迁移的影响
两组早期内皮祖细胞分别于不同浓度的β2肾上腺素受体拮抗剂孵育24 h后,Transwell迁移实验显示:COPD组迁移细胞数明显少于对照组,差异具有统计学意义(P<0.05);随着β2肾上腺素受体拮抗剂浓度的增加,COPD组迁移细胞数逐渐增多,当β2肾上腺素受体拮抗剂浓度为15 nmol/L时,两组迁移细胞数比较差异无统计学意义(P>0.05).见表2.

表2 不同浓度β2肾上腺素受体拮抗剂对早期内皮祖细胞迁移的影响Tab.2 Effects of different concentrations of β2 adrenergic receptor antagonists on early migration of endothelial progenitor cells
2.4 不同浓度去甲肾上腺素对早期内皮祖细胞迁移的影响
两组早期内皮祖细胞分别于不同浓度的去甲肾上腺素孵育24 h后,Transwell迁移实验显示:COPD组迁移细胞数明显少于对照组,差异具有统计学意义(P<0.01);随着去甲肾上腺素浓度的增加,COPD组迁移细胞数逐渐减少.见表3.

表3 不同浓度去甲肾上腺素对早期内皮祖细胞迁移的影响Tab.3 Effects of norepinephrine at different concentrations on migration of early endothelial progenitor cells
2.5 下调β2肾上腺素受体表达对早期内皮祖细胞迁移的影响
siRNA转染早期内皮祖细胞72 h后,下室细胞计数显示:对照组、COPD组的迁移细胞数分别为(63.56±10.87)个、(23.31±5.94)个.COPD组迁移细胞数明显少于对照组,差异具有统计学意义(P<0.01).
3 讨 论
COPD是一种可防治的呼吸系统常见慢性病,以呼吸道气流持续受限为主要特征,病情呈进行性发展,与肺组织对有害气体或颗粒的炎症反应有关[8].有研究[9]发现:外界有害刺激可减弱血管内皮细胞的舒张活性,导致内皮功能紊乱,引发心血管疾病,一氧化氮在其中发挥重要调控作用.一氧化氮是人体主要的内源性血管舒张因子,在血管张力调节、抑制血管平滑肌细胞增生、维持肺血管正常阻力方面发挥重要作用[10].内皮祖细胞是血管内皮细胞的前体,具备内皮特性[11].内皮祖细胞分化的成熟内皮细胞能够补充人体内皮细胞的缺失,在维持血管结构、生理功能的完整性方面发挥重要作用[12];同时内皮祖细胞通过分泌一氧化氮促进血管重构,保护血管内皮功能[13].内皮祖细胞的功能状态能够反映出体内血管内皮功能,在血管内皮功能评价中具有重要的参考价值[14].
目前,关于内皮祖细胞的研究主要集中在对血管内皮功能的影响,进而探讨与心脑血管疾病发生、发展的相关性.此外,血管内皮功能变化还与COPD病情严重程度密切相关,患者内皮细胞修复功能的强弱直接影响到血管内皮功能.但关于内皮祖细胞在COPD患者中的活性变化及调控途径的研究仍十分少见.β2肾上腺素受体是一种广泛存在于人体组织中的肾上腺素能受体,介导体内多种生理学功能[15];交感神经可作用于β2肾上腺素受体对细胞增殖、迁移发挥调节作用[16].有研究[17-20]发现:骨髓中CD34+细胞的迁移、归巢受交感神经的调节,β2肾上腺素受体在交感神经作用下影响细胞迁移,β2肾上腺素受体表达可能会影响COPD患者内皮祖细胞的活性.本研究通过分离外周血早期内皮祖细胞,在体外进行验证实验,旨在探讨β2肾上腺素受体表达对COPD患者内皮祖细胞活性的影响.
本研究结果显示:COPD组早期内皮祖细胞中β2肾上腺素受体mRNA和蛋白表达水平明显高于对照组;COPD组迁移细胞数明显少于对照组,使用β2肾上腺素受体拮抗剂干预后可明显提升COPD组迁移细胞数量,去甲肾上腺素干预后可明显降低COPD组迁移细胞数量,且随着β2肾上腺素受体拮抗剂、去甲肾上腺素的浓度增加而改变逐渐明显.进一步通过siRNA转染下调β2肾上腺素受体表达后,COPD患者早期内皮祖细胞迁移细胞数明显升高.提示COPD患者呼吸系统持续慢性炎症反应导致肺组织细胞因子增加,外周血早期内皮祖细胞进入肺组织后,在肺组织停留时受外源性β2肾上腺素受体激动剂刺激,改变了早期内皮祖细胞上β2肾上腺素受体的表达水平,抑制了早期内皮祖细胞由肺组织向外周血迁移,进而引发外周血早期内皮祖细胞数量下降,影响受损血管内皮的修复.我们在后续研究中将进一步探讨β2肾上腺素受体改变早期内皮祖细胞迁移能力的分子机制.
